NSTE-ACS患者应用碘对比剂后甲状腺功能减退的风险因素预测
2023-11-08韩楚仪丛洪良王乐张敬霞
韩楚仪 丛洪良 王乐 张敬霞
摘要:目的 探討非ST段抬高型急性冠脉综合征(NSTE-ACS)患者经皮冠状动脉介入治疗(PCI)后碘对比剂(ICM)对甲状腺功能的影响及发生甲状腺功能减退的危险因素。方法 627例患者根据基线甲状腺激素水平分为甲状腺功能减退组(H组,62例)和甲状腺功能正常组(ET组,565例)。在PCI后1 d、1周、1个月、6个月监测患者甲状腺功能变化,多因素分析PCI前后患者发生甲状腺功能减退的危险因素。结果 2组促甲状腺激素(TSH)水平在PCI后1 d、1周均显著升高(均P<0.05),ET组在6个月时仍然高于基线水平(均P<0.05)。在6个月时,H组62例中43例仍为甲状腺功能减退状态;ET组发生ICM诱发性甲状腺功能减退133例(23.9%),至6个月时34例仍为甲状腺功能减退,发生碘诱导性甲状腺功能亢进事件4例。ICM后发生甲状腺功能减退的风险因素与发生基线甲状腺功能减退的独立危险因素并不完全一致。ICM用量是预测PCI后患者远期发生甲状腺功能减退的可靠工具(曲线下面积为0.674),其最佳阈值为190 mL。结论 NSTE-ACS患者在ICM暴露后发展为显性甲状腺功能减退的风险较低,将ICM暴露后6个月作为研究评估的时间窗可能会掩盖一些延长的ICM诱导性甲状腺功能不全事件。
关键词:造影剂;甲状腺功能减退症;冠心病;非ST段抬高型心肌梗死;急性冠状动脉综合征;经皮冠状动脉介入治疗
中图分类号:R541.4文献标志码:ADOI:10.11958/20221362
Prediction of risk factors for hypothyroidism in NSTE-ACS patients exposed to
iodine contrast media
HAN Chuyi CONG Hongliang WANG Le ZHANG Jingxia
1 Clinical School of Thoracic, Tianjin Medical University, Tianjin 300222, China; 2 The Eighth Department of Cardiology, Tianjin Chest Hospital
Corresponding Author E-mail: zhangjingxia001@126.com
Abstract: Objective To explore the effect of iodine contrast media (ICM) on thyroid function and the risk factors of hypothyroidism in patients with non-ST segment elevation acute coronary syndrome (NSTE-ACS) after percutaneous coronary intervention (PCI). Methods According to the baseline thyroid stimulating hormone (TSH) level, 627 patients were divided into the hypothyroidism group (group H, n=62) and the euthyroid group (group ET, n=565). Changes of thyroid function were monitored at 1 day, 1 week, 1 month and 6 months after PCI, and the risk factors of hypothyroidism before and after PCI were analyzed by multivariate analysis. Results The levels of TSH increased significantly on the 1 day and 1 week after PCI in both groups (P<0.05), and group ET was still higher than its baseline value at 6 months (P<0.05). At 6 months, 43 of 62 cases in the group H were still in the state of hypothyroidism, but the event of overt hypothyroidism did not increase. In the group ET, there were 133 cases of ICM-induced hypothyroidism (23.9%), 34 cases of hypothyroidism and 4 cases of iodine-induced hyperthyroidism at 6 months. The independent predictors for hypothyroidism after ICM were not entirely consistent with the independent predictors for baseline hypothyroidism. The dosage of ICM was a reliable predictor for long-term hypothyroidism after PCI (AUC=0.674), and the best security threshold was 190 mL. Conclusion Patients with NSTE-ACS have a lower risk of developing overt hypothyroidism after ICM exposure. Taking 6 months after ICM exposure as a time window for study evaluation may mask some events of prolonged ICM-induced thyroid insufficiency.
Key words: contrast media; hypothyroidism; coronary disease; non-ST elevated myocardial infarction; acute coronary syndrome; percutaneous coronary intervention
在临床实施放射性检查或治疗如经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)时,患者常接受碘对比剂(iodine contrast media,ICM)。机体突然暴露于超生理剂量的碘负荷可破坏甲状腺激素调节稳态,导致短暂的甲状腺功能减退(Wolff-Chaikoff效应)或甲状腺功能亢进(J?d-Basedow現象)。机体在接受ICM后的临床结局取决于机体的含碘状态和潜在的甲状腺疾病[1-2]。目前ICM暴露对冠状动脉粥样硬化性心脏病(coronary artery disease,CAD)患者甲状腺功能的影响仍未完全阐明[3],特别是亚临床甲状腺功能减退(subclinical hypothyroidism,SCH)在中老年人群中的发病率达4%~10%[4],而ICM暴露对基线SCH患者的甲状腺功能影响尚鲜见报道。为此,笔者选择接受PCI的非ST段抬高型急性冠脉综合征(non-ST segment elevation acute coronary syndrome,NSTE-ACS)患者进行了研究。
1 对象与方法
1.1 研究对象 本研究队列包括2018年5月—2020年5月在天津市胸科医院心内八科接受PCI(单纯球囊血管成形术或支架置入术)的1 998例因CAD而未计划行PCI或冠状动脉旁路移植术(coronary artery bypass grafting,CABG)的NSTE-ACS患者。3个月内有手术史及重大外伤史、既往患有甲状腺疾病、术前化验显示甲状腺功能亢进及严重肝肾功能不全、近1年接受影响甲状腺功能的药物和进行ICM相关检查或治疗的患者均被排除在外。最终共纳入627例。本研究通过天津市胸科医院医学伦理委员会批准(伦理号:2022LW-018)。
1.2 检测指标 患者入院后48 h内行经胸超声心动检查和实验室检查。冠状动脉造影术日清晨及PCI后1 d、1周、1个月、6个月采集外周静脉血标本。应用全自动生化分析仪测定血脂全项、肾功能及血常规等;采用化学发光免疫法测定血清促甲状腺激素(TSH,正常参考值范围0.27~4.2 mIU/L)、游离三碘甲状腺原氨酸(FT3,正常参考值范围3.1~6.8 pmol/L)和游离甲状腺素(FT4,正常参考值范围12.0~22.0 pmol/L)水平。
1.3 甲状腺功能定义及分组 SCH定义为TSH值高于正常参考值范围;显性甲状腺功能减退症(overthypothyroidism,OH)为TSH高于正常参考值范围、FT4低于正常参考值范围;亚临床甲状腺功能亢进症(subclinical hyperthyroidism,SHyper)定义为TSH低于正常参考值范围;显性甲状腺功能亢进症(overt hyperthyroidism,OHyper)定义为TSH低于正常参考值范围、FT4和FT3高于正常参考值范围。ICM诱发性甲状腺功能减退/亢进(ICM-induced hypothyroidism,IIH/ ICM-induced hyperthyroidism,IIHyper)的定义:甲状腺功能减退/亢进的临床表现、实验室发现和ICM暴露史[3]。
依据PCI前基线甲状腺激素水平,将患者分为甲状腺功能减退组(H组,包括SCH及OH)和甲状腺功能正常组(ET组)。
1.4 PCI相关过程 PCI前所有患者均接受负荷量双联抗血小板聚集药物治疗(阿司匹林300 mg、氯吡格雷300 mg或替格瑞洛180 mg)。术中使用非离子型ICM,包括碘克沙醇(含碘270 g/L)、碘普罗胺或碘帕醇(含碘300 g/L)和碘佛醇(含碘320 g/L)。介入专家根据患者的体质量和手术方式决定ICM用量,并用Gensini评分来评价冠状动脉病变的严重程度[5]。
1.5 统计学方法 采用SPSS 22.0、MedCalc 19.6.4软件进行数据分析。符合正态分布的连续变量用x±s表示,组间比较采用独立样本t检验。不符合正态分布的计量资料以M(P25,P75)表示,组间比较采用Mann-Whitney U检验。计数资料以例(%)表示,组间比较采用χ2检验。用两相关样本的Wilcoxon符号等级检验比较ICM后TSH、FT3、FT4水平与术前水平的差异。用多相关样本秩和检验(Friedman检验)及Bonferroni校正比较患者PCI前后不同时间点之间TSH水平的差异。用多因素Logistic逐步回归分析评估PCI前后患者发生甲状腺功能减退事件的独立危险因素。受试者工作特征(ROC)曲线及曲线下面积(AUC)用于评价变量对于预后的预测价值。P<0.05为差异有统计学意义。
2 结果
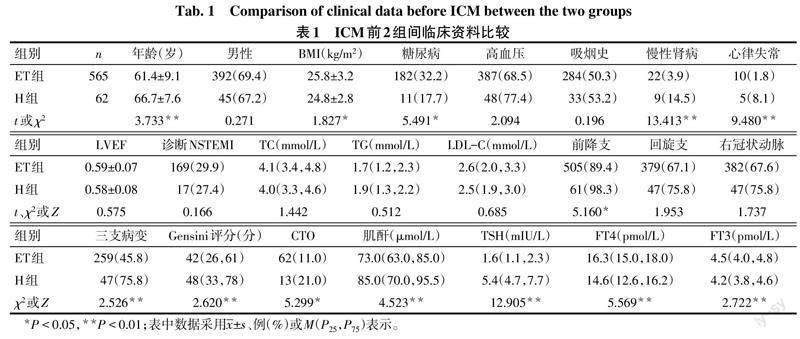
2.1 基线和血管造影特征 627例入选患者中,男437例,女190例。年龄29~83岁,平均(61.9±9.1)岁。PCI时ICM的用量80~450 mL,平均(157.6±51.5)mL。ICM前H组62例(61例SCH、1例OH),ET组565例。与ET组相比,H组患者年龄更高,体质量指数(BMI)更低,合并糖尿病的比例下降,具有慢性肾病和心律失常史、前降支病变及冠脉三支病变、慢性闭塞病变(CTO)的比例及Gensini评分更高,肌酐、TSH水平更高且FT3、FT4水平更低(P<0.05),见表1。
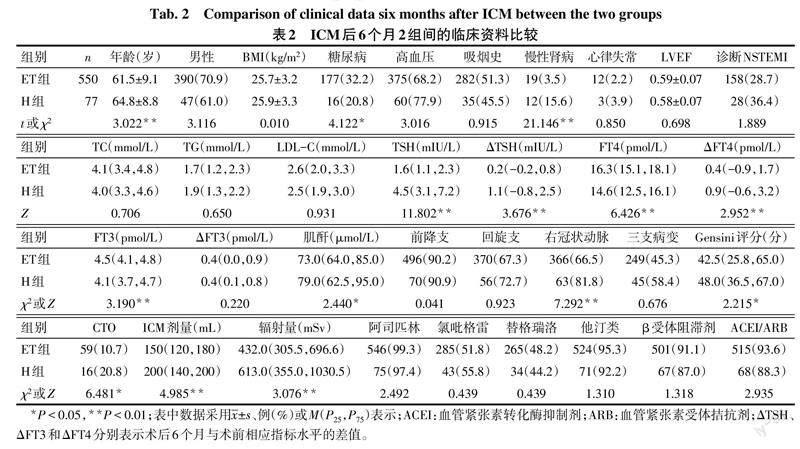
ICM后6个月时,全组共发生甲状腺功能减退77例(H组43例,ET组34例),这些患者的年龄、合并糖尿病的比例更低,具有慢性肾病史的比例更高,右冠状动脉病变及CTO数目更多且具有更高的Gensini评分,TSH、ΔTSH和ΔFT4水平更高,FT3和FT4水平更低,肌酐水平、ICM用量及辐射量更高(P<0.05),见表2。2组出院时用药情况差异无统计学意义(P>0.05)。
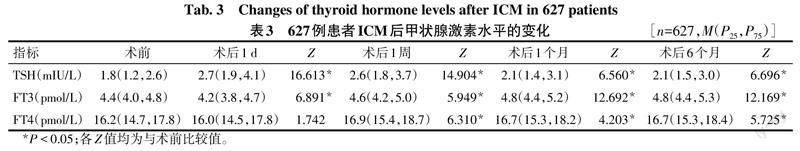
2.2 甲状腺激素的变化趋势 627例患者在ICM后6个月时TSH水平仍然高于基线水平;在ICM后1 d FT3水平下降,在1周至6个月均高于术前水平。除术后1 d FT4水平和术前水平相比无显著变化外,其余各测量时刻TSH、FT3、FT4水平与术前激素水平相比差异均有统计学意义(P<0.05),见表3。
H组TSH水平在ICM暴露后1 d和1周均较基线水平显著升高,1个月时TSH水平较ICM暴露后1 d显著降低,6个月时该组TSH水平较术后1 d和1周均降低,与1个月时相比差异无统计学意义。ET组在ICM暴露后各测量时刻的TSH水平均显著高于基线水平,1个月时该组TSH水平较术后1 d和1周显著下降,6个月时TSH水平较术后1 d和1周下降,与1个月相比差异无统计学意义,见表4。
2.3 ICM前后甲状腺功能减退的时间分布和进程 H组中TSH峰值出现在ICM前有5例,术后1 d 33例、1周17例、1个月3例、6个月4例。ICM后6个月时仍为甲状腺功能减退状态者共43例,包括41例SCH(66.1%)、2例OH,其中1例OH为SCH进展而来。
ET组ICM后6个月发生IIH事件133例,发生时间分别为:术后1 d 97例、术后1周27例、1个月3例、6个月6例。术后6个月时仍有34例IIH患者,包括28例SCH、6例OH;术后6个月时发生ICM诱发性亚临床甲状腺功能亢进3例、ICM诱发性显性甲状腺功能亢进1例并接受治疗。
2.4 ICM前后发生甲状腺功能减退的影响因素 将表1、表2中P<0.05的变量以及具有重要临床意义的变量(高血压)纳入多因素Logistic回归分析。以ICM前是否诊断为甲状腺功能减退(否=0,是=1)为因变量,以年龄、BMI、肌酐、高血压、糖尿病、心律失常(均赋值为有=1,无=0)为自变量,进行Logistic多因素回归分析。结果显示,年龄、肌酐、高血压和糖尿病是患者PCI前发生甲状腺功能减退的影响因素,见表5。以ICM后是否诊断为甲状腺功能减退(否=0,是=1)为因变量,以年龄、肌酐、Gensini评分、CTO、ICM用量和辐射量、高血压、糖尿病(均赋值为有=1,无=0)为自变量,结果显示高龄、肌酐水平升高、高血压、糖尿病和ICM用量大是患者PCI后6个月发生甲状腺功能减退的独立危险因素,见表6。
以ICM后是否诊断为甲状腺功能减退(否=0,是=1)为因变量,以性别(男=0,女=1)、慢性肾病、吸烟史、右冠状动脉病变(均赋值为有=1,无=0)及ICM用量为自变量,对ET亚组进行分析。结果显示女性、右冠状动脉病变和慢性肾病是基线ET的NSTE-ACS患者接受ICM后6个月发生甲状腺功能减退的独立危险因素。见表7。
2.5 ICM用量对患者安全性的预测价值 ICM用量的AUC为0.674(95%CI:0.636~0.711,P<0.001)。ICM用量的最佳阈值为190 mL,敏感度为58.4%,特异度为78.4%,见图1。
3 讨论
本研究采用前瞻性队列研究探讨了ICM对基线甲状腺功能减退并接受PCI的NSTE-ACS患者甲状腺功能变化,发现高龄、肌酐水平升高、高血压、糖尿病、ICM用量大独立于其他的传统危险因素,是NSTE-ACS患者PCI后6个月发生甲状腺功能减退的独立危险因素。女性、右冠状动脉病变和慢性肾病是基线ET的NSTE-ACS患者PCI后发生甲状腺功能减退的独立危险因素。
3.1 ICM暴露后甲状腺功能的动态变化 过量碘暴露对机体甲状腺功能的影响尚未完全确定。考虑到既往研究中在碘暴露后患者发生的甲状腺延迟反应多在6个月内恢复正常[1],笔者谨慎选择了NSTE-ACS患者ICM后6个月内的4个随访时点监测甲状腺激素水平。结果显示2组患者TSH中位水平在ICM给药后1周内均显著升高,至6个月时总体甲状腺功能减退发生率仍然高达12.3%,但OH的发生率较低(1.3%),与近期研究结果基本一致[2],表明在ICM给药后NSTE-ACS患者面临短暂的SCH风险。但本研究ICM后所有甲状腺功能减退患者中,85.6%(167例)患者的TSH峰值出现在ICM给药后1周内,但直到研究结束时仍有11例TSH水平升高达到峰值,同时出现6例新发的ICM诱发性甲状腺功能减退患者,表明过量碘暴露6个月发生Wolff-Chaikoff效应逃逸的病例依然存在。最近有报道从ICM给药到发生甲状腺功能减退的易受攻击时间窗中位时间为117 d~10.8个月,碘暴露后对甲状腺功能的评估时间不同,诱发性事件的发生率和发生的确切时间难以预测[6-7]。然而,目前关于ICM暴露后对患者甲状腺功能进行监测的时间点选择和意义在国际上仍存在争议[8-9]。
迄今对基线甲状腺功能减退患者在ICM暴露后甲状腺功能的动态变化以及发生OH风险的研究很少。有研究认为碘暴露后TSH变化似乎取决于最初的甲状腺状态[10]。本研究入选NSTE-ACS患者中基线甲状腺功能减退发生率为9.9%,在ICM暴露后基线H组TSH中位水平、升高幅度均高于ET组,然而仅1例ET组患者发展为OH。基线H组中有5例TSH峰值出现在PCI前,这种现象迄今尚未见文献描述或解释。同时,基线H组中唯一一例OH患者在ICM暴露后6个月仍维持OH。但由于本研究条件所限,未在入院后测量患者的甲状腺自身抗体,因此不能确定出现这种现象的具体原因。笔者认为,在甲状腺功能减退和过量碘刺激共同存在的情况下,个体发生甲状腺功能障碍事件的可能性及发生时间取决于患者甲状腺功能状态或已存在的甲状腺疾病[3,11],其结果也具有高度可变、不可预测性。基线H组患者,特别是OH患者在ICM暴露后是否增加了发展为OH的风险仍有待今后研究进一步证实。
3.2 ICM前后发生甲状腺功能减退症的影响因素 本研究NSTE-ACS群体在调整了传统混杂因素情况下,ICM用量是独立于其他公认传统危险因素以外的发生诱导性甲状腺功能减退事件风险的独立危险因素,尤其是单次ICM用量大于190 mL时患者发生甲状腺功能减退的风险显著增高。同时,除年龄、肌酐、高血压、糖尿病外,ICM用量对PCI后发生甲状腺功能减退的影响也不容忽视。有研究证实,查尔森共病指数较高患者在碘暴露后发生甲状腺功能障碍的风险更高[12]。这一结论与本研究的亚组分析结果一致,即除女性及右冠状动脉病变外,慢性肾病也是基线ET的NSTE-ACS患者接受ICM后6個月发生甲状腺功能减退的独立危险因素。这可能与基线ET患者在ICM给药后尿碘浓度平均恢复正常时间长达1个月以上有关[13]。因此,笔者建议在ICM暴露后应该对全部具有诱发甲状腺功能减退高危风险的患者及时监测、评估甲状腺功能,特别是基线ET的女性、具有右冠状动脉病变、慢性肾病史且合并潜在的不稳定心血管疾病的患者。对中重度肾功能不全、甲状腺功能严重异常等患者建议应用超低剂量ICM[14]。
3.3 局限性 由于本研究納入的病例在PCI前未实施甲状腺超声筛查和监测甲状腺自身抗体(TPOAB和TGAB)等,基线甲状腺功能减退的病因难以确定。此外,本研究中基线OH患者(仅1例,0.2%)以及发生ICM诱导性甲状腺功能亢进的患者数量较少(4例,2.9%),无法进行亚组分析以确定其特征。未来需更多大样本、多中心、随机对照研究探讨ICM对基线OH及亚临床甲状腺功能亢进患者远期甲状腺功能的影响。
综上所述,NSTE-ACS患者在ICM暴露后具有发生甲状腺功能障碍的风险,ICM用量大可作为独立危险因素预测NSTE-ACS患者PCI后发生甲状腺功能减退的风险。临床医生需优化ICM给药剂量并严密监测ICM后NSTE-ACS患者的甲状腺功能变化,及时调整临床治疗方案。
参考文献
[1] RHEE C M,BHAN I,ALEXANDER E K,et al. Association between iodinated contrast media exposure and incident hyperthyroidism and hypothyroidism[J]. Arch Intern Med,2012,172(2):153-159. doi:10.1001/archinternmed.2011.677.
[2] KUBICKI R,GROHMANN J,KUNZ K G,et al. Frequency of thyroid dysfunction in pediatric patients with congenital heart disease exposed to iodinated contrast media-along-term observational study[J]. J Pediatr Endocrinol Metab,2020,33(11):1409-1415. doi:10.1515/jpem-2020-0032.
[3] BEDNARCZUK T,BRIX T H,SCHIMA W,et al. 2021 European Thyroid Association Guidelines for the Management of Iodine-Based Contrast Media-Induced Thyroid Dysfunction[J]. Eur Thyroid J,2021,10(4):269-284. doi:10.1159/000517175.
[4] PASCHOU S A,BLETSA E,STAMPOULOGLOU P K,et al. Thyroid disorders and cardiovascular manifestations:an update[J]. Endocrine,2022,75(3):672-683. doi:10.1007/s12020-022-02982-4.
[5] RAMPIDIS G P,BENETOS G,BENZ D C,et al. A guide for Gensini score calculation[J]. Atherosclerosis,2019,287:181-183. doi:10.1016/j.atherosclerosis.2019.05.012.
[6] JICK S S,HEDDERSON M,XU F,et al. Iodinated contrast agents and risk of hypothyroidism in young children in the United States[J]. Invest Radiol,2019,54(5):296-301. doi:10.1097/RLI.0000000000000541.
[7] BARR M L,CHIU H K,LI N,et al. Thyroid dysfunction in children exposed to iodinated contrast media[J]. J Clin Endocrinol Metab,2016,101(6):2366-2370. doi:10.1210/jc.2016-1330.
[8] LEIDIG-BRUCKNER G. Iodinated contrast medium in patients with thyroid disorders[J]. Radiologe,2019,59(5):413-424. doi:10.1007/s00117-019-0520-y.
[9] RUSANDU A,SJ?VOLD B H,HOFSTAD E,et al. Iodinated contrast media and their effect on thyroid function - Routines and practices among diagnostic imaging departments in Norway[J]. J Med Radiat Sci,2020,67(2):111-118. doi:10.1002/jmrs.390.
[10] GARTNER W,WEISSEL M. Do iodine-containing contrast media induce clinically relevant changes in thyroid function parameters of euthyroid patients within the first week?[J]. Thyroid,2004,14(7):521-524. doi:10.1089/1050725041517075.
[11] LEE S Y,RHEE C M,LEUNG A M,et al. A review:Radiographic iodinated contrast media-induced thyroid dysfunction[J]. J Clin Endocrinol Metab,2015,100(2):376-383. doi:10.1210/jc.2014-3292.
[12] KORNELIUS E,CHIOU J Y,YANG Y S,et al. Iodinated contrast media increased the risk of thyroid dysfunction:a 6-year retrospective cohort study[J]. J Clin Endocrinol Metab,2015,100(9):3372-3379. doi:10.1210/JC.2015-2329.
[13]LEE S Y,CHANG D L,HE X,et al. Urinary iodine excretion and serum thyroid function in adults after iodinated contrast administration[J]. Thyroid,2015,25(5):471-477. doi:10.1089/thy.2015.0024.
[14] 中華医学会心血管病学分会介入心脏病学组,中华医学会心血管病学分会大血管病学组,中华心血管病杂志编辑委员会. 经动脉心血管介入诊治中含碘对比剂相关不良反应防治的中国专家共识(2021)[J]. 中华心血管病杂志,2021,49(10):972-985.Interventional Cardiology Group,Chinese Society of Cardiology,Chinese Medical Association,Macrovascular Group,Chinese Society of Cardiology,Chinese Medical Association,Editorial Board ofChinese Journal of Cardiology,et al. Chinese expert consensus on management strategies for adverse events related tointra?arterial use of iodine contrast media during cardiovascular intervention[J]. Chin J Cardiol,2021,49(10):972-985. doi:10.3760/cma.j.cn112148-20210315-00224.
(2022-09-14收稿 2022-11-21修回)
(本文编辑 李鹏)
