不同处理核桃雄花中多酚类化合物的变化
2023-01-30于晨晨徐萌李升云袁友卫齐国辉田益玲
于晨晨,徐萌,李升云,袁友卫,齐国辉,田益玲,3,4*
(1.河北农业大学食品科技学院,河北 保定 071000;2.河北农业大学林学院,河北 保定 071000;3.河北省核桃工程技术中心,河北 邢台 054000;4.河北省(邢台)核桃产业技术研究院,河北 邢台 054000)
核桃雄花(walnut staminate flowers)是核桃生殖生长过程中的副产物,少量用于授粉,其余均予疏除,因而其产量与核桃相当。刚采摘的核桃雄花蛋白质含量达18.8%,干燥后的核桃雄花高达21%~25%,不仅高于核桃仁,而且是干蕨菜和脱水白菜蛋白质的3倍[1-3]。在少数地区核桃雄花被用做蔬菜食用,制作炸菜、炒菜、凉拌菜等[4]。核桃雄花还具有抗氧化、抗炎、降血糖等功能活性,这与其多酚含量高有关[5-6]。研究表明,核桃花中槲皮素与山萘酚的含量分别达0.23%和0.08%[7]。Chrzanowski等[8]在核桃花序中鉴定出绿原酸、香草酸、对羟基苯甲酸等11种酚酸,其中香草酸为雄花中主要成分,含量达359.5 μg/g。贾忠等[9]通过核磁共振波谱法对核桃花中黄酮类物质进行分析,鉴定出山柰酚-3-O-α-L-鼠李糖苷、槲皮素-3-O-β-D-葡萄糖苷、槲皮素等7个黄酮类物质。然而,加工处理储藏方式对其生物活性物质影响方面的研究较少。
另外,多酚类化合物是引发褐变的主要因素之一,其在酶促褐变和非酶促褐变中都起着重要的作用,因此,深入研究核桃雄花中酚类物质的组分不仅有助于了解其褐变物质及作用机制,还为核桃雄花产品开发和防褐变提供一定的依据。超高分辨液相色谱质谱技术(ultra-high resolution liquid chromatography-mass spectrometry,UHPLC-MS/MS)是植物化学成分分析和鉴定的重要技术,具有高分辨率、高选择性、高灵敏度等优点[10]。本研究以新鲜、真空冷冻干燥和自然晾干核桃雄花为研究材料,采用UHPLC-MS/MS法,结合数据库及文献报道对其多酚类化合物的质谱裂解途径和结构进行分析,为进一步研究核桃雄花提供参考。
1 材料与方法
1.1 材料与试剂
供试核桃雄花(绿岭)采于河北省绿岭有限公司生产基地。
乙醇、甲醇、甲酸(均为分析纯):天津富宇化工有限公司;乙腈(色谱纯):美国Sigma-Aldrich化学试剂公司。
1.2 仪器与设备
Q Exactive Plus Orbitrap高分辨液质联用仪:赛默飞世尔科技公司;5425R低温离心机:德国Eppendorf公司;scilogex可调混合仪:上海珂淮仪器有限公司;LG10冷冻干燥机:新阳速冻设备制造有限公司;DiKMA Platisil ODS色谱柱:中国Dikma公司。
1.3 采收后核桃雄花的不同处理
将新鲜采摘的核桃雄花分别进行真空冷冻干燥(真空度 100 Pa、温度-50℃、24 h)、冷冻(-20℃、12 h)和自然晾干(25℃、5 d)处理。
1.4 样品溶液制备
取适量新鲜、真空冷冻干燥和自然晾干核桃雄花样,在乙醇浓度60%、料液比1∶25(g/mL)、温度60℃、提取时间60 min下通过超声辅助提取多酚类化合物,再经大孔树脂纯化、浓缩、冻干得核桃雄花多酚纯化物,-20℃条件保存备用。将核桃雄花多酚粉末溶于50%甲醇,超声30 min,14 000 r/min离心5 min取上清液,过0.22 μm微孔滤膜,待UHPLC-MS/MS分析。
1.5UHPLC-MS/MS分析条件
色谱条件:Dionex Ultimate 3000超高效液相系统;色谱柱:DiKMA Platisil Octadecylsilyl(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%甲酸水(B);柱温:30℃;流速:0.5 mL/min;进样量:10 μL;波长:280 nm;梯度洗脱程序:0~2 min,8%~10%A;2 min~27 min,10%~30%A;27 min~50 min,30%~90%A;50 min~52 min,90%~100%A;52 min~56 min,100%A;56 min~60 min,100%~8%A。
质谱条件:Q Exactive Orbitrap高分辨质谱;扫描范围m/z 100~1 200、离子源电压3.2 kV、鞘气流速40 L/min、辅助气体流量15 L/min、毛细管温度320℃、辅助燃气加热器温度350℃。
1.6 数据分析
采用Compound discover 3.2软件进行原始质谱数据特征峰提取,以对供试样品溶液中多酚成分的保留时间和质谱信息进行分析;通过mzcloud在线数据库和本地自建mzvault天然产物数据库对化学成分作进一步推断。
2 结果与分析
2.1 不同处理的核桃雄花
对核桃雄花进行不同处理后的结果见图1。

图1 核桃雄花Fig.1 Walnut staminate flowers
由图1可知,真空冷冻干燥能较好地保留核桃雄花原本的绿色特征,而自然晾干及低温冷冻的核桃雄花发生严重的褐变现象,呈褐色。真空冷冻干燥过程中不仅降低环境中的氧气分压,而且能够去除氧化反应介质水分,从而有效地阻止酚类物质的氧化反应,因此保持其绿色,而冻藏和自然晾干发生较大的褐变。
2.2 核桃雄花中多酚物质的UHPLC-MS/MS分析
采用UHPLC-MS/MS对不同处理核桃雄花多酚提取物的化学成分进行定性分析,在电喷雾离子源(electrospray ionization,ESI)正负离子模式下,样品中的化合物具有良好的响应,结果见图2。
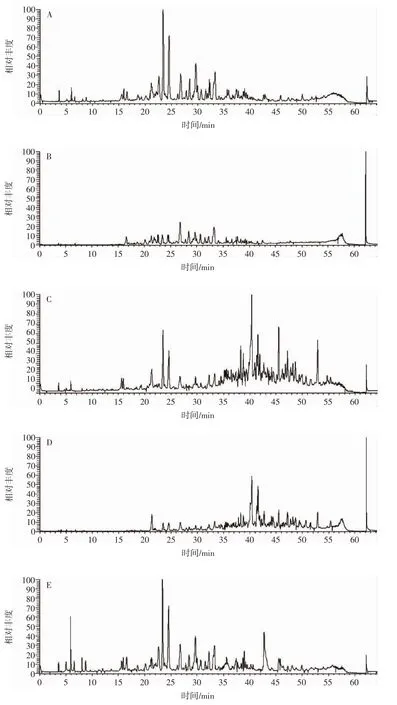
通过利用化合物主要碎片离子、保留时间、分子离子峰等信息,结合相关文献报道及mzcloud和mz-Vault数据库收录的天然产物,对新鲜、真空冷冻干燥和自然晾干后的核桃雄花中主要多酚类物质进行分析,表1汇总了初步鉴定的41种活性成分,包含17种黄酮类、9种单宁类、9种酚酸类和6种香豆素类。

表1 不同处理核桃雄花中多酚类成分的鉴定分析结果Table 1 Identification and analysis of polyphenols in walnut staminate flowers with different treatments

续表1 不同处理核桃雄花中多酚类成分的鉴定分析结果Continue table 1 Identification and analysis of polyphenols in walnut staminate flowers with different treatments
由表1可知,山奈酚、金丝桃苷和槲皮苷等为新鲜、真空冷冻干燥及自然晾干褐变核桃雄花的共有组分,新鲜样品还有异鼠李素、高黄芩素、瑞香素等为褐变样中未检测到物质,而肉桂酸和7-羟基香豆素为自然晾干褐变后核桃雄花独有成分。推测鲜样中检测到的物质为发生褐变的主要酚类物质,而肉桂酸和7-羟基香豆素为褐变产物,但其发生过程有待进一步深入研究。
2.2.1 黄酮类物质分析
黄酮类化合物主要有脱去中性碎片、失去羰基、逆狄尔斯-阿德尔(retro-diels-alder,RDA)裂解重排、糖苷键断裂等裂解方式。例如化合物18母离子为m/z 287[M+H]+,裂解的二级离子峰有m/z 121[M-H-COH2O-C6H4O]+,m/z 153[M+H-134]+,m/z 241[M+H-COH2O]+,与已有报道结果相一致[11-12],因此推测化合物18为山奈酚。
化合物36负离子模式下母离子为m/z 301[M-H]-,由此得知其分子量为302,同时化合物36具有特征碎片离子m/z 179和m/z 151,结合文献[13]及数据库推断化合物36为槲皮素。由于槲皮素A、B苯环结构稳定,质谱裂解产生碎片主要在C环的RDA裂解,由此可知碎片离子m/z 179为母离子通过发生RDA裂解获得,丢失一分子CO产生碎片m/z 151,继续掉下CO2得到m/z 107碎片。化合物25母离子为m/z 463[M-H]-,确定分子量为464。碎片离子m/z 301[M-H-Glc]-是母离子失去葡萄糖残基得到,碎片m/z 301再裂解生成m/z 179和m/z 151两个特征离子,或发生RDA裂解得碎片m/z 151,再失去一个CO2获得m/z 107离子。结合断裂信息和文献[14],确定化合物25为异槲皮苷。化合物32准分子离子峰为m/z 447[M-H]-,二级裂解得碎片m/z 301和m/z 283,经分析,m/z 301是母离子失去一分子鼠李糖基得到,m/z 283是失去一分子己糖基团得到,与槲皮苷的裂解规律一致,结合数据库及已有文献[15]报道,确定化合物32为槲皮苷。
化合物39分子离子峰为m/z 285[M-H]-。丢失中性分子H2O得离子m/z 267[M-H-H2O]-,再连续失去一分子CO得碎片m/z 239[M-H-H2O-CO]-和m/z 211[MH-H2O-2CO]-;C环发生RDA裂解产生m/z 167和m/z 117离子,结合分析及数据库检索推断化合物39为高黄芩素。
化合物40准分子离子峰m/z 315[M-H]-,二级裂解产生典型碎片离子m/z 300[M-H-CH3]-,再丢失一个CHO得碎片m/z 271;母离子发生RDA裂解得碎片离子m/z 151。与文献[16]报道一致,因此确定化合物40为异鼠李素。
2.2.2 单宁类物质的分析
化合物1母离子为m/z 305[M-H]-,二级碎片离子为 m/z 179[M-H-C6H6O3]-、m/z 165[M-H-C7H8O3]-、m/z 137、m/z 125[M-H-C9H8O4]-,因此推测其分子式为C14H15O7,结合文献[17]数据和数据库,推断化合物1为表没食子儿茶素。化合物16分子离子峰为m/z 457[M-H]-,进而确定其分子量为458。二级特征碎片离子为 m/z 305、m/z 169、m/z 125。其中碎片离子 m/z 305[M-H-152]-为母离子通过RDA反应产生;离子m/z 169和m/z 125是表儿茶素/儿茶素没食子酸酯的特征离子碎片,表明化合物16的结构中含有没食子酰基[18]。由上述质谱信息及数据库检索,推断化合物16为表没食子儿茶素没食子酸酯。
化合物6母离子为m/z 577[M-H]-,分子量为578,是两个单体通过C4-C8或C4-C6键连接的二聚体典型分子量。其二级裂解的主要碎片离子有:m/z 407、m/z 289、m/z 245、m/z 125,其中最强峰离子 m/z 125[M-H-452]-为母离子发生杂环裂解(heterocyclic ring fission,HRF)反应,丢失一分子间苯三酚所产生;分子离子先发生RDA反应再丢失一分子水获得碎片离子m/z 407[M-H-C8H8O3-H2O]-;离子m/z 289和m/z 245分别为母离子由分子间断裂失去C15H12O6,再失去一分子CO2产生。此结果与文献[19]报道相似,因此推断化合物6为B型原花青素二聚体。
化合物10负离子模式下母离子m/z 169[M-H]-,进而推断其分子量为170,二级碎片离子为m/z 151、m/z 125和m/z 107。其中m/z 125和m/z 151是没食子酸特征碎片离子[20],没食子酸脱水得到离子峰m/z 151,m/z 125失去一分子水得到碎片m/z 107,因此推断化合物10为没食子酸。
2.2.3 酚酸类物质的分析
化合物2正离子模式下出现分子离子峰m/z 181[M+H]+,分子量为180。二级碎片离子有m/z 163、m/z 135以及m/z 117,由母离子脱水、脱羧和连续脱水获得,说明化合物2结构中可能含有羧基和邻二羟基,因此推断化合物2为咖啡酸。化合物38准分子离子峰为m/z 207[M-H]-,则分子量为208,其二级碎片离子为m/z 179、m/z135和m/z134,其中m/z 179为咖啡酸,再掉下一分子CO2得到碎片m/z 135,失去一分子羧酸得到碎片m/z 134,结合数据库及文献[21]确定化合物38为咖啡酸乙酯。
化合物4和12的准分子离子峰均为m/z 353[MH]-,分子量为354;二级裂解得到离子m/z 191、m/z 179、m/z 173和m/z135,然而,它们的碎片离子丰度不同。经分析,母离子失去1个咖啡酰基得m/z 191,其再失去一分子水[191-H2O]-得到m/z 173,m/z 179为咖啡酸根,m/z 135为[179-COO]-,因此推测二者为绿原酸的两个同分异构体。结合数据库分析及文献[22],确定化合物4为隐绿原酸,化合物12为绿原酸。
化合物29正离子模式下对母离子m/z 149[M+H]+进行碰撞诱导裂解,得到主要碎片离子m/z131、m/z103、m/z 121和m/z 79。碎片m/z 121[M+H-CO]+为母离子失去一个CO产生;m/z 131[M+H-H2O]+为丢失一分子H2O形成,再失去一分子CO产生碎片m/z 103[M+H-H2OCO]+,二者分别为失去羰基和羧基形成的特征碎片离子。结合数据库检索,推断化合物29为肉桂酸。
化合物34经母离子m/z 195裂解产生碎片离子m/z177、m/z164和m/z149,母离子失去一分子水得到碎片m/z 177[M+H-H2O]+,丢失一分子羧基产生m/z 149[M+H-COOH]+,与文献报道一致[23],再结合数据库确定化合物34为阿魏酸。
2.2.4 香豆素类物质的分析
该类化合物反映的主要特征是母离子丢失中性分子。例如化合物13的准分子离子峰为m/z 147,则分子量为146,其二级裂解碎片离子有m/z 119和m/z 91,碎片m/z 119[M+H-CO]+是由母离子失去一分子CO得到的,再失去一分子CO得到碎片m/z 91,即为C7H7+,因此确定化合物13为香豆素,此数据与文献[24]质谱数据一致。化合物5母离子m/z 161[M-H]-进行反应,二级裂解产生特征碎片离子m/z 133、m/z 105和m/z 99,其反应途径为连续失去两个CO基团,可能为环上的CO破裂,也可能是酯键上的CO破裂,而环上的CO更易失去[18]。碎片m/z 99为母离子连续失去一分子CO2和H2O所得。结合数据库检索,推断化合物5为7-羟基香豆素。
3 结论
本研究通过UHPLC-MS/MS法对不同处理后的核桃雄花多酚类化合物进行定性分析,共鉴定出41个活性成分,包括17种黄酮类、9种单宁类、9种酚酸类和6种香豆素类,其中山奈酚、金丝桃苷、槲皮苷、芦丁、紫云英苷等为新鲜样品、真空冷冻干燥样品和自然晾干样品的共有组分,自然晾干褐变后核桃雄花中另有7-羟基香豆素和肉桂酸两种酚类组分。多酚类化合物是引发褐变的主要底物,黄烷醇类易与酚酸类反应生成棕色聚合物,而山奈酚、金丝桃苷、槲皮苷、异鼠李素等在自然晾干褐变样品中变化明显,金丝桃苷、槲皮苷和紫云英苷等结构中还含有糖苷键,易被水解并发生美拉德反应生成糠醛,化学性质活泼的糠醛经过积累进而发生褐变。此结果表明核桃雄花发生的褐变与酚类物质导致的非酶褐变有极大的关系,但酚类化合物与雄花褐变之间的具体相关性还需进行进一步稳定性试验来验证。本研究通过对不同处理核桃雄花多酚的变化进行研究,从而发现导致核桃雄花褐变的酚类成分,为核桃雄花防褐变研究提供一定参考。
