血浆β-羟丁酸对ST段抬高型心肌梗死患者心源性死亡的影响*
2022-12-23刘微蒋智姚雨彤刘会宋勃邓世燕潘裕佳韦方吴强
刘微, 蒋智**, 姚雨彤, 刘会, 宋勃, 邓世燕, 潘裕佳,2, 韦方,2, 吴强,2
(1.贵州省人民医院 心内科, 贵州 贵阳 550002; 2.贵州医科大学 临床医学院, 贵州 贵阳 550025)
ST段抬高型心肌梗死(ST-segment elevation myocardial infarction, STEMI)是进展为心力衰竭的重要危险因素[1-2]。正常心肌主要利用脂肪酸和葡萄糖供能[3],但STEMI后心肌细胞不能有效利用脂肪酸和葡萄糖,肝脏生成的酮体成为了心肌细胞的主要能量来源[4]。血酮体水平与多种慢性疾病的心肌梗死和脑卒中风险相关[5-7],亦与STEMI患者的梗死面积和左室射血分数(left ventricular ejection fraction, LVEF)相关[8],但血酮体水平与STEMI患者预后的关系尚未见报道。β-羟基丁酸(β-hydroxybutyric acid, β-HB)是临床上用于检测血酮体的替代指标[9],因此,本研究拟通过分析STEMI患者入院时血浆β-HB水平与随访期间发生的心源性死亡事件,探索血浆β-HB水平与心源性死亡的关系。
1 对象与方法
1.1 研究对象
选取2016年1—12月心内科住院的18~80岁STEMI患者,要求STEMI的诊断和治疗符合《急性ST段抬高型心肌梗死诊断和治疗指南》[10]相关推荐,排除严重消化道出血、脑出血、严重肝肾功能不全(胆红素升高3倍,谷丙转氨酶/谷草转氨酶升高10倍,或估算肾小球滤过率≤30 mL/(min×1.73m2)。共纳入STEMI患者282例,男235例(83%)、女47例(17%),年龄34~99岁、平均(62.4±12.2)岁;根据血浆β-HB值大小分为β-HB正常组(β-HB<0.3 mmol/L,n=189)和β-HB升高组(β-HB≥0.3 mmol/L,n=93),入选患者的一般特征见表1。本研究获得医院伦理委员会审查批准(〔2018〕17号)。
1.2 研究方法
1.2.1临床资料及分组 患者一般临床资料、实验室检验及辅助检查数据均从医院信息系统(hospital information system,HIS)数据库收集,包括年龄、性别、既往史、现病史、用药情况[如阿司匹林、嘌呤能受体2型Y12亚型(purinergic receptor type 2 subtype Y12, P2Y12)抑制剂、他汀和血管紧张素转化酶抑制剂/血管紧张素受体抑制剂(angiotensin converting enzyme inhibitor/angiotensin receptor blocker,ACEI/ARB)]、血运重建、心脏超声、血脂及血生化;所有检验、检查均在医院检验科和心功能室完成,均为患者入院后第1次结果;血浆β-HB均在患者入院后12 h内抽、用生化免疫自动化流水线系统(ACCELERATOR a3600,雅培)检测。
1.2.2研究终点和随访 研究终点为心源性死亡,定义为任何与心肌梗死、低心排、恶性心律失常及心血管手术相关的死亡,也包括无旁观者死亡和不明原因死亡[11]。患者出院后于第1、3、6及12月进行随访,通过门诊或电话方式、采用预制的随访表格记录患者情况,之后每隔6月随访。
1.3 统计学分析

2 结果
2.1 一般临床资料
2组STEMI患者年龄、性别、高血压患病率、吸烟率、血脂、LVEF、估算肾小球滤过率、阿司匹林、 P2Y12抑制剂、他汀和ACEI/ARB抑制剂的使用率比较,差异无统计学意义(P>0.05);2组患者的糖尿病患病率、心功能Killip Ⅲ~Ⅳ级率、起病时间、血红蛋白、急诊血运重建率、择期血运重建率及β-受体阻滞剂使用率比较,差异有统计学意义(P<0.05)。见表1。
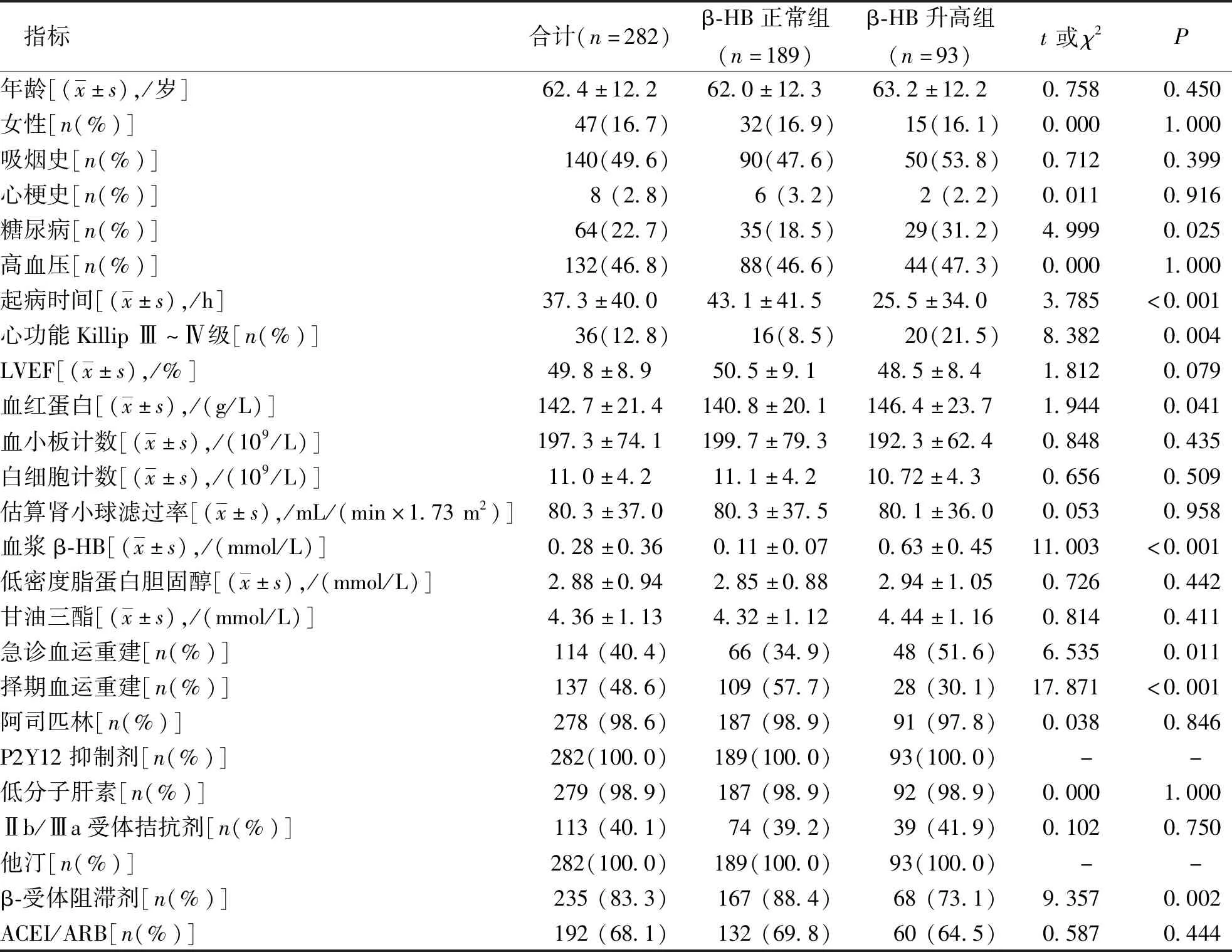
表1 β-HB正常和升高组STEMI患者的一般临床资料Tab.1 General clinical data of STEMI patients between β-HB normal and elevation groups
2.2 β-HB正常组和升高组STEMI患者的Kaplan-Meier生存分析
所有STEMI患者随访时间0~3年、平均(2.7±0.7)年,β-HB正常组和升高组患者中发生心源性死亡分别为12例(6.3%)和19例(20.4%);Kaplan-Meier生存分析显示(图1),β-HB正常组STEMI患者的3年累积生存率明显高于β-HB升高组,差异有高度统计学意义(P<0.001)。

图1 STEMI患者的Kaplan-Meier生存曲线Fig.1 Kaplan-Meier survival curves of STEMI patients
2.3 STEMI患者的Cox回归分析
STEMI患者生存资料的Cox回归分析结果显示(表2),女性、高血压、急诊血运重建、LVEF、估算肾小球滤过率及血浆β-HB与STEMI患者的心源性死亡相关(P<0.05);血浆β-HB升高均明显增加全体STEMI患者(P=0.029)和无糖尿病亚组患者的心源性死亡风险(P<0.001),提示血浆β-HB升高是STEMI患者心源性死亡的独立危险因素;此外,糖尿病亚组患者中未发现血浆β-HB与心源性死亡风险相关(P=0.594)。

表2 糖尿病组和无糖尿病组STEMI患者发生心源性死亡危险因素的Cox回归分析Tab.2 Cox regression analysis of risk factors for cardiac death in STEMI patients between diabetic and no diabetic groups
3 讨论
本研究Cox回归分析结果表明,β-HB可增加STEMI患者的心源性死亡风险,但其中糖尿病STEMI患者预后差且更易出现β-HB升高。为排除糖尿病对β-HB和心源性死亡相关性的影响,本研究进一步分析得出β-HB和无糖尿病亚组的心源性死亡相关,提示血浆β-HB升高是STEMI患者心源性死亡的独立危险因素。因糖尿病亚组样本量太少检验效能不足,尚不能认为β-HB和糖尿病亚组患者的心源性死亡无相关性。
本研究结果与既往临床研究一致,血浆β-HB水平是心血管疾病预后不良的预测因素。血浆β-HB升高可预测心律失常性心肌病先证者的心血管事件及其临床无症状亲属的疾病进展[12],与心衰患者的心血管事件和心源性死亡密切相关[6,13]。推测可能机制为:(1)血浆β-HB升高是心肌缺血缺氧的一种机体代偿表现,血浆β-HB越高提示心肌缺血缺氧越严重、心功能越差[8];(2)血浆酮体和脂肪酸浓度升高与慢性心功能不全的严重程度相关[5];(3)心肌细胞主要利用β-HB供能的过程中会造成三羧酸循环中间物质的匮乏,可能加剧心脏的收缩功能障碍[14];(4)酮体在血浆和细胞中堆积过多可能引起酸中毒,即使是轻度的酸中毒也可显著降低心肌细胞收缩力[15];(5)β-HB可阻断心室肌细胞瞬时K+外流,延长复极时程、增加复极离散度,可能促进恶性心律失常发生[16]。
与本研究结果不同的是,在动物实验中β-HB参与了抗炎或促炎、内质网应激等病理生理过程的调控,具有潜在的心血管保护作用[17]。通过低碳水饮食或药物促进血酮体生成可以减轻小鼠心肌缺血再灌注损伤并降低死亡率[18-20],外源性补充β-HB能显著改善心肌损伤后后心室重构并预防心衰发生[21-22]。条件性剔除心肌细胞酮体代谢相关基因的小鼠在心衰模型下表现为早发心力衰竭并加速恶化[23-24]。因此,β-HB对心血管疾病的潜在作用及其机制尚存在争议,利用酮体代谢及机制来治疗心血管疾病仍需要更多的研究进行验证。
本研究有以下局限性。首先,单中心回顾性研究难以避免样本量较小及研究偏倚的问题;其次,未能动态检测血浆β-HB水平,患者起病时间和空腹状态可能影响血浆β-HB值;再次,少数患者入院时可能漏诊2型糖尿病,从而可能影响非糖尿病亚组分析结果;最后,未检测肝脏酮体生成和心肌酮体代谢水平,不能分析β-HB在心肌中的直接作用。
综上所述,血浆β-HB是STEMI患者心源性死亡的独立危险因素,阐明β-HB在心血管疾病中的作用和机制将为改善患者预后发掘更多有效的治疗措施。
