液相色谱-串联质谱法测定猪肉中恩诺沙星残留量的不确定度评定
2022-07-14孟千军赛丽诺
孟千军 赛丽诺 刘 玉
潍坊市检验检测中心 山东潍坊 260000
畜牧养殖业的发展与各类抗生素药物的使用息息相关,这些抗生素药物广泛用于畜牧养殖时的预防或疾病治疗,以保证产量增加,并降低成本。这些药物中喹诺酮类的抗真菌药物(Antifungal Drugs)是应用非常广泛、重要的一类药物,以抑制细菌的DNA回旋酶为机理,抗菌作用强大,抗菌谱较广,广泛应用于畜牧养殖行业。研究表明[1~4],喹诺酮类抗真菌药物不是完全安全的,养殖者或生产企业没有严格遵守停药期宰杀或者滥用药物会导致药物及其代谢物残留超标,会对人体的健康产生不良影响,增加消费者的潜在食品安全风险[5]。而在日常的食品监督抽检中,喹诺酮类恩诺沙星药物残留被检出的几率非常大,经常会出现是否合格的临界值判定情况,这也成为畜肉食用安全关注的焦点之一。2021年9月实施的GB 31650-2021《食品安全国家标准 食品中农药最大残留限量》[6]中明确规定了恩诺沙星的限量要求,为了保证畜肉食用安全,灵敏、准确的药物残留检测技术必不可少,而在检测结果与规定合格限值接近时,需要给出测量结果的可信程度,以明确样品是否存在食品安全风险。
在恩诺沙星等药物残留的检验检测工作中,标准溶液的配制、样品称取以及样品净化过程等方面,都会使检验检测结果产生一定的不确定性。由于检测过程不可避免地存在不确定度,当不确定度越小,检测结果可信度越高;反之越低[7~12]。不确定度数值的大小反映了检验检测结果可信度高低,代表检验检测值的可信区间,若检验检测结果刚好在限量值附近,会直接与产品的合格判定相关,对提高检验检测结果的质量、降低误判风险具有重要意义[12~15]。
本研究分别采用国家标准GB 31658.17-2021 《食品安全国家标准 动物性食品中四环素类、磺胺类和喹诺酮类药物残留量的测定 液相色谱-串联质谱法》[16]方法,定量检测畜肉中恩诺沙星药物残留量,依据 JJF 1135-2005《化学分析测量不确定度评定》[17]和 JJF 1059.1-2012《测量不确定度评定与表示》[18],评定猪肉中以恩诺沙星为代表的喹诺酮类药物残留量的不确定度,分析检验检测结果的可靠性[19]。
1 材料与方法
1.1 材料、试剂与仪器
猪肉样品:空白基质,购于当地的超市;阳性样品,实验室制备。
液相色谱三重四级杆质谱联用仪Xevo TQ-S,美国沃特世公司;
分析天平MS2204TS,梅特勒-托利多;
涡旋混合器VIBRAX VXR,德国IKA公司;
氮吹仪N-EVAP,美国Organomation公司;
冷冻离心机ST16R,赛默飞世尔公司;
固相萃取装置,美国沃特世公司;
乙腈、甲醇、乙酸乙酯、甲酸色谱纯,德国默克;
乙二胺四乙酸二钠、浓氨水、磷酸氢二钠、磷酸二氢钠、柠檬酸、氢氧化钠分析纯,国药集团;
固相萃取柱HLB,美国沃特世公司;
恩诺沙星标准品,浓度100mg/mL,农业部环保科研监测所。
1.2 方法
1.2.1 标准品的配制
1.2.1.1 标准储备液的配制
依次吸取的恩诺沙星标准品溶液1mL于10、100mL容量瓶中,用甲醇溶液稀释到刻度,得到0.1μg/mL标准储备液。
1.2.1.2 基质匹配标准工作溶液配制
准确吸取适量的标准储备液,分别加入按经提取和净化等相应的前处理方法制得的6份的空白试样残渣中,加入复溶液定容1mL,依次配制成2、10、50、100、250、500μg/L的基质匹配系列的标准工作液,经0.22μm滤膜过滤后,待液相色谱-串联质谱测定。
1.2.2 样品前处理
按照GB 31658.17-2021的要求,取称取样品1.00g,加EDTA缓冲液8mL,匀浆,超声20min,-2℃、10 000r/min离心5min,收集上清液。残渣加磷酸盐缓冲液8mL,重复提取1次,合并2次提取液,混匀后过HLB固相萃取柱,收集洗脱液45℃氮气吹干,加入1.0mL复溶液溶解,过膜,待液相色谱-串联质谱测定。
1.2.3 仪器条件
1.2.3.1 液相色谱条件
方法:色谱柱为C18,柱温为35℃,进样量为1.0μL,流速为0.3mL/min,流动相为0.1%甲酸水溶液+甲醇-乙腈溶液(2+8+0.1%甲酸,体积比)=80+20。
1.2.3.2 质谱条件
离子源为电喷雾离子源,检测方式为多反应监测,扫描方式为正离子扫描,离子源温度为110℃,雾化温度为450℃,电离电压为3.0kV,锥孔气流速为30L/h,雾化气流速为1 000L/h。定性离子对、定量离子对及锥孔电压和碰撞能量,见表1。

表1 定性离子对、定量离子对、锥孔电压和碰撞能量
1.2.4 数学模型的建立
试样中恩诺沙星药物残留含量(X)按公式(1)计算。
(1)
式中:
X,试样中被测恩诺沙星药物残留含量(μg/kg);
CS,基质匹配标准溶液中恩诺沙星药物浓度数值(μg/L);
A,试样溶液中恩诺沙星药物的色谱峰面积;
AS,基质匹配标准溶液中恩诺沙星药物的色谱峰面积;
V,试样最终定容体积(mL);
m,试样质量(g)。
本方法标准工作曲线由最小二乘法进行线性拟合而成,外标法定量。
2 结果分析
2.1 测量不确定度的来源分析
多元素回归分析本检验检测过程中标准溶液配制、试样称量、体积量取、重复性、回收率等影响不确定度的相关因素,存在因果关系,为不确定度的分量来源。
2.2 测量不确定度的评定
2.2.1 标准溶液的配制引入不确定度u(C)
2.2.1.1 储备液的配制过程引入的不确定度u(C1)
由标准品证书可知,恩诺沙星标准溶液相对不确定度均为urel(C1)=0.0400。
2.2.1.2 标准溶液配制引入的不确定度u(C2)
分别用1mL单标线移液管依次移取1.0mL、100μg/mL恩诺沙星标准液于100mL、10mL容量瓶中,甲醇定容至刻度,摇匀,得到恩诺沙星为0.1μg/mL的标准储备溶液。按照矩形分布处理,数据参考JJG 196-2006《常用玻璃量器》[20]和GB/T 12806-2011《实验室玻璃仪器 单标线容量瓶》的要求[21],按照A类不确定度评定,移液管、容量瓶及其温度波动引入的不确定度、储备液稀释过程中引入的相对标准不确定度结果见表2所示。
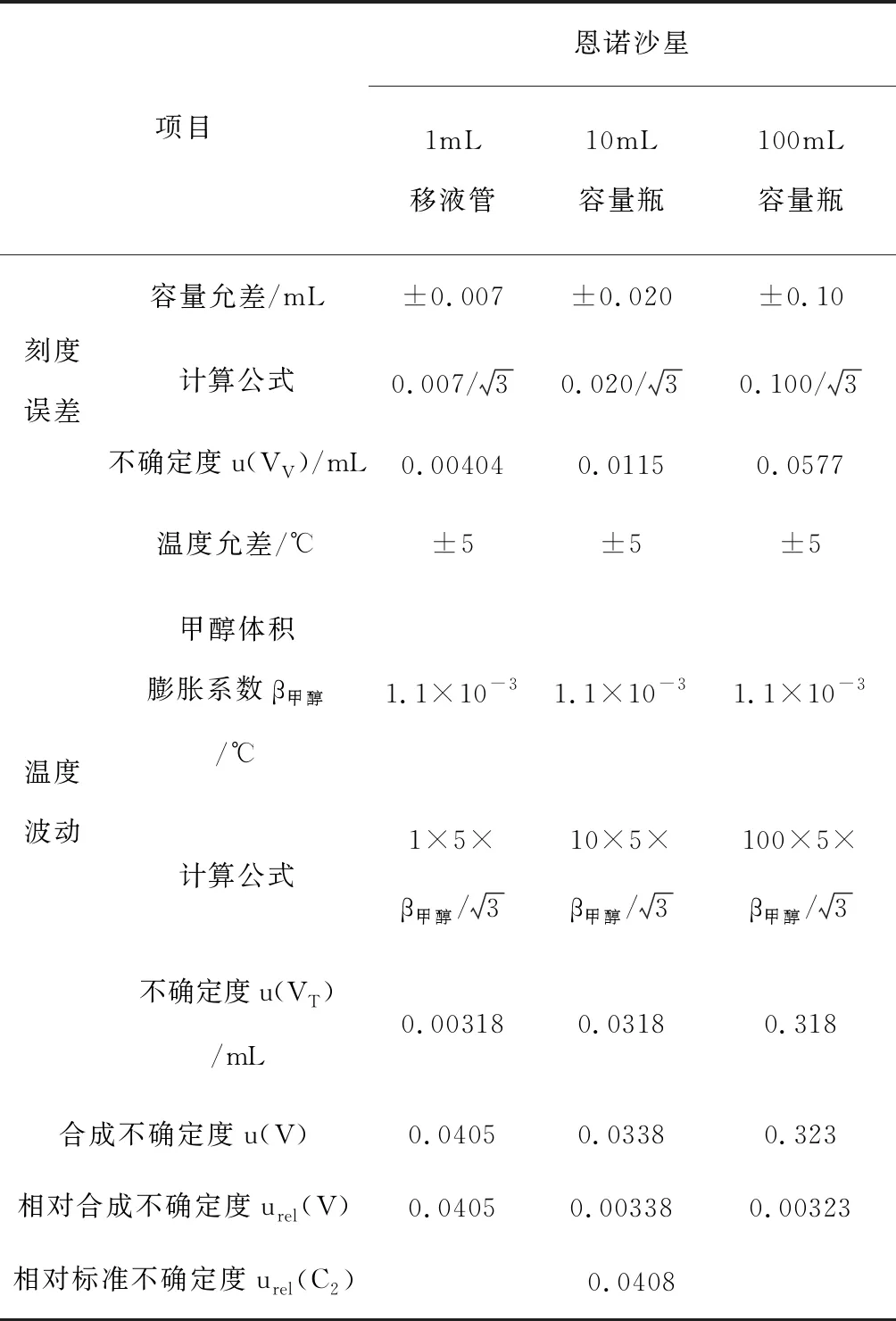
表2 标准储备液稀释过程中引入的不确定度
2.2.1.3 基质标准溶液配制过程产生的不确定度u(C3)
使用20、100、250、1 000μL移液器分别移取2、10、50、100、250、500μL标准储备溶液于空白基质残渣中,定容至1mL,得到浓度分别为2、10、50、100、250、500ug/L的基质匹配标准系列工作溶液。移液管的刻度误差参考JJG 646-2006《移液器检定规程》的要求[22],按A类不确定度评定。猪肉空白基质匹配标准系列溶液配制过程引入的相对标准不确定度的结果详见表3所示。
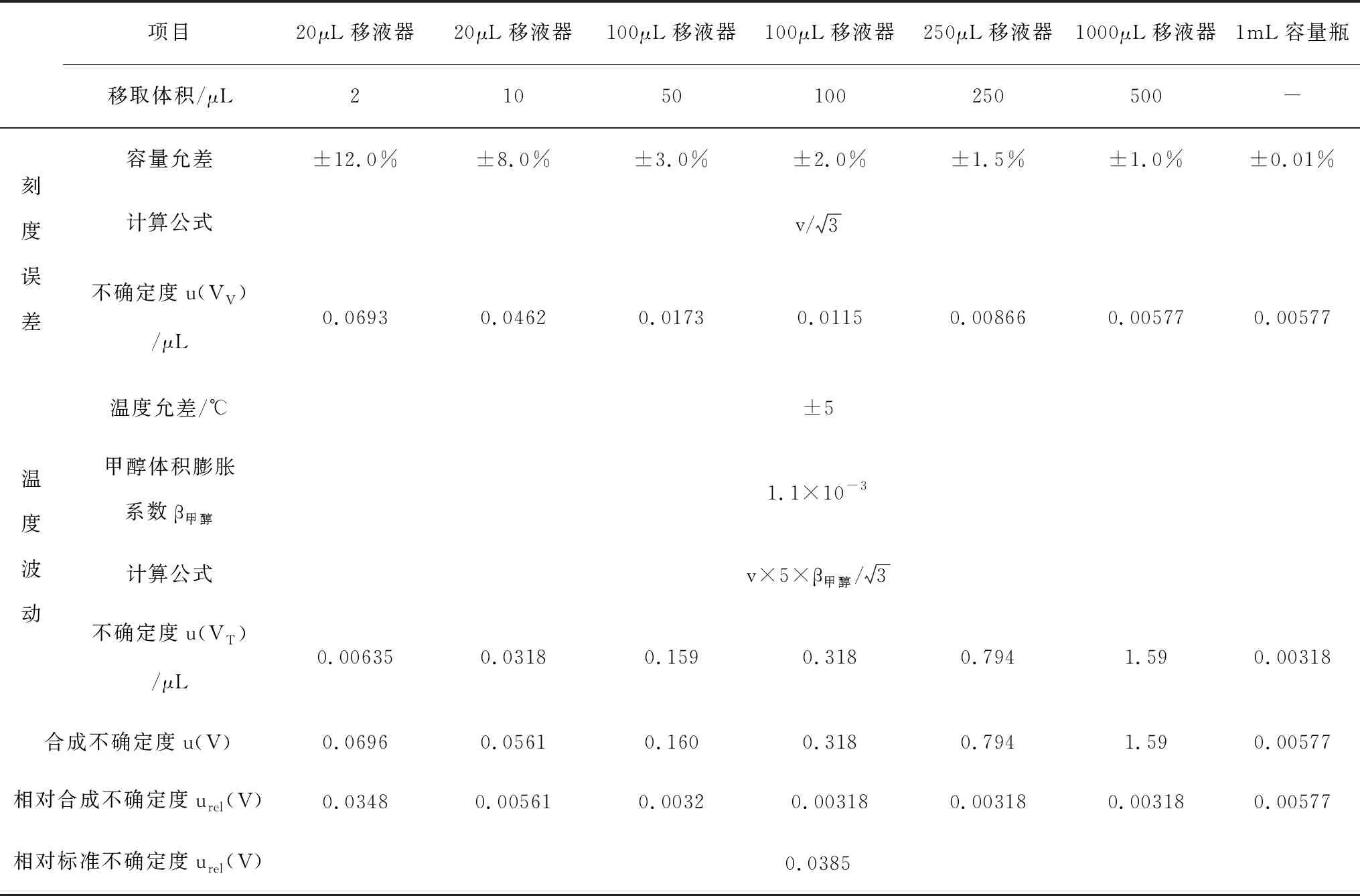
表3 基质匹配标准系列溶液配制过程中引入的不确定度
2.2.2 试样称量产生的不确定度u(m)
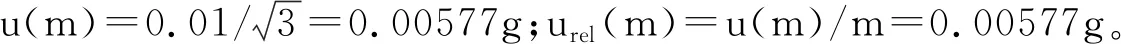
2.2.3 体积量取产生的测量不确定度u(V)
2.2.3.1 提取液体积产生的不确定度u(V1)
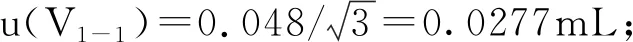
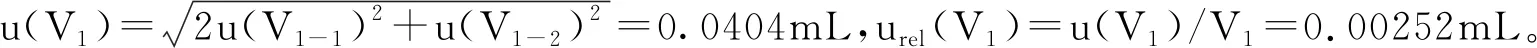
2.2.3.2 最终定容体积引入的不确定度u(V2)
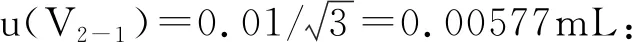
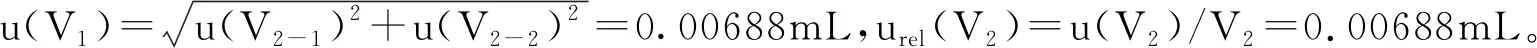
2.2.4 标准曲线拟合产生的不确定度u(X)
将6种不同浓度的猪肉空白基质匹配的标准系列溶液,各取1.0μL分别重复3次进仪器测定,以标准溶液的浓度作为横坐标(C),峰面积作为纵坐标(A),采用最小二乘法拟合而成的线性回归方程则为A=aC+b,检验检测数据及计算结果如表4所示。取一猪肉阳性样品,经样品提取、净化、浓缩后3次重复进仪器测定测定,其结果见表5,则由标准曲线拟合产生的不确定度按(2)式计算。
(2)
式中:
SR为基质匹配标准溶液待测物峰面积残差的标准差,详见公式(3);
a为斜率;
b为截距;
nY为对样品溶液CY的测定次数,nY=3;
nS为标准溶液测试次数,本实验中6个基质匹配质量浓度重复测定3次,nS=6×3=18;
Ai为标准溶液各点的待测物的峰面积;
Ci为标准溶液各点的待测物的质量浓度;
CY为校准方程求得的阳性样品溶液中待测物的质量浓度;
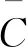
其中:
(3)
(4)
基质匹配标准曲线结果、阳性样品的结果、曲线拟合引入的不确定度相关量urel(X)=u(X)/C0,结果见表4、表5、表6。
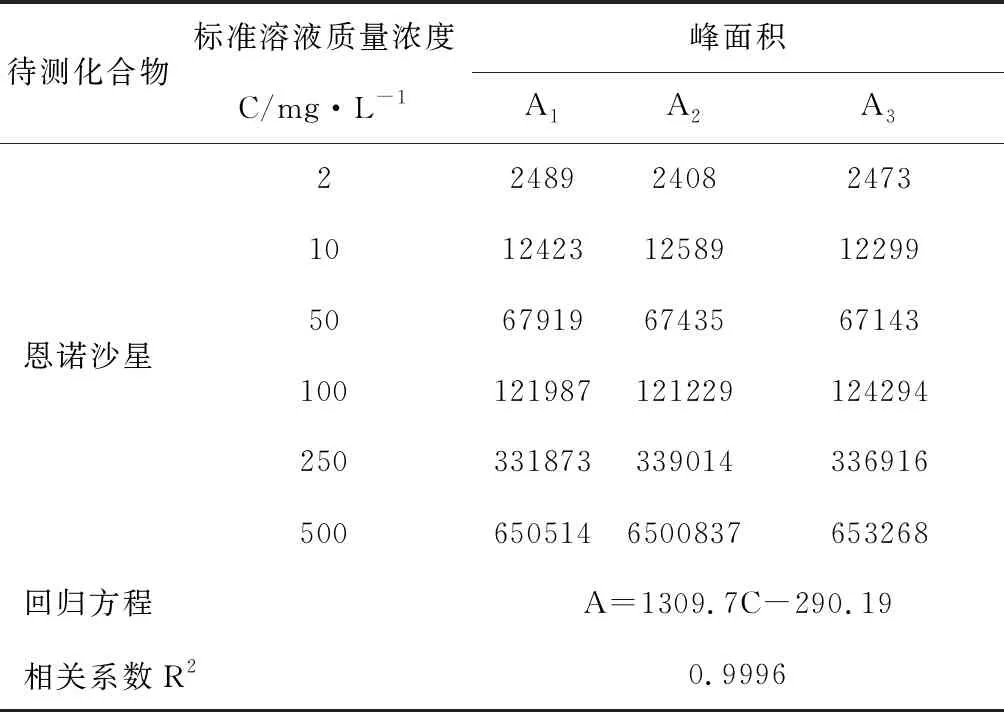
表4 基质匹配标准曲线结果表
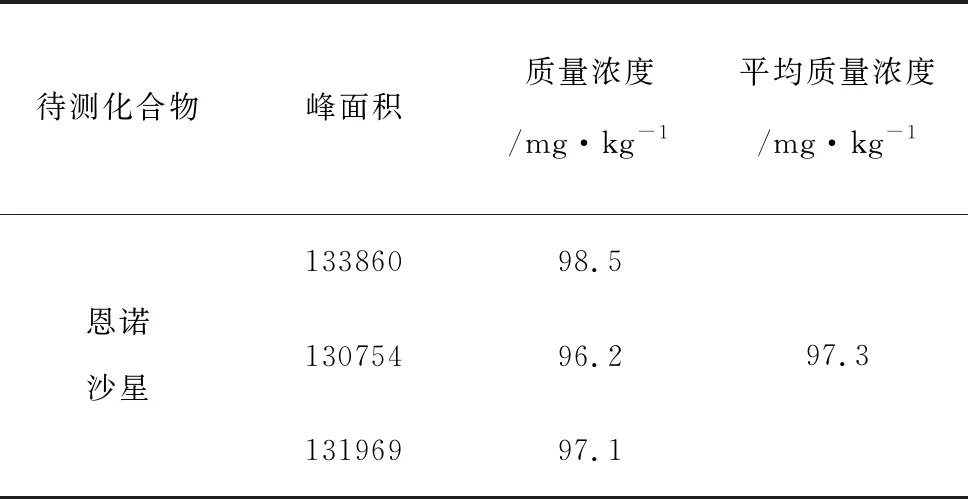
表5 阳性样品的结果

表6 曲线拟合引入的不确定度相关量
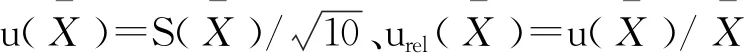
2.2.6 回收率产生的不确定度u(R)
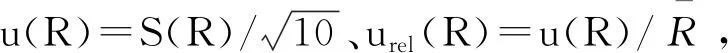

表7 猪肉中恩诺沙星的重复性和回收率测定结果
2.3 合成不确定度
猪肉中恩诺沙星的相对不确定度分量见图1所示,若不考虑各不确定度的相关性,则其合成不确定度按公式(5)计算,结果详见表8。
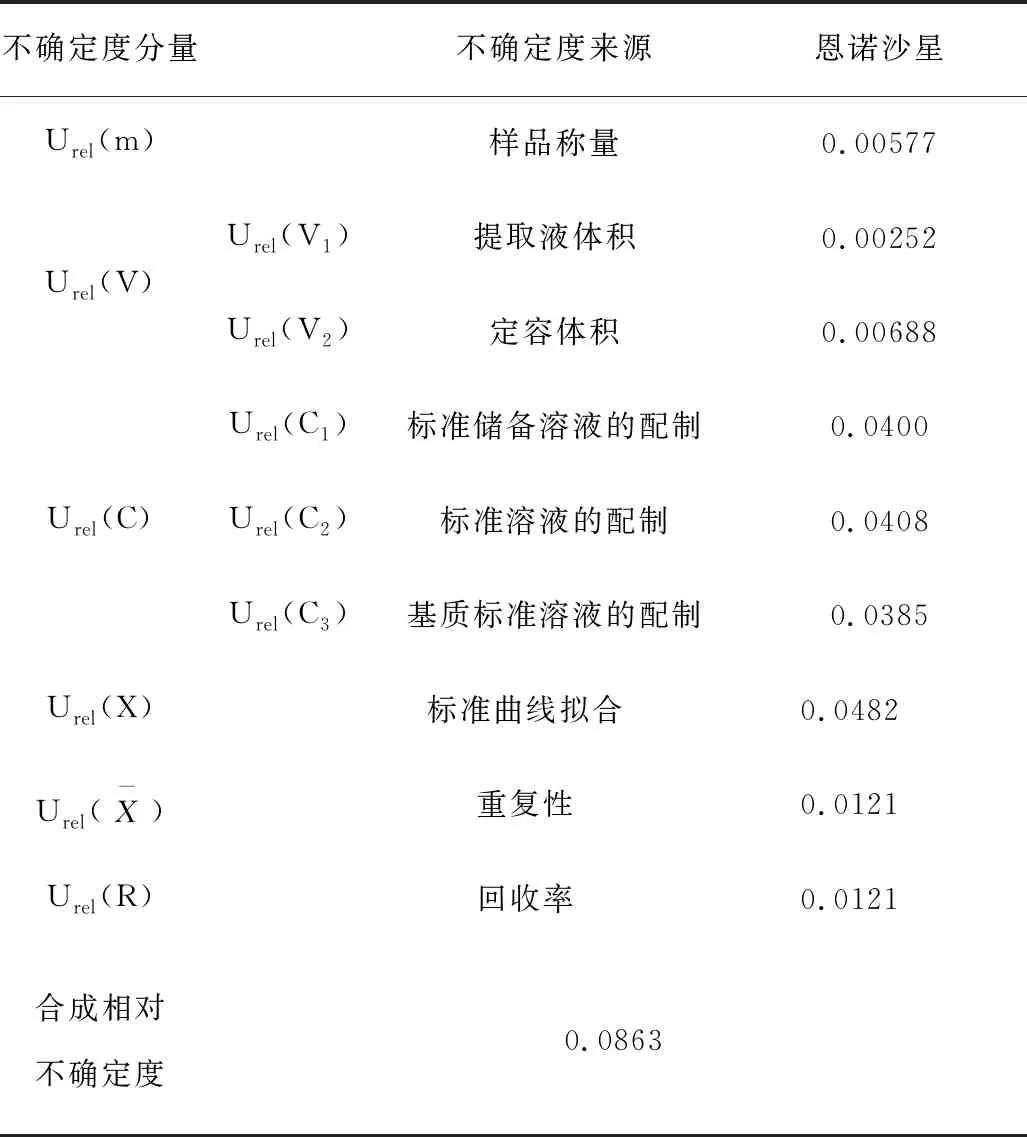
表8 恩诺沙星测定不确定度分量
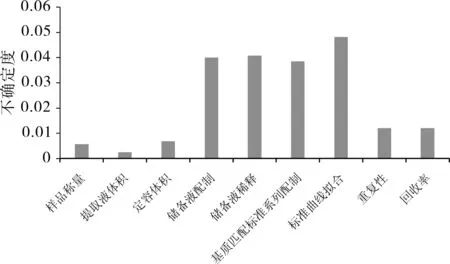
图1 恩诺沙星测定不确定度分量图
Urel=
(5)
2.4 扩展不确定度及结果表示
依据CNAS-GL006:2018《化学分析中不确定度的评估指南》[22],在95%置信区间,选择包含因子k=2,则扩展不确定度U=urel(X)×2×X,计算猪肉中恩诺沙星药物残留测定的不确定度,评定结果详见表9。

表9 恩诺沙星测定不确定度评定结果
3 结论
从猪肉中恩诺沙星药物残留的测量不确定度评定过程可知,检验检测实验的样品提取、净化、液相质谱测定、结果拟合分析等过程都会引入相应的不确定度分量。通过对猪肉中恩诺沙星检测过程中样品称量、标准溶液的稀释、猪肉空白基质标准溶液的配制、温度波动、重复性、回收率等因素进行综合考查分析,结果表明,当猪肉中恩诺沙星含量为97.4μg/kg时,其扩展不确定度为16.8μg/kg(k=2)。猪肉恩诺沙星检测过程中引入的较显著不确定度是标准储备溶液的配制、标准溶液的稀释、基质标准溶液的配制和标准曲线拟合,不确定度分别为0.0400、0.0408、0.0385、0.0482,而其他分量引入的不确定度对结果影响较小。因此,在日常的检验检测操作过程中,需重点关注移液管和移液枪的检定和体积校准,提高液质检测仪器的稳定性,选择合适的标准曲线浓度点范围,获得更好的拟合结果,最大程度减小测量的不确定度,从而确保检测结果的有效性,为食品安全提供精准的技术保障。
