心率减速力变化对老年稳定性冠心病患者长期预后的影响
2022-07-11高燕钟萍张长青
高燕,钟萍,张长青
1 中国人民解放军联勤保障部队第九六〇医院全科医学科,济南 250031;2 中国人民解放军联勤保障部队第九六〇医院卫勤部住培办;3 济南市天桥人民医院全科医学科
据《中国心血管健康与疾病报告2019》推算,我国冠心病患者有1 100万例,冠心病已成为城乡居民致残、致死的主要原因之一[1]。随着我国冠心病二级预防的逐步普及和深入,急性冠状动脉综合征(ACS)在冠心病就诊人群中的比例正逐年下降,稳定性冠心病(SCAD)比例升高,其临床诊治更加重要[2]。SCAD 包括慢性稳定性劳力型心绞痛、缺血性心肌病和ACS 之后稳定的病程阶段。SCAD 的诊断主要依据临床症状、冠心病危险因素和辅助检查,通过胸痛性质、性别和年龄3 个因素,综合推断SCAD的验前概率(PTP),PTP≥85%可确诊SCAD。SCAD的治疗主要是缓解症状,延缓或阻止冠状动脉病变进展,减少冠状动脉事件的发生[3]。目前我国尚无关于SCAD发病率、患病率和病死率的数据[4]。心率减速力(DC)作为一项预测心脏自主神经功能的指标,不仅在心肌梗死及心力衰竭患者中对预后有很强的预警作用,而且对晕厥、急性脑卒中等疾病的预后以及不同海拔环境对心脏的影响中均有很好的预测作用[5-8]。但是DC 对老年SCAD 患者长期预后的影响仍不明确。本研究用住院SCAD 患者的队列数据,探讨DC 变化对老年SCAD 患者长期预后的影响。
1 资料与方法
1.1 临床资料 选择2015 年1 月—2016 年1 月在中国人民解放军联勤保障部队第九六〇医院住院的SCAD患者116例。其中男111例、女5例,年龄74.5(69.0,86.0)岁。SCAD 诊断标准参照我国2007 年慢性稳定型心绞痛诊断与治疗指南[9]与2018 年SCAD 诊断与治疗指南[3]。纳入标准:年龄≥60 岁;有基线动态心电图结果且有完整的DC 数据;截至2022 年3 月31 日有完整的终点事件记录。排除标准:有恶性肿瘤病史;合并心房颤动;不能获取后期临床资料。随访(5.59±1.84)年,共发生全因死亡23例(死亡组)、存活93例(存活组)。本研究遵守赫尔辛基宣言原则,并通过中国人民解放军联勤保障部队第九六〇医院伦理委员会审核批准[2022 科研伦理审第(28)号],申请免知情同意。
1.2 资料收集 通过数字病历系统收集患者的临床资料,包括性别、年龄、合并疾病、合并用药[抗血小板药物、硝酸酯类药物、β 受体阻滞剂、血管紧张素转化酶抑制剂(ACEI)、血管紧张素受体阻滞剂(ARB)、他汀类药物(statins)]及血清同型半胱氨酸(HCY)、TC、TG、LDL-C及HDL-C。吸烟定义为每天≥1支,持续1年以上;高血压、糖尿病及高脂血症的诊断依据病历系统中记录的入院或出院诊断。
1.3 DC检测 应用美国DMS公司的动态心电图仪,对SCAD患者进行24 h动态心电图监测,经自动分析系统计算DC值。当DC<4.5 ms时,表示指标异常[10-11]。参考文献[11],根据DC将患者分为3组:DC<2.6 ms组17例、DC 2.6~4.5 ms组34例、DC>4.5 ms组65例。
1.4 随访 以观察对象在2015 年1 月1 日—2016年1 月1 日住院期间行第一次动态心电图检查为随访起点,以全因死亡或心血管死亡或至随访结束(2022 年3 月31 日)为随访终点。数据统计由经过培训的医务人员双人独立完成,对终点事件进行重复核实确认。主要终点事件为随访期内的全因死亡和心血管死亡。随访事件依据患者每年在查体信息或住院信息。
1.5 统计学方法 采用SPSS21.0 统计软件及风锐统计1.5软件。符合正态分布的计量资料以±s表示,两组比较采用t检验;非正态分布计量资料以M(P25,P75)表示,两组间比较采用Wilcoxon 秩和检验。计数资料比较采用χ2检验。用Cox 回归模型分析DC 与SCAD 全因死亡的关系,将DC 值以连续性变量带入Cox模型,分析DC每增加1 ms发生全因死亡的HR值(95%CI);将DC 值按分组变量纳入Cox 模型,以DC>4.5 ms 组作为参照组,计算DC<2.6 ms组、DC 2.6~4.5 ms 组全因死亡风险的HR值(95%CI);根据年龄、糖尿病及β 受体阻滞剂使用进行分层亚组分析,计算各分层全因死亡的HR值(95%CI)。P<0.05为差异有统计学意义。
2 结果
2.1 死亡组与存活组临床资料比较 死亡组年龄、糖尿病患者比例、抗血小板药物和硝酸酯类药物使用比例及DC 与存活组比较差异均有统计学意义(P均<0.05);两组其他资料比较差异无统计学意义(P均>0.05)。见表1。
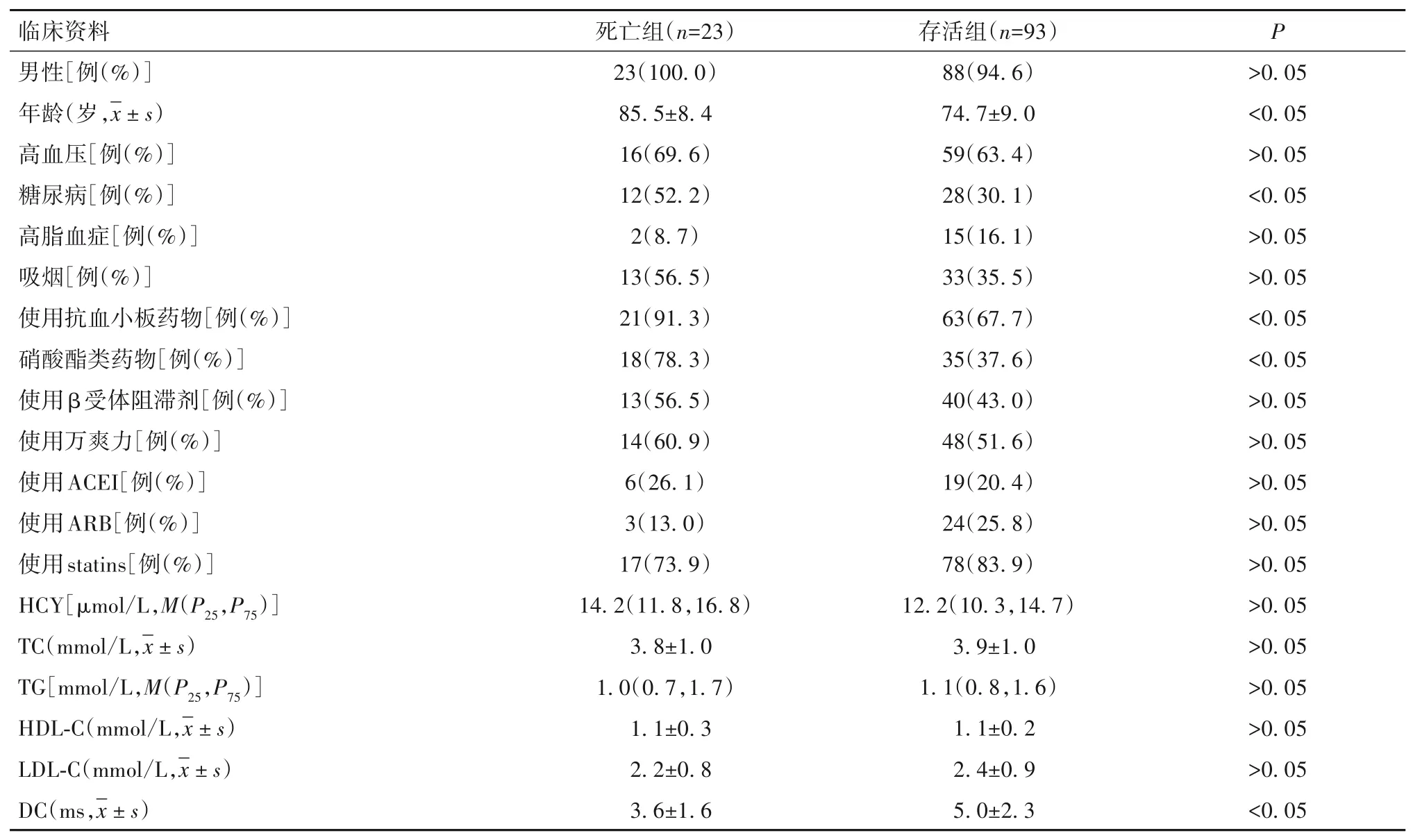
表1 死亡组与存活组临床资料比较
2.2 DC 与SCAD 全因死亡的关系 将DC(以连续性变量的形式)作为自变量,全因死亡为因变量,进行Cox 风险回归分析。协变量的入选依据为Cox 单因素分析对结局有影响或加入该变量后回归效应值变化>10%,最终纳入以下变量:年龄、高血压、高脂血症、硝酸酯类药物、抗血小板药物、他汀类药物和LDL-C(因纳入糖尿病、β受体阻滞剂后模型不稳定,将二者纳入分层分析,同时进行交互作用检验)。结果显示,DC、年龄是全因死亡的影响因素。见表2。

表2 冠心病患者全因死亡的Cox风险回归分析
2.3 不同DC 水平对各类SCAD 校正模型患者全因死亡风险的影响 模型1 校正年龄后,DC 作为连续变量,每增加1个单位,全因死亡风险降低26%(HR=0.74,95%CI:0.58~0.94);而DC 作为分组变量后,DC 2.6~4.5 ms 组及DC<2.6 ms 组的全因死亡风险分别是DC>4.5 ms 组的2.83、3.52 倍。模型2 在模型1 的基础上进一步校正高血压和高脂血症,DC 作为连续变量和分组变量效应值的变化趋势与模型1一致。模型3 在模型2 基础上校正了LDL-C 和他汀类药物,DC 作为连续变量,每增加1 个单位,全因死亡风险降低25%(HR=0.75,95%CI:0.58~0.96),与DC>4.5 ms 组相比,DC 2.6~4.5 ms 组及DC<2.6 ms组全因死亡风险分别增加2.03、2.30倍。见表3。
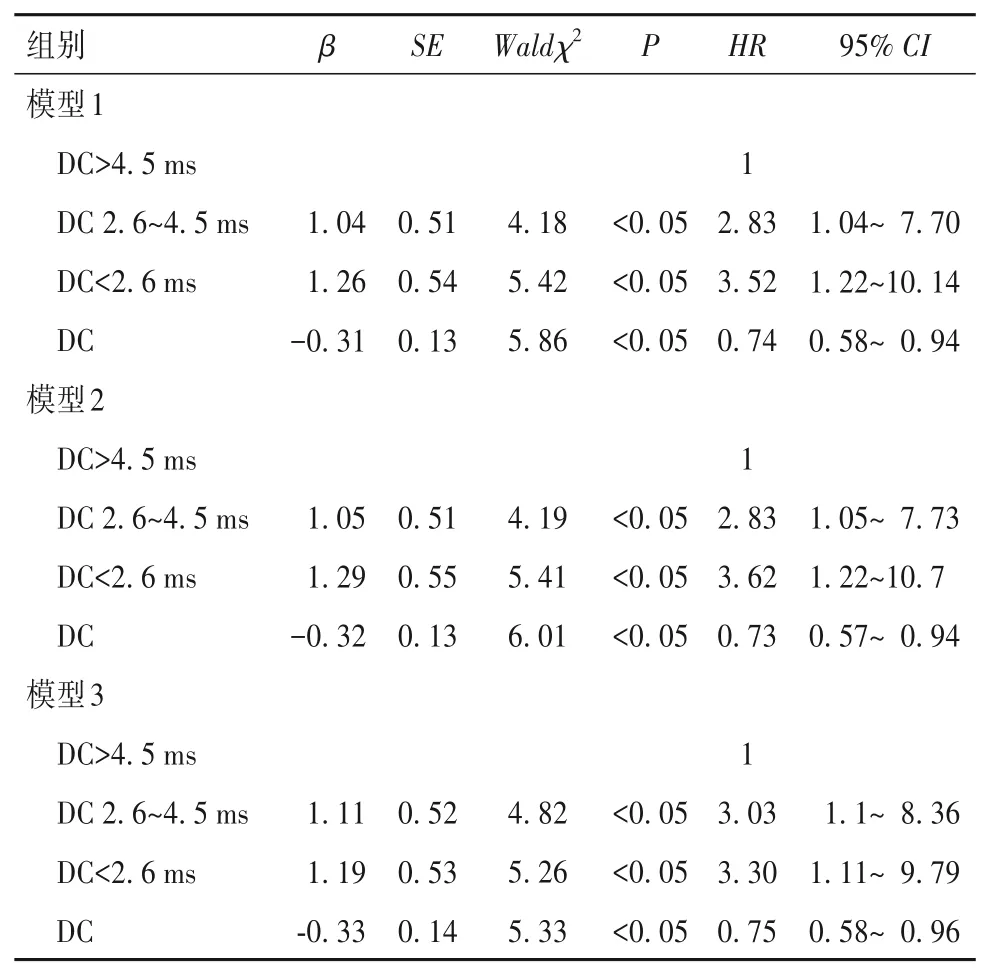
表3 不同DC对全因死亡事件影响的Cox比例风险回归模型
2.4 DC 与SCAD 患者全因死亡风险关联分析的亚组及交互作用分析 以DC 连续变量为自变量,全因死亡为因变量,以模型3 纳入的校正变量为混杂因素,包括年龄、高血压、高脂血症和LDL-C及他汀。分层变量为年龄(按80岁分层)、是否有糖尿病及是否应用他汀,进行Cox 多因素分层回归分析。当对年龄进行分层分析时,校正混杂因素中的年龄不纳入分析。结果显示,在这三个分层因素中,随着DC的增加,全因死亡风险下降的趋势不变。交互作用分析显示,年龄、2 型糖尿病和β 受体阻滞剂与DC在SCAD 患者全因死亡风险的分析中均不存在交互作用。
3 讨论
DC是通过位相整序信号平均技术,利用数学方法,对心动周期中的调节痕迹进行提取,将每次细微的心率调节数字化,近似定量地评估迷走神经张力及功能受损程度[11]。研究证实,DC是心肌梗死后和心力衰竭患者不良预后的重要预测因子[12-14]。BAUER等[12]在慕尼黑开展了一项心肌梗死后队列研究,该研究通过分析1 455 例患者的24 h 的Holter 记录,探讨DC 对心肌梗死后全因死亡的预测价值,结果显示,心率减速能力受损是心肌梗死后全因死亡风险的预测因素,比LVEF 和传统的心率变异性更准确。这一研究结果在另外两组即英国伦敦(n=656)和芬兰奥卢(n=600)心肌梗死患者中也得到验证。LIU等[13]研究发现,在LVEF≥35%的心肌梗死患者中,心率变异性降低、24 h内所有正常RR间期的标准差减低以及DC 降低均与突发心律失常的风险增加独立相关。另外,DC可预测心力衰竭患者的心律失常和总病死率[14]。DC对很多疾病预后有预测价值,但具体机制尚不明确[6,15]。DUCKHEIM 等[6]研究发现,DC是晕厥患者180 d内死亡的危险因素,借助DC可以识别高风险的晕厥患者。另外,该研究团队还用DC 对88 例急性缺血性卒中患者进行快速风险分层,结果显示DC 可用于缺血性卒中患者的客观和独立风险分层。阵发性心房颤动患者的低心率减速能力与较高的卒中风险有关[15]。DC 的下降还可作为特发性帕金森病的早期心脏自主功能障碍的标志物[16]。
张丽娜等[17]研究发现,糖尿病心脏自主神经病变发病率高,而年龄是糖尿病自主神经病变的独立危险因素。β 受体阻滞剂抑制交感神经系统的激活,降低心肌耗氧量,是改善SCAD 预后的重要药物。鉴于年龄、糖尿病和β 受体阻滞剂是影响自主神经功能的三个重要因素,把这三个因素纳入分层分析。本研究发现,年龄是SCAD 患者全因死亡的独立危险因素。以80岁为界,把年龄进行COX分层分析也发现,无论在≥80 岁组还是<80岁组,随着DC值的升高,全因死亡风险均下降。在无论是否合并糖尿病及是否应用β 受体阻滞剂的分层分析中,同样发现随着DC 的升高,全因死亡风险下降。交互作用检验结果发现上述三个变量在DC 与全因死亡的关联分析中不存在交互作用,提示在上述人群中研究结果是稳定的。本研究随访时间长达(5.59±1.84)年,以基线DC 水平作为连续变量分析,结果显示,DC 降低是SCAD 患者全因死亡的危险因素。经过校正年龄、高血压、高脂血症及LDL-C、他汀后,DC 作为连续变量,每增加1 个单位,全因死亡风险降低25%;进一步进行模型校正发现,与DC>4.5 ms组相比,DC=2.6~4.5 ms 组及DC<2.6 ms 组全因死亡风险分别增加2.03、2.30 倍。提示临床对DC<2.6 ms 的SCAD 患者应高度重视。本研究是基于住院SCAD 人群开展的队列研究,发现DC 的降低与SCAD 患者的全因死亡风险增加相关,DC<2.6 ms组及DC 2.6~4.5 ms 组患者的死亡风险均高于DC>4.5 ms 患者,校正多种混杂因素后结论一致,提示DC下降为SCAD患者全因死亡的危险因素。
综上所述,DC 受损为SCAD 患者长期预后不良的独立危险因素,在不同年龄、是否合并糖尿病及是否应用β 受体阻滞剂的患者中,DC 对SCAD 患者预后的影响趋势稳定。本研究有以下局限性:单中心研究,样本量偏小,我们发现DC 受损与SCAD 全因死亡相关,但在心血管死亡终点事件评估上未发现阳性结果,仍需扩大样本量,进一步研究验证。
