甲磺酸阿帕替尼在晚期消化系统恶性肿瘤中的疗效与安全性
2020-04-07施秀华王银华
叶 斌,张 玲,胡 俊,刘 飞,施秀华,王银华
(芜湖市第二人民医院 肿瘤科,安徽 芜湖 241000)
化疗是治疗晚期消化系统肿瘤的重要手段之一,但由于化疗药物的不良反应及耐药性,导致其在晚期肿瘤中治疗效果不是很好。由于恶性肿瘤细胞增殖和迁移的关键在于血管生成,如何采取有效的药物抑制血管生成对改善患者预后具有重要的意义。甲磺酸阿帕替尼(mesylate apatinib)是一种新型的口服制剂,由我国自主研发,能抑制肿瘤血管生成,切断肿瘤所需的营养,抑制、杀死恶性肿瘤[1-2]。阿帕替尼目前已被批准用于晚期胃腺癌的三线治疗。此外,阿帕替尼治疗其他恶性肿瘤的疗效也陆续得到一系列临床研究的证实[3-5],但目前有关阿帕替尼治疗其他晚期消化系统恶性肿瘤疗效及安全性的相关报道较少。因此本文选取了芜湖市第二人民医院收治的晚期恶性消化系统肿瘤患者为对象,探讨阿帕替尼在晚期消化系统恶性肿瘤治疗中的疗效和安全性。
1 资料与方法
1.1 一般资料 分析我院2017年6月~2019年6月收治的24例接受阿帕替尼治疗的晚期消化系统肿瘤患者作为对象,男18例,女6例,年龄41~79岁,平均(56.83±5.77)岁。纳入标准:①均经病理组织检查确诊;②肿瘤分期均为Ⅳ期,且均接受二线及以上化疗;③患者预计生存期>3个月,且患者至少存在1个以上可测量病灶;④所有纳入研究对象均自愿接受阿帕替尼治疗,均签署相关知情同意书。排除标准:①合并凝血异常、精神异常及伴有自身免疫疾病者;②有化疗或分子靶向治疗相关禁忌证的患者;见表1。
表1 24例患者基线资料

临床参数n(%)性别男18(75)女6(25)年龄/岁≤6012(50)>6012(50)ECOG评分0~119(79.2)2分5(20.8)肿瘤原发部位胃癌10(41.7)肝癌5(20.8)肠癌7(29.2)食管癌2(8.3)
1.2 治疗方法 所有患者入院后评估身体状态,给予阿帕替尼单药或联合化疗,其中阿帕替尼单药治疗组14例(58.3%),卡培他滨片联合阿帕替尼治疗组6例(25%),替吉奥联合阿帕替尼治疗组4例(16.7%)。联合化疗组:卡培他滨1.5g,每天2次,21 d为1个周期;替吉奥40 mg,每天2次,21 d为1个周期。对于伴有严重高血压、手足综合征者或无法耐受治疗者,降低阿帕替尼剂量至250 mg/d,以2~4周评价毒性,4~8周评价近期疗效,持续用药至进展或不良反应不能耐受。
1.3 疗效标准及毒副反应 ①疗效率。参考RECIST 1.1标准分别从完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD)对患者近期疗效进行评估。客观缓解率(objective response rate,ORR)=CR率+PR率。疾病控制率(disease control rate,DCR)=CR率+PR率+SD率。②毒副反应。参考NCI CTC4.0版标准从0~4级对患者毒副反应进行评估。
1.4 随访 利用电话随访方式对患者进行随访,随访时间到2019年6月30日。所有患者随访期间均无失访。

2 结果
2.1 治疗耐受性分析 24例患者中2例无法耐受药物毒副反应,未达到8周疗效评估时间,其余患者均遵医完成治疗。
2.2 近期疗效 治疗4周后24例患者均可评价疗效,无CR病例,PR 6例、SD 15例、PD 3例,ORR为25%(6/24),DCR为87.5%(21/24)。4周后疾病进展的3例患者更换治疗方案,治疗8周后22例可评价疗效的患者中,获PR 4例、SD 12例、PD 6例,RR为18.2%(4/22),DCR为72.7%(16/22),见表2。阿帕替尼单药治疗和联合化疗4周和8周后疗效的差异无统计学意义(P>0.05),见表2。
表2 24例恶性消化系统肿瘤患者近期疗效评价
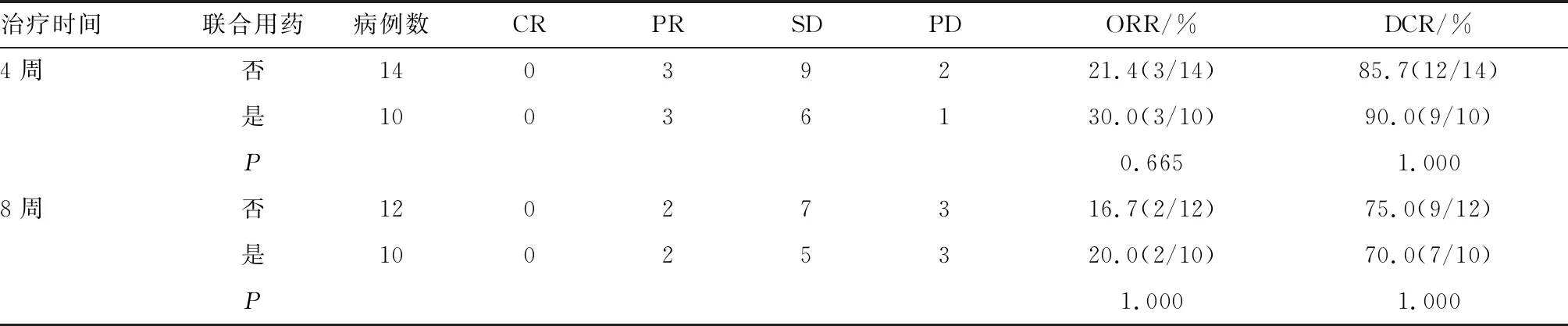
治疗时间联合用药病例数CRPRSDPDORR/%DCR/%4周否14039221.4(3/14)85.7(12/14)是10036130.0(3/10)90.0(9/10)P0.6651.0008周否12027316.7(2/12)75.0(9/12)是10025320.0(2/10)70.0(7/10)P1.0001.000
注:Fisher确切概率法。
2.3 远期疗效 所有患者中位随访时间为10个月,表明:24例患者的中位无进展生存期(PFS)为3.5个月(95%CI:2.44~4.56)。患者PFS与性别、年龄、肿瘤原发部位、是否联合化疗无统计学意义(P>0.05)。见图1和表3。

图1 入组患者PFS曲线
2.4 安全性分析 阿帕替尼单药或联合化疗组中高血压及手足综合征的发生率较高,分别为7例(29.2%)和4例(16.7%),蛋白尿3例(12.5%),乏力2例(8.3%),腹泻2例(8.3%),骨髓抑制3例(12.5%)。发生3~4级手足综合征1例,3~4级蛋白尿1例。剩余患者出现不同程度3级以下毒副反应,并均能耐受。两治疗组不良反应发生率差异无统计学意义(P>0.05),见表4。
表3 24例晚期消化道系统恶性肿瘤PFS影响单因素分析

临床病理参数中位PFS/月P肿瘤原发部位 胃癌2.30.705 肝癌3.5 肠癌3 食管癌4.3年龄/岁 ≤603.50.231 >603.0性别 男2.80.917 女3.0是否联合化疗 是3.00.185 否3.0ECOG评分 0~13.50.776 22.8
表4 阿帕替尼单药或联合化疗毒副反应分析[n(%)]
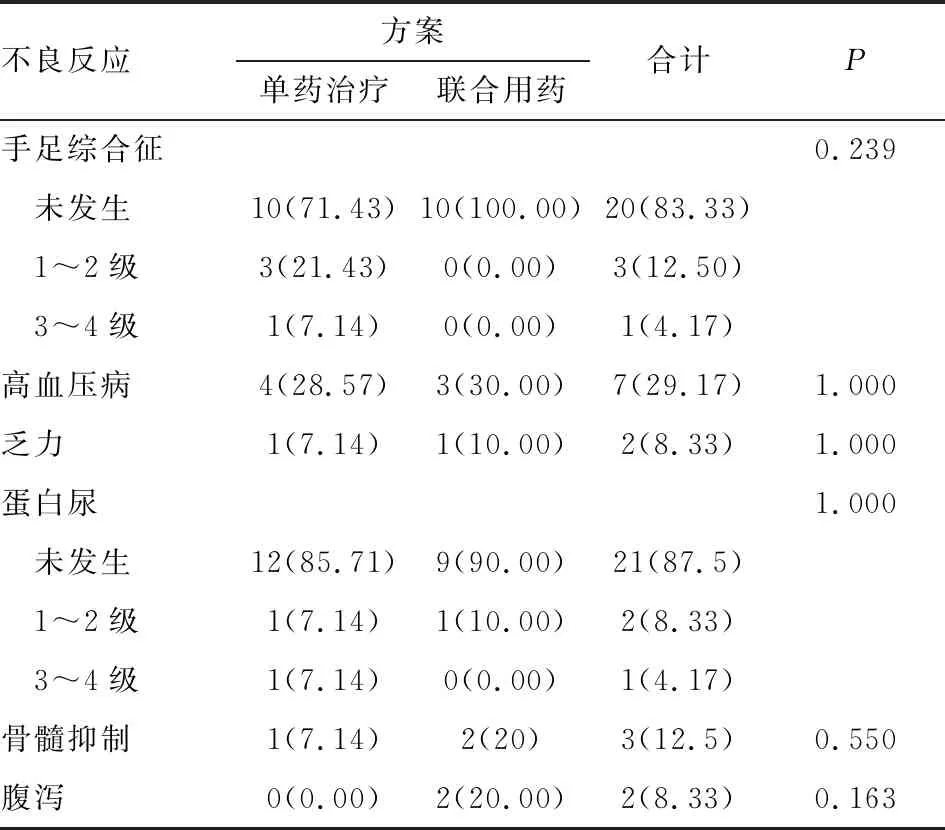
不良反应方案单药治疗联合用药合计P手足综合征0.239 未发生10(71.43)10(100.00)20(83.33) 1~2级3(21.43)0(0.00)3(12.50) 3~4级1(7.14)0(0.00)1(4.17)高血压病4(28.57)3(30.00)7(29.17)1.000乏力1(7.14)1(10.00)2(8.33)1.000蛋白尿1.000 未发生12(85.71)9(90.00)21(87.5) 1~2级1(7.14)1(10.00)2(8.33) 3~4级1(7.14)0(0.00)1(4.17)骨髓抑制1(7.14)2(20)3(12.5)0.550腹泻0(0.00)2(20.00)2(8.33)0.163
注:Fisher确切概率法。
3 讨论
消化系统恶性肿瘤是临床上常见的疾病,随着人们不良生活习惯及生活环境污染等因素,导致消化系统患者发病率呈增加趋势。早期消化系统肿瘤主要以外科手术切除,然后根据术后分型分期选择相应的辅助治疗[6]。化疗、放疗为晚期消化系统恶性肿瘤患者常用的治疗方法,虽能杀死恶性肿瘤,但化疗、放疗均具有明显的毒副反应[7],且临床推荐药物治疗效果有限,导致患者5年生存率较低。
随着对肿瘤的分子机制研究的不断深入,发现肿瘤组织的生长离不开其内部新生血管的营养支持[8]。甲磺酸阿帕替尼为小分子酪氨酸激酶抑制剂,通过与VEGFR-2结合,竞争性抑制VEGF与VEGFR-2结合及VEGFR-2磷酸化,从而抑制肿瘤血管生成,达到抑制肿瘤生长的目的及发挥其抗肿瘤作用,同时还可抑制血小板衍生生长因子受体b、c-kit、Ret以及c-src等酪氨酸激酶[9-10]。阿帕替尼已被批准用于晚期胃腺癌或胃食管结合部腺癌治疗[11]。同时其在肺癌、乳腺癌及妇科恶性肿瘤等恶性肿瘤方面也表现出较好的疗效。
综上所述,甲磺酸阿帕替尼用于二线及以上治疗失败晚期消化系统恶性肿瘤中能获得较高的近期疗效,同时大部分患者均可耐受不良反应,具有较高的安全性,可以作为多线治疗失败的晚期消化系统恶性肿瘤患者的一种有效的治疗选择。但是,本研究中亦存在诸多局限性,一方面实验中纳入患者数相对较少,需要大样本量进一步验证;另一方面对患者完成数据统计、分析时,可能存在人为误差,均需要进一步分析与研究。
