髓芯减压联合纳米骨植入治疗早期股骨头坏死的近期疗效
2016-07-01张二洋党晓谦王坤正
张 晨, 张二洋, 李 苗, 高 玲, 党晓谦, 王坤正*
(1西安交通大学第二附属医院骨一科,西安 710004; 2西安交通大学第二附属医院超声科;*通讯作者:E-mail:wkzh1955@163.com)
髓芯减压联合纳米骨植入治疗早期股骨头坏死的近期疗效
张晨1, 张二洋1, 李苗2, 高玲1, 党晓谦1, 王坤正1*
(1西安交通大学第二附属医院骨一科,西安710004;2西安交通大学第二附属医院超声科;*通讯作者:E-mail:wkzh1955@163.com)
摘要:目的分析髓芯减压联合纳米骨植入术治疗早期股骨头坏死的近期疗效。方法纳入2007-03~2012-06因股骨头坏死行单纯髓芯减压或单纯髓芯减压联合纳米骨植入术患者49例(54髋)。其中FicatⅠ期12髋,FicatⅡ期42髋。根据病人经济状况及病人意愿等选择具体手术方式,具体分为两组:单纯髓芯减压组和单纯髓芯减压联合纳米骨植入组。术后每3月随访一次,通过Harris髋关节评分、X线片影像学分期进展情况等综合评估临床疗效。结果经过平均12.6个月(7-30个月)的随访,46髋获得较完整资料。髓芯减压组手术前后Harris评分优良率分别为20%和75%(P<0.05);髓芯减压联合植骨组手术前后Harris评分优良率分别为19.2%和88.5%(P<0.05);两组间术后Harris评分优良率具有统计学意义(P<0.05)。Ficat Ⅰ期患者行单纯髓芯减压及单纯髓芯减压联合纳米骨植入术手术前后Harris评分总优良率分别为25%和100%(P<0.05),Ficat Ⅱ期患者手术前后Harris评分总优良率分别为17.6%和76.5%(P<0.05)。两组影像学稳定的有40髋,6髋出现不同程度的影像学分期进展,组间及Ficat分期间差异无统计学意义(P>0.05)。结论单纯髓芯减压术及髓芯减压联合纳米骨植入术都是治疗早期股骨头坏死的有效方法,髓芯减压联合纳米骨植入术治疗早期股骨头坏死的近期疗效优于单纯髓芯减压术。
关键词:股骨头坏死;髓芯减压;纳米骨植入
髓芯减压术最早由Arlet和Ficat用于骨功能探查而开展,他们发现做完骨功能探查后的大部分患者均诉患髋疼痛消失或明显减轻[1],此后陆续有学者对此进行了深入研究,髓芯减压逐渐成为股骨头坏死的重要治疗方法之一[2-5]。临床中,早期股骨头坏死选择髓芯减压术具有手术简单、操作方便、对患者损伤小、易于接受,而且据报道髓芯钻孔减压对于Ficat 0期和Ⅰ期的疗效较好,可以阻止股骨头的塌陷[6]。由于髓芯钻孔减压术后长期随访效果报道不一,特别是对其预防病变股骨头进一步塌陷方面的作用出现越来越多的争议,在髓芯减压基础上植骨越来越受到骨科界重视,但是由于取自体骨作为植骨材料损伤较大,并发症较多,患者不易接受等因素,许多学者把目光投向在减压通道内植入人工骨的做法。纳米羟基磷灰石/聚酰胺66纳米骨具有良好的生物相容性、良好的生物力学性能、良好的骨传导性能,临床应用广泛。本研究回顾性分析我院近年来接受股骨头坏死髓芯减压联合纳米骨植入手术患者的病例资料,分析其近期疗效,为今后治疗方案的选择提供一定参考。
1材料与方法
1.1一般资料
本研究经西安交通大学第二附属医院伦理委员会批准。回顾性分析我科2007-03~2012-06实施股骨头坏死单纯髓芯减压或单纯髓芯减压联合纳米骨植入手术患者49例(54髋),其中男29例(32髋),女20例(22髋),年龄26-47岁,平均32.7岁。根据Ficat分期分为Ficat Ⅰ期12髋,Ficat Ⅱ期42髋。所有患者均于术前详细记录姓名、性别、年龄等相关人口统计学资料,均采用Harris髋关节评分系统进行评分。
根据病人经济状况及病人意愿等选择具体手术方式,具体分为两组,其中单纯髓芯减压组24髋(22例),其中男性12例13髋,女性10例11髋;髓芯减压+纳米骨植入组30髋(27例),男性15例17髋,女性12例13髋;两组年龄、性别、术前Harris评分无明显统计学差异。术后通过电话、书信、网络及直接上门等方式进行疗效随访。随访的指标主要是手术前后Harris髋关节评分结果,X线片影像学分期进展情况,并发症的情况以及是否最终进行人工髋关节置换。
采用医用纳米羟基磷灰石/聚酰胺66复合骨充填材料(商品名:纳艾康),生产企业:四川国纳科技有限公司,产品标准:YZB/国0063-2003。
1.2病例纳入与排除标准
纳入标准:①入选患者均为有症状的Ficat Ⅰ-Ⅱ期的患者;②所有患者无重要脏器病变且可耐受麻醉及手术;③术前无严重并发症;④术区皮肤条件好,全身无感染灶;⑤所有患者术前都曾以限制负重或药物治疗等非手术治疗手段治疗至少6个月,疗效欠佳。
排除标准:①创伤性股骨头坏死;②股骨头骨骺未完全闭合者;③有患侧髋部手术史或其他侵入性治疗者;④术区皮肤条件差,有感染或他处有感染灶者;⑤依从性差的患者;⑥属于流动人口难以随访者。
1.3手术方法
所有手术均由同一手术医师完成,手术麻醉采用连续硬膜外麻醉。术前患者知情同意,手术体位取仰卧位,患侧臀部垫高8-10 cm,维持患肢外展位固定。髓芯减压组手术步骤:首先行体表定位,确定髓芯减压进针点。取患侧大粗隆下4-5 cm为中心长约4 cm纵行皮肤切口,逐层切开,显露大转子及股骨外侧,采用2.0克氏针在C臂正侧位像引导下钻入坏死区,注意勿突破软骨下骨。随后将8 mm空心钻头套入导针,沿导针钻透坏死区,至距软骨下骨约5 mm处止。取出导针及钻头,以弯头小号刮匙伸入坏死区,充分刮除死骨,冲洗后逐层关闭切口。髓芯减压+植骨组手术方式同上,充分刮除死骨后,首先应用骨导入器将预先准备好的纳米骨颗粒送入坏死区,随后通过钻孔通道向减压通道植入1根圆柱状纳米骨柱,冲洗后逐层关闭切口。
1.4术后处理
患肢术后6周内严禁负重,6-12周可扶支具保护下部分负重,12周后去除支具完全负重,负重量逐渐加大。
1.5临床疗效评价
分别于术前和术后每3个月随访一次,随访时评估患髋Harris评分(优90-100分、良80-89分、可70-79分、差<70分)。术后每3月随访时行X线检查,根据Ficat分期评估股骨头坏死影像学分期进展情况。
1.6统计学分析
采用SPSS11.0统计软件包进行分析。计数资料组间比较采用χ2检验,检验水准ɑ值取双侧0.05,P<0.05认为差异有统计学意义。
2结果
2.1患者随访情况分析
所有患者有6例失访,失访率为12.2%,其中6例因患者所留联系方式错误或地址更改而失访。最终获得较完整随访资料共43例(46髋),其中髓芯减压组19例(20髋),髓芯减压+植骨组24例(26髋),所有病例平均随访12.6个月(7-30个月)。
2.2不同手术组间Harris髋关节评分结果
髓芯减压组手术前后Harris评分优良率分别为20%(4/20)和75%(15/20),差异有统计学意义(χ2=8.1,P<0.05,见表1);髓芯减压+植骨组手术前后Harris评分优良率分别为19.2%(5/26)和88.5%(12/26),差异有统计学意义(χ2=17.05,P<0.05)。两组术后Harris评分优良率差具有统计学意义(χ2=3.92,P<0.05,见表1)。
表1不同手术组间Harris髋关节评分
Table 1Comparison of excellent rate of Harris score between two groups
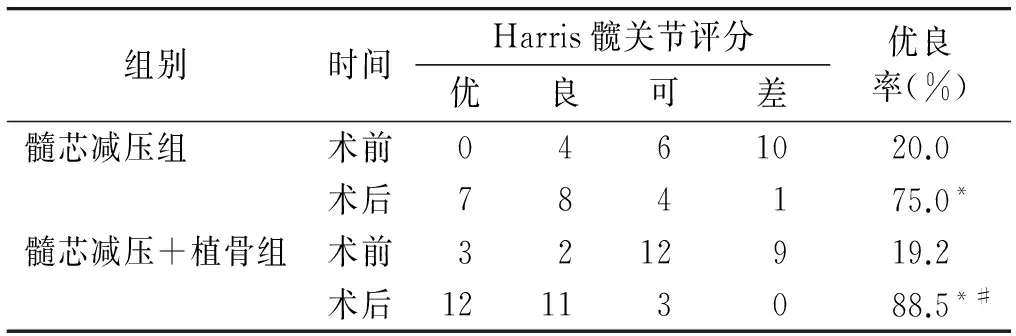
组别时间Harris髋关节评分优良可差优良率(%)髓芯减压组术前0461020.0术后784175.0*髓芯减压+植骨组术前3212919.2术后12113088.5*#
同组与术前比较,*P<0.05;术后与髓芯减压组比较,#P<0.05
2.3不同Ficat分期间Harris髋关节评分结果
Ficat Ⅰ期患者行单纯髓芯减压及单纯髓芯减压联合纳米骨植入术手术前后Harris评分总优良率分别为25%和100%,差异有统计学意义(χ2=7.11,P<0.05)。FicatⅡ期患者手术前后Harris评分优良率分别为17.6%和76.5%,差异有统计学意义(χ2=18.05,P<0.05,见表2)。
表2不同Ficat分期间Harris髋关节评分
Table 2Comparison of excellent rate of Harris score before and after surgery in different Ficat stages

组别时间Harris髋关节评分优良可差优良率(%)FicatⅠ期术前127225.0术后8400100.0*FicatⅡ期术前24111717.6术后12147176.5*
同分期与术前比较,*P<0.05
2.4不同组别及分期间术后影像学稳定性比较
单纯髓芯减压及单纯髓芯减压联合纳米骨植入术组共46髋随访,依据Ficat分期,影像学稳定40髋,6髋出现不同程度的影像学分期进展,两组各有3髋,组间影像学稳定率差异无统计学意义(χ2=0.12,P>0.05,见表3)。按Ficat 分期来看,Ficat Ⅰ期共12髋,2髋出现影像学分期进展;Ficat Ⅱ期共34髋,4髋出现影像学分期进展,分期间影像学稳定率无统计学差异(χ2=0.19,P>0.05,见表3)。手术前后影像学稳定患者X线片结果显示Ficat Ⅱ期患者术后股骨头影像学稳定无塌陷,股骨头形态良好(见图1);手术前后影像学分期进展患者X线片显示Ficat Ⅱ期患者术后股骨头塌陷,形态较影像学稳定者差(见图2)。
表3不同组别及分期间术后影像学稳定性比较
Table 3Comparison of graphic stability between different operation groups and different Ficat stages after operation
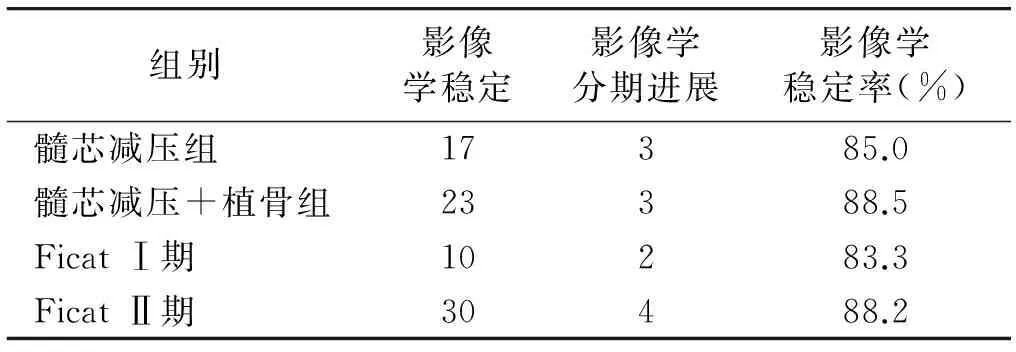
组别影像学稳定影像学分期进展影像学稳定率(%)髓芯减压组17385.0髓芯减压+植骨组23388.5FicatⅠ期10283.3FicatⅡ期30488.2
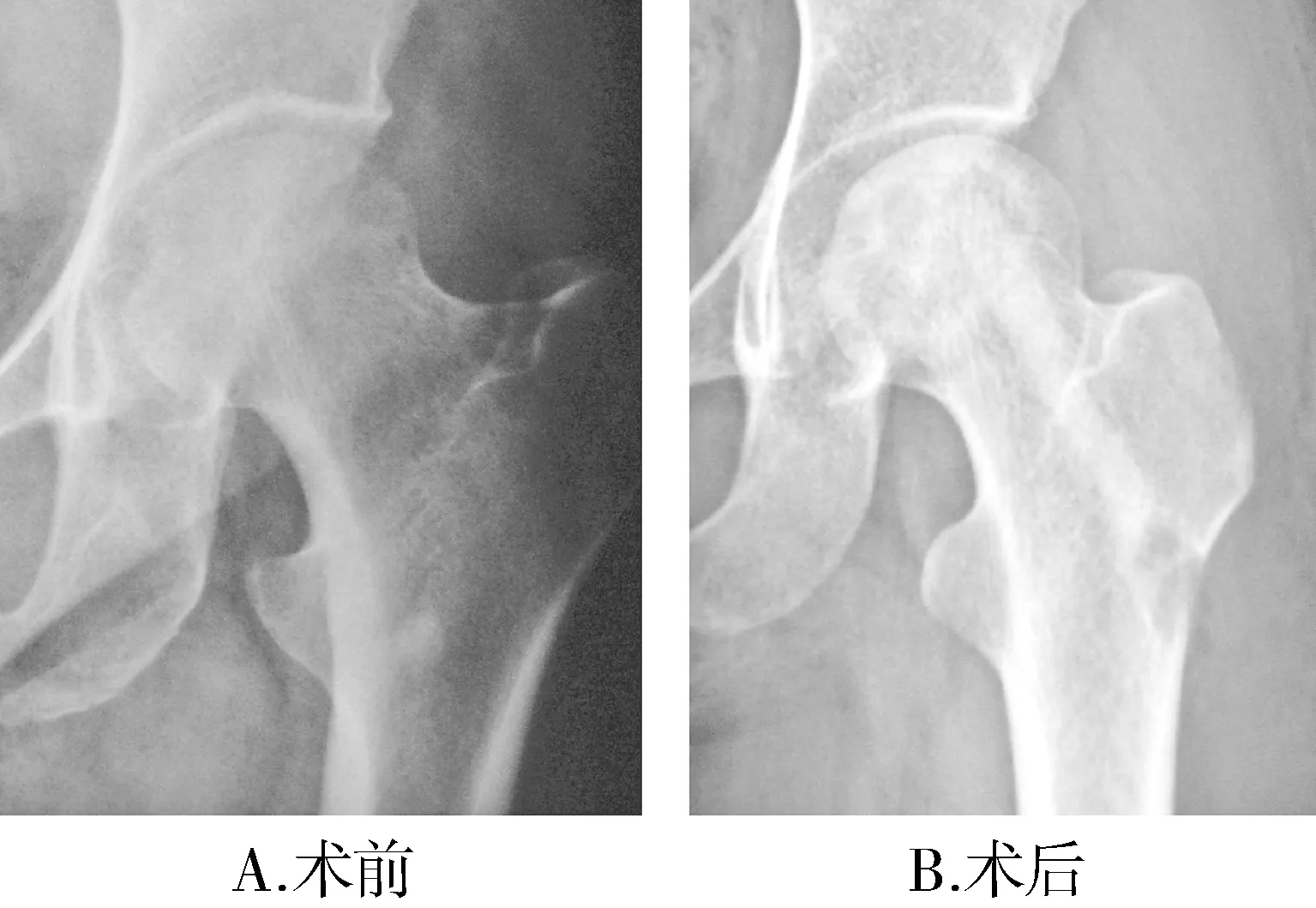
图1 Ficat Ⅱ期患者手术前后影像学稳定X线片比较 Figure 1 Comparison of X ray film with graphic stability of a Ficat Ⅱpatient before and after operation
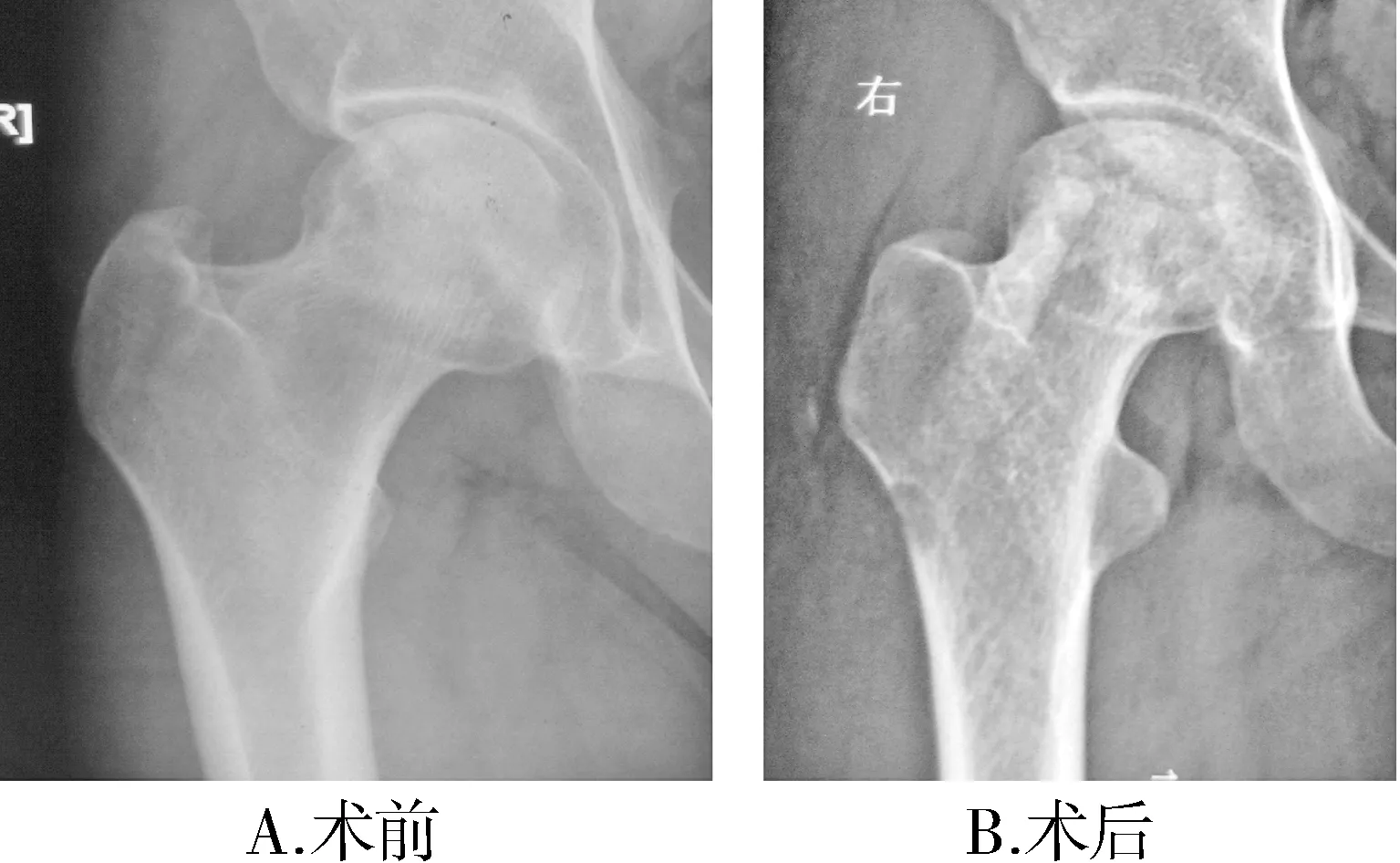
图2 Ficat Ⅱ期患者手术前后影像学分期进展X线片比较Figure 2 Comparison of X ray film with graphic progression of a Ficat Ⅱ patient before and after operation
2.5患者术后并发症情况分析
获得随访的43例(46髋)患者出现2例浅表切口感染,3例皮下血肿,1例经减压通道骨折,未出现穿孔(减压钻头穿破股骨颈或钻入太深穿破股骨头关节面)、下肢深静脉血栓、肺动脉栓塞等并发症。
3讨论
股骨头坏死早期手术治疗的目标是阻止股骨头坏死进展为股骨头塌陷,早期手术治疗股骨头坏死的方法主要有髓芯减压、细胞移植、骨移植、截骨术等[7]。髓芯减压术有以下优点:①手术操作简单、手术时间短,术中出血量少;②手术积累多年经验,技术成熟,各国开展广泛;③在此基础上可以进行细胞移植、骨移植、组织工程等手术;④不影响将来的关节置换手术。
为了保证髓芯减压的手术效果并尽量避免手术并发症,在C臂监视下进行操作已经成为共识,并已被广泛应用于临床,此法可以较准确地控制钻孔的位置、方向和深度,确保减压通道与坏死区相通。另外,有学者指出在钻头准备突破位于软骨下骨下方的硬化死骨时,要特别小心,不能用力太大,否则有导致股骨头破裂的风险。减压通道尽量靠外上,避开主要负重力线,且要避免过早负重,这样可以减少经减压通道骨折的发生率。坏死区硬化死骨的处理很重要,要尽量刮除硬化死骨,保证彻底减压。
在负重时机的选择上,我们的做法是:患肢术后6周内严禁负重(单侧患者术后3 d就可扶支具下地,注意患肢勿负重即可),6-12周可扶支具保护下部分负重,12周后去除支具完全负重,负重量逐渐加大。这样可以减少经减压通道骨折的发生率,更重要的是给股骨头坏死区重建创造有利条件,减少股骨头在坏死区重建前塌陷的发生率。单纯髓芯减压在缓解疼痛方面效果显著,我们的研究结果显示:末次随访时,术后Harris评分较术前提高,差异有统计学意义,单纯髓芯减压术是治疗早期股骨头坏死的有效方法。
髓芯减压术联合骨移植为塌陷前的股骨头坏死提供许多有利条件:股骨头减压、移除坏死骨、填补坏死骨移除后的缺损,还可以提供足够的力学支撑而预防塌陷,给骨修复和软骨下的重建提供条件。目前骨移植的途径主要有3种[7-10]:①通过髓芯减压通道植骨;②通过股骨颈开窗的途径植骨;③trapdoor途径植骨,即经股骨头关节软骨面开活门植骨的途径。临床应用最为广泛的方法为通过髓芯减压通道植骨。由于自体骨移植创伤大,并发症多,于是许多学者尝试用自体骨以外的人工骨材料植入清除死骨后的缺损区,也取得了较好的疗效,并且相对自体骨移植而言,创伤小,并发症少,恢复快,具有较明显的优势,也是最近研究的热点[11-13]。我们的研究结果显示,髓芯减压联合植骨术手术前后Harris评分优良率分别为19.2%和88.5%,术后Harris评分提高高于单纯髓芯减压组,差异有统计学意义。结果显示髓芯减压联合植骨术治疗早期股骨头坏死的疗效要优于单纯髓芯减压术。其原因我们认为与植入的纳米骨材料的特性密切相关。
多孔纳米羟基磷灰石/聚酰胺66人工骨以其良好的生物相容性、无全身及局部毒性、无溶血现象及良好的生物力学性能等优势近年来广泛应用于骨科植骨术。其强度近似于人体的正常皮质骨,可保证临床要求的初期强度,也能避免其刚度过高产生应力屏蔽。多孔纳米羟基磷灰石/聚酰胺66人工骨具有良好的骨传导性能,其纳米磷灰石晶体表面的极性离子与人体细胞、多糖和蛋白质能以氢键结合,具有较强的亲和力,同时还可起到钙盐沉积的支点作用,诱发新骨的形成,直接和人体硬组织形成骨性键合,在骨骼修复中发挥重要作用。聚酰胺与胶原有类似结构,含有极性酰胺键、羟基以及羟基基团,使其能引导组织细胞生长,促进细胞生成类骨质进而矿化,加快骨愈合,最终形成纳米羟基磷灰石/聚酰胺复合材料与新骨共同构成具有生命力的,可长期发挥作用的重建骨[14-17]。
虽然髓芯减压手术操作相对简单,创伤相对小,但仍存在一些术后并发症,主要有:感染、经减压通道骨折、穿孔、血肿及术后肺动脉栓塞、下肢深静脉血栓等。Smith等[18]报道92例股骨头坏死(114髋)接受髓芯减压治疗后,10例患者出现了并发症,包括3例浅表伤口感染,2例经减压通道骨折,2例血肿,1例肺动脉栓塞,1例深静脉血栓,1例交感反射性营养不良。Bozic等[19]报道34例非创伤性股骨头坏死(54髋)行CD治疗后,2例出现并发症,1例经减压通道骨折,1例血肿。我们获得随访的43例(46髋)患者中2例出现浅表切口感染,3例出现皮下血肿,1例出现经减压通道骨折。发生的并发症与先前报道类似。针对髓芯减压术的术后并发症,学者们提出相应注意事项,总结如下:①钻孔应在C臂监视下进行,可相对准确地确定钻孔位置、钻头角度及钻入深度,并可大大降低穿孔的发生率,在钻头准备突破位于软骨下骨下方的硬化死骨时,也要特别小心,不能用力太大和过猛,否则有导致股骨头破裂的风险;②减压隧道尽量靠外上,避开力线,并且要避免过早负重,可减少经隧道骨折的发生率;③切口内置引流装置可降低血肿的发生率;④术前半小时及术后常规预防性应用抗生素,可预防感染;⑤术后早期鼓励病人行下肢不负重的关节活动,特别是小腿的屈伸肌群的舒缩可明显改善静脉回流,避免静脉瘀滞而形成深静脉血栓。
本研究在设计之初选择了Ficat分期系统,此系统并没有把股骨头受累范围作为分期的标准之一。尽管本研究发现不论在单纯减压组或减压联合植骨组之间还是在Ficat Ⅰ期和Ficat Ⅱ期之间影像学稳定率之间的差异在统计学上均无显著意义,但是我们发现,坏死股骨头影像学稳定率和股骨头的受累范围密切相关,分期进展的6髋有5髋股骨头受累范围都是超过15%,仅1髋受累范围小于15%。目前。Pennsylvania分期体系及国际骨循环研究会(ARCO)分期体系将股骨头受累范围作为分期的标准之一,若选择后两种分期体系可能对塌陷的预测以及临床病例的选择更具有意义。
本研究结果表明,单纯髓芯减压术及髓芯减压联合纳米骨植入术都是治疗早期股骨头坏死的有效方法,髓芯减压联合纳米骨植入术治疗早期股骨头坏死的近期疗效优于单纯髓芯减压术。但是由于本研究属早期研究,随访时间较短,失访率较高,髓芯减压联合复合人工骨植入术治疗早期股骨头坏死的中远期疗效仍需进一步观察。
参考文献:
[1]Arlet J,Ficat P,Lartigue G.Mode of onset of primary osteonecrosis of the femoral head.(Stage I.Uncomplicated).Study of 20 cases histologically verified by punch biopsy[J].Rev Rhum Mal Osteoartic,1968,35(5):239-249.
[2]Wang CJ,Huang CC,Wang JW,etal.Long-term results of extracorporeal shockwave therapy and core decompression in osteonecrosis of the femoral head with eight-to nine-year follow-up[J].Biomed J,2012,35(6):481-485.
[3]Beckmann J,Schmidt T,Schaumburger J,etal.Infusion,core decompression,or infusion following core decompression in the treatment of bone edema syndrome and early avascular osteonecrosis of the femoral head[J].Rheumatol Int,2013,33(6):1561-1565.
[4]Zhao DW,Yu XB.Core decompression treatment of early-stage osteonecrosis of femoral head resulted from venous stasis or artery blood supply insufficiency[J].J Surg Res,2015,194(2):614-621.
[5]Jiang JJ,Hussain WM,Bielski RJ.Bone impaction grafting of the lateral femoral condyle in a pediatric patient[J].Orthopedics,2012,35(10):e1533-1536.
[6]Mont MA,Carbone JJ,Fairbank AC.Core decompression versus nonoperative management for osteonecrosis of the hip[J].Clin Orthop Relat Res,1996,324:169-178.
[7]Jawish R,Chamseddine A,Abou SP.The core decompression of the femoral head for stage I idiopathic osteonecrosis[J].J Med Liban,2008,56(3):144-152.
[8]Phemister DB.Treatment of the necrotic head of the femur in adults[J].J Bone Joint Surg Am,1949,31:55-66.
[9]Ganz R,Buchler U.Overview of attempts to revitalize the dead head in aseptic necrosis of the femoral head-osteotomy and revascularization[J].Hip (Jan),1983,1:296-305.
[10]Rosenwasser MP,Garino JP,Kiernan HA,etal.Long-term follow-up of thorough debridement and cancellous bone grafting of the femoral head for avascular necrosis[J].Clin Orthop Relat Res,1994,306:17-27.
[11]Roth A,Beckmann J,Smolenski U,etal.S3 guideline.Part 2:non-traumatic avascular femoral head necrosis in adults-untreated course and conservative treatment[J].Z Orthop Unfall,2015,153(5):488-497.
[12]汪亮,刘耀升,刘蜀彬,等.多孔钽棒植入治疗早中期股骨头坏死的生存率分析和预后因素评估[J].中华骨与关节外科杂志,2015(5):396-402.
[13]吴刚,张永锋.复合自体骨髓的骨诱导材料结合髓芯减压钛棒支撑修复Ⅱ期股骨头坏死[J].中国组织工程研究,2015(28):4460-4464.
[14]刘耀升,刘蜀彬,周诗国,等.髓芯减压BMMCs移植羟基磷灰石复合人工骨植入治疗股骨头坏死[J].中华医学杂志,2013,93(27):2126-2130.
[15]鹿鸣,张雪松,徐辉,等.碳纤维增强纳米羟基磷灰石/聚酰胺66复合材料与动物体内骨组织的相容性[J].中国组织工程研究,2015,19(16):2523-2528.
[16]刘星,田利军,邓志刚,等.纳米人工骨在颈前路植骨融合中的应用[J].中国组织工程研究,2015,19(34):5468-5472.
[17]徐显春,王治,侯铁奇.纳米羟基磷灰石/聚酰胺材料的体内成骨能力[J].中国组织工程研究,2015,19(30):4769-4773.
[18]Smith SW,Fehring TK,Griffin WL,etal.Core decompression of the osteonecrotic femoral head[J].J Bone Joint Surg,1995,77(5):674-680.
[19]Bozic KJ,Zurakowski D,Thornhill TS.Survivorship analysis of hips treated with core decompression for nontraumatic osteonecrosis of the femoral head[J].J Bone Joint Surg,1999,81(2):200-209.
The recent curative efficacy of marrow core decompression combined with nanometer bone implantation in the treatment of early femoral head necrosis
ZHANG Chen1, ZHANG Eryang1,LI Miao2,GAO Ling1,DANG Xiaoqian1, WANG Kunzheng1*
(1DepartmentofOrthopedics,SecondAffiliatedHospitalofXi’anJiaotongUniversity,Xi’an710004,China;2DepartmentofUltrasound,SecondAffiliatedHospitalofXi’anJiaotongUniversity;*Correspondingauthor,E-mail:wkzh1955@163.com)
Abstract:ObjectiveTo analyze the short-term efficacy of marrow core decompression combined with nanometer bone implantation for early femoral head necrosis.MethodsFrom March 2007 to June 2012, 49 patients were recruited in our study(32 hips of 29 male and 22 hips of 20 female). In all 54 hips, 12 hips were scored with Ficat stage Ⅰ and 42 hips with Ficat stage Ⅱ. They underwent marrow core decompression or marrow core decompression combined with nanometer implantation, and were followed-up every 3 months after operation. The clinical efficacy was evaluated by Harris hip scores and imaging stages.ResultsAfter follow-up for 7-30 months (12.6 months on average), a total of 46 cases had complete information. In marrow core decompression group, the excellent rates of Harris scores were 20% and 75% before and after surgery, respectively(P<0.05). In marrow core decompression combined with nanometer bone implantation group, the excellent rates of Harris scores was 19.2% and 88.5% before and after surgery(P<0.05). The excellent rate of Harris scores showed significant statistical difference after surgery between two groups(P<0.05). The excellent rates of Harris scores were 25% and 100% before and after surgery in the patients with Ficat Ⅰ stage,respectively(P<0.05), while the excellent rates of Harris scores were 17.6% and 76.5% before and after surgery in the patients with Ficat Ⅱ stage(P<0.05).Forty hips exhibited imaging stability and 6 hips with graphic progression after surgery. There was no statistical difference within groups or between different Ficat stage groups(P>0.05).ConclusionMarrow core decompression and marrow core decompression combined with nanometer bone implantation are both effective treatments for early femoral head necrosis. The recent clinical efficacy of marrow core decompression combined with nanometer bone implantation is superior to marrow core decompression.
Key words:femoral head necrosis;marrow core decompression;nanometer bone implantation
基金项目:国家自然科学基金资助项目(81301562);西安交通大学第二附属医院人才培养专项科研基金资助项目(RC(XM)201501)
作者简介:张晨,男,1982-11生,博士,副研究员,主治医师,E-mail:osteozhang@163.com
收稿日期:2016-03-28
中图分类号:R681.8
文献标志码:A
文章编号:1007-6611(2016)06-0565-05
DOI:10.13753/j.issn.1007-6611.2016.06.019
