温度和pH敏感高分子含钆核磁共振成像造影剂的合成及性能
2016-04-08刘瑞清徐祖顺徐海波
刘瑞清, 梁 爽, 江 存, 徐祖顺, 徐海波
(1. 湖北大学有机化工新材料湖北省协同创新中心, 武汉 430062;
2. 华中科技大学同济医学院协和医院放射科, 武汉 430030)
温度和pH敏感高分子含钆核磁共振成像造影剂的合成及性能
刘瑞清1, 梁爽2, 江存1, 徐祖顺1, 徐海波2
(1. 湖北大学有机化工新材料湖北省协同创新中心, 武汉 430062;
2. 华中科技大学同济医学院协和医院放射科, 武汉 430030)
摘要以N-异丙基丙烯酰胺为温度敏感单体, 以甲基丙烯酸为pH敏感单体, 与三丙烯酸菲洛啉钆进行无皂乳液聚合, 一步合成了具有温度和pH敏感的高分子含钆核磁共振成像(MRI)造影剂(TPRPP). 动态光散射测试结果表明, TPRPP的粒径随温度或pH值的变化而发生较大的改变. 体外MRI测试结果表明, TPRPP的横向弛豫时间(T1)的加权弛豫率约为11.3 L/(mmol·s), 为临床造影剂Magnevist®的2.6倍. 体内MRI结果表明, TPRPP在肝和脾中具有明显的正增强效果. 研究结果表明, TPRPP是一种优异的多功能MRI造影剂, 具有极大的临床研究价值.
关键词温度和pH敏感高分子; 核磁共振成像; 无皂乳液聚合; 钆造影剂
徐海波, 男, 教授, 主要从事核磁共振成像研究. E-mail: xuhaibo1120@hotmail.com
近年来, 核磁共振成像(MRI)在临床诊断中应用广泛, 尤其在癌症和肿瘤的检测上具有独特的优势. 为了能更精确地分辨病变组织, 造影剂是不可或缺的. 目前, 低分子量的含钆配合物如Magne-vist®, Omniscan®和Dotarem®等由于具有低毒性和高稳定性成为临床仅有的一类MRI造影剂. 但此类造影剂具有体内循环时间短、弛豫率低和用量大等缺点[1]. 功能高分子改性的含钆MRI造影剂不仅能有效地克服上述小分子造影剂的缺点, 同时还能赋予其特殊的功能, 如pH敏感性[2]、靶向性[3]和载药性[4]等. 其中, 环境敏感高分子改性的含钆MRI造影剂由于在药物的可控释放中具有重要的应用而受到广泛关注. 由于病变组织具有较低的pH值和较高的温度[5], 可作为有效的控制条件来调控药物的释放, 因而pH或温度敏感高分子含钆MRI造影剂备受关注[2,6~9]. 目前, 合成pH或温度敏感高分子含钆MRI造影剂的方法主要是先合成能与钆离子配位的高分子, 再与钆离子配位形成高分子含钆MRI造影剂[8,10~12]. 这类合成方法至少需要经过两步反应, 比较繁琐; 此外, 直接配位在高分子上的钆离子容易脱离母体, 使合成的pH或温度敏感高分子含钆MRI造影剂具有潜在的生物毒性[1,13,14]. 如果先将钆离子和不饱和单体反应生成含钆的单体, 再与pH或温度敏感单体共聚合, 既能减少合成步骤, 又可以使钆离子在聚合中固定在高分子网络中, 对钆离子进行多重固定, 减小了钆离子脱离高分子母体的机率. 由此可见, 开发一种简单易行且能一步合成温度和pH敏感的高分子含钆MRI造影剂的聚合方法具有重要意义和迫切需要.
本文以N-异丙基丙烯酰胺(NIPAM)为温度敏感单体, 甲基丙烯酸(MAA)为pH敏感单体, 与三丙烯酸菲洛啉钆[Gd(AA)3phen·H2O]进行无皂乳液聚合, 一步合成了具有温度和pH敏感的含钆高分子MRI造影剂(TPRPP), 研究了TPRPP的pH和温度敏感性、稳定性、生物毒性及MRI造影性能, 结果表明, TPRPP可作为一种温度和pH敏感的MRI造影剂. 本文的合成方法简单易行, 便于实施, 简化了传统方法的合成步骤, 使钆在聚合过程中结合在高分子中, 有利于降低高分子的生物毒性; 在合成过程中以水作为介质, 具有低毒性和环境友好的特点.
1实验部分
1.1试剂与仪器
NIPAM(纯度99%)和MAA(纯度99%), 阿拉丁试剂公司; 苯乙烯(St)、过二硫酸钾(KPS)、二甲亚砜、正己烷和甲苯均为分析纯, 国药集团化学试剂有限公司; MAA和St采用减压蒸馏后置于冰箱中, 备用; KPS和NIPAM分别在水和正己烷/甲苯(体积比, 1∶1)中重结晶后真空干燥备用.
美国Thermofisher公司Nicolet iS50型傅里叶变换红外光谱(FTIR)仪, 溴化钾压片; 美国FEI公司Tecnai G20型透射电子显微镜(TEM); 英国Malvern公司ZS90型动态光散射仪(DLS); 美国PE公司Optimal 8000型电感耦合等离子光谱发生仪(ICP); 美国Rayto 公司Rt2100c型酶标仪; 德国Siemens公司Magnetom Trio型临床扫描仪.
1.2温度和pH敏感高分子含钆微粒的合成
参照文献[15]方法合成Gd(AA)3phen·H2O. 采用无皂乳液聚合法一步合成TPRPP(反应过程见Scheme 1). 将NIPAM(1.000 g), MAA(0.201 g), St(0.500 g)和KPS(0.150 g)分散于80 mL去离子水中, 于冰浴中超声3 min后, 转移至装有回流冷凝管、聚四氟乙烯搅拌装置、氮气导管的250 mL四口烧瓶中, 充分搅拌混合均匀后水浴加热至80 ℃, 10 min后逐滴加入0.09 g Gd(AA)3phen·H2O的水溶液(15 mL). 滴加完毕后于80 ℃充分反应3 h, 得到TPRPP.
按同样的方法制备不添加Gd(AA)3phen·H2O量的样品作为参照, 标记为TPRPP1.
将TPRPP1和TPRPP分别装入透析袋(截留分子量14000)中, 在去离子水中透析提纯7 d, 每隔6 h换一次新鲜的去离子水. 将部分提纯后的样品于40 °C真空干燥48 h得到固体粉末样品, 将纯化后的乳液及干燥后的粉末样品储存备用.
1.3温度和pH敏感性测试
将TPRPP乳液用去离子水稀释后用DSL测试粒径, 温度每升高2 ℃记录一次数据. 为了检测TPRPP的重复使用性, 检测温度在25和37 ℃之间交替变化时TPRPP粒径的变化情况.
将TPRPP用不同pH值的三羟甲基氨基甲烷缓冲液(Tris-buffer)稀释后用DLS测试不同pH条件下TPRPP的粒径. 同时测试pH值在2和7.4之间交替变化时TPRPP粒径的变化情况.
1.4体外细胞毒性测试
采用典型的3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐(MTT)法检测TPRPP的细胞毒性. 将HeLa细胞以1×104Cell/孔的浓度接种于含有细胞培养基的96孔板中, 在37 ℃, 5%(体积分数)CO2的条件下培养24 h; 然后加入不同浓度的TPRPP继续培养24 h, 向每个孔板中加入5 μL 新鲜 MTT试剂(5 mg/mL), 于37 ℃继续培养4 h; 摇床振荡后移除上清液, 并用磷酸盐(PBS)缓冲液反复洗涤, 加入200 μL二甲亚砜后摇匀, 用酶标仪测定570 nm处的吸光值(OD). 相对细胞活性(Cell viability, %)用下式计算:
Cell viability(%)=(ODtreated/ODcontrol)×100%
式中, ODtreated为TPRPP培养后的吸光值; ODcontrol为培养液的吸光值.
1.5体外弛豫率测试
将TPRPP稀释至钆离子浓度为0.025, 0.05, 0.1, 0.2和0.4 mmol/L后, 移至96孔板中, 置于临床Siemens Magnetom Trio 3.0 T MR成像仪中扫描, 测得不同浓度的横向弛豫时间(T1). 仪器参数为: 扫描视野10 cm×10 cm; 回波时间(TE): 9 ms; 矩阵大小: 128×128; 层厚为3 mm. 重复时间(TR)为300, 400, 500, 600, 800, 1000, 1500和2000 ms. 弛豫率(r1)由横向弛豫时间T1的倒数对钆离子浓度进行线性拟合得到.
1.6体内MRI测试
将250 g的Sprague-Dawley大鼠用10%的三氯乙醚麻醉剂麻醉(40 mg/kg), 尾静脉注射TPRPP(约0.05 mmol Gd/kg), 置于3.0 T Siemens Magnetom Trio上扫描. 分别收集0, 15, 30, 60, 120和360 min时T1加权图像. 仪器参数TE/TR=10/0.44, 平均值6. 动物实验在国家动物保护机构和湖北大学动物使用委员会的允许下进行.
2结果与讨论

Fig.1 FTIR spectra of Gd(AA)3phen·H2O(a), TPRPP1(b) and TPRPP(c)

2.2TPRPP的形貌和尺寸分析
图2为TPRPP1和TPRPP的TEM照片. 可以看出, TPRPP1和TPRPP呈单分散的球形结构, 粒径约为200 nm. 在25 ℃时, DLS测得TPRPP1和TPRPP的平均水合粒径(Dh)分别为 257.4和267.0 nm, 单分散指数(PDI)均小于0.1, 说明TPRPP1和TPRPP具有单分散性, 与TEM结果吻合. TEM测得的粒径小于DLS测得的粒径, 这是由于在TPRPP1和TPRPP中, 亲水性高分子含量较大, 在水合体系中产生部分溶胀, 从而具有较大的尺寸.

Fig.2 TEM images of TPRPP1(A) and TPRPP(B)

Fig.3 Dh of TPRPP as function of temperature(A), pH(B), variation in Dh of TPRPP as alternate temperature of 25 and 37 ℃(C) and alternate pH value of 2.0 and 7.4(D) The pH of (A) and (C) is 6.0; the temperature of (B) and (D) is 25 ℃.
2.3TPRPP的温度和pH敏感性
用DLS测试温度在25~43 ℃之间变化时TPRPP粒径的变化. 由图3(A)可知, TPRPP的Dh随温度的升高而减小,Dh从267.0 nm减小至218.8 nm, 共减小约50 nm. 这是因为, 温度敏感性的本质是高分子链间或链内的氢键相互作用, 当温度高于TPRPP的低临界转变温度(LSCT, 约为33 ℃)时, TPRPP内部的氢键遭到破坏, 氢键的减小使其水溶性降低, 进而TPRPP收缩,Dh减小[20].
液相色谱-质谱联用法简称LC-MS,是具有很高的分离能力和定性鉴别能力的技术,在检测时能够实现对复杂样品的快速、高效分离。在LC-MS检测苯并芘的研究方面,刘玉兰等[21]用此方法对食用油中苯并芘的含量进行检测,定量时采用内标法对样品的量进行标定,对样品进行分析得出苯并芘的检测限为0.2~30μg/L,检出限是0.1μg/L。该检测方法主要适用于样品的精确检测,但是由于费时比较长,对检测人员的要求比较高,当需要对大批量的样品进行快速检测时,此方法并不适用。
用DLS检测TPRPP乳液在不同pH缓冲液(Tris-buffer)中的粒径[图3(B)], 当pH从2增加到8时,Dh从260.1 nm增大至318.4 nm, 粒径增大约60 nm. 这是因为, 在低pH值条件下, 强烈的氢键作用使高分子链结合相对紧密; 当pH值高于PMAA的pKa值(约为6)[21,22]时, PMAA中的羧基离子化, 使得高分子链的亲水性增强, TPRPP溶胀, 从而Dh变大[13].
为了进一步研究TPRPP的重复使用性, 检测了温度和pH值反复变化时Dh的变化情况, 由图3(C)可知, 当温度在25和37 ℃之间交替变化时,Dh呈交替变化规律. 当温度回到25 ℃时,Dh的最终变化也在可控的误差范围内. 当pH值在2.0和7.4之间交替变化时,Dh的变化呈现与温度交替变化类似的规律[图3(D)]. 表明所得TPRPP同时具有较好的温度和pH敏感性, 并具有较好的重复使用性. 在载药和药物的可控释放中具有潜在的应用价值.
2.4TPRPP的稳定性
为了检验TPRPP在类似生物体环境中的稳定性, 选择接近肿瘤pH值(pH=4)和人体正常pH值(pH=7.4)作为实验条件, 将10 mL TPRPP乳液在三羟甲基氨基甲烷缓冲液(tris-buffer, 0.01 mol/L, 50 mL)中透析(截留分子量: 14000)7 d, 检测透析袋外缓冲液中钆离子的含量, 考察TPRPP在不同pH值条件下的稳定性. ICP结果显示, 透析袋外的缓冲液中, 钆离子的含量为0.003 mg/L, 可以忽略不计. 透析前后TPRPP乳液的Zeta电位均小于-30 mV, 且透析前后几乎无变化. 结果说明钆离子在TPRPP中具有较强的结合力和稳定性.
2.5TPRPP的细胞毒性
TPRPP体外毒性用MTT法进行衡量. 由图4可见, 当TPRPP浓度大于2.0 g/L时, 相对细胞活性仍然高于95%, 表明所得TPRPP具有很低的毒性和较高的生物相容性.
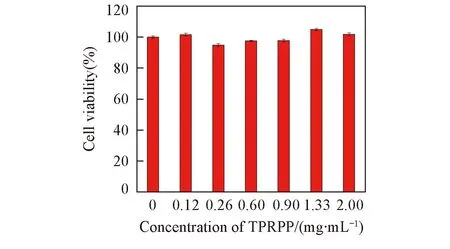
Fig.4 Cell viability against Hela cells assessed by standard MTT assay

Fig.5 T1-weighted relaxivity of TPRPPThe longitudinal relaxation time(T1) is measured on a clinical 3.0 T MR scanner at various Gd(Ⅲ) concentrations.
2.6体内和体外MRI成像
由图5体外MRI成像结果可以看出, TPRPP具有明显的MRI正增强效果,T1加权弛豫率(r1)为11.3 L/(mmol·s), 约为临床造影剂Magnevist®[约4.3 L/(mmol·s)]的2.6倍. 高弛豫率主要归功于TPRPP中含有亲水的PMAA和PNIPAM, 由Solomon-Bloembergen-Morgan理论可知, PMAA和PNIPAM能有效地提高造影剂的旋转相关时间(τr)和水交换速率(τm), 有效地提高了TPRPP的弛豫率[23]. 此外, 在TPRPP中的高分子网络中形成了钆离子的多网络中心, 这对于获得高弛豫率也做出了有效的贡献[24]. 为了进一步验证TPRPP在体内的增强效果, 采用尾静脉注射法将TPRPP注射到老鼠体内, 在不同时间点对老鼠的肝和脾进行MRI扫描. 图6为不同时间点的MRI成像图. 可以看出, 当注入TPRPP 15 min后, MRI的图像开始变白, 在3 h达到最亮, 6 h后仍然具有明显的造影效果. 表明所得的TPRPP具有很好的MRI造影功能, 是一种潜在的MRI造影剂.
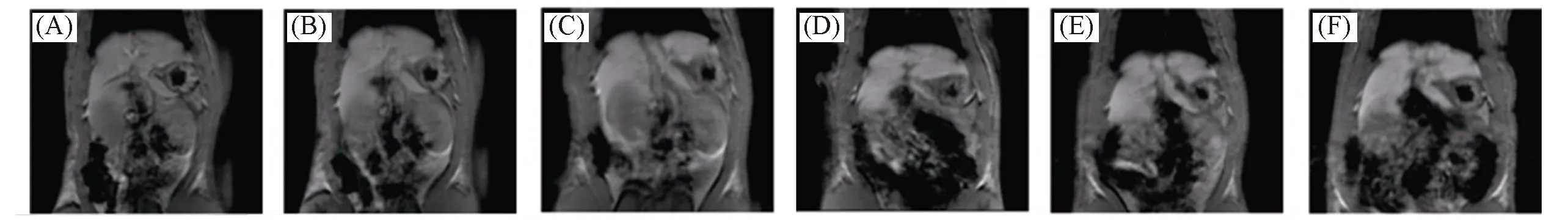
Fig.6 T1-weighted MR images taken at different time points T1/min: (A) 0; (B) 15; (C) 30; (D) 60; (E) 120; (F) 360.
综上所述, 通过无皂乳液聚合一步合成了具有温度和pH敏感的含钆高分子MRI造影剂, 此方法简单易行, 便于推广, 为合成多功能MRI造影剂提供了新的选择. 结果表明, TPRPP呈球形, 粒径分布均一, 平均粒径约200 nm. 无论是温度或pH值变化,Dh均变化约60 nm, 表明TPRPP呈现较好的温度和pH敏感性. 此外, TPRPP具有低细胞毒性、高稳定性和较高的弛豫率, 为临床造影剂Magne-vist®的2.6倍, 且具有优异的体内MRI造影成像功能. 可作为一种潜在的诊疗材料.
参考文献
[1]Li Y., Beija M., Laurent S., Elst L. V., Muller R. N., Duong H. T. T., Lowe A. B., Davis T. P., Boyer C.,Macromolecules, 2012, 45(10), 4196—4204
[2]Liu Y. J., Feng L. X., Liu T. X., Zhang L., Yao Y., Yu D. X., Wang L. L., Zhang N.,Nanoscale, 2014, 6(6), 3231—3242
[3]Cheng Z., Thorek D. L., Tsourkas A.,Angew.Chem.Int.Ed.Engl., 2010, 49(2), 346—350
[4]Liu Y. G., Zhang N.,Biomaterials, 2012, 33(21), 5363—5375
[5]Wu X., Wang Z., Zhu D., Zong S., Yang L., Zhong Y., Cui Y.,ACSAppl.Mater.Interfaces, 2013, 5(21), 10895—10903
[6]Davies G. L., Kramberger I., Davis J. J.,Chem.Commun.(Camb), 2013, 49(84), 9704—9721
[7]Nwe K., Huang C. H., Tsourkas A.,J.Med.Chem., 2013, 56(20), 7862—7869
[8]Kim K. S., Park W., Hu J., Bae Y. H., Na K.,Biomaterials, 2014, 35(1), 337—343
[9]Kono K., Nakashima S., Kokuryo D., Aoki I., Shimomoto H., Aoshima S., Maruyama K., Yuba E., Kojima C., Harada A., Ishizaka Y.,Biomaterials, 2011, 32(5), 1387—1395
[10]Liu Q. M., Zhu H. Z., Qin J. Y., Dong H. Q., Du J. Z.,Biomacromolecules, 2014, 15(5), 1586—1592
[11]Liu Q. M., Chen S., Chen J., Du J. Z.,Macromolecules, 2015, 48(3), 739—749
[12]Shuhendler A. J., Staruch R., Oakden W., Gordijo C. R., Rauth A. M., Stanisz G. J., Chopra R., Wu X. Y.,J.Control.{Release, 2012, 157(3), 478—484
[13]Shalviri A., Foltz W. D., Cai P., Rauth A. M., Wu X. Y.,J.Control.Release, 2013, 167(1), 11—20
[14]Li X., Qian Y., Liu T., Hu X., Zhang G., You Y., Liu S.,Biomaterials, 2011, 32(27), 6595—6605
[15]Xu Z. S., Liu R. Q., Liang S., Jiang C., Wang X.,TheSynthesisandApplicationofaPolymerizableGadoliniumComplex, CN 104672258A, 2015-06-03(徐祖顺, 刘瑞清, 梁爽, 江存, 汪鑫. 一种含双键水溶性钆配合物及其合成方法和应用, CN 104672258A, 2015-06-03)
[16]Peng J., Qi T., Liao J., Fan M., Luo F., Li H., Qian Z.,Nanoscale, 2012, 4(8), 2694—2704
[17]Zhu H. E., Tao J., Wang W. H., Zhou Y. J., Li P. H., Li Z., Yan K., Wu S. L., Yeung K. W., Xu Z. S., Xu H. B., Chu P. K.,Biomaterials, 2013, 34(9), 2296—2306
[18]Ding X., Sun Z., Zhang W., Peng Y., Chan A. S. C., Li P.,Colloid.Polym.Sci., 2000, 278, 459—463
[19]Niu S. Y., Jin J., Jin X. L., Yang Z. Z.,SolidStateSciences, 2000, 4, 1103—1106
[20]Chan A., Orme R. P., Fricker R. A., Roach P.,Adv.Drug.Deliv.Rev., 2013, 65(4), 497—514
[21]Kharlampieva E., Sukhishvil S. A.,Macromolecules, 2003, 36, 9950—9956
[22]Rahane S. B., Floyd J. A., Metters A. T., Kilbey S. M.,Adv.Funct.Mater., 2008, 18(8), 1232—1240
[23]Villaraza A. J., Bumb A., Brechbiel M. W.,Chem.Rev., 2010, 110(5), 2921—2959
[24]Shen C., New E. J.,Curr.Opin.Chem.Biol., 2013, 17(2), 158—166
Synthesis and Proporties of Temperature and pH-sensitive and Gadolinium
Contained Polymeric Magnetic Resonance Imaging Contrast Agent†
LIU Ruiqing1, LIANG Shuang2, JIANG Cun1, XU Zushun1*, XU Haibo2*
(1.HubeiCollaborativeInnovationCenterforAdvancedOrganicChemicalMaterials;MinistryofEducationKey
LaboratoryfortheGreenPreparationandApplicationofFunctionalMaterials,HubeiUniversity,Wuhan430062,China;
2.DepartmentofRadiology,UnionHospital,TongjiMedicalCollege,HuazhongUniversityof
ScienceandTechnology,Wuhan430030,China)
AbstractParamagnetic, temperature and pH-sensitive polymeric particles were prepared with N-isopropylacrylamide, methacrylic acid, styrene, and polymerizableGd(AA)3phen·H2O using emulsifier-free emulsion polymerization technique. Dynamic light scattering result shows that the diameter of the polymeric particles changes by about 60 nm as a result of variations in either the temperature or pH, indicating that the particles are pH and temperature-sensitive. TheT1-weighted relaxivity values at 3 T are about 11.3 L/(mmol·s) which is 2.6 times higher than clinical Magnevist®.InvivoMR imaging reveals that the TPRPPs can be effectively imaged in the liver and spleen, suggesting that they are excellent magnetic resonance imaging agents.
KeywordsTemperature and pH-sensitive polymer; Magnetic resonance imaging(MRI); Emulsifier-free emulsion polymerization; Gadolinium contrast agent
(Ed.: W, Z)
† Supported by the National Natural Science Foundation of China(Nos.51273058, 81171386, 81372369).
doi:10.7503/cjcu20150570
基金项目:国家自然科学基金(批准号: 51273058, 81171386, 81372369)资助.
收稿日期:2015-08-20. 网络出版日期: 2015-12-20.
中图分类号O633
文献标志码A
联系人简介:徐祖顺, 男, 教授, 主要从事功能高分子研究. E-mail: zushunxu@hubu.edu.cn
