均匀设计法优选复方天麻钩藤口腔崩解片的半仿生提取工艺
2014-04-11李钦青柴金苗张俊龙
李钦青, 郭 蕾, 柴金苗, 张俊龙
(山西中医学院, 山西 太原 030024)
均匀设计法优选复方天麻钩藤口腔崩解片的半仿生提取工艺
李钦青, 郭 蕾*, 柴金苗, 张俊龙
(山西中医学院, 山西 太原 030024)
目的 均匀设计法优选复方天麻钩藤口腔崩解片半仿生提取 (SBE) 的最佳工艺条件。 方法 采用均匀设计,以天麻素、钩藤总碱、芍药苷、阿魏酸的量及干浸膏得率为指标,综合评判,优选半仿生提取的工艺条件。结果 两次提取用水的 pH分别为2.0、 8.5, 加水倍量为12 倍, 提取时间为2 h。 结论 优选出的半仿生工艺条件稳定、 可行,适合工业生产。
均匀设计;口腔崩解片;半仿生提取
复方天麻钩藤口腔崩解片由天麻、钩藤、白芍、当归等药味组成,为突出剂型特性,保证疗效,以得膏率及天麻素、钩藤总碱、芍药苷、阿魏酸的含量为指标, 在比较传统水煎煮、 70%乙醇回流和半仿生温浸提取3种生产工艺,得出半仿生温浸提取工艺最优的基础上,为进一步优化工艺参数,通过均匀设计综合分析评判,确定最优的提取工艺。
1 药物、 试剂与仪器
天麻素对照品 (110807-200205)、 芍药苷对照品 (110736-200833)、阿 魏 酸 对 照 品 (110773-200611),购自中国食品药品检定研究院; 钩藤碱对照品 (10172-080114) 购自南昌贝塔生物科技有限公司;甲醇、乙腈为色谱纯,水为纯化水,其他试剂均为分析纯。
LC—2010A型高效液相色谱仪 (日本岛津公司); UV1100 型紫外分光光度计 (上海天美科学仪器有限公司); PL6001-S 型电子天平、 AL204 型电子天平、 AB135-S 型电子天平 (METTLER TOLEDO); DZKW-D-4 型电热恒温水浴锅 (上海仪器仪表有限公司); KQ-500E型超声波清洗器 (昆山市超声仪器有限公司)。
2 方法与结果
2.1 实验设计 根据 SBE法理论[1], 在 药材粒度、提取温度、滤过、浓缩等条件相同的前提下,采用均匀设计 U9(91×33) 表, 确定考察的主要因素及水平, 见表1。
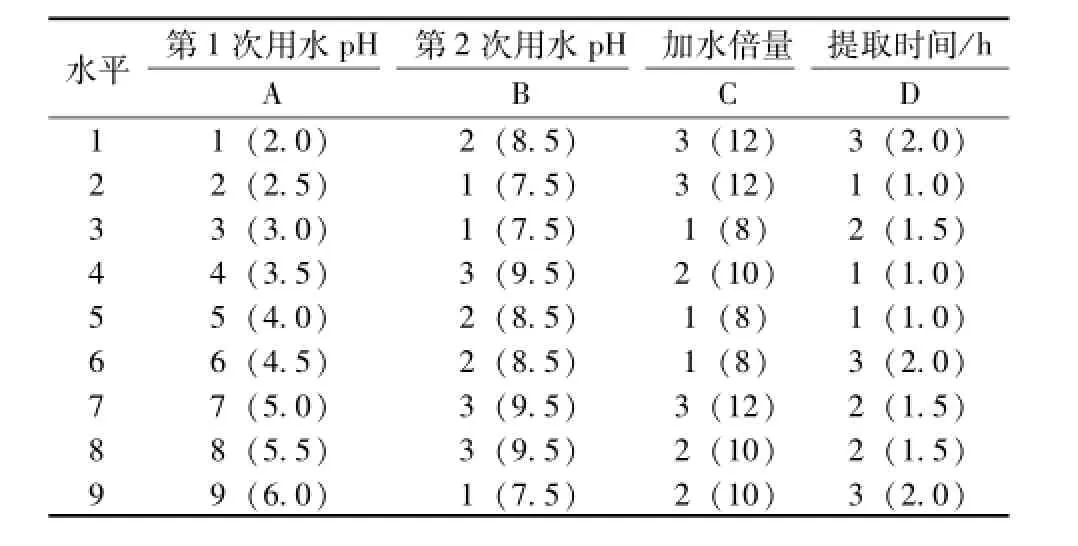
表 1 U9(91×33) 实验设计Tab.1 Experiment design w ith U9(91×33)
2.2 实验方法
2.2.1 样品贮备液的制备 取处方药材, 按均匀设计表安排,分别半仿生温浸提取两次,提取液合并, 调节 pH至近中性, 减压浓缩至相对密度为1.10 ~1.15(60 ℃) 的浸膏, 加乙醇使含醇量达70%, 静置12 h, 滤过, 滤液减压回收乙醇并调整至总量为 1 000 mL, 制得 1 ~9 号样品贮备液。
2.2.2 供试液制备 精密吸取 “2.2.1”项下贮备液 SBE1-9各 10 m L, 分别置蒸发皿中, 水浴浓缩至近干, 残渣加乙腈-水 (3 ∶97) 混合溶液溶解, 转移至 5 mL量瓶中, 并用乙腈-水 (3 ∶97) 混合溶液稀释至刻度,摇匀,即得供测定天麻素含量的供试液 A1~9。
精密量取贮备液 SBE1~9各 10 mL, 水浴挥干,残渣用2%硫酸溶液 10 mL使溶解,滤过, 用 2%硫酸溶液2mL洗涤残渣和滤纸, 再用5mL以上的pH 3.6 的邻苯二甲酸氢钾-盐酸缓冲溶液清洗残渣和滤纸, 合并滤液和洗涤液, 并调 pH至 3.6, 转移至25 mL量瓶中, 用 pH 3.6 的邻苯二甲酸氢钾-盐酸缓冲溶液稀释至刻度,即得供测定钩藤总碱含量的供试液 B1~9。
精密量取贮备液 SBE1~9各 2 mL, 装入 25 mL量瓶,用甲醇稀释并定容至刻度,摇匀,即得供测定芍药苷含量的供试液 C1~9。
精密量取贮备液 SBE1-9各 10 m L, 分别置蒸发皿中,水浴浓缩至近干,残渣用甲醇溶解并转移至10 mL量瓶中, 甲醇定容至刻度, 摇匀, 即得供测定阿魏酸含量的供试液 D1~9。
2.3 天麻素的测定
2.3.1 色 谱 条 件[2]Kromasil C18色 谱 柱 (4.6 mm×250 mm, 5 μm); 流动相为乙腈-0.05%磷酸溶液 (3 ∶97); 检测波长220 nm;柱温 30 ℃;体积流量 1 m L/min; 进样量 10 μL。
2.3.2 对照品溶液的制备 取天麻素对照品适量,精密称定 (11.95 mg), 置 25 mL量瓶中,加甲醇至刻度, 摇匀, 作为贮备液 (0.478 mg/mL); 精密量取 5.0 m L置 25 mL量瓶中, 加流动相至刻度,摇匀,即得天麻素对照品溶液 (天麻素质量浓度为 95.6 μg/mL)。
2.3.3 线性关系考察 分别精密量取 “2.3.2”项下天麻素对照品贮备液 1.0、 2.0、 3.0、 4.0、5.0、 6.0 mL, 分别置于 25 m L量瓶中, 加流动相至刻度, 摇匀。 分别进样 10 μL, 测得峰面积,计算回归方程 y=885 321 x-7 264.9, r=0.999 9,天麻素进样量在0.191 2 ~1.147 2 μg范围内线性关系良好。
2.3.4 精密度试验 精密吸取 “2.3.2”项下天麻素 对 照 品 溶 液 (95.6 μg/mL)10 μL, 按“2.3.1” 项下色谱条件, 连续进样 6 次, 天麻素峰面 积 分 别 为 8 328 763、 8 310 438、 8 343 845、8 264 765、 8 330 487、 8 273 854, 平 均 值 为8 308 692, RSD为 0.39%。
2.3.5 稳定性试验 取 “2.2.2” 项下供试液 A1,分别于 0、 1、 2、 4、 6、 8 h 按 “2.3.1” 项下色谱条件 测 定。 天 麻 素 峰 面 积 分 别 为 8 557 638、8 533 279、8 418 474、8 504 743、8 464 738、8 514 765, 平均值为8 498 939.5, RSD为 0.59%。
2.3.6 重复性试验 取 “2.2.2” 项下供试液 A16 份, 按 “2.3.1”项下色谱条件, 进行测定。 供试液中天麻素质量浓度分别为 97、 97、 96、 97、96、 96 μg/mL, 平 均 质 量 浓 度 为 96.5 μg/mL,RSD为 0.57%。
2.3.7 加样回收试验 精密吸取 “2.2.1” 项下贮备液 SBE16 份, 每 份 5 mL(含天麻素 48.25 μg/mL), 每份分别加入天麻素对照品溶液 (47.8 μg/m L)5 mL按 “2.2.2” 项下天麻素供试液的制备方法平行制备 6 份,按 “2.3.1” 项下色谱条件, 进行含量测定。加样回收率分别为 97.74%、99.23%、 97.21%、 99.05%、 99.67%、 96.39%,平均回收率为 98.215%, RSD为 1.32%。
2.3.8 含量测定 取供试液 A1~9, 用 0.45 μm微孔滤膜滤过,取滤液各 10 μL进样, 结果见表 2。
2.4 钩藤总碱的测定
2.4.1 对照品溶液的制备 取钩藤碱对照品适量,精密称定 (6.92 mg), 置 25 mL量瓶中,加甲醇至刻度,摇匀, 精密量取2.0mL置50mL量瓶中,加甲醇至刻度,摇匀,即得钩藤碱对照品溶液(钩藤碱质量浓度为 11.072 μg/m L)。
2.4.2 线性关系考察[3]分别精密量取 “2.4.1”项下 钩 藤 碱 对 照 品 溶 液 1.0、 2.0、 3.0、 4.0、5.0、 6.0 m L, 挥干甲醇, 残渣加入 pH 3.6 邻苯二甲酸氢钾-盐酸缓冲液 5.0 m L, 再加入溴甲酚绿酸性染料溶液 5.0 mL, 摇匀, 加入三氯甲烷 4 mL,振摇 2 min, 静置 5 min,分出下 层,反复萃 取 3次, 合并三氯甲烷萃取液, 加入 0.4 g无水硫酸钠脱水, 转移至 25 mL量瓶中, 并加三氯甲烷至刻度, 摇匀;另取 1.0 mL蒸馏水如法操作后作为空白对照, 照紫外-可见分光光度法 ( 《中国药典》2010 年版一部部附录 V A), 在 412 nm波长处测定吸光度。 回归方程 为 y=0.008 9 x-0.002 1,r=0.999 1,在 11.072 ~66.432 μg范围内线性关系良好。
2.4.3 精密度试验 精密吸取 “2.4.1” 项下钩藤碱 对 照 品 溶 液 (11.072 μg/m L)5 mL, 按“2.4.2” 项下方法测定, 连续测定 6 次, 吸收度分 别 为 0.497、 0.497、 0.497、 0.497、0.496、0.497, 平均值为0.496 8, RSD为 0.08%。
2.4.4 稳定性试验 取 “2.2.2” 项下供试液 B15 mL, 按 “2.4.2” 项下方法制备样品,分别于 0、0.5、1、 1.5、2、 2.5 h 测 定。吸 收 度 分 别 为0.480、 0.480、 0.479、 0.479、 0.478、 0.477, 平均值为0.478 8, RSD为 0.24%。
2.4.5 重复性试验 取 “2.2.2” 项下供试液 B15 mL, 按 “2.4.2” 项下方法平行制备 6 份供试品液,并测定。供试液中钩藤总碱质量浓度分别为51、 51、 52、 50、 50、 51 μg/mL, 平均质量浓度为 50.83 μg/mL, RSD为 1.48%。
2.4.6 加样回收试验 精密吸取 “2.2.1” 项下贮备液 B16 份, 每份 2 m L(含钩藤总碱 590.83 μg/mL), 每 份 分 别 加 入 钩 藤 碱 对 照 品 溶 液(55.36 μg/mL)2mL, 按 “2.4.2” 项下方法平行制备6份供试品液,并测定。加样回收率分别为95.82%、 98.29%、 95.21%、 99.88%、 98.85%、96.12%, 平 均 回 收 率 为97.378%, RSD为 1.96%。
2.4.7 含量测定 取供试液 B1~9, 按 “2.4.2”项下方法测定, 结果见表2。
2.5 芍药苷的测定
2.5.1 色 谱 条 件[4]Kromasil C18色 谱 柱 (4.6 mm×250 mm, 5 μm); 流动相为乙腈 -0.1%磷酸溶液 (14 ∶86); 检测波长为 230 nm; 柱温 25 ℃;体积流量 1 m L/min; 进样量 10 μL。
2.5.2 对照品溶液的制备 取芍药苷对照品适量,精密称定 (10.60 mg), 置 25 mL量瓶中,加甲醇至刻度, 摇匀, 作为贮备液 (0.424 mg/m L); 精密量取2.0 mL置 25 mL量瓶中, 加甲醇至刻度,摇匀,即得芍药苷对照品溶液 (芍药苷质量浓度为 33.92 μg/mL)。
2.5.3 线性关系考察 分别精密量取 “2.5.2”项下芍药苷对照品贮备液 1.0、 3.0、 5.0、 7.0、9.0 mL,分别置于 25 mL量瓶中,加甲醇至刻度,摇匀。 分别进样 10 μL, 测得峰面积, 计算回归方程 y=1 491 458.2x+6 075.8, r=0.999 9, 芍药苷进样量在0.169 2 ~1.526 4 μg范围内线性关系良好。
2.5.4 精密度试验 精密吸取 “2.5.2”项下芍药苷 对 照 品 溶 液 (33.92 μg/mL)10 μL, 按“2.5.1” 项下色谱条件, 连续进样 6 次, 芍药苷峰 面 积 分 别 为 507 354、506 947、 508 543、505 440、 504 686、 509 831, 平均值为507 133.5,RSD为 0.38%。
2.5.5 稳定性试验 取 “2.2.2” 项下供试液 C1,分别于 0、 1、 2、 4、6、 8 h 按 “2.5.1” 项下色谱条件 测 定。芍 药 苷 峰 面 积 分 别 为 557 785、559 658、 556 833、 552 542、 558 314、 551 771,平均值为 556 150.5, RSD为 0.58%。
2.5.6 重复性试验 取 “2.2.2” 项下供试液 C16份供试品液, 按 “2.5.1”项下色谱条件, 进行测定。 供试液中芍药苷含有量分别为 37、 37、 37、38、 37、 37 mg/m L, 平 均 质 量 浓 度 为 37.167 μg/mL, RSD为 1.10%。
2.5.7 加样回收试验 精密吸取 “2.2.1” 项下贮备液 SBE16 份, 每份 1 m L(含芍药苷464.587 5 μg/mL), 每份分别加入芍药苷对照品溶液 (424 μg/mL)1 mL按 “2.2.2” 项下芍药苷供试液的制备方法平行制备 6 份,按 “2.5.1” 项下色谱条件, 进行含量测定。 加样回收率分别为 95.77%、99.69%、 98.59%、 98.08%、 97.85%、 96.01%,平均回收率为 97.665%, RSD为 1.55%。
2.5.8 含量测定 取供试液 C1~9, 用 0.45 μm微孔滤膜滤过, 取滤液各 10 μL进样, 结果见表 2。
2.6 阿魏酸的测定
2.6.1 色 谱 条 件[5]Kromasil C18色 谱 柱 (4.6 mm×250 mm, 5 μm); 流动相乙腈 -0.1%磷酸溶液 (17:83); 检测波长 316 nm; 柱温 35 ℃; 体积流量 1 m L/min; 进样量 10 μL。
2.6.2 对照品溶液的制备 取阿魏酸对照品适量,精密称定 (10.10 mg), 置 100 mL量瓶中, 加甲醇至刻度, 摇匀, 作为贮备液 (0.101 mg/mL);精密量取3.0 m L置50 m L量瓶中, 加甲醇至刻度,摇匀,即得阿魏酸对照品溶液 (阿魏酸质量浓度为 6.06 μg/mL)。
2.6.3 线性关系考察 分别精密量取 “2.6.2”项下阿魏酸对照品贮备液 1.0、 3.0、 5.0、 7.0、9.0 mL,分别置于 50 mL量瓶中,加甲醇至刻度,摇匀。 分别进样 10 μL, 测得峰面积, 计算回归方程 y=4 054 482.7x-168 9.8, r=0.999 9, 阿魏酸进样量在0.020 2 ~0.181 8 μg范围内线性关系良好。
2.6.4 精密度试验 精密吸取 “2.6.2”项下阿魏酸 对 照 品 溶 液 (6.06 μg/mL)10 μL, 按“2.6.1” 项下色谱条件, 连续进样 6 次, 阿魏酸峰 面 积 分 别 为 242 523、244 061、 244 795、243 794、 244 850、 243 103, 平均值为 243 854.3,RSD为 0.38%。
2.6.5 稳定性试验 取 “2.2.2” 项下供试液 D1,分别于 0、 1、 2、 4、6、 8 h 按 “2.6.1” 项下色谱条 件 测 定。阿 魏 酸 峰 面 积 分 别 为 250 835、251 479、250 632、249 260、247 094、248 758,平均值为249 676.3, RSD为 0.65%。
2.6.6 重复性试验 取 “2.2.2” 项下供试液 D16 份供试品液, 按 “2.6.1” 项下色谱条件, 进行测定。 供试液中阿魏酸含量分别为 6.25、 6.24、6.39、 6.20、6.26、6.31 μg/mL, 平均质量浓度为 6.275 μg/mL, RSD为 1.06%。
2.6.7 加样回收试验 精密吸取 “2.2.1” 项下贮备液 SBE16 份, 每 份 5 mL( 含阿魏酸 6.275 μg/mL), 每 份 分 别 加 入 阿 魏 酸 对 照 品 溶 液(6.06μg/m L)5 mL按 “2.2.2” 项下阿魏酸供试液的制备方法平行制备 6 份, 按 “2.6.1” 项下色谱条件,进行含量测定。加样回收率分别为99.90%、 97.99%、 97.09%、 95.67%、 96.67%、98.64%, 平均回收率为 97.66%, RSD为 1.54%。
2.6.8 含量测定 取供试液 D1~9, 用 0.45 μm微孔滤膜滤过,取滤液各 10 μL进样, 结果见表 2。
2.7 干浸膏量的测定 精密量取 “2.2.1” 项下贮备液 SBE1~9各 10 mL, 分别置恒定质量的蒸发皿中, 水浴蒸干, 105 ℃烘干 3 h 以上至恒质量[2],计算干浸膏得率, 结果见表2。
2.8 工艺条件的优化[3]将天麻素、 钩藤总碱、芍药苷、阿魏酸、得膏率等5项指标汇总按下列公式进行标 准 化 处 理/sj式 中为 标准化后的值,xij为样品液 i中成分 j的含量,为各种样品液 i中成分 j的平均值, sj为成分 j的标准偏差。将标准化后的值根据各指标在工艺选择中的主次,给予不同的加权系数,得综合评价指标Y值,Y= [ (天麻素 +芍药苷 +阿魏酸) ÷3] ×5+钩藤总碱 ×3+干浸膏 ×2, 结果见表 2。
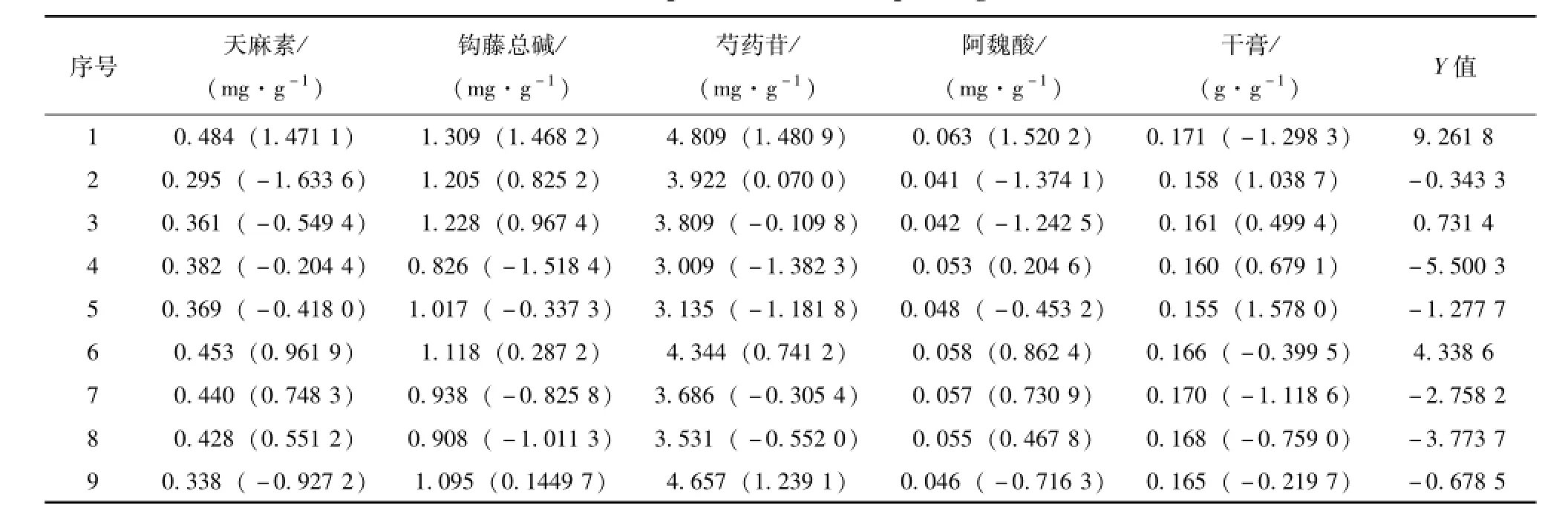
表2 各指标成分含量、 标准化处理结果Tab.2 Values of the samples and the corresponding standardized values
将以上结果输入计算机,用沈阳药科大学编写的均匀设计软件处理,进行平方项的逐步回归,得回 归 方 程:F=-210.85+50.233B+ 0.024 286AC-0.946 08 AD-0.232 92 BC+ 1.206 3BD-2.983 2 B2+0.104 09D2,F(7,1)= 3.843 ×105, 查 F值表 F0.05(7,1)=236.8, F0.05(7,1)<F, P<0.05, 所以 F检验通过, 回归方程有意义。再将方程在计算机上进行优化处理,Y的期望值方向大者为佳。得出的优化条件为 A=2.0,B= 8.355 3, C=12, D=2, (预测值 Y=9.322 0)。结合生产实际,确定复方天麻钩藤口腔崩解片半仿生法提取的工艺条件为两煎用水 pH分别为 2.0、8.5;加水倍量为 12 倍;提取时间为 2 h。
2.9 验证优化条件 用 “2.8” 项下优选出的工艺条件, 照 “2.2 ~2.7” 项下样品制备和测定方法,依法测得各指标含量,并将进行数据标准化处理, 求得 Y'值, 所得 Y'值 9.488 非常接近预测值Y=9.322 0, 结果见表 3。

表3 验证实验各指标成分的含量、标准化处理结果Tab.3 Values of the sam p les and the corresponding standardized values in confirm atory experiment
3 讨论
半仿生法是从生物药剂学角度模拟口服给药时药物经过胃肠道消化吸收的过程,为中药制剂设计的一种新的提取工 艺[6-7], 用选定 pH 值 的 酸 性 水和碱性水依次连续提取得到含指标成分高的 “活性混合物”。本方药味较少,应根据各成分理化性质,设计适宜生产工艺,去除杂质,保留活性成分,方中钩藤生物碱受热易破坏,不宜高温煎煮提取,半仿生温浸提取既保留了活性部位钩藤总碱,又保证了其他活性成分的转移率。
在均匀设计优选工艺中,按照各指标在提取工艺选择中的主次地位,给予不同的加权系数,以标准化后的值加权后求和,即得综合评价值。这样做可以消除各指标之间的单位和量纲的不同,提高了组间综合评判数据的相关性和可比性,更科学、合理。
[1] 彭 英,凯赛尔,霍仕霞,等.均匀设计优选驱白巴布期胶囊半仿生提取法工艺[J].中国中医药信息杂志, 2011,18(9):59-61.
[2] 蔡梅超,徐 男,张 超,等.半夏白术天麻汤方药用半仿生提取法工艺条件优选[J].中国实验方剂学杂志,2011, 17(19):21-25.
[3] 曾长青, 罗北亮.酸性染料比色法测定钩藤的总生物碱含量[J].中药材, 2007, 30(8):1021-1024.
[4] 李 芳,张兆旺,孙秀梅,等.均匀设计法优选桂枝茯苓丸方药的半仿生提取工艺条件[J].中国中药杂志, 2010,35(16):2151-2156.
[5] 阿古拉,张兆旺,孙秀梅.用均匀设计优选慈航软胶囊方药的半仿生提取工艺条件[J].中成药, 2006, 28(7): 956-958.
[ 6 ] 张兆旺, 孙秀梅.“半仿生提取方法” 的特点与应用[J].世界科学与技术-中药现代化, 2000, 1(2):35.
[7] 张瑞亭,张兆旺, 孙秀梅,等.思维方式的转换与中药“半仿生提取法” [J].中国中药杂志, 1997, 22(9):542-545.
Optim ization of extraction for decoction of Fufang Tianm a Gouteng Orally Disintegrating Tablets by sem i-bionic extraction
LIQin-qing, GUO Lei*, CHAI Jin-miao, ZHANG Jun-long
(Shanxi University of Traditional Chinese Medicine, Taiyuan 030024, China)
uniform design; orally disintegrating tablets; semi-bionic extraction
R944
:A
:1001-1528(2014)02-0291-05
10.3969/j.issn.1001-1528.2014.02.016
2013-05-07
国家自然科学基金资助项目 (30873236); 太原市科学技术局资助项目 (11014918)
李钦青 (1978—) , 男, 助教, 医学硕士, 从事中药药效物质及新药研究。 Tel:(0351)2272269, E-mail:lqqlqq@126.com
*通信作者: 郭 蕾 (1968—), 女, 教授, 医学博士, 从事于中医基础理论的研究。 Tel:(0351)2272664, E-mail:glqzl123@163.com
