顶空气相色谱法测定阿齐沙坦酯原料药中有机残留溶剂的残留量*
2013-04-18王家明
苏 旭,王家明
(1.天津市中心妇产科医院,天津 300100; 2.工业发酵微生物教育部重点实验室,天津科技大学生物工程学院,天津 300457)
阿齐沙坦酯(azilsartan medoxomil,TAK-491),是由日本武田公司开发的新一代选择性 AT1亚型血管紧张素Ⅱ受体拮抗剂,为阿齐沙坦(azilsartan)的前药,临床前和临床研究证实其有平稳持久的抗高血压作用。 2011年2月美国FDA批准阿齐沙坦酯(商品名为Edarbi)用于治疗成人高血压。临床前研究显示,阿齐沙坦酯作为新一代双重功能ARBs不仅拮抗血管紧张素Ⅱ的1型受体(AT1受体),还可能通过多种机制降低心血管疾病及糖尿病的风险[1]。在产品生产过程中,需要用到甲醇、乙醇、异丙醇、二氯甲烷和乙酸乙酯5种有机溶剂,这些溶剂会对人体健康造成危害,在生产过程中完全去除比较困难,但必须确保产品中的这些溶剂残留量是人体可以接受的,《中国药典》和ICH对各类溶剂残留量有严格的规定[2, 3]。
本实验首次建立了毛细管柱顶空气相色谱法,测定阿齐沙坦酯工艺中用到的5种溶剂,并进行了方法学研究。结果显示,该方法准确,灵敏度高,可用于阿齐沙坦酯原料药中残留溶剂的检测。
1 仪器与试药
HP 6890N 气相色谱仪(Agilent公司),7694E 顶空进样器(Agilent公司),Agilent气相工作站(Agilent公司)。甲醇、乙醇、异丙醇、二氯甲烷、乙酸乙酯均购买于天津康科德试剂公司。阿齐沙坦酯原料药(中央药业提供,批号20121203、20121204、20121205),水为纯净水。
2 方法与结果
2.1色谱条件与系统适应性 DB-624毛细管柱(30.0 m×0.53 mm×3.00 μm)(6%氰丙基苯-94%二甲基硅氧烷共聚物),50 ℃维持10 min,载气N2,流速4.0 ml/min。7694E顶空瓶进样器,进样体积1 μl,进样口温度为200 ℃,分流比为5∶1;顶空瓶温度80 ℃,定量环温度90 ℃,传输管线温度100 ℃/瓶,加热时间20 min,顶空瓶体积10 ml,加入被测液体1 ml,加盖密封。火焰离子化检测器(FID)温度250 ℃,氢气流速 40 ml/min,空气流速 400 ml/min,尾吹30 ml/min。
2.2溶液制备
2.2.1对照储备溶液的配制 分别精密移取甲醇71 μl、乙醇119 μl、异丙醇119 μl、二氯甲烷9 μl和乙酸乙酯104 μl到装有适量水的50 ml量瓶中,用水稀释至刻度,混匀。
2.2.2对照溶液的配制 吸取上述对照储备溶液1 ml置25 ml量瓶中,用水稀释到刻度,混匀。残留限度见表1。

表1 溶剂残留限度表
2.3空白溶剂试验 取3 ml水置顶空瓶中,加盖密封,顶空进样测定,记录色谱图。结果表明:空白溶剂对甲醇、乙醇、异丙醇、二氯甲烷和乙酸乙酯的测定不干扰。色谱图见图1。
2.4专属性试验 精密量取上述对照溶液,按上述色谱条件进样测定,出样顺序:甲醇(RT=2.670)、乙醇(RT=3.381)、异丙醇(RT=4.020)、二氯甲烷(RT=4.489)、乙酸乙酯(RT=6.950)。5个成分之间分离度均大于3.0,且理论塔板数均大于10 000, 对称性好,色谱图见图1。
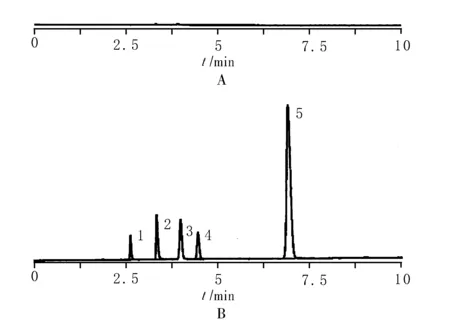
1. 甲醇 2. 乙醇 3. 异丙醇 4. 二氯甲烷 5. 乙酸乙酯
2.5检测限试验 分别精密移取甲醇70 μl、乙醇20 μl、异丙醇20 μl、二氯甲烷3 μl和乙酸乙酯6.8 μl到装有适量水的50 ml量瓶中,用水稀释至刻度,混匀;精密量取此液10 μl置25 ml量瓶中,用水稀释到刻度。在本试验条件下,各色谱峰响应值约为基线噪音的3倍。甲醇、乙醇、异丙醇、二氯甲烷和乙酸乙酯的最低检测浓度分别为0.4435、0.1264、0.1256、0.0318和0.048 96 μg/ml。
2.6线性关系测定 分别移取对照贮备液0.4、0.8、1.0、1.2和1.8 ml置25 ml量瓶中,用水稀释到刻度,混匀,配成不同浓度的测试溶液;分别取各溶液3 ml置10 ml顶空瓶中,加盖密封,依次进样测定。分别以色谱峰面积(Y)为纵坐标,以各自的浓度X(mg/ml)为横坐标,进行线性回归。结果见表2。
2.7精密度试验 取对照溶液3 ml置10 ml顶空瓶中,加盖密封。依次连续进样测定,以峰面积计算,对照溶液中甲醇、乙醇、异丙醇、二氯甲烷和乙酸乙酯峰面积的RSD分别为1.93%、2.83%、3.94%、8.05%和4.29%。
2.8稳定性试验 分别于0、2、6、8和24 h取标准溶液3 ml置10 ml顶空瓶中,加盖密封,顶空进样测定,记录色谱图。计算各溶剂峰面积的RSD。甲醇、乙醇、异丙醇、二氯甲烷和乙酸乙酯色谱峰积分面积的RSD分别为2.14%、3.76%、5.19%、18.89%和7.64%,表明甲醇、乙醇、异丙醇、乙酸乙酯对照溶液在24 h内基本稳定,二氯甲烷对照溶液在24 h内不稳定。

表2 线性关系试验结果
2.9回收率试验 分别移取对照贮备液0.8、1.0和1.2 ml到25 ml量瓶中,用水稀释到刻度,摇匀,配成三种浓度的回收率溶液(80%、100%和120%)。取20121203批样品45 mg共9份,精密称定,分别加入上述溶液3 ml,密封后混匀,进行测定。结果见表3。甲醇的平均回收率为103.96%,RSD为2.66%;乙醇的平均回收率为97.51%,RSD为3.71%;异丙醇的平均回收率为101.19%,RSD为4.75%;二氯甲烷的平均回收率为95.06%,RSD为6.99%;乙酸乙酯的平均回收率为97.50%,RSD为6.18%。
2.10样品测定 分别取20121203、20121204和20121205批样品,精密称取45 mg到顶空瓶中,加水3 ml溶解,加盖密封,按上述色谱条件以外标法进行测定。结果见表4。
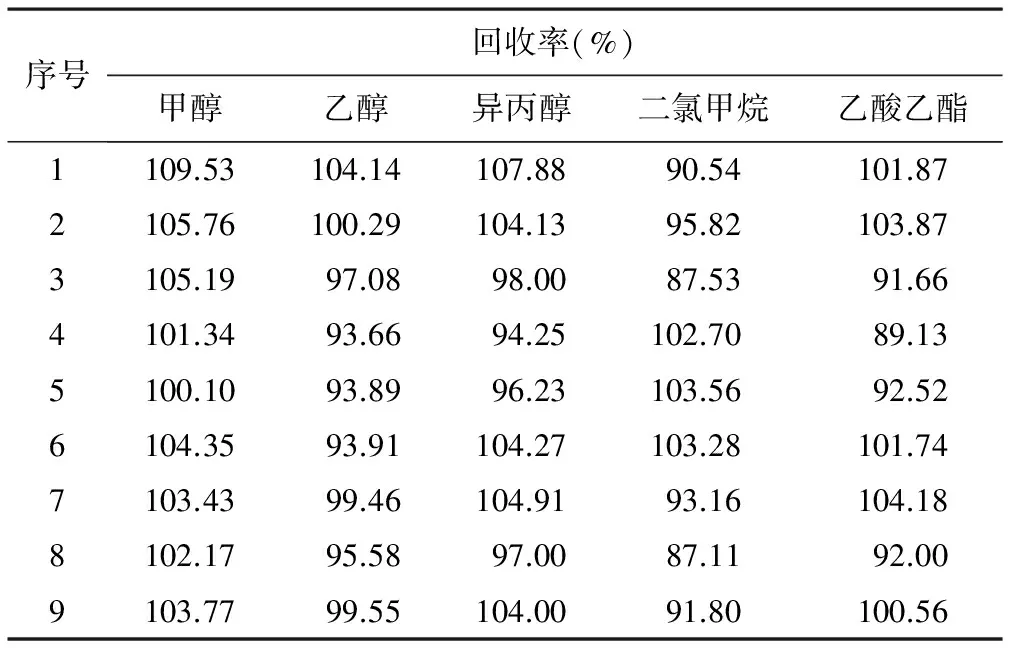
表3 回收率试验结果

表4 样品测定结果
3 讨论
本文首次采用顶空气相色谱法对阿齐沙坦酯原料药的5种残留溶剂进行检测。方法验证证明:该方法色谱条件分离良好,灵敏度高,在考查的浓度范围内线性关系良好(r>0.999),回收率符合规定,符合《中国药典》 2010版附录Ⅷ P中有机溶剂残留量测定的要求,可以作为阿齐沙坦酯原料药中残留溶剂的质量控制方法。
1 张亚安.抗高血压新药选择性AT1亚型血管紧张素Ⅱ受体拮抗剂—阿齐沙坦酯[J]. 药学与临床研究,2011, 19(3):262
2 中国药典[S]. 二部. 2010: 附录61
3 周海钧. 药品注册的国际技术要求(质量部分)[M]. 北京: 人民卫生出版社, 2001: 82
