液相色谱-串联质谱法测定乳制品中四种常用香料
2021-11-23林正锋李实飞黄杰英禤开智王朝政
林正锋,李实飞,黄杰英,禤开智,王朝政
(海口海关技术中心,海南海口 570311)
乳制品是非常重要的营养补充,是日常饮食的重要组成部分,对增强国民身体素质具有重要的意义,尤其是婴幼儿乳粉作为婴幼儿阶段的主要营养来源,更是人们关注的重点[1−2]。香兰素和乙基香兰素具有强烈的奶香味,麦芽酚和乙基麦芽酚是广谱香味增效剂,此四种香料广泛用于各种具有奶香味的食品中[3−5]。乳制品中添加食用香精香料可以提高食品的风味,但长期食用添加香精的奶粉可能使新生儿对其产生依赖性,过量摄入会引发潜在的健康问题[6−7],因此香精香料的超范围及过量使用问题日益引起人们的关注[8−9]。国家卫计委发布实施的GB 2760-2014 《食品添加剂使用标准》中明确指出不得添加食用香料、香精有27 种食品,其中包括巴氏杀菌乳、灭菌乳、发酵乳、无水黄油、稀奶油和婴幼儿配方乳粉等多种乳制品[10]。因此,建立灵敏度高、准确可靠的乳制品中4 种常用香料的检测方法对乳制品质量安全监管具有重要意义。
目前,此四种化合物同时检测的方法主要有分光光度法[11],高效液相色谱法(high performance liquid chromatography, HPLC)[12−13],二维液相色谱法(two-dimensional liquid chromatography, 2DLC)[14],气相色谱-质谱法(gas chromatography-mass spectrometry, GC-MS)[15],液相色谱-串联质谱法(liquid chromatography-tandem mass spectrometry, LCMS/MS)[16−17]等。其中,分光光度法和液相色谱法检测限较高,多种乳制品中要求不得添加食用香精,较高的检测限可能会导致低含量的添加样品无法检出;气相色谱-质谱法分析时间较长;液相色谱-串联质谱法具有灵敏度高、特异性强、分析速度快等优点,广泛应用于食品中香料物质的检测[18−19]。然而,在LCMS/MS 分析中,基质效应严重影响定量分析的准确度和精密度,目前文献报道LC-MS/MS 测定乳粉中四种常用香料化合物均存在较强的基质效应,需采用基质匹配曲线或者内标法进行定量分析[16−17],大大增加了检测成本,此外,前处理过程需要对净化液进行浓缩,而挥发性较强的香料化合物在浓缩过程中易损失[20−21]。受酚类化合物可采用酸碱分配法净化的启发[22−23],本文采用水-醚体系对乳制品样品进行提取,经碱液反萃除去杂质后采用高灵敏度高选择性的液相色谱串联质谱分析四种化合物。通过研究不同比例碱醚比的碱液反萃醚相中的香料化合物,实现样品净化和富集同步进行,整个过程无需氮吹浓缩,避免挥发性较强的香料化合物在氮吹浓缩过程中损失,以期建立一种灵敏度高、简便快捷、准确可靠的乳制品中四种常用香料的检测方法,为相关部门建立相关测定标准提供参考,保障乳制品的质量安全。
1 材料与方法
1.1 材料与仪器
甲醇、乙腈、叔丁基甲醚 色谱纯,美国TEDIA 公司;甲酸 色谱纯,德国CNW 公司;盐酸、氢氧化钠、氨水、无水硫酸钠 分析纯,广州化学试剂厂;麦芽酚(纯度≥99%)、乙基麦芽酚(纯度≥99%)、香兰素(纯度≥98%)、乙基香兰素(纯度≥98%) 美国Sigma 公司;乳制品样品(包括婴幼儿配方乳粉、炼奶、黄油、奶酪、鲜牛奶、纯牛奶、稀奶油、酸奶等共15 份) 均购自海口市本地大型超市。
色谱柱:HSS T3 色谱柱(100 mm×2.1 mm,2.5 μm) 、 BEH C18色谱柱( 100 mm×2.1 mm,1.7 μm)、HLB 固相萃取柱(100 mg, 3 mL)、TQD 超高效液相色谱-质谱联用仪 美国Waters 公司;PXA 固相萃取柱(150 mg, 6 mL) 迪马公司;KQ3200DE 超声波清洗器 昆山市超声仪器有限公司;MS3 涡旋仪 德国IKA 公司;320 R 低温离心机德国Hettich 公司;Advantage A10 超纯水净化仪美国Millipore 公司;Genevac EZ-2 型溶剂蒸发工作站 英国SP Scientific 公司。
1.2 实验方法
1.2.1 样品前处理 奶粉、奶酪、炼奶、黄油等类固体乳制品:称取2 g 试样(精确至0.01 g),置于50 mL聚丙烯离心管中,加入5 mL 50 ℃的水(黄油样品置于100 ℃烘箱中加热使之溶解,炼奶用4 mL 水溶解),3000 r/min 涡旋混匀2 min,40 ℃下超声提取15 min,超声频率为37 kHz,再加入20 mL 叔丁基甲醚,3000 r/min 涡旋混匀3 min, 再加入10 g 无水硫酸钠除水,3000 r/min 涡旋混匀2 min,9000 r/min离心3 min,吸取上清液10 mL 转移至另一离心管中,再加入2 mL 0.2 mol/L 氢氧化钠溶液反萃,3000 r/min 涡旋混匀1 min 后,3000 r/min 离心3 min,用移液器准确移取下层清液0.9 mL 至刻度试管中,加甲酸定容至1.0 mL 过0.22 μm 微孔滤膜,供液相色谱-质谱测定。
过柱净化富集过程:吸取上清液5 mL 转移至另一离心管,加入5 mL 0.2 mol/L 氢氧化钠溶液反萃,去掉上清液,40 ℃下用 Genevac EZ2 溶剂蒸发工作站浓缩20 min,除去微量的叔丁基甲醚。
HLB 过柱方法:除醚后用盐酸调节pH 至3.0,先后加入3 mL 甲醇,3 mL 超纯水活化固相萃取柱,然后全部上样,样液体积约为4.5 mL,重力过柱后,用5 mL 纯水淋洗,弃去淋洗液,接着用5 mL 注射器抽干,最后用1 mL 甲醇洗脱。
PXA 过柱方法:先后加入3 mL 甲醇,3 mL 超纯水活化固相萃取柱,然后全部上样,样液体积约为4.5 mL,重力过柱后,分别用3 mL 5%氨水甲醇和3 mL 甲醇淋洗,抽干,最后用1 mL 5%甲酸甲醇洗脱。
巴氏杀菌乳、灭菌乳、发酵乳、稀奶油等液体乳制品,直接称取5 g 试样于50 mL 聚丙烯离心管中,再加入20 mL 叔丁基甲醚提取,后处理步骤同奶粉等样品。
1.2.2 色谱-质谱条件 色谱柱:HSS T3 色谱柱(100 mm×2.1 mm, 2.5 μm, Waters);流速:0.4 mL/min;进样体积:3 μL;柱温:30 ℃;流动相,A 相为甲醇,B 相为0.05%甲酸水,梯度洗脱程序为0~1.0 min,10%~25%A, 1.0~5.0 min, 25%A, 5.0~5.1 min,25%~60%A,5.1~6.0 min,60%A,6.0~6.1 min,60%~90%A, 6.1 ~7.0 min, 90%A, 7.0~7.1 min, 90%~10%A,7.1 ~8.0 min,10%A。
MS 条件:电喷雾正离子源(ESI+),毛细管电压:3.0 kV,离子源温度:150 ℃,脱溶剂管温度:350 ℃,雾化气:150 L/h 氮气,干燥气:650 L/h 氮气,碰撞气:氩气。扫描模式:多反应监测模式(MRM),具体条件见表1,带星号离子为定量离子。

表1 四种化合物保留时间及质谱参数Table 1 Retention times and mass spectrum parameters for 4 compounds
1.3 数据处理
通过Masslynx 工作站及数据处理系统采集分析质谱图,外标法定量。实验结果采用平均值表示,每个实验平行三次,采用Excel 2010 进行数据处理。
2 结果与分析
2.1 色谱-质谱条件的优化
配制1 μg/mL 的混合标准溶液于进样瓶中,采用仪器自动进样进入质谱仪,在Masslynx 软件中设置质谱条件,并对标准液进行离子调谐,根据响应稳定、信号强度较高、干扰少的碎片确定定量离子对和定性离子对,具体参数见表1。
本文比较了HSS T3 色谱柱和BEH C18色谱柱对四种化合物的分离效果,两种色谱柱对四种化合物的分离效果见图1。由图1 可以看出,HSS T3 色谱柱对四种化合物的分离效果明显优于BEH C18色谱柱,且峰形良好。尤其是对于麦芽酚和乙基麦芽酚的峰形和响应有很好的改善作用,这是由于T3 色谱柱可以更好地保留麦芽酚等极性较大的化合物。杨华梅等[16]采用BEH C18色谱柱分离四种化合物时存在香兰素和乙基麦芽酚保留时间重叠严重的现象,而林仙军等[24]采用HSS T3 色谱柱分离乙基麦芽酚和香兰素时,两种化合物可实现基线分离且峰形较好。考察了水-乙腈和水-甲醇流动相体系对四种化合物的分析效果影响,发现以水-甲醇作为流动相时,四种化合物的响应明显优于水-乙腈流动相体系。并在此基础上考察了甲醇-水、甲醇-0.05%甲酸水、甲醇-0.1%甲酸水对色谱峰的影响,发现添加甲酸后,质谱响应增强,0.05%甲酸水和0.1%甲酸水响应无明显差别,故最终采用甲醇-0.05%甲酸水作为流动相,在此条件下,四种化合物色谱图见图1B。

图1 两种色谱柱分离效果比较Fig.1 Comparison of separate effect of two kinds of chromatographic columns
2.2 净化富集方法的选择
为了提高方法检出限和准确度,需要对提取液进行富集及净化,本文采用富集倍数同为5 倍的4 种方式对空白加标样品进行处理,分别为:a.取5 mL叔丁基甲醚直接吹干后定容上机分析;b.取5 mL 叔丁基甲醚用5 mL 碱液反萃后调节pH 用HLB 富集;c.取5 mL 叔丁基甲醚用5 mL 碱液反萃后用PAX富集;d.取5 mL 叔丁基甲醚用1 mL 碱液反萃后调酸上机分析;结果发现,四种香料化合物在氮吹的过程中均有一定程度的损失,尤其是香兰素和麦芽酚回收率低于80%。采用固相萃取柱富集时,微量的叔丁基甲醚会造成目标物大量损失,即使采用真空除去叔丁基甲醚后,麦芽酚回收率仍低于80%难以满足要求。而采用碱液和叔丁基甲醚比例为1:5 进行反萃时四种化合物的回收率均大于90%,故最终采用的净化富集方式为碱液反萃。不同处理下四种化合物回收率见表2。

表2 不同净化富集方式四种香料化合物回收率Table 2 Recoveries of four flavor compounds by different purification and enrichment methods
麦芽酚、乙基麦芽酚、香兰素和乙基香兰素均呈弱酸性,在高碱性条件下能形成离子状态,使其在水中溶解性大大提高,可从醚相中提取出来[25]。考察了在不同碱液和叔丁基甲醚比例下,四种化合物的回收率和基质效应,由图2 可以看出,当碱液和叔丁基甲醚比例低于1:5 时,四种化合物回收率超过90%,而碱液和叔丁基甲醚比例达到1:10 时,麦芽酚和乙基麦芽酚回收率大大降低。以阴性的奶粉基质按照方法进行提取,按相应的碱醚比例反萃得到的基质液配制50 ng/mL 浓度的标准品与纯溶剂配制的50 ng/mL混合标准品的响应值进行比较考察其基质效应,基质效应(ME)=阴性样品基质添加标准溶液的色谱峰面积/纯溶剂配制标准溶液的峰面积)×100[26]。结果表明,随着碱醚比例的降低,基质效应逐渐减弱,说明减少碱醚体积比可以有效去除杂质,当碱醚比例为1:1 和1:3 时,麦芽酚存在较强的基质抑制效应,而当碱醚比低于1:5 时,各项目的基质效应均在80%~100%之间。为获得最大的富集倍数,提高方法的灵敏度,同时保证较好的回收率,最终采用碱液和叔丁基甲醚比例为1:5 进行反萃,可实现5 倍富集并获得良好的净化效果。
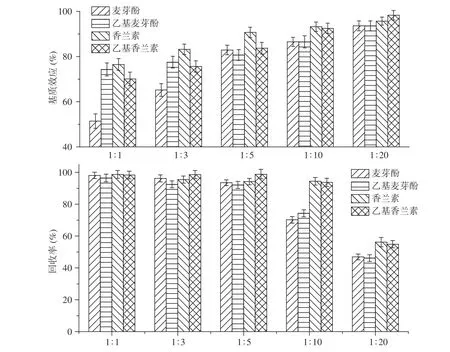
图2 不同碱醚比例碱液萃取时目标物的回收率和基质效应Fig.2 Recoveries and matrix effects of target compounds using different ratios of alkali solution and MTBE
2.3 线性范围和定量限
将混合标准溶液配制成系列标准溶液,(浓度范围为2~100 ng/mL),在本方法所确定的实验条件下进行分析,以定量离子峰面积为纵坐标,标准工作液浓度为横坐标作图建立标准曲线,四种化合物线性方程见表3,结果表明,四种化合物在2~100 ng/mL 范围内线性决定系数均大于0.995。根据3 倍信噪比,并计入试样量和定容体积,计算检出限(limit of detection, LOD),定量限(limit of quantity, LOQ)则根据10 倍信噪比计算,结果见表3,从表3 中可以看出,乳粉等固体样品中麦芽酚和乙基香兰素定量限为2 μg/kg,乙基麦芽酚定量限为4 μg/kg,香兰素定量限为8 μg/kg,均低于10 μg/kg。

表3 四种化合物线性回归方程、相关系数、检出限和定量限Table 3 Linear regression equation, correlation coefficient, LOD and LOQ of 4 compounds
2.4 基质效应
采用液质联用分析复杂基质时通常存在基质效应,基质效应对检测结果有重要影响[27],因此需要考察本方法的基质效应。本实验以阴性的8 种基质按照方法分别进行提取净化,用得到的净化液配制50 ng/mL 的标准品,每种做3 个平行,将得到的响应值的平均值和纯溶剂配制的50 ng/mL 混合标准品的响应值进行比较,通过二者比值来评价基质效应,得出目标化合物在8 种基质中的基质效应。四种化合物在各种乳制品中的基质效应在80%~100%的范围内,具体结果见表4。说明乳制品基质对四种化合物存在微弱的基质抑制效应,实际检测过程中可采用溶剂配制曲线直接定量[26]。本方法基质效应低于水体系提取固相萃取柱净化方法[16−17],说明前处理取得了很好的净化效果。这主要是因为加入大量的硫酸钠形成盐析使蛋白质沉淀,通过碱液反萃可有效去除脂肪等不溶于碱性水溶液的有机化合物杂质[22−23],从而明显降低基质效应,有助于更准确地定量。

表4 四种化合物在不同乳制品中的基质效应Table 4 Matrix effects of 4 compounds in different dairy products
2.5 加标回收实验
在上述确定的色谱条件和前处理条件下,在未标注添加食用香精的不同基质中添加三个不同浓度水平的香料进行添加回收实验,其平均回收率与精密度见表5,从表5 可以看出,四种化合物在各基质中三种浓度水平下,相对标准偏差在2.5%~11.9%,除炼奶和黄油外,其它基质中平均回收率在80.4%~104.8%之间,加标回收率和精密度均符合GB/T 27404-2008[28]的要求,整个结果表明本方法检测稳定性较好。炼奶和黄油的回收率相对偏低,平均回收率在67.7%~84%之间,可能是由于炼奶基质较为粘稠,提取效率低,而黄油在加热溶解过程中易造成目标物的损失,此两种乳制品中四种香料化合物的测定应采用基质标准溶液进行校正。
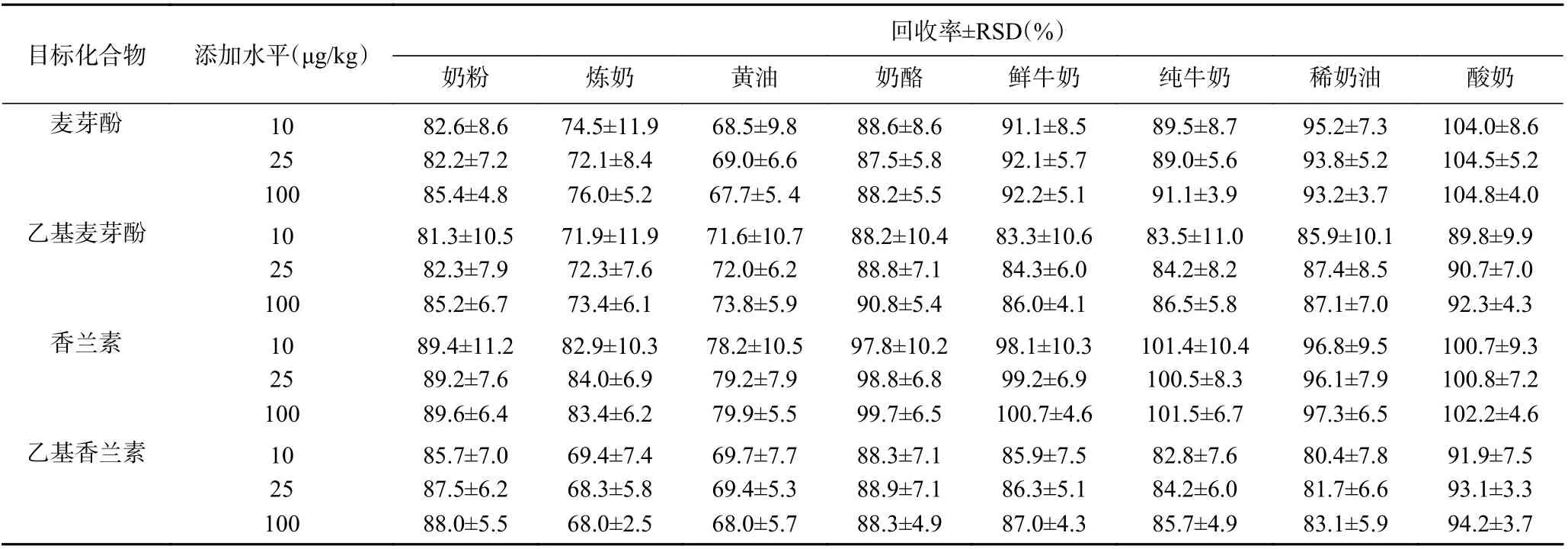
表5 乳制品中四种化合物加标回收和相对标准偏差(n=6)Table 5 Recoveries and relative standard deviations(RSDs)of 4 spices in dairy products(n=6)
2.6 与其它方法的比较
针对奶粉中四种香料化合物的检测,将所建立的方法与文献报道中的方法进行比较(表6),结果表明,此方法具有灵敏度高(检出限为0.6~2.4 μg·kg−1),分析时间短,基质效应小等优点。

表6 本方法与文献方法的比较Table 6 Comparison of methods from literature reports and this work
2.7 实际样品分析
应用该方法对市售15 件乳制品样品(4 份样品标注添加食用香精,1 份奶粉样品标注添加香兰素)进行分析测定。检测结果见表7,由表7 可知,标注添加食用香精样品确实检出了四种香料中的一种或多种,说明了此四种化合物在乳制品中的应用较为广泛。需要注意的是,GB 2760-2014 规定发酵乳不得添加食用香精香料,但是有的乳制品生产企业按照GB 19302-2010[30]生产的酸奶配料表仍含有食用香精,此外,麦芽酚在多个未标注添加香精的乳制品中有检出,而其它三种香料化合物在未标注添加香精均未检出,可能是因为在乳制品热加工过程中,发生美拉德反应生成麦芽酚[31−32],不同样品麦芽酚含量差异较大,应研究其内源性产生的麦芽酚水平以便制定合适的限量值以判断是否有额外添加。

表7 实际样品中4 种化合物含量的检测结果Table 7 Analysis results of four compounds in actual samples
3 结论
建立了高效液相色谱-串联质谱测定乳制品中麦芽酚、乙基麦芽酚、香兰素和乙基香兰素含量的方法,前处理采用水-叔丁基甲醚提取,氢氧化钠溶液反萃实现富集和净化后调酸分析。此方法前处理成本低,快速高效,净化效果好,仪器分析时间短,灵敏度高,四种化合物在各种乳制品中呈弱基质抑制效应,无需采用基质曲线或者内标校正补偿其基质效应。结果表明该检测分析方法稳定、可靠、易于推广,可应用于不同乳制品中四种香料化合物的检测,有望为相关检测标准的建立提供依据。
