氮掺杂碳纳米管活化过硫酸盐降解丁基黄药
2021-06-17陈绍华
熊 玲,张 敏,陈绍华
(中南民族大学 资源与环境学院,湖北 武汉 430074)
丁基黄药是一种广泛使用的硫化矿浮选药剂,有毒、难生物降解,对人和动物的神经、造血系统和肝脏等器官均有损害[1],同时给生态环境造成了严重的危害[2]。因此,急需研究一种高效、快速去除浮选废水中丁基黄药的新方法。
高级氧化技术是一种高效降解有机污染物的方法。近年来,基于硫酸根自由基(SO4-·)的新型高级氧化技术受到了广泛关注。与H2O2等传统氧化剂相比,过硫酸盐(PS)安全稳定、价格低,pH适用范围广[3]。SO4-·的氧化能力比PS更强、反应速率更快[4]。通常利用热[5]、紫外光[6]、过渡金属[7]等方法活化PS产生SO4-·。其中过渡金属活化法不需外加能量,效率高,是应用最广泛的方法[8],但过渡金属会对环境造成二次污染。因此,开发一种高效、环保的活化剂,对有机污染物的降解具有重要意义。
碳纳米管(CNT)具有稳定性好、比表面积大、导电性好、价格低廉、无二次污染等特点,表面含有醌基、羧基、羰基等含氧官能团,可以活化PS产生SO4-·,见式(1)~式(3)[9]。
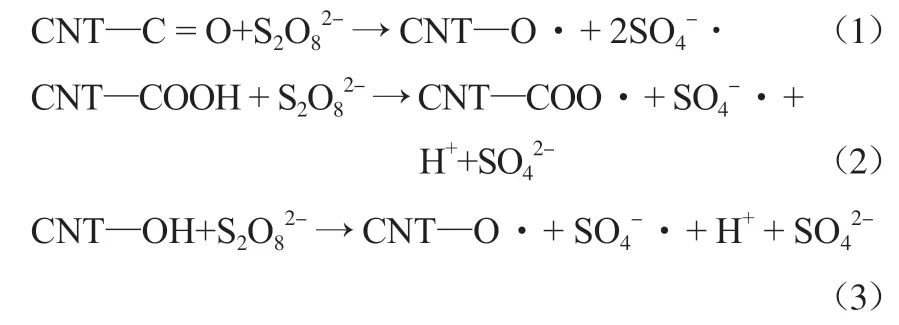
氮掺杂不会对碳材料晶格产生影响,还可以增加碳材料缺陷边缘、改善电子迁移能力及电荷密度,可以显著提高碳纳米管的活化性能[10]。目前,利用氮掺杂碳纳米管(N-CNT)活化PS降解丁基黄药未见文献报道。
本工作采用N-CNT活化SPS降解丁基黄药,并研究N-CNT加入量、SPS浓度、共存腐殖酸、共存阴离子等因素对丁基黄药降解的影响,最后探讨了其活化机理,旨为含丁基黄药浮选废水的高效处理提供理论基础。
1 实验部分
1.1 试剂、材料和仪器
丁基黄药、过硫酸钠(SPS)、碳酸氢钠、甲醇(MA)、叔丁醇(TBA)、腐植酸、氯化钠:均为分析纯。
N-CNT:购于南京先丰纳米材料科技有限公司,直径为30~50 nm,长度为0.5~2.0 μm。
ASAP 2020 型比表面积测定仪:美国麦克默瑞提克仪器有限公司;Hitachi SU8010型扫描电子显微镜:日本日立有限公司;VG Multilab2000型X射线光电子能谱仪:美国赛默飞世尔科技公司;NEXUS-6700型红外光谱仪:美国热电尼高力公司;DR6000型分光光度计:美国哈希水质分析仪器有限公司;THZ-C型恒温振荡器:金坛市宏华仪器厂;PHS-3C型酸度计:上海仪电科学仪器股份有限公司;BSA124S-CW型分析天平:德国赛多利斯公司。
1.2 实验方法
取一定体积的质量浓度为200 mg/L的丁基黄药废水于250 mL锥形瓶中,用浓度为0.1 mol/L的NaOH溶液或H2SO4溶液调节废水pH至7,加入适量的N-CNT和SPS,摇匀后置于恒温振荡器内,在转速160 r/min、温度35 ℃的条件下进行反应。每隔一定时间取样10 mL,并迅速加入0.5 mL甲醇,混合均匀后用孔径为0.45 μm的微孔滤膜过滤,然后在301 nm处测定滤液吸光度,计算丁基黄药的质量浓度。每组实验同时做两组平行样,结果取平均值。
1.3 分析方法
丁基黄药质量浓度按照HJ 756—2015《水质 丁基黄原酸的测定 紫外分光光度法》测定[11]。
2 结果与讨论
2.1 N-CNT的表征
N-CNT的N2吸附−脱附等温线见图1。由图1可见,N-CNT吸附曲线符合第Ⅳ类吸附等温曲线的特征,其BET比表面积为40.96 m2/g。不同直径的碳材料比表面积不同,本研究选用的N-CNT是直径较大的N-CNT,所以比表面积较小。
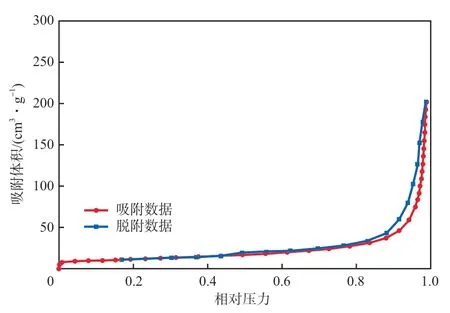
图1 N-CNT的N2吸附-脱附等温线
N-CNT的孔径分布曲线见图2。由图2可见,N-CNT的孔隙结构主要为介孔(2~20 nm)和大孔(>50 nm)。
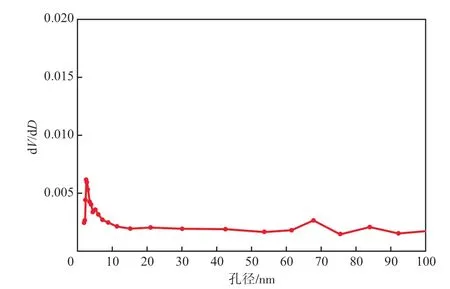
图2 N-CNT的孔径分布曲线
N-CNT的SEM照片见图3。由图3可见,N-CNT无序堆积在一起,并存在一定的团聚。

图3 N-CNT的SEM照片
N-CNT的FTIR谱图见图4。由图4可见,在波数为1 054,1 140,1 398,1 630,3 204 cm-1处的吸收峰分别对应 C—O、C—O—C 、O—C=O 、C=O和O—H的伸缩振动吸收峰,说明N-CNT表面含有一定量的含氧活性基团[10]。
N-CNT的XPS谱图见图5。由XPS总谱图可见,N-CNT表面主要含有C(w=81.24%)、O(w=17.04%)、N(w=1.73%)3种元素。由C1s谱图可见,结合能为284.7 eV和285.3 eV处的谱峰分别归属于C=C键和C—OH或C—O—C键。由O1s谱图可见,结合能为531.9 eV和533.1 eV处的谱峰分别归属于C=O键、C—OH或C—O—C键。由N1s谱图可见,结合能为399.1 eV、401.2 eV、402.5 eV处的谱峰分别归属于吡咯氮、石墨氮和氮氧键。该结果表明,N-CNT表面有不同结构的氮,并且含有大量的含氧官能团,这些官能团可以作为活化PS的活性位点。
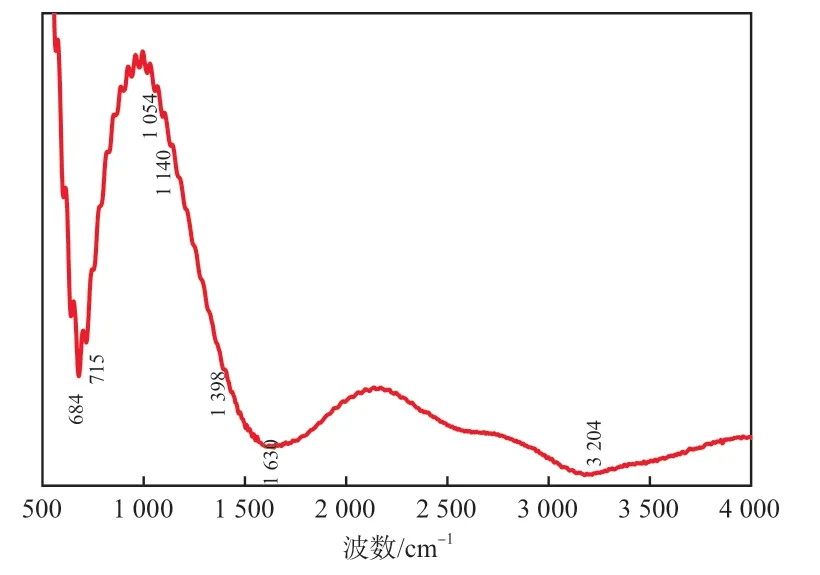
图4 N-CNT的FTIR谱图
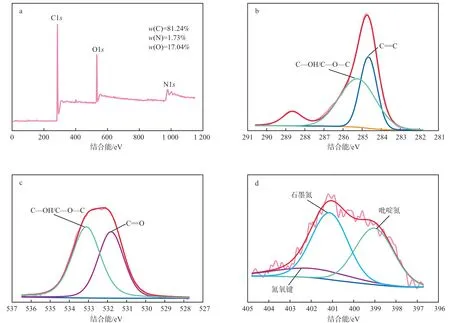
图5 N-CNT的XPS谱图
2.2 不同体系下丁基黄药的降解效果
在N-CNT加入量为0.40g/L、SPS浓度为0.50 mmol/L、pH=7的条件下,不同体系下丁基黄药的降解率见图6。由图6可见:SPS单独存在时,120 min时丁基黄药的降解率为25.71%,说明SPS对丁基黄药的氧化能力有限;只有N-CNT时,120 min时丁基黄药的降解率为35.06%,这是因为N-CNT具有较大的比表面积,可吸附一部分丁基黄药;在N-CNT+SPS体系中,60 min时丁基黄药的降解率即已高达97.72%,80 min即可完全降解,说明N-CNT可以高效活化SPS,促进丁基黄药的降解。
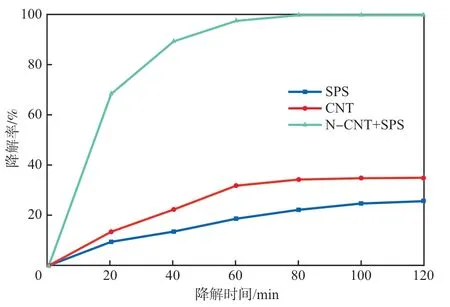
图6 不同体系下丁基黄药的降解率
2.3 N-CNT加入量对丁基黄药降解效果的影响
在N-CNT+SPS体系中,SPS浓度为0.50 mmol/L、pH=7的条件下,N-CNT加入量对丁基黄药降解率的影响见图7。由图7可见:当采用加入量为0.05,0.10,0.20,0.30,0.40g/L的N-CNT降解20 min时,丁基黄药的降解率分别为15.82%,22.17%,31.83%,37.46%,68.58%;进一步延长时间,丁基黄药的降解率进一步增大,降解80 min时,加入量为0.40g/L的N-CNT即可将丁基黄药完全降解;降解120 min时,加入量为0.05,0.10,0.20,0.30g/L的N-CNT对丁基黄药的降解率分别为53.57%,60.36%,76.64%,84.46%。可见,丁基黄药的降解率随着N-CNT加入量的增加而逐渐增大,这主要是因为N-CNT加入量增大,可以提供更多的活化位点用于吸附和活化SPS[12]。
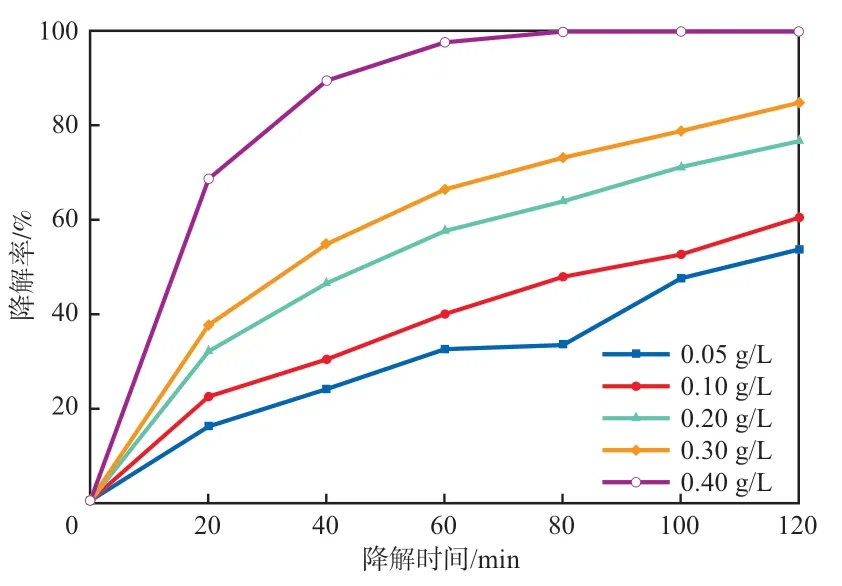
图7 N-CNT加入量对丁基黄药降解率的影响
2.4 SPS浓度对丁基黄药降解效果的影响
在N-CNT+SPS体系中,N-CNT加入量为0.40g/L、pH=7的条件下,SPS浓度对丁基黄药降解率的影响见图8。由图8可见:SPS浓度在0.05~0.50 mmol/L范围内,丁基黄药降解率随着其浓度的增加而显著增大;当SPS浓度为0.05,0.10,0.30 mmol/L时,120 min时的丁基黄药降解率分别为65.49%、69.58%和92.81%,而当SPS浓度为0.50 mmol/L时,80 min时丁基黄药可被完全降解;然而,当SPS浓度进一步增大至0.70 mmol/L时,丁基黄药的降解率增加很小。这是因为PS 浓度增大,会活化产生更多的自由基,导致更高的丁基黄药的降解率;但当PS浓度进一步增大,过量的PS也会淬灭SO4-·(见式(4))[13],同时SO4-·之间也会相互反应(见式(5))[12]。因此,确定SPS的最佳浓度为0.50 mmol/L。

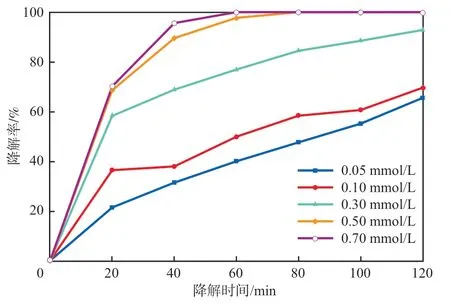
图8 SPS浓度对丁基黄药降解率的影响
2.5 共存腐殖酸对丁基黄药降解效果的影响
腐殖酸广泛存在于各种废水中,含有大量的含氧官能团,对地球生物化学过程产生重要的影响。在N-CNT+SPS体系中,N-CNT加入量为0.40g/L、SPS浓度为0.50 mmol/L、pH=7的条件下,共存腐殖酸质量浓度对丁基黄药降解率的影响见图9。
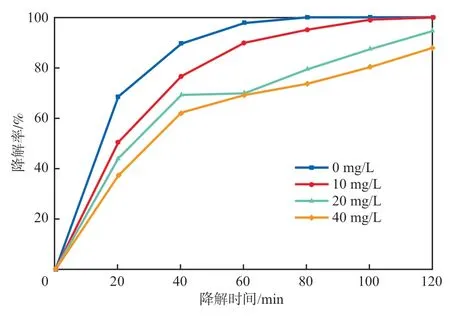
图9 共存腐殖酸质量浓度对丁基黄药降解率的影响
由图9可见:当废水中不含有腐殖酸时,120 min时丁基黄药的降解率为100%;当加入10,20,40 mg/L的腐殖酸后,120 min时丁基黄药的降解率分别降为99.93%,94.63%,87.95%。可见,共存腐殖酸会抑制丁基黄药的降解,并且抑制作用会随着腐殖酸浓度的增加而逐渐增大。其主要原因是腐殖酸为大分子物质,并且含有许多含氧官能团,很容易被吸附在N-CNT的表面,导致N-CNT表面的活性位点数减少[14],从而影响丁基黄药的降解速率。
2.6 共存Cl-、HCO3-和SO42-对丁基黄药降解效果的影响
含丁基黄药的浮选废水中常共存有Cl-、HCO3-和SO42-等阴离子。在N-CNT+SPS体系中,N-CNT加入量为0.40g/L、SPS浓度为0.50 mmol/L、pH=7的条件下,共存Cl-、HCO3-和SO42-浓度对丁基黄药降解率的影响见图10。
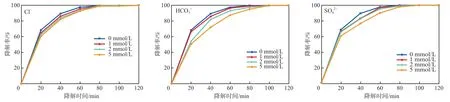
图10 共存Cl-、HCO3-和SO42-浓度对丁基黄药降解率的影响
由图10可见:不添加Cl-、HCO3-和SO42-时,60 min时丁基黄药的降解率为97.72%,80 min时可以完全降解;加入1,2,5 mmol/L的Cl-后,60 min时丁基黄药的降解率分别为89.43%、87.50%和85.94%,在100 min时丁基黄药都能全部降解;加入1,2,5 mmol/L HCO3-后,60 min时丁基黄药的降解率分别为96.62%、93.25%和87.73%,100 min时,丁基黄药也都能完全降解;加入1,2,5 mmol/L SO42-后,降解0 min时丁基黄药的降解率分别为96.97%、95.35%和90.14%,100 min时丁基黄药完全降解。可见,Cl-、HCO3-和SO42-对N-CNT活化PS降解丁基黄药有一定的抑制作用。其原因是Cl-和HCO3-可以与SO4-·反应,生成氧化性比SO4-·低的Cl·、Cl2-·、ClHO-·和CO3-·等自由基[15],见式(6)~式(9)。SO42-会使反应的平衡向左移动,抑制SO4-·的生成,见式(2)~式(3)[16]。
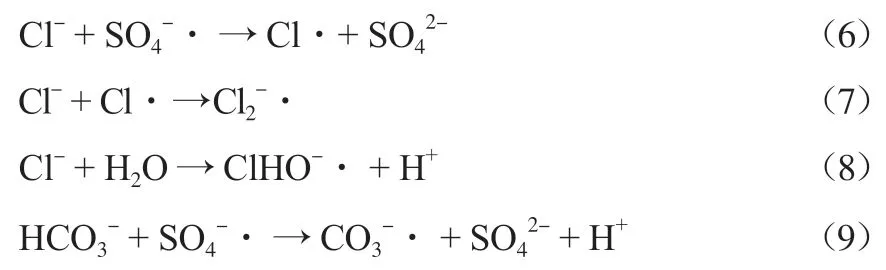
2.7 金属氧化物和N-CNT活化PS降解丁基黄药效果对比
在N-CNT+SPS体系中,金属氧化物和N-CNT加入量均为0.40g/L、SPS浓度为0.50 mmol/L、pH=7的条件下,不同活化剂对丁基黄药降解率的影响见图11。由图11可见:与一些常规含金属活化剂相比,CNT活化PS降解丁基黄药的效果更好;Fe0(还原铁粉)、Al2O3、Fe2O3和MnO2作为活化剂时,120 min时丁基黄药的降解率分别为89.94%,66.43%,16.54%,15.27%;以CNT作为活化剂降解80 min时,丁基黄药即可完全降解。可见,与常规含金属活化剂相比,N-CNT表现出更好的活化效果,同时还可以避免重金属离子造成的二次污染,具有更好的应用前景。
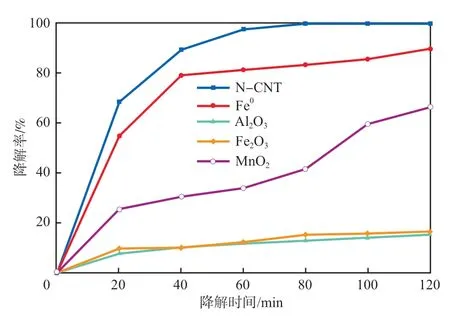
图11 不同活化剂对丁基黄药降解率的影响
2.8 活化机理
SO4-·和·OH是活化PS体系中主要自由基,为了确定N-CNT活化PS降解丁基黄药过程中是何种自由基起作用,可以通过加入自由基淬灭剂验证。MA是·OH和SO4-·的有效淬灭剂,而TBA仅为·OH的猝灭剂。在N-CNT+SPS体系中,N-CNT加入量为0.40g/L、SPS浓度为0.50 mmol/L、pH=7的条件下,不同淬灭剂对丁基黄药降解率的影响见图12。
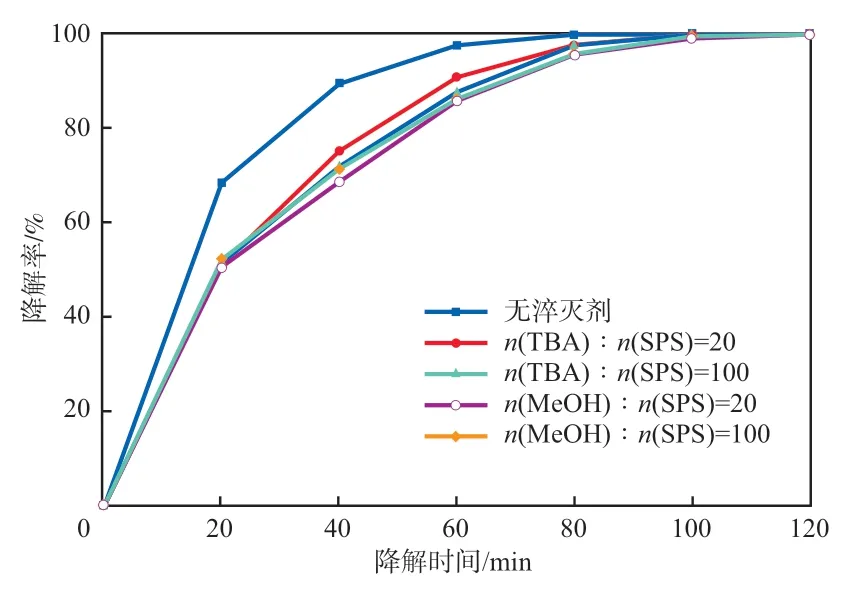
图12 不同淬灭剂对丁基黄药降解率的影响
由图12可见,在体系中加入MA或TBA后,丁基黄药的降解都受到了一定的抑制,说明在N-CNT活化SPS降解丁基黄药过程中产生了少量的SO4-·和·OH(见式(1)~式(3)及式(10));同时还可以看出,加入过量的MA并没有完全抑制丁基黄药的降解,说明不仅有·OH和SO4-·的自由基机制对丁基黄药的降解起作用,而且还有非自由基机制对丁基黄药的降解起作用,并且非自由基机制起主导作用。

非自由基机制可能是基于N-CNT作为电子传递介体促进电子从丁基黄药传递给PS,导致丁基黄药的氧化降解(见式(11)~式(12))。

为了证明上述假设,进一步研究了N-CNT在SPS浓度变化中的作用。不同N-CNT加入量条件下SPS浓度的变化见图13。由图13可见,不加N-CNT、降解120 min时,SPS的质量浓度下降率为34.57%;而加入量为0.40g/L的N-CNT存在时,SPS的质量浓度下降率显著提高,高达99.89%,表明N-CNT在SPS浓度下降过程中发挥着重要作用。结合图12可知,减少的SPS只有少量活化产生SO4-·和·OH,大部分SPS是通过N-CNT电子传递作用直接从丁基黄药获得电子,通过非自由基机制实现丁基黄药的降解。即丁基黄药通过与N-CNT表面的大量离域π电子结合形成活性复合物,并将电子传递给N-CNT,然后SPS从N-CNT获得电子,从而实现丁基黄药的氧化降解。在这个过程中,丁基黄药是电子供体,N-CNT是电子传递介体,而SPS是电子受体。
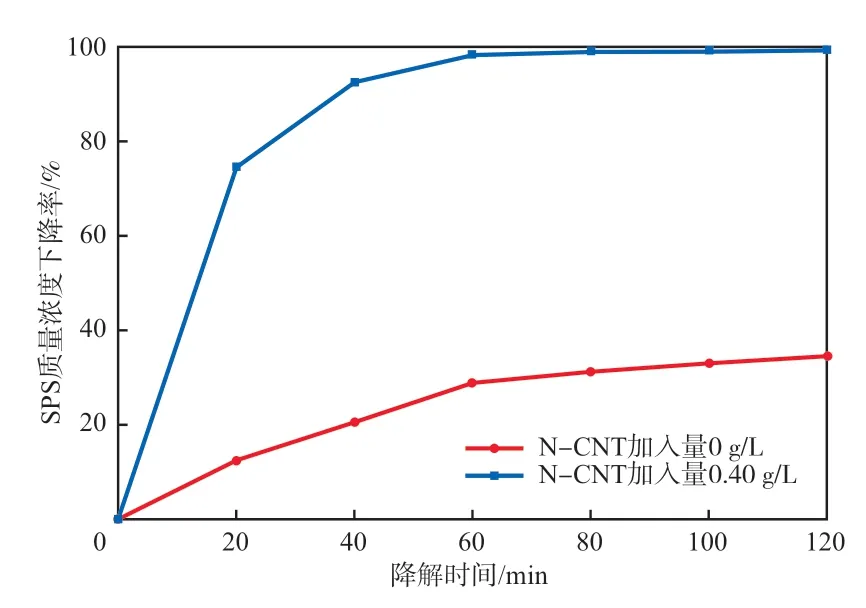
图13 不同N-CNT加入量条件下SPS浓度的变化
3 结论
a)N-CNT作为一种非金属催化剂可以高效活化PS降解丁基黄药,不会产生重金属等二次污染,具有良好的应用前景。在丁基黄药质量浓度为200 mg/L、N-CNT加入量为0.4g/L、SPS浓度为0.5 mmol/L、pH=7时,降解80 min时丁基黄药可以被完全去除。
b)废水中共存HA会抑制丁基黄药的降解,其抑制作用随着HA浓度的增大而增大。
c)Cl-、HCO3-和SO42-对N-CNT活化SPS降解丁基黄药有一定的抑制作用。
d)在N-CNT活化SPS降解丁基黄药过程中,自由基机制和非自由基机制二者共同导致了丁基黄药的降解,并且非自由基机制占主导。
