蒿甲醚pH 依赖型固体分散体处方研究
2020-03-24李文婷张国丽张锐武段国蕾杨兆祥
李文婷,张国丽,张锐武,段国蕾,杨兆祥*
1 楚雄医药高等专科学校,云南楚雄 675005;2 昆药集团股份有限公司,昆明650106
蒿甲醚(Artemether)为青蒿素的甲基乙醚衍生物(结构式见图1),临床上常用于治疗恶性疟和脑型疟。近年来大量研究发现,青蒿素及其衍生物可选择性的杀伤肿瘤细胞,而对正常组织细胞的毒性较小,与传统化疗药不存在交叉耐药。结直肠癌已经发展成为世界三大肿瘤之一,发病率与致死率均居高不下,而青蒿素类衍生物对结肠癌细胞SW480、SW602 有杀灭活性[1],蒿甲醚能使小鼠结直肠癌移植瘤的生长减缓[2],蒿甲醚有很大的潜力成为治疗结直肠癌的新型药物。但蒿甲醚是含有过氧基团的倍半萜内酯,在水中的溶解度较差,造成药物的普通口服制剂在生物体内的溶出速率很低,影响药物的吸收,导致药物生物利用度较低。
固体分散体(Solid dispersions,SD)是指药物高度分散在适宜的载体材料中形成的一种固态物质,药物由于在载体材料中高度分散,使比表面积增大,溶出性能提高[3]。利用载体材料溶解的特殊pH条件,可以使药物的释放具有pH 依赖性。按照人体胃肠道pH 有缓慢升高的特点,本研究选择肠溶性的载体材料,以pH 依赖型口服结肠定位释药系统[4]为模型,设计并筛选蒿甲醚pH 依赖型SD 最佳处方,制备稳定性较高的SD,并且使药物在达到胃肠道上端时不释放而至结直肠处开始释放。
1 仪器与药品、试剂
1.1 仪器
高效液相色谱仪1200(美国Agilent 公司);电子天平(德国赛多利斯公司);pH 酸度计(姆特勒-托利多公司);Mini Spray Dryer B-290 喷雾干燥器(瑞士Buchi 公司);Titroline KF 卡式水分滴定仪(德国肖特公司公司);智能溶出仪(德国Pharmatest公司);KBF720 恒温恒湿箱(德国Binder 公司);HORIBA LA-960 型激光粒度仪(日本堀场公司);D/max-TTRⅢ型X 衍射仪(日本理学公司);Quanta 200 型扫描电子显微镜(美国Fei 公司)。
1.2 药品与试剂
蒿甲醚(含量99%,批号IP2014003,昆药集团股份有限公司);蒿甲醚对照品(纯度99.8%,批号100271-201003,江莱生物制药);醋酸羟丙甲纤维素琥珀酸酯(HPMCAS-HF,批号65F-510005,亚什兰),羟丙基甲基纤维素邻苯二甲酸酯(HP-55,批号5102235,大连业建公司);Eudragit S100(批号B160605004,日本信越);所用试剂为分析纯。
2 方法与结果
2.1 建立分析方法
2.1.1 色谱条件 色谱柱:Kromasil C18(4.6 mm×250mm,5μm);流动相:乙腈-水(75∶25);流速:1 mL·min-1;检测波长:216 nm;柱温:25 ℃;进样量20 μL。
2.1.2 线性关系考察 称取蒿甲醚对照品适量,置量瓶中,用乙腈溶解后定容至刻度,作为蒿甲醚储备液(浓度:1 g·mL-1)。分别量取一定体积的蒿甲醚对照品储备液用乙腈稀释,配制成10、50、100、200、500、800μg·mL-1的溶液,分别移取上述溶液至高效液相色谱仪中检测,得到回归方程:Y=588.8X+0.7979,r2=0.999 9,线性范围:10~800 μg·mL-1。
2.1.3 药物溶出度的测定 按《中国药典》2015 版第四部0931“溶出度与释放度测定法”;其溶出度的测定按第二法进行,转速100r·min-1,温度37℃±0.5℃。取不同方法制得的SD,按比例称量相当于蒿甲醚50 mg,分别置于装有900 mL 溶出介质的释放杯中,在规定取样时间点,吸取溶液10 mL(及时补充10 mL 相同温度的溶出介质),经0.45 μm 微孔滤膜过滤,取续滤液,进样测定溶液中蒿甲醚含量,计算累积溶出度,制备时间-溶出度曲线。
2.2 SD 种类的筛选
选择能够在偏碱性环境下溶解的HPMCASHF[5]、HP-55、Eudragit S100 作为载体[6],分别与蒿甲醚以1∶1 比例用喷雾干燥的方法制备成SD。以溶出度和稳定性为指标,筛选最佳载体种类。
2.2.1 SD 制备工艺 处方量的蒿甲醚和HPMCAS-HF 加入适量的乙醇溶解至澄明,将混合液用喷雾干燥仪进行喷雾干燥[7]。操作参数为:设置进口温度50 ℃,最大抽气速度百分比100%,氮气流量30 mm,进料速度5 mL·min-1,B295 冷凝温度0 ℃。经喷雾干燥直接得到蒿甲醚SD,备用[8]。
2.2.2 溶出度特性 将各SD 在pH 1.2、pH 4.5、pH 6.8、pH7.6 下测定溶出度,制备累积溶出曲线。见图2。
从图2 看出,3 种载体制备的SD 溶出均表现出一定的pH 依赖性,且在高pH 环境下,都提高了蒿甲醚的溶出。用HPMCAS-HF 制得的SD,在高pH环境下,溶出度表现为pH 6.8<pH 7.6 的趋势,溶出呈现随着pH 升高而缓慢升高的特点;用Eudragit S100 制得的SD 在两个高pH 环境下溶出没有区别;用HPMCP(HP-55)制备的SD 在pH 1.2 的条件下溶出度超过了10%,在pH 4.5 的条件下溶出度达到了63%,说明药物在胃部就可能开始释放,不符合设计要求。故下一步,最佳载体需对HPMCAS-HF、Eudragit S100 制得SD 进行稳定性实验考察。
2.2.3 稳定性 由于易老化一直是固体分散体最大的缺陷[9],其中水分的影响最容易使固体分散体发生老化[10],因此选择高湿实验作为进一步筛选最佳载体的指标。分别取HPMACAS-HF、Eudragit S100 与蒿甲醚制得的SD 样品,开口置于恒湿密闭容器中,在25 ℃分别于相对湿度90%±5%条件下放置30 天,于第5、10、30 天取样,检测含量、水分以及在pH 7.6 条件下的溶出。结果见表1。
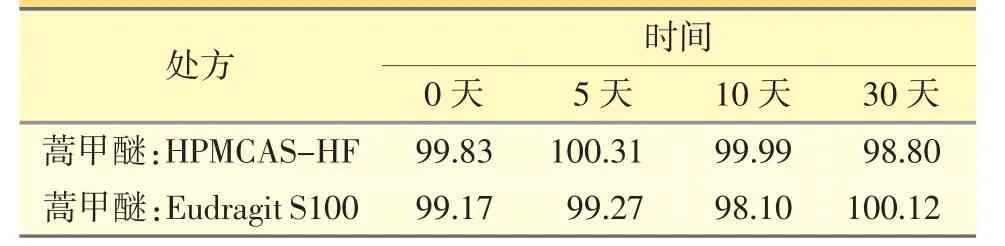
表1 高湿实验含量测定结果(%)
由表1 可知,在两种载体制得的SD 中,蒿甲醚含量在高湿实验条件下基本上没有变化。由图3 看出,处方蒿甲醚:Eudragit S100 的吸水性比处方蒿甲醚:HPMCAS-HF 大。由图4 看出,在pH 7.6 条件下,处方蒿甲醚:HPMCAS-HF 溶出变化不大,而处方蒿甲醚:Eudragit S100 有降低的现象,说明处方蒿甲醚:HPMCAS-HF 更稳定。
经过溶出特性测定、稳定性筛选,HPMCAS-HF作为载体制备的蒿甲醚SD,有很好的稳定性,在高pH 环境下增加了蒿甲醚的溶出,表现出一定的结直肠定位释放特性,是蒿甲醚pH 依赖型固体分散体最佳的载体。
2.3 SD 中药物与载体比例筛选
用蒿甲醚与最优载体HPMCAS-HF 制备成不同比例(2∶1、1∶1、1∶2、1∶3、1∶5、1∶7、1∶9)的SD,考察它们在pH 6.8、pH 7.6 环境中的溶出状态。从图5 看出,不同比例HPMCAS-HF 制得的蒿甲醚SD 比原料药的溶出都有所增加,随着其用量的增加,各SD在较高pH 中的表现趋近相同,都能达到快速释放,只有1∶1 的样品溶出度在pH 6.8 时低于pH 7.6,而且在喷干制备过程中,随着辅料量的增加,静电吸附会加重,收率亦降低,因此1∶1 的比例为最优。
2.4 固体分散体有关性能(参数)的评价
2.4.1 物理混合物的制备 称取适量的蒿甲醚和HPMCAS-HF 按1∶1 混合,置于乳钵中研磨均匀,过80 目筛,密封备用[下称SD(1∶1)]。
2.4.2 粒径的测定 用LA-960 型激光粒度仪干法测定,实验结果见表2、图6。
2.4.3 电子扫描显微镜(SEM)观察 分别取蒿甲醚、HPMCAS-HF、物理混合物、SD(1∶1)样品,用扫描电子显微镜进行不同放大倍数的观察,并记录样品图像,见图7。
表2 粒径分布(,n=3)

表2 粒径分布(,n=3)
注:d(0.5)为中位粒径,表示所测样品中50%小于该值;d(0.9)为中位粒径表示所测样品中90%小于该值。
由图7 看出,蒿甲醚呈多棱、片状晶体;HPMCAS-HF 呈不规则状;物理混合物可明显看到蒿甲醚只是和HPMCAS-HF 简单混合的状态;SD(1∶1)中蒿甲醚的多棱状晶体形态消失,呈不规则球状,表明蒿甲醚以喷雾干燥法制成SD(1∶1)后,可能转变成为无定型态或呈分子状态分散,增大了药物的比表面积,药物溶出需要的能量少,这可能是其体外溶出度提高的一个重要原因。
2.4.4 X 射线粉末衍射法分析(XRD)蒿甲醚、HPMCAS-HF、物理混合物、SD(1∶1)分别进行X 射线粉末衍射分析,扫描范围3°~90°,得到X 衍射图谱,见图8。
从图8-A 看出,蒿甲醚在5°~25°有3 个强的晶体衍射峰,说明蒿甲醚原料药以晶体形式存在;图8-B 载体HPMCAS-HF 没有强衍射峰;图8-C 物理混合物是药物与辅料简单混合,药物特征晶体峰仍然明显,但强度有所减弱;而在图8-D 中,蒿甲醚在5°~25°特征峰明显减弱或部分消失,且固体分散体较物理混合物的衍射峰减少和降低,说明蒿甲醚在固体分散体中可能部分以微晶状态存在,部分以无定型状态存在,这为其溶出度的提高提供了依据。
2.4.5 溶出度测定 取SD(1∶1)样品、物理混合物、蒿甲醚,测定pH 7.6 环境下的溶出度,制备溶出曲线,见图9。
从图9 看出,虽然物理混合物比蒿甲醚溶出度有所增加,但无法在2 h 内达到完全溶出。SD(1∶1)明显的提高了溶出度,与物理混合物溶出差异较大。
取SD(1∶1)样品,分别测定在pH 1.2、pH 4.5、pH 6.8、pH 7.6 环境下的溶出曲线,见图10。
从图10 看出,SD(1∶1)样品随着pH 升高,溶出速率加快,溶出度提高。
3 讨论
由于蒿甲醚难溶于水,因此将其制成SD 以提高其溶解度,并且采用特殊pH 条件下溶解的载体材料,使药物的释放具有pH 依赖性,制备成蒿甲醚pH 依赖型SD。研究结果表明,采用醋酸羟丙甲纤维素琥珀酸酯(HPMCAS-HF)与蒿甲醚1∶1 制备成的SD 样品,其释放具有pH 依赖性,在较高pH 环境下溶出完全。
对筛选出的处方进行评价,表现出较好的稳定性,所制得的固体分散体大小均匀,粒度较小,形成了不同于物理混合物的新形态;在SD(1∶1)中蒿甲醚部分以无定型状态、部分以微晶状态分散,具有典型的SD 特征,随着pH 的升高溶出度增加,符合胃肠道pH 特点,达到设计要求。
本研究制备的以醋酸羟丙甲纤维素琥珀酸酯(HPMCAS-HF)为载体的SD,载体材料易得,制备工艺简单,稳定性好,质量容易控制,经济安全,有利于开发成蒿甲醚结直肠定位释药制剂。
