表现为间质性肾炎的骨髓瘤肾损伤临床病理特征分析
2021-07-12刘萌萌王喜凤刘兴华王轶娟
刘萌萌, 王喜凤, 刘兴华, 刘 鹏, 王轶娟, 刘 灵, 魏 丽
浆细胞骨髓瘤(plasma cell myeloma,PCM)又名多发性骨髓瘤(multiple myeloma,MM),是一种发生于骨髓的浆细胞克隆性增殖性肿瘤,骨髓病变为多灶性、播散性分布,血和(或)尿中常能检测出肿瘤性浆细胞分泌的单克隆球蛋白(M蛋白)[1],其往往导致多器官损害,其中肾功能损害是PCM的常见并发症,也是主要死亡原因之一[2]。PCM是造血系统肿瘤中位列第二位的常见恶性肿瘤[3],发病年龄多在65~74岁,男性多于女性,患者常因溶骨性病变或骨质疏松导致躯干骨或四肢骨骼疼痛,首发症状多为骨痛、贫血或肾功能异常,首诊科室大多不是血液病科室,临床症状无特异性[4],极容易被误诊为骨质疏松、压缩性骨折及急性肾功能不全,而导致延误治疗。本文通过对1例初诊以急性肾功能不全入院患者的临床资料、肾穿刺标本特征分析,并结合相关文献,探讨此病病变的病理特点、诊断与鉴别诊断,以提高对此病病变的认识和鉴别要点的把握,避免漏诊、误诊。
1 资料与方法
1.1病例资料 患者,男,34岁,因“恶心、纳差、乏力3月余,加重半天”为主诉入院,入院肌酐575 μmol/L,尿素氮20.5 mmol/L,血钾5.37 mmol/L,尿酸616 μmol/L,尿蛋白阳性。患者有4年焦虑病史,以急性肾功能不全收入院。血常规:血红蛋白82 g/L,红细胞计数2.65×1012/L,白细胞计数4.5×109/L,血小板计数307×109/L,血钙及血脂正常。
1.2分析方法 肾穿刺组织三条,一条做冰冻切片,进行免疫荧光染色IgA、IgG、IgM、C3、C1q和纤维蛋白,试剂均购自中山金桥试剂公司;另一条用10%中性福尔马林固定,石蜡包埋,切片后作苏木精-伊红(hematoxylin-eosin,HE)染色,高碘酸-无色品红(periodic acid-Schiff,PAS)染色、Masson及六胺银特殊染色,免疫组织化学染色CD3、CD20、CD38、CD138、kappa及Lambda,分别于光学显微镜下观察结果;第三条组织为电镜标本,送广州金域检验中心检查。骨髓穿刺组织用10%中性福尔马林固定,脱钙,石蜡包埋,切片后作HE染色,Gomori、PAS染色,分别于光学显微镜下观察结果;免疫组织化学染色采用EnVision二步法,包括CD38、CD138、kappa、Lambda、CD56、CD3、CD20、CD117、CD34、MPO、CD61、CD235a蛋白均购自福建迈新试剂公司。
2 结果
2.1肾免疫荧光结果 可见6个肾小球,免疫荧光染色IgG、IgA、IgM、C3、C1q及纤维蛋白均阴性。
2.2肾光镜结果 见24个肾小球,肾小球毛细血管袢开放好,未见明显病变,六胺银及Masson染色阴性。肾小管上皮细胞肿胀,刷状缘脱落、颗粒变性及空泡变性,灶状肾小管上皮细胞扁平,肾小管腔内可见蛋白管型及细胞碎屑,见PAS弱阳性的蛋白管型,个别管型周围见炎细胞包绕,可见少量白细胞管型,多灶性肾小管萎缩、基膜增厚。免疫组化CD3、CD20、CD38、CD138显示间质多灶性T、B淋巴细胞及散在少量浆细胞浸润。间质灶状纤维组织增生。肾组织刚果红染色阴性。免疫组化显示肾小管及部分管型κ轻链阳性、λ轻链阴性。见图1ⓐ~ⓕ。
2.3肾电镜结果 肾小球毛细血管内细胞无明显增生,毛细血管袢开放,壁层细胞无明显增生,基底膜无明显增厚,厚度270~380 nm,基底膜肾节段性皱缩,基底膜内侧可见泥沙样电子致密物沉积,足突部分融合,上皮下未见电子致密物沉积,系膜细胞和基质增生,系膜区、内皮下未见确切电子致密物沉积,肾小管基底膜增厚,基底膜内侧及外侧可见泥沙样电子致密物沉积,肾间质少量炎症细胞浸润。考虑轻链沉积病。见图1ⓖⓗ。
2.4骨髓光镜结果 骨髓穿刺活检示骨髓增生明显活跃,有核细胞密度约80%,大量浆细胞样细胞弥漫成片分布,胞体大,胞浆丰富,核圆形或不规则,核偏位,占有核细胞比例约70%,粒系及红系细胞散在分布,增生受抑制,巨核细胞可见,以分叶核细胞为主,网状纤维染色MF-1级。免疫组化显示CD138、CD38阳性细胞弥漫分布,κ、λ轻链显示κ轻链有限制性表达。骨髓涂片中可见约21.2%原幼浆细胞,少数红细胞呈缗线样排列。病理诊断为PCM。见图2。
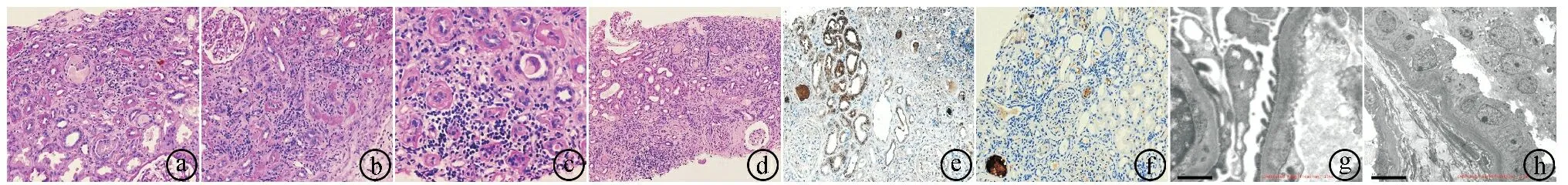
ⓐ肾小管上皮细胞肿胀、空泡变性及颗粒变性,管腔内可见蛋白管型,部分管型可见裂隙(PAS×100);ⓑ肾小管多灶萎缩(PAS×100);ⓒ间质单一核细胞浸润(PAS×200);ⓓ局灶纤维组织增生(HE×40);ⓔ肾小管上皮细胞及管型免疫组化κ轻链阳性(×100);ⓕ肾小管上皮细胞及管型免疫组化λ轻链阴性(×100);ⓖ肾小球基底膜内侧可见泥沙样电子致密物沉积(电镜);ⓗ肾小管基底膜内外侧可见泥沙样电子致密物沉积(电镜)
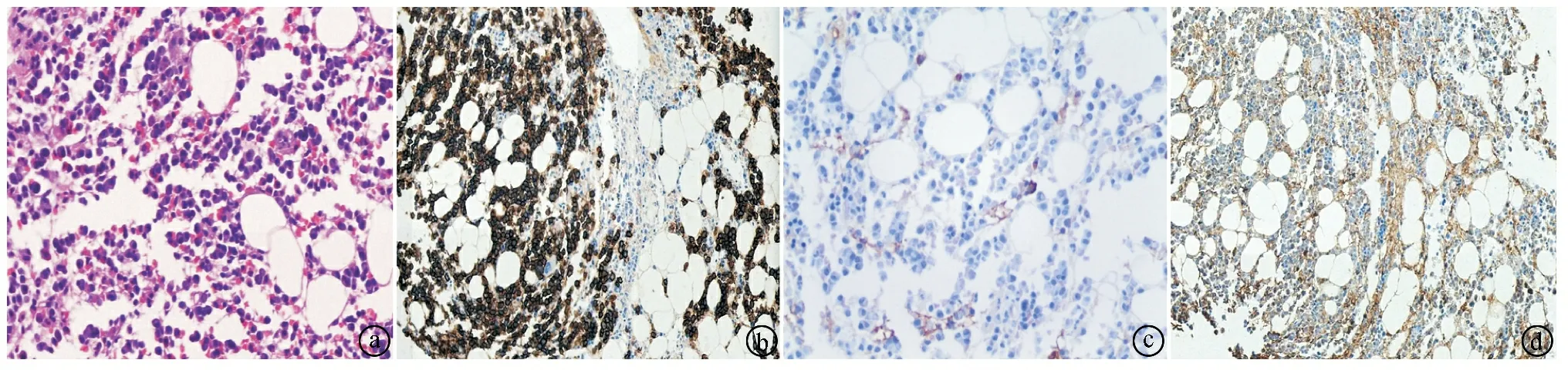
ⓐ骨髓组织内浆样肿瘤细胞弥漫成片分布(HE×100);ⓑ免疫组化CD138显示肿瘤细胞弥漫阳性(HE×100);ⓒⓓ免疫组化κ及λ轻链显示κ轻链限制性表达(HE×100)
2.5其他检查结果 血清及尿免疫固定电泳k泳道发现异常单克隆条带。尿本周蛋白阳性,类型为k游离轻链型。骨髓细胞流式可见约8.4%的单克隆浆细胞,表达CD38、CD138、CD20、CD34及ckappa,提示为单克隆浆细胞。X线示骨盆、双侧股骨上中段多发斑点状低密度影。染色体为46,XY。荧光原位杂交检测显示肿瘤细胞示RB1(13q14)缺失,IgH重排阴性,P53(17p13.1)无缺失,CKS1B(1q21)无扩增。最后诊断为PCM伴肾损害(肾小管间质性肾炎)。
3 讨论
3.1PCM好发于中老年男性,肿瘤在骨髓中克隆性生长,呈多灶分布,导致骨质破坏、贫血,多数患者以骨痛起病,瘤细胞产生大量M蛋白会引发多器官功能损害,肾功能损害为常见症状。本例患者为青年男性,以肾功能不全起病,发病隐匿,无骨痛症状。肾脏穿刺活检标本主要表现为肾小管间质性损伤,电镜显示肾小球泥沙样物沉积,提示轻链沉积可能,血清、尿游离轻链检查出现异常κ轻链,尿M蛋白(+),骨髓穿刺明确诊断为PCM。
3.2PCM导致的肾脏损伤表现为多种病理类型[5-6],主要包括管型肾病、单克隆免疫球蛋白沉积病(包括轻链沉积病、重链沉积病和轻重链沉积病)、肾淀粉样变性及急性间质性肾炎等。本例光镜下未观察到淀粉样物质,刚果红染色阴性,故不考虑肾淀粉样变性。肾组织κ轻链染色阳性,电镜下在肾小球及肾小管基底膜内外均可见泥沙样物沉积,特点符合单克隆球蛋白沉积病中的轻链沉积病。但单克隆免疫球蛋白沉积病累及肾脏时往往以肾小球损伤为主,但也有文献报道轻链沉积病会出现以肾小管间质损伤为主而无明显肾小球受累的情况[7],本例肾损伤的主要表现就是肾小管损伤的间质性肾炎。而导致间质性肾炎又有两种情况:一是管型肾病伴有急性间质性肾炎[8];另一种是单纯的急性间质性肾炎[9-10]。管型肾病是指肾小管管腔内的轻链蛋白可与小管上皮分泌的Tamm-Horsfal蛋白结合,形成浓稠、光镜下呈骨折线样的蛋白管型。本例患者临床表现为急性肾功能不全,出现以轻链蛋白为主的大量蛋白尿,无低蛋白血症和高脂血症;光镜下肾远端小管和集合管中有PAS弱阳性的管型,管型中间有裂隙,少数管型周围可见炎细胞和多核巨细胞的包绕[11],同时间质中有淋巴细胞和少量浆细胞浸润,肾小管多灶性萎缩,符合管型肾病伴间质性肾炎。PCM相关单纯的急性间质性肾炎组织学无特征性病变,浸润细胞以浆细胞和单核巨噬细胞为主。
3.3PCM导致肾小管间质损害的病理生理过程现在一般认为是大量异常单克隆免疫球蛋白及其轻链堵塞管腔,并与肾小球毛细血管基底膜结合、原位沉积,改变了内源性组织抗原,促进机体释放细胞因子,导致间质单核细胞的吸引和活化[12-14];大量游离轻链在近端肾小管上皮细胞重吸收,在溶酶体内降解后,部分溶酶体破裂释放其内容物及各种酶,导致小管上皮细胞的损伤,出现细胞脱落、崩解及坏死,引起急性肾损伤;轻链蛋白也可渗入并沉积于肾小管基底膜外侧及肾间质,改变原有的组织抗原,通过肾小管周围毛细血管释放细胞因子,导致间质单核炎症细胞趋化和激活,形成慢性间质性肾炎表现[13]。
3.4PCM肿瘤细胞具有明显的异质性,细胞遗传学研究显示多数表现为多种遗传学异常并存,包括染色体易位、片段缺失及扩增等[15]。研究[16]显示在遗传学异常中,肾损伤组RB1缺失发生率高于非肾损伤组,表明存在RB1缺失的PCM患者发生肾损伤的风险可能更高。Chavan等[17]的研究发现RB1缺失与PCM不良预后有关,而本例患者基因检测发现RB1基因出现了缺失。
综上所述,PCM会引起多种器官损害,肾损害表现多样,当以肾损害初诊时,需要结合临床、光镜、免疫荧光和电镜综合评估,避免误诊漏诊,以期积极治疗原发病,早期干预肾损害,规范治疗,从而改善患者的预后。
