阿帕替尼联合多西他赛二线治疗晚期非小细胞肺癌的临床观察
2020-12-22陈大可
王 娟 陈大可
(南通市通州区人民医院,江苏南通 226300)
根据2018年全国癌症报告统计,肺癌位居全国发病的首位。非小细胞肺癌(NSCLC)占比约80%,其中大部分患者最终出现复发或转移[1]。晚期NSCLC的一线标准化疗方案为含铂类双药联合治疗,多西他赛单药为二线化疗方案,其有效率在10%左右,平均总生存时间仅为5~8 个月。多项研究表明[2],在既定的铂类方案中再增添化疗药物,对患者的预后并没有明显的改善,而且可能导致药物的不良反应增加。在晚期NSCLC治疗的研究中发现[3],抗血管生成的靶向药物发挥至关重要的作用,目前应用化疗联合抗血管生成治疗成为治疗晚期NSCLC的研究热点之一。阿帕替尼为我国生产的新型小分子血管内皮生长因子受体抑制剂,它不仅具有很强的抗血管生成活性,而且给药方便、依从性好。因此,本研究以南通市通州区人民医院收治的60例晚期非小细胞肺癌患者为例,旨在探讨阿帕替尼联合多西他赛作为二线治疗方案在晚期非小细胞肺癌中的治疗效果及安全性,结果如下。
1 资料与方法
1.1 一般资料
选取南通市通州区人民医院2016年6月至2019年2月收治的60例晚期非小细胞肺癌患者作为研究对象,按照随机数字表法分为治疗组(30例)与对照组(30例)。治疗组中,男性19例,女性11例;年龄33~75岁,平均年龄(62.23±10.11)岁;病理类型:鳞状细胞癌8例,腺癌22 例;卡式(Karnofsky)评分70~100分,平均Karnofsky评分(89.33±8.28)分。对照组中,男性18例,女性12例;年龄40~75岁,平均年龄(62.83±8.96)岁;病理类型:鳞状细胞癌9例,腺癌21例;Karnofsky评分70~100分,平均Karnofsky评分(86.26±8.55)分。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 纳入与排除标准
纳入标准:①所有患者均经胸部CT、病理或细胞学诊断为晚期非小细胞肺癌,且具有明确的可测量病灶;②要求螺旋CT扫描每层厚度大于10 mm,符合《非小细胞癌诊疗指南》[4]中的诊断标准;③一线治疗失败;④预计生存期≥3个月;⑤患者知情且同意参与本次研究,并签署知情同意书。
排除标准:①既往一线治疗使用过多西他赛或贝伐单抗者;②肝、肾功能不全者;③高血压控制不佳者;④有出血倾向或者正在接受抗凝治疗者。
1.3 方法
治疗组选择甲磺酸阿帕替尼(江苏恒瑞,国药准字H20140103,规 格:250 mg×10片)口 服,500 mg/次,1 次/d。多西他赛(江苏恒瑞,国药准字H20020543,规格:20 mg×1 支)静脉滴注,75 mg/m2,每个周期的第1天静脉滴注时间需大于60 min,其余每天小于60 min,治疗21 d为1个周期。
对照组选择多西他赛75 mg/m2静脉滴注,每个周期的第1天静脉滴注时间需大于60 min,其余每天小于60 min,以治疗21 d为1个周期。每2个周期进行一次疗效评价,直至患者病情进展或不良反应不耐受。应用多西他赛前1 d开始给予地塞米松(天津天药药业股份有限公司,国药准字H20033553,规格:0.75 mg×100片)口服,7.5 mg/次,2次/d,连续服用3 d。如果中性粒细胞<0.5×109/L,血小板<25×109/L,下1个周期的化疗药物的剂量需降低25%;当出现3~4级阿帕替尼相关不良反应,需根据阿帕替尼的临床特征,给予对症处理,并根据患者病情将阿帕替尼减量至250 mg/d或短期停服。
1.4 观察指标
疗效评价采用符合《非小细胞癌诊疗指南》中的诊断标准,分为完全缓解(CR),部分缓解(PR),稳定(SD)和进展(PD)。PR+CR为客观缓解效率(ORR),PR+CR+SD为疾病控制率(DCR)。治疗中每2个周期复查CT进行疗效评价。不良反应(中性粒细胞减少,血小板减少症、乏力、恶心、高血压、蛋白尿、手足综合症、出血、心包炎、心律失常)的分级采用(美国)国家癌症研究所(NCI)毒性分级标准进行评价,分为0~Ⅳ级,共5个分级。分级越小,则代表患者症状越轻。于每个化疗周期前均留取患者的空腹血液,检测血清癌胚抗原(CEA)指标,分析其血液中表达水平的变化趋 势。
1.5 统计学分析
采用SPSS 22.0软件进行数据处理分析。计量资料以(±s)表示,采用t检验;计数资料以[例(%)]表示,采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者的近期治疗效果比较
两组患者治疗后均未发生CR。治疗组患者的ORR为30.0%,高于对照组的6.67%;治疗组患者的DCR为60.00%,高于对照组的33.33%,组间比较差异有统计学意义(P<0.05),见表1。

表1 两组患者的近期治疗效果比较[例(%)]
2.2 两组患者治疗前后血清CEA指标表达水平比较
治疗前,两组患者的血清CEA指标水平比较差异无统计学意义(P>0.05);治疗后,两组患者的CEA水平均有所下降,且治疗组下降幅度大于对照组(P<0.05),见表2。
表2 两组患者治疗前后血清CEA指标表达水平比较(±s,ng/mL)
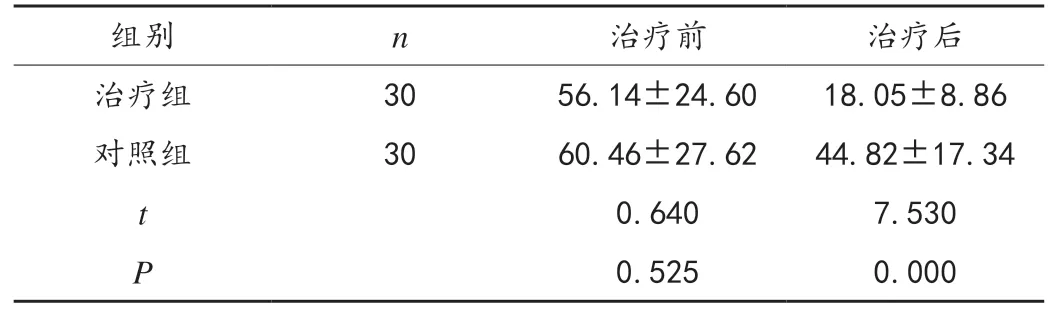
表2 两组患者治疗前后血清CEA指标表达水平比较(±s,ng/mL)
组别 n 治疗前 治疗后治疗组 30 56.14±24.60 18.05±8.86对照组 30 60.46±27.62 44.82±17.34 t 0.640 7.530 P 0.525 0.000
2.3 两组患者不良反应发生情况及安全性比较
对照组患者发生的不良反应以中性粒细胞减少、血小板减少症、乏力及恶心为主,而治疗组联合阿帕替尼治疗,高血压、蛋白尿、手足综合症等不良反应的发生率有所上升,但未发生出血及其他严重的不良反应,经对症处理均有所好转,见表3。
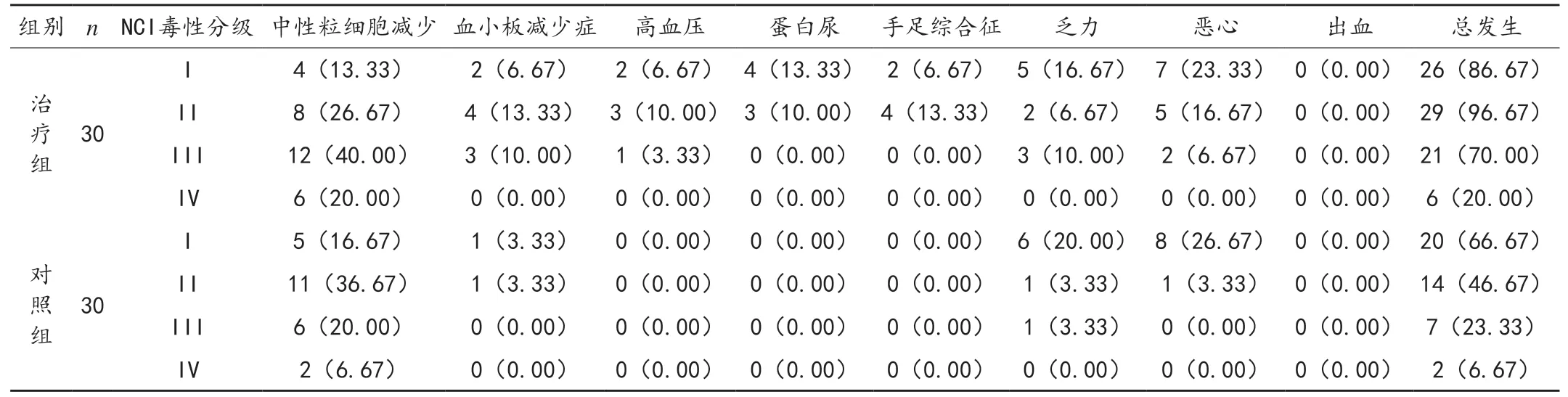
表3 两组患者不良反应发生情况比较[例(%)]
3 讨论
由于肺癌在早期呈隐匿发展,大多症状不明显,所以大部分患者发现时已处于肺癌晚期。目前晚期非小细胞肺癌的主要治疗手段以放射、化学治疗及酪氨酸激酶抑制剂(TKI)靶向治疗为主,但大部分患者经多程放射、化学治疗及TKI靶向治疗后,仍会出现病情进展。国际指南对晚期NSCLC的二线化疗推荐单药化学治疗,主要包括培美曲塞和多西他赛,而二线单药化学治疗的有效率仅为10%~20%[5],效果并不满意。
近年来,肺癌治疗在抗血管生成方面的研究越来越受到重视,其中阿帕替尼是我国自主研发的小分子抗血管生成靶向药物,它的主要作用是抑制血管内皮生长因子受体-2(VEGFR-2)酪氨酸激酶。VEGFR-2与肿瘤血管生成关系最为密切,当阿帕替尼结合到VEGFR-2酪氨酸激酶的ATP上时,VEGFR-2酪氨酸激酶将不能激活,从而依赖VEGFR-2通路的血管内皮生长因子生成减少,最终达到抑制肿瘤血管生成的目的。多项研究表明[6-7],阿帕替尼单药可以提高不同类型肺癌患者的临床治疗有效性。还有研究表明[8],化疗药物联合抗血管生成的靶向治疗可以提高晚期NSCLC的疗效,但联合治疗3级以上的不良反应发生率较高。基于此,本研究采用较低剂量阿帕替尼联合多西他赛化疗对晚期非小细胞肺癌进行二线治疗,结果显示,治疗组患者的DCR为60.00%,高于对照组的33.33%(P<0.05);治疗后,治疗组患者的血清CEA水平下降幅度显著大于对照组(P<0.05)。这一结果表明阿帕替尼联合多西他赛的临床治疗效果更佳,但联合治疗方案的血液学毒性(中性粒细胞减少、血小板减少症)及非血液学毒性(手足综合症、乏力)均有所提高。其中阿帕替尼相关的不良反应主要为高血压、蛋白尿、乏力等,根据阿帕替尼在胃癌治疗中的临床症状,予以相应的对症处理,均好转,未见严重不良反应,药物总体耐受性良好。
综上所述,阿帕替尼联合多西他赛二线治疗晚期NSCLC,可显著提高DCR,虽然阿帕替尼联合多西他赛的不良反应相对增多,但通过降低剂量或暂停药物及对症支持治疗后,总体安全可控,值得临床推广应用。
