来曲唑联合拮抗剂对体外受精-胚胎移植中低反应患者受孕结局的影响
2020-09-16杨素娟许月明张杰姚朝辉王会霞王少卿郝桂敏
杨素娟 许月明 张杰 姚朝辉 王会霞 王少卿 郝桂敏
卵巢低反应(POR)是指虽然对卵巢进行各种的刺激,但仍未达到满意的卵巢反应。有学者认为,对卵巢低反应的患者可以实施促性腺激素释放激素拮抗剂(GnRHA)方案可能会达到预期的效果[1]。拮抗剂方案在最初开始时没有垂体降调节阶段,并且在早卵泡期也就是卵泡募集关键时期可以抑制促黄体生成素峰值不会过早的出现,同时也不能抑制卵巢,这种现象对于卵巢低反应的患者具有一定的影响[2]。来曲唑属于第三代非甾体类芳香化酶抑制剂,抑制睾酮向雌激素和雄烯二酮的转化,从而降低雌激素负反馈作用,同时也可以减少雌激素的合成,帮助分泌更多的内源性促性腺激素[3]。在体位受精-胚胎移植中,来曲唑属于一种辅助性的药物,如果和拮抗剂方案联合一起使用,可以为卵巢低反应的患者更好的优化卵巢刺激的新型方法[4]。本研究使用来曲唑联合拮抗剂方案对体外受精-胚胎移植中低反应患者进行试验,报告如下。
1 资料与方法
1.1 一般资料 选取2011年5月至2017年6月河北医科大学第二医院收治的体外受精-胚胎移植中低反应患者150例,采用随机数字表法分为对照组和研究组。对照组75例,年龄20~32岁,平均年龄(25.6±2.3)岁;研究组75例,年龄21~31岁,平均年龄(24.1±3.2)岁。2组资料具有均衡性。2组患者均自愿参与本研究,并经过医院伦理委员会批准。
1.2 纳入与排除标准
1.2.1 纳入标准:①纳入对象均符合POR(博洛尼亚卵巢低反应),在常规的刺激下可获得≤3枚卵子;②年龄≥39岁;③在使用相关仪器进行检查中显示发生低储备可能,其中抗苗勒氏管激素水平0.6~1.0 ng/ml;肺泡液清除双侧共有6~7枚窦卵泡。④在治疗前的3个月内未进行过体外受精-胚胎移植以及促排卵等。
1.2.2 排除标准:①有严重的内异症患者;②多囊卵巢综合症(PCOS)患者;③使用来曲唑后无效;④来曲唑未使用在治疗体外受精-胚胎移植而用在非拮抗剂方案中的患者;⑤应用在其他促排卵药物的研究中。
1.3 方法 胚胎移植后的14 d检测血β-HCG水平,如果≥31 U/L可以在月经周期的第2天检测,如血清E2<281 pmol/L,FSH<16 U/L,并且使用超声检查,未见到卵巢直径>1 cm的卵泡,可以实施促排卵的治疗[5]。
1.3.1 对照组:单独使用拮抗剂方案。月经后的3~5 d注射尿促性素或者尿促卵泡素160~299 U,当卵泡直径13 mm左右或在第5天对患者注射西曲瑞克0.26 mg/d,根据卵泡生长情况选择合适的药物用量。如果卵泡直径>17 mm或数量≥2,可以使用0.1 mg的醋酸曲普瑞林,继后的35 h左右用超声取出卵泡[6]。
1.3.2 研究组:来曲唑联合拮抗剂:月经周期的3~5 d 应用来曲唑5 mg/d的来曲唑,并在周期的第5天另外使用小剂量促性腺激素151~224 U/d[7]。小剂量促性腺激素组使用药物:在月经周期的第2天开始使用,最初的剂量为299~451 U/d。
1.3.3 2组在使用到第7天时,可以开始使用0.24 mg/d的拮抗剂醋酸西曲瑞克(思则凯)直至产生人体绒毛膜促性腺激素时(HCG)[8]。所有患者在第7天开始用阴道超声测量子宫内膜厚度以及监测卵泡。并在HCG日以及周期的第7天对P、E2、LH水平进行测定。如果出现直径≥17 mm的3个卵泡,需要重新注射HCG 250 μg(上海抚生生物科技有限公司)[9]。继后36 h,经阴道取卵,并在5~6 h内受精,在取卵后的3 d内进行胚胎移植。从取卵日开始,每天注射黄体酮60 mg[10]。在胚胎移植后的30 d阴道B超扫描妊娠囊、胎儿心管搏动以确定临床妊娠[11]。如果β-HCG只是升高,但是经过检查未发现妊娠囊,可能为生化妊娠[12]。
1.4 观察指标 (1)比较2组周期特点。包括 Gn(促性腺激素):Gn总用量、Gn起始量、平均用量、使用时间,人绒毛膜促性腺激素(hCG),内膜厚度,促黄体生成素(LH),雌二醇(E2),孕酮(P)。(2)比较2组妊娠结局。包括:自然流产率、胚胎种植率、活产率、临床妊娠率。(3)比较2组着床率。

2 结果
2.1 2组患者周期特点比较 研究组Gn总用量、使用时间、平均用量、起始量、E2、内膜厚度均低于对照组(P<0.05),LH、P高于对照组(P<0.05)。见表1。

表1 2组患者周期特点比较
2.2 2组患者妊娠结局比较 研究组临床妊娠率、活产率、胚胎种植率均高于对照组(P<0.05),自然流产率低于对照组,差异有统计学意义(P<0.05)。见表2。
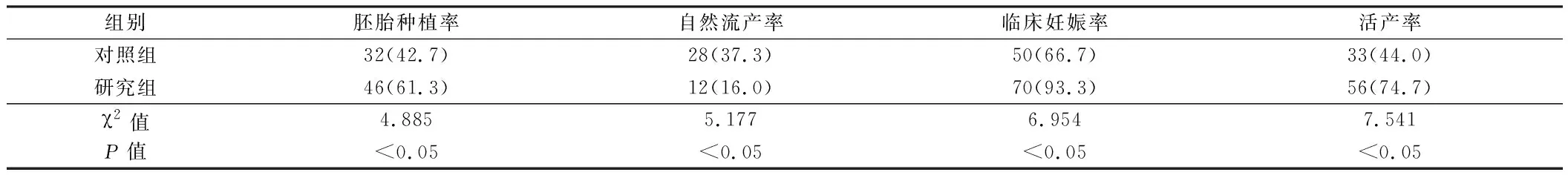
表2 2组患者妊娠结局比较 n=75,例(%)
2.3 2组着床率比较 研究组患者着床率为92.0%高于对照组的69.3%,差异有统计学意义(P<0.05)。见表3。
3 讨论
体外受精-胚胎移植技术潜在的价值以及实用价值均具有一定的临床意义,并不断的受到推广和发展[13]。1978年Edwards以及Steptoe创造出的第一代试管婴儿,1992年Palermo创造的ICSI(单精子卵胞浆内注射)属于第二代试管婴儿,在种植前对患者的遗传学进行相关的诊断属于第三代[14]。但是随着更多人们的需求,自我控制的生殖处于不断发展和更新中[15]。

表3 2组着床率比较 n=75,例(%)
我国生殖医学工程虽然发展较晚,但是经过近几年的不断发展,具有一定的效果[16]。1988年北京医科大学第1例显微受精试管婴儿诞生[17]。1996年中山医科大学第1例ICSI(显微受精试管婴儿)诞生,并且第三代试管婴儿也获成功,当前我国逐渐有卵子冻存、冻融胚胎移植、辅助孵出、囊胚期培养等各项前卫技术,促进各家庭的妊娠计划[18]。
来曲唑不仅可以减少雄激素转化成雌激素,还可以阻断垂体和下丘脑的负反馈,减少血清中的雌激素浓度,帮助卵泡发育[19-22]。拮抗剂方案可以使卵泡更加贴近自然,不会影响到生物的活性状态,并且还可以较大限度的升高卵巢的Gn反应性,因此,本研究中来曲唑联合拮抗剂方案中研究组着床率为92.07%明显高于对照组的69.3%(P<0.05),说明联合使用可以改善患者的内分泌环境,有效的增加患者妊娠机会,减少流产事件的发生。
研究组Gn总用量、起始量、平均用量、使用时间、E2、内膜厚度均低于对照组(P<0.05),LH、P高于对照组(P<0.05)。来曲唑联合拮抗剂方案可以增加妊娠机会,减轻患者的精神负担,以及治疗费用,并且无不良反应。
本研究将来曲唑和拮抗剂方案联合应用后,研究组临床妊娠率、活产率、胚胎种植率均高于对照组(P<0.05),自然流产率低于对照组(P<0.05),说明来曲唑可以帮助患者较好的排卵,配合拮抗剂方案后促使效果更好,因此患者妊娠、活产等的概率均高于单独使用来曲唑患者。
综上所述,来曲唑联合拮抗剂方案对体外受精-胚胎移植中低反应患者的妊娠结局的影响以及着床率具有一定的效果,此方法可以作为临床中改善卵巢提供较为科学的依据。
