血糖控制情况对糖尿病周围神经病变(DPN)患者下肢神经减压术疗效的影响
2019-05-16丁佐佑陈增淦
丁佐佑 陈增淦
(复旦大学附属中山医院骨科 上海 200032)
糖尿病周围神经病变(diabetic peripheral neuropathy,DPN)是指在排除其他原因的情况下,糖尿病患者出现周围神经相关的症状和/或体征。DPN是糖尿病最为常见的慢性并发症之一,有较高的致残率和死亡率。在所有DPN的临床表现中,疼痛是最突出的症状,也是促使患者就诊的主要原因。DPN影响患者的生活质量,增加患者及家庭的经济负担,进一步加重患者对截肢的焦虑。DPN的治疗方法尚无定论,传统的内科治疗包括控制血糖、对症治疗、营养神经等,可于早期延缓DPN的进展,但对已经存在疼痛、麻木或感觉异常,甚至缺失的患者不能有效缓解其神经病变的症状。因此,外科治疗(即周围神经减压术)为DPN提供了一种新的治疗选择。
周围神经减压术由Dellon于1992年提出并应用于松解DPN患者四肢多处神经,目前已在临床逐步推广。其理论基础是高血糖使神经组织内的山梨醇产生过多,高渗性的山梨醇会导致神经细胞水肿、髓鞘肿胀、使神经产生病变,尤其在解剖狭窄的部位,体积增加的神经会受到卡压而造成损伤。因此以手术方式在解剖狭窄部位对受慢性卡压的周围神经进行松解,可在一定程度上缓解疼痛,使患者病变肢体部位的感觉得以恢复。随着周围神经减压术的推广应用,相关研究也发现多种因素,如患者的血脂水平、糖尿病病程长短、疼痛的性质和分布、解剖变异等,均会对手术疗效产生影响[1-2]。良好的血糖控制是延缓DPN病情进展的基本方法,但对患者神经症状的改善效果有限。有研究表明血糖控制良好的DPN患者接受相同剂量的三环类抗抑郁药后,疼痛缓解的程度要优于血糖控制不佳的患者[3]。但血糖控制情况是否会对DPN患者接受手术治疗后的预后产生影响,目前尚无定论。本研究以糖化血红蛋白(glycosylated hemoglobin,HbA1c)反映DPN患者近期血糖控制情况,分析40例DPN患者实施下肢周围神经减压术之后的疗效差异。
资料和方法
一般资料40例患者均于2014年12月至2016年6月于复旦大学附属中山医院诊断为DPN并行单侧下肢周围神经减压术,其中男性患者24例、女性患者16例,左侧手术17例、右侧手术23例,平均年龄(64.7±9.08)岁,糖尿病平均病程(12.7±5.6)年,患肢出现疼痛的平均时间(1.97±1.46)年。空腹血糖(fasting blood glucose,FBG)平均值(7.03±0.83)mmol/L,HbA1c平均值9.43%±2.84%。将HbA1c≤8%(18例)的患者定义为血糖控制尚可,HbA1c>8%(22例)的患者定义为血糖控制不佳。血糖控制尚可组有男性9例,女性9例,平均年龄(69.11±6.54)岁,糖尿病平均病程(13.39±5.19)年,患肢出现疼痛的平均时间(1.54±0.94)年,FBG平均值(6.59±0.81)mmol/L,HbA1c平均值7.32%±0.51%。血糖控制不佳组有男性15例,女性7例,平均年龄(61.14±9.41)岁,糖尿病平均病程(12.25±5.96)年,患肢出现疼痛的平均时间(2.32±1.72)年,FBG平均值(7.19±0.67)mmol/L,HbA1c平均值11.14%±2.82%。本研究经医院伦理委员会审核批准,所有患者均签署手术知情同意书。
纳入标准(1)Ⅱ型糖尿病的诊断符合1999年WHO提出的诊断标准;(2)术前严格控制血糖:术前空腹血糖<8.0 mmol/L;(3)神经电生理检查证实下肢神经存在神经传导速度减慢,动作电位波幅降低;(4)符合以下外科手术指征(全部):①出现周围神经病变,如麻木、疼痛、感觉减退等表现;②糖尿病是患者神经症状的唯一病因,排除血管病变、酒精中毒、放射线损害、重金属中毒、维生素缺乏、尿毒症等;③患肢外周血管功能正常;④两点辨别觉(two point discrimination,TPD)增宽:拇趾TPD>9 mm;⑤病变部位Tinel征阳性;(5)足部无溃疡创面或溃疡病史。无心、肝、肾功能不全等严重合并症。
手术方法[4]由同一经验丰富的外科医生对患者行下肢四联周围神经减压手术,松解胫后神经、腓总神经、腓深神经和腓浅神经等4条神经。
胫后神经减压术 在患肢踝管胫后神经走行处作一长约6 cm的切口,分离皮下组织,显露并切开屈肌支持带,于踝管内暴露胫后神经,游离胫后神经主干。将足底内外侧神经之间的筋膜予以切除,仔细游离胫后神经的3个分支,即足底内侧支、足底外侧支及足跟支。
腓总神经减压术 于患肢腓骨颈下方作一长约3~4 cm的斜形切口,切开深筋膜,定位并充分暴露腓总神经,游离神经周围粘连组织直至腓总神经进入肌肉处,用显微器械分离神经外膜,彻底减压神经。
腓深神经减压术 于足背第一、二趾骨近足趾端作一长约4 cm的切口,切开皮下组织,游离腓深神经。由于拇短伸肌腱横跨于腓深神经之上,是造成腓深神经卡压的原因之一,因此需由近端和远端切断并切除拇短伸肌腱,彻底松解神经。
腓浅神经减压术 在外踝近端10~12 cm处作一平行腓骨的切口,分离皮下组织及神经周围存在的粘连组织。由于腓浅神经变异较多,应仔细探查可能的分支以充分减压,并使用显微器械解压神经外膜,彻底松解神经。
术前和术后检测指标随访期间嘱咐患者维持原先的糖尿病治疗方案,注意监测血糖水平。在术后6个月由专人对患者进行随访,采用视觉模拟评分(visual analogue scale,VAS)、TPD和10 g单丝测验(10 g-monofilament examination)来评估患者下肢疼痛、麻木的感觉症状,比较患者术前和术后下肢感觉的变化,并记录溃疡及截肢发生率。感觉神经功能的评估采用TPD和10 g单丝测验。
疼痛程度的评估 采用VAS评分,以0~10分表示疼痛程度逐渐增强。以手术前后VAS评分的下降率来评定疼痛缓解的程度,若术后VAS评分下降>80%为明显缓解,20%~80%为缓解,<20%为无变化,VAS上升者为恶化。
TPD 选择患者第1、3、5足趾掌侧面进行测量。测试前告知患者流程并嘱咐其保持闭眼。在室温下将探针作用于固定的足趾部位且不引起疼痛,询问患者认为接触是单点还是两点。偶尔使用单根探针,这样可以避免受试者认为被传递的总是双点刺激。当受试者多次感知单点而不是两点时,达到阈值,并将该阈值记录在数据表中。
10 g单丝测验 以患肢的大脚趾,中趾,小趾,1、3、5跖骨头掌面,足底中央,足侧面,足背及足跟等10处为检查部位,测试前向告知患者流程并嘱咐其保持闭眼;采用触觉检查笔的10 g尼龙丝端,将其垂直于测试处皮肤,施压使尼龙丝弯曲约1 cm,询问患者是否感受到刺激;如重复2次均不能感觉到刺激,判断此点为阴性,检查部位顺序随机。将能感觉到刺激的部位数目详细记录,若患侧感觉到 8个刺激点或不足8个点视为异常[5]。
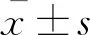
结 果
患者一般资料血糖控制尚可患者(HBA1c≤8%)与血糖控制不佳患者(HBA1c>8%)在性别、体重指数(body mass index,BMI)、糖尿病病程等和DPN病程方面差异均无统计学意义(表1)。
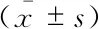
表1 两组间人口统计学资料及相关指标的比较Tab 1 Comparison of demographic data and relevant index between the two groups
术后血糖控制情况术后6个月随访时患者FBG平均值为(7.37±1.28)mmol/L,与术前相比差异无统计学意义;HbA1c平均值8.15%±1.93%,较术前明显下降(P<0.05)。
术后溃疡发生率及截肢率在术后6个月随访过程中,所有患者下肢手术切口愈合良好,未出现感染,未发生因DPN所致的溃疡和截肢。
下肢VAS的检测结果术后6个月随访时,37.5%(15/40)的患者手术侧下肢疼痛症状得到明显缓解,47.5%(19/40)的患者手术侧下肢疼痛症状缓解,所有患者VAS评分由术前(6.83±0.96)分下降至(3.73±1.28)分,差异有统计学意义(P<0.01)。血糖控制尚可患者的术前VAS评分与血糖控制不佳患者的评分无明显差异,而前者术后VAS评分显著低于后者(P<0.01,表2)。
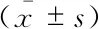
表2 DPN患者术前和术后VAS评分Tab 2 VAS values before and after operation in DPN patients
下肢10 g单丝测验的结果术后6个月随访,10 g单丝测验的均值由术前3.83±0.78上升至5.30±0.88,差异有统计学意义(P<0.01)。血糖控制尚可患者的术前10 g单丝测验的分值与血糖控制不佳患者的分值无明显差异,而术后的10 g单丝测验结果前者显著高于后者(P<0.01,表3)。
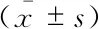
表3 DPN患者术前和术后10g单丝测验Tab 3 10 g-monofilament examination before and after operation in DPN patients
下肢TPD的检测结果术后6个月随访时,77.5%(31/40)的患者手术侧下肢麻木症状有明显缓解,术侧拇趾TPD平均值由术前(13.10±1.36)mm下降至(7.35±1.59)mm,术侧第3趾TPD平均值由术前(10.45±1.48)mm下降至(6.10±1.32)mm,术侧小趾TPD平均值由术前(10.08±1.19)mm下降至(7.03±1.05)mm,差异均有统计学意义(P<0.01)。血糖控制尚可患者第1、3、5足趾术前TPD与血糖控制不佳患者无明显差异,而前者术后TPD均显著低于后者(P<0.05)(表 4)。
表4 DPN患者术前和术后TPDTab 4 TPD before and after operation in DPN patients
讨 论
周围神经减压术通过松解神经通路上的受压部位,使神经纤维恢复正常的营养和血供,从而缓解症状。自Dellon于1992年首先应用周围神经减压术治疗多发DPN,国内外相关研究也证实了这项技术在DPN治疗中的效果。一项包含1 526名糖尿病患者的队列研究描述了周围神经减压手术的结果,并指出该技术对患者的疼痛症状、感觉功能及神经传导速度的恢复有积极作用[1]。然而,有学者对该技术持保留态度,认为报道的研究多为观察性研究,缺乏随机对照研究,且部分研究长期随访后反馈的疗效要略差于术后短期内的疗效。最近一项对42例DPN患者进行的单中心、非盲、随机对照试验,以同一患者的术测下肢为试验组,对侧下肢作为对照组。在这项研究中,74%的患者在术后3、6、12月的随访中显示疼痛及感觉功能障碍症状改善,但第12个月时的疗效略差于第3个月[6]。周围神经减压术可以解除慢性卡压造成的外周神经损伤,恢复感觉、缓解疼痛和麻木等症状,但不是所有DPN患者都具有手术指征。该术式适用于伴有疼痛、麻木等症状的确诊为糖尿病的Tinel征阳性的患者。Tinel征是判断手术预后的重要标志,Tinel征阳性提示神经再生能力尚存,在术后获得满意疗效的概率较高[7]。此外TPD也是评估外周神经受压程度的重要指标,TPD丧失提示患者周围神经轴索缺失,预后较差。
以往研究多集中在对周围神经减压术治疗DPN临床效果的评估和各种评估方式的比较。很少有研究对可能影响手术疗效的因素进行分析。本研究中,将40例DPN患者以HbA1c=8%为界限,分为血糖控制尚可组和血糖控制较差组。这一分组标准考虑到DPN患者糖尿病病程多超过10年,对血糖的长期监测和控制不够严格。根据美国糖尿病协会(ADA)2017年发布的糖尿病诊疗标准,血糖控制不佳患者HbA1c目标值可定为8%。HbA1c可有效反映患者2~3个月内血糖的控制情况。本研究采用VAS评分、10 g单丝测验和TPD作为评估手术疗效的指标。虽然这3项指标都较为主观,但成本低廉、应用方便且能直观反映患者术后恢复情况。神经电生理检查是在评估DPN病情的多种方法中最为客观、敏感、可靠,然而由于其费时、费力及成本高,难以在门诊随访过程中广泛应用;因此本研究仅将其作为DPN的诊断标准之一。研究结果表明,血糖控制尚可患者和血糖控制不佳患者术前各项指标均无显著差异(P>0.05),前者术后疼痛和感觉障碍的改善程度均明显高于后者(P<0.05)。由此说明血糖控制尚可患者接受周围神经减压术的效果要优于血糖控制不佳患者。长期良好的血糖控制不仅可预防、延缓DPN发生与进展,还可改善神经减压术的治疗效果,因此严格控制血糖是治疗DPN的基础。
本研究结果表明,周围神经减压术可有效缓解DPN患者的疼痛和感觉障碍症状,术前血糖控制情况对手术患者的预后至关重要。VAS评分、10 g单丝测验和TPD的结合对DPN患者的术前术后综合评估有重要价值。
