碳酸钙沉淀法从钨酸钠溶液中深度脱除磷的研究
2019-05-06方君娟王水龙
方君娟,王水龙,杨 亮
(1.浙江省残疾人体育训练指导中心,浙江 杭州 310000;2.赣州海创钨业有限公司,江西 赣州 341500;3.江西理工大学 材料冶金化学学部,江西 赣州 341000)
0 引 言
目前,我国黑钨矿资源逐渐枯竭,低品位白钨矿和黑白钨混合矿已成为我国钨冶炼工业的主要原料[1-4]。我国钨冶炼企业多采用氢氧化钠分解和碳酸钠压煮工艺处理低品位白钨矿和黑白钨混合矿,但都存在浸出剂用量过大的缺点[5-7],需要加入3~5倍理论用量的浸出剂才能获得较高钨浸出率(90%以上)。磷酸钠和氢氧化钠混合分解工艺能够实现低品位白钨矿和黑白钨混合矿的高效浸出[8],且浸出试剂用量相对较低,并已在我国部分钨冶炼企业实现工业化应用。美中不足的是,为了实现高的钨浸出率,需要加入过量的磷酸钠,导致浸出液中残留磷浓度较高[9],后续强碱性阴离子交换过程得到的钨酸铵溶液磷含量难以达到要求,从而使得仲钨酸铵产品磷含量超标。为此,需要从浸出液(钨酸钠溶液)中净化除磷。
经典化学沉淀法采用加入氯化镁,使浸出液中磷以磷酸镁沉淀除去[10-11],但该方法使钨酸钠溶液中氯离子含量增加,降低后续离子交换过程钨交换容量;另外反应过程形成胶体状氢氧化镁,致渣含钨较高,钨损较大。研究者提出采用伯胺和TBP(磷酸三丁酯)从弱碱性钨酸钠溶液中以磷钨杂多酸萃取除磷[12],但由于浸出液中磷含量较高,采用该法萃取除磷会造成钨的大量损失,此外浸出液中含有一定的游离碱,需要加入酸中和至弱碱性。此外,还有研究者采用季铵盐萃取剂三辛基甲基氯化铵从碱性钨酸钠溶液中萃取钨酸根,使磷进入萃余液实现钨磷分离,但需经7级逆流萃取才能达到较好的分离效果[13]。
根据难溶化合物溶度积理论可知,溶液中化合物溶度积越小,则该化合物越稳定。由无机化合物热力学手册可知[14],磷酸钙、碳酸钙和钨酸钙的溶度积常数依次增大(25℃时,KSPCa3(PO4)2=2.0×10-29,KSPCaCO3=4.5×10-9,KSPCaWO4=8.7×10-9)。鉴于此,本研究采用往钨酸钠溶液中加入碳酸钙使得磷生成难溶的磷酸钙沉淀除去,而钨酸根存于溶液中,实现低钨损条件下磷的高效去除,且不会引入有害杂质离子,反应过程见方程式(1)。
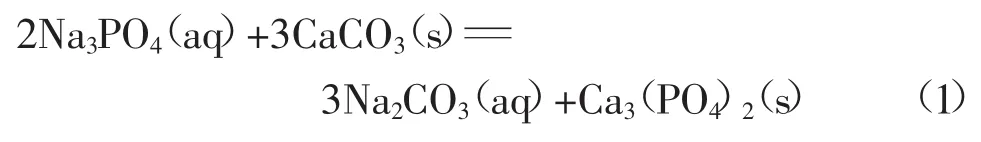
1 试验部分
1.1 试验原料与试剂
试验原料:磷酸钠和氢氧化钠分解白钨矿所得的粗钨酸钠溶液,其主要成分如表1所示。

表1 粗钨酸钠溶液主要成分Tab.1 The main composition of sodium tungstate solution
试验试剂:碳酸钙、磷酸钠、氢氧化钠、钨酸钠和盐酸均为分析纯。
1.2 试验方法
分别取一定体积的粗钨酸钠溶液,将其倒入烧杯并放置在恒温水浴锅中,保持一定温度,然后加入一定量的碳酸钙,反应一定时间后,进行固液分离,采用磷钼蓝分光光度法测定滤液中的磷浓度,并计算除磷率;滤渣洗涤烘干后,分析其中WO3含量,计算钨的损失率。通过改变碳酸钙用量、反应温度、反应时间、粗钨酸钠溶液中初始磷浓度和氢氧根浓度,比较一定条件下对除磷效果的影响,选出最佳工艺参数。
2 结果与讨论
2.1 碳酸钙用量对除磷的影响
在150 mL的粗钨酸钠溶液中分别加入1.1倍、1.2 倍、1.4 倍、1.6 倍、1.8 倍理论用量的碳酸钙,反应温度为65℃,反应时间90min,搅拌速率为300r/min,碳酸钙用量对除磷效果的影响如图1所示。
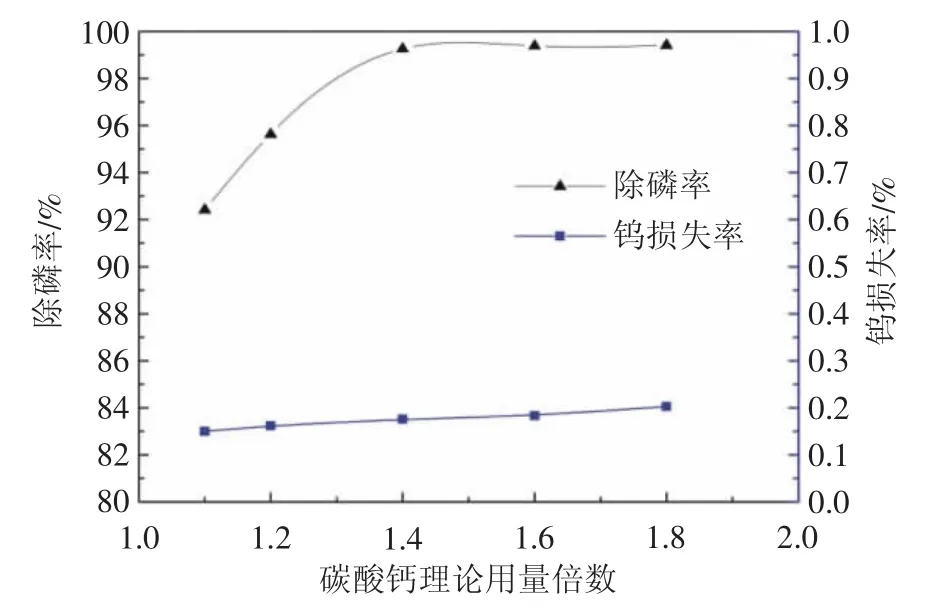
图1 碳酸钙用量对除磷效果影响Fig.1 Effect of calcium carbonate dosage on phosphorus removal
由图1可知,随着碳酸钙用量增大,钨酸钠溶液中磷的去除率逐渐增大,但对沉淀渣中钨损失率影响很小。当碳酸钙用量从1.1倍增大至1.4倍时,除磷率由92.41%上升至99.26%,渣中钨损失率由0.15%缓慢升高至0.176%;继续增大碳酸钙用量至1.8倍时,除磷率几乎保持不变,渣中钨损失也变化很小。综合考虑碳酸钙用量和除磷效果,选用1.4倍理论用量碳酸钙较好,此时钨酸钠溶液中残留磷浓度仅为7 mg/L,实现了深度除磷。
2.2 反应温度对除磷的影响
在150 mL的粗钨酸钠溶液中加入1.4倍理论量的碳酸钙,反应时间90 min,搅拌速率为300 r/min,反应温度分别为30℃、50℃、65℃、80℃,温度对除磷效果的影响如图2所示。
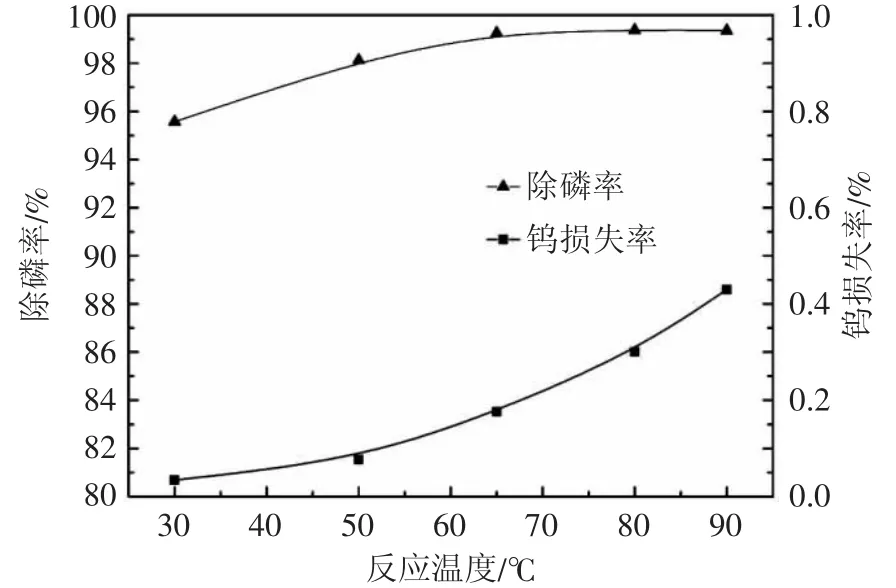
图2 反应温度对除磷的影响Fig.2 Effect of temperature on phosphorus removal
由图2可知,反应温度对碳酸钙脱磷的影响较大,且温度越高除磷效果越好,当反应温度由30℃上升至65℃时,除磷率从95.57%增大到99.26%;继续增大反应温度至90℃,除磷率几乎保持不变。另一方面,反应温度对沉淀渣中钨的损失影响也较大,随着反应温度升高,渣中钨损失呈逐步升高的趋势,当反应温度由30℃上升至90℃时,渣中钨损失从0.03%增大至0.43%。温度升高虽然有利于碳酸钙和磷酸根反应生成磷酸钙沉淀,但同时也促进了碳酸钙和钨酸根生成钨酸钙,从而使得除磷率和渣中钨损失率同时增大。综合考虑,选取65℃较为合适。
2.3 反应时间对除磷的影响
在150 mL的粗钨酸钠溶液中加入1.4倍理论量的碳酸钙,反应温度为65℃,搅拌速率为300r/min,反应时间分别控制为 60min、90min、120min、150min,结果如图3所示。
由图3可知,延长反应时间有利于磷的脱除,当反应时间由30 min增大至90 min,除磷率由82.69%增大至99.26%,之后再继续延长反应时间,除磷效果变化不大。由于碳酸钙为难溶固体,为液-固反应体系,其在溶液中首先发生溶解释放出游离的钙离子,再与磷酸根离子结合形成磷酸钙沉淀,相比于液-液反应体系,反应速度更慢,因此,反应时间达到90 min,除磷率才逐渐趋于稳定。当反应时间从30 min增大至60 min时,渣中钨损失从0.085%上升至0.158%,之后基本保持不变。因此,选择反应时间90 min较为合适。
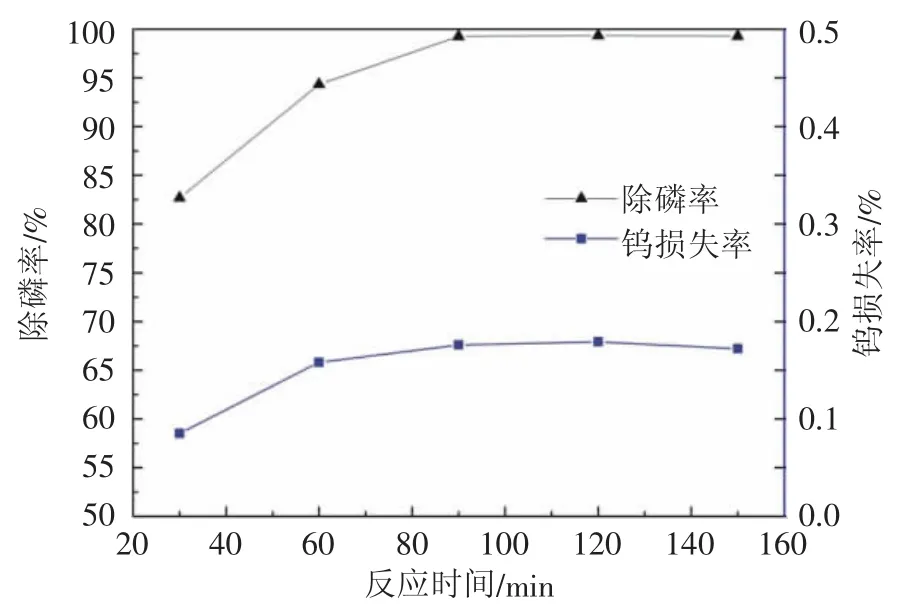
图3 反应时间对除磷的影响Fig.3 Effect of reaction time on phosphorus removal
2.4 溶液中初始磷浓度对除磷的影响
在4份体积为150 mL的粗钨酸钠溶液通过补加一定量的磷酸钠使得溶液中磷浓度分别为0.95g/L、1.20 g/L、1.50 g/L、2.0 g/L,分别加入 1.4 倍理论量的碳酸钙,反应温度为65℃,搅拌速率为300 r/min,反应时间为90 min,结果如图4所示。

图4 溶液中初始磷浓度对除磷的影响Fig.4 Effect of initial phosphorus concentration on phosphorus removal
由图4可知,当溶液中初始磷浓度在0.95~2.0 g/L范围内,除磷效果相差甚微,除磷率都保持了99%以上。经净化除磷后的钨酸钠溶液,磷浓度非常低,W/P浓度比高达1.5×104,达到了深度净化除磷的要求。另外,随着溶液中初始磷浓度增加,沉淀渣中钨的损失率基本保持不变,但溶液中初始磷浓度越高,相应需要碳酸钙用量也越大。
2.5 溶液中氢氧化钠浓度对除磷的影响
在5份体积为150 mL的粗钨酸钠溶液通过补加一定量的氢氧化钠或盐酸使得溶液中OH-浓度分 别为 1.75 g/L、6.52 g/L、10.68 g/L、15.34 g/L、21.62 g/L,分别加入 1.4 倍理论量的碳酸钙,初始磷浓度为0.95 g/L,反应温度为65℃,搅拌速率为300r/min,反应时间为90 min,结果如图5所示。
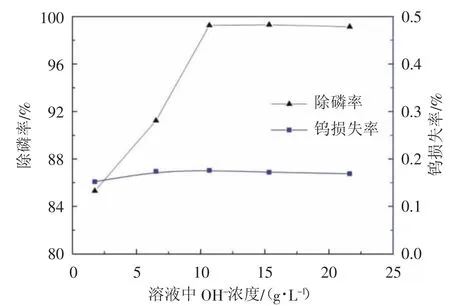
图5 溶液中氢氧化钠浓度对除磷的影响Fig.5 Effect of sodium hydroxide concentration on phosphorus removal
由图5可知,溶液中氢氧化钠浓度对除磷效果影响很大,当溶液中氢氧根离子浓度由1.75 g/L上升至10.68 g/L时,除磷率从85.31%急剧增大至99.26%,之后再增大氢氧化钠浓度,除磷率基本保持不变。这主要是因为磷酸根离子在溶液中离子形态与溶液pH密切相关。当溶液呈弱碱性时,磷主要以HPO42-离子存在,而CaHPO4溶度积大于CaCO3,因此不利于磷的脱除,因此表现为氢氧化钠浓度较低时,除磷率较低。当溶液中氢氧化钠浓度较高时,磷则以PO43-离子存在,因此,有利于形成磷酸钙沉淀,除磷率也随之升高。另外,氢氧化钠浓度对沉淀渣中钨损失率影响很小,钨损失率几乎都保持在0.17%左右。因此,粗钨酸钠溶液中保持一定的碱度有利于磷的脱除。
3 结 论
经过对磷酸钠和氢氧化钠分解白钨矿得到的浸出液,采用加入碳酸钙沉淀除磷的试验,可得出以下结论:
(1)含磷的粗钨酸钠溶液中,碳酸钙是有效的除磷试剂,能够满足深度除磷的要求,且不会引入杂质离子,同时渣中钨损失小,实现了深度选择性脱磷。
(2)考查了碳酸钙用量、反应温度、反应时间、溶液中初始磷浓度和氢氧化钠浓度对粗钨酸钠中除磷效果的影响。当溶液中初始磷浓度0.95~2.0 g/L,氢氧根浓度10.68 g/L,碳酸钙用量为1.4倍理论量,温度65℃,搅拌反应90 min,除磷率达到99%以上,沉淀渣中钨损失率约0.17%。
