固相萃取-气相色谱法测定茶叶中氟环唑
2018-12-03李峥嵘黄晓东
李峥嵘,黄晓东
(安徽工程大学 生物与化学工程学院,安徽 芜湖 241000)
氟环唑(epoxiconazole),分子式C17H13ClFN3O,是德国巴斯夫公司研发的内吸型、长效、低毒三唑类含氟杀菌剂,在预防和防治一系列禾谷类作物病害方面取得了良好效果[1-2]. 近年来随着三唑类杀菌剂的使用和乱用,对生态环境造成极大危害[3-4].2015年,氟环唑被欧盟划分为“(1类、2类)生殖毒性”和“(2类)致癌”的农药[5].欧盟规定了氟环唑在茶叶上的MRLS(最大残留量)值为0.05 mg/kg.目前我国在此方面无明确规定,可能会导致我国茶叶出口在欧盟受阻,故研究氟环唑残留量检测方法具有现实经济意义.
目前对氟环唑残留量的检测大多数集中在蔬菜和谷物中,检测方法有UPLC-MS/MS[6-9],GC-MS/MS[10-11]等.茶叶中的氟环唑残留分析净化多用中性氧化铝[12]、GCB柱(石墨化炭黑)[13]、TPT混合填料柱[14-15]、GPC(凝胶渗透色谱)[16]以及QuEChERs(分散固相萃取)[17]等净化方法,以上方法均可靠,但步骤较为繁琐.实验采用Florlisil柱-气相色谱法检测茶叶中氟环唑残留量,简化了前处理步骤,提高了实验精确性和稳定性,是有效监督控制氟环唑残留量的检测方法.
1 材料与方法
1.1 材料与试剂
绿茶,产自芜湖;乙腈、丙酮、正己烷、甲醇、氯化钠(色谱纯或分析纯);C18萃取柱;NH2萃取柱;Florlisil柱;氟环唑标样(浓度≥99%,德国Dr.Ehrenstorfer);超纯水.
1.2 仪器与设备
GC-2010气相色谱仪(配有ECD)(日本岛津公司);VX-200涡旋混合器(美国Labnet);旋转蒸发浓缩仪(上海弘懿仪器设备有限公司);TGL-16G离心机(上海安亭仪器厂).
1.3 实验方法
(1)气相色谱条件.色谱柱:DB-17柱(30 m×0.32 mm×0.25 μm);温度:INJ为250 ℃ ;DET为300 ℃;COL为180 ℃(1 min),8 ℃/min ,250 ℃(10 min);载气 :高纯氮气 ,柱流量 2.0 mL/min;进样方式:不分流,进样量1 μL.
(2)标准曲线的绘制.准确称取10 mg氟环唑标准品,用正己烷溶解配制成1.0 mg/mL的氟环唑标准储备母液(不用时置于-18 ℃以下冰箱避光储存)和0.01 mg/mL的氟环唑储备液(不用时置于0 ℃~4 ℃冰箱避光储存).用正己烷稀释成1.0 μg/mL、0.2 μg/mL、0.1 μg/mL、0.06 μg/mL、0.02 μg/mL的氟环唑标准溶液,在选定色谱条件下进行GC-ECD检测,并计算氟环唑标准曲线线性关系方程.
(3)样品前处理.用粉碎机将茶叶粉碎成末,过100目筛.称取1.0 g茶叶粉样品于50 mL加盖离心管中,加入18 mL乙腈和0.4 g NaCl,涡旋混匀,超声辅助提取12 min,8 000 r/min离心10 min,转移上清液至鸡心瓶中,真空旋转浓缩近干,加入5 mL正己烷-丙酮(7+3)超声溶解,上样至Florlisil柱+GCB混合柱,接出流出液,再每次用2 mL正己烷-丙酮(7+3)3次清洗鸡心瓶,并将洗涤液加入柱中,继续加入20 mL正己烷-丙酮(7+3)洗脱,旋转浓缩近干,其后加入1 mL甲醇-水(9+1)超声溶解,涡旋混匀,过0.22 μm滤膜转移至进样瓶,供GC-ECD分析.
(4)固相萃取条件选择.
①提取剂的选择.准确称取4组相等的茶叶样品,同时添加质量浓度为0.05 mg/kg的氟环唑标准液,分别用正己烷、乙腈、丙酮和甲醇作为提取剂,在其他实验条件保持不变的情况下,按照上述步骤进行样品前处理,供GC-ECD分析,计算回收率,确定提取剂的种类.
②提取剂体积的选择.准确称取5组相等的茶叶样品,同时添加质量浓度为0.05 mg/kg的氟环唑标准液,只改变提取剂的体积,分别用10 mL、15 mL、20 mL、25 mL和30 mL选定的提取剂提取,计算回收率,确定提取剂的体积.
③NaCl加入量的选择.准确称取5组相等的茶叶样品,同时添加质量浓度为0.05 mg/kg的氟环唑标准液,只改变NaCl固体加入量,NaCl加入量分别为0.0 g、0.4 g、0.8 g、1.2 g、1.6 g,计算回收率,确定NaCl加入量.
④超声处理时间的选择.为了使净化效果达到最佳,实验采用超声辅助的方法,超声时间分别设定为0 min、5 min、10 min、15 min和20 min,其他条件不变,计算回收率,确定超声处理时间.
⑤洗脱液比例的优化.准确称取4组相等的茶叶样品,同时添加质量浓度为0.05 mg/kg的氟环唑标准液,只改变洗脱液正己烷、丙酮的体积比,体积比分别为6∶4、7∶3、8∶2、9∶1,计算回收率,确定洗脱液比例.
⑥固相萃取柱选择.为了使净化效果达到最佳,分别选用C18,NH2和Florlisil 3种固相萃取柱,氟环唑标准液质量浓度为0.05 mg/kg,其他条件不变,计算回收率,确定最佳萃取柱.
⑦方法的重复性实验.在选定的最佳实验条件下对加标水平为0.05 mg/kg的茶叶样品进行处理及测定,连续5天每天测一次,计算其精密度.
⑧方法的回收率实验.取3份等量的茶叶样品,选择3种不同质量浓度的氟环唑标准液进行加标,添加水平分别为0.02 mg/kg、0.05 mg/kg、0.1 mg/kg,采用最佳的实验条件进行分析,连续测定5次,取平均值,计算回收率和变异系数.
⑨结果计算公式.氟环唑质量含量c1(ug/g)按下式计算
式中,c1为样品中氟环唑含量(μg/g);c为仪器检测的质量浓度(mg/L);V为最终定容体积(mL);m为样品质量(g).
2 结果与讨论
2.1 提取剂的选择
氟环唑在不同提取剂中的溶解度是不一样的,在满足实验要求的前提下,不同的提取剂对氟环唑的回收率有一定的影响.提取剂对氟环唑回收率的影响如图1所示.由图1可知,乙腈和丙酮作为提取剂,回收率较高,实验过程中发现丙酮萃取液中含有大量的色素,导致后续的净化过程存在一定的困难,故选择乙腈作为提取剂.
2.2 提取剂体积的选择
选定乙腈作为提取剂,改变乙腈的体积,考察乙腈体积对氟环唑回收率的影响, 结果如图2所示.由图2可知,乙腈体积为20 mL时回收率最高;乙腈体积小于20 mL时,提取的不够充分;乙腈体积大于20 mL时,导致后续浓缩过程的氟环唑的损失,故选择最优提取剂体积20 mL.
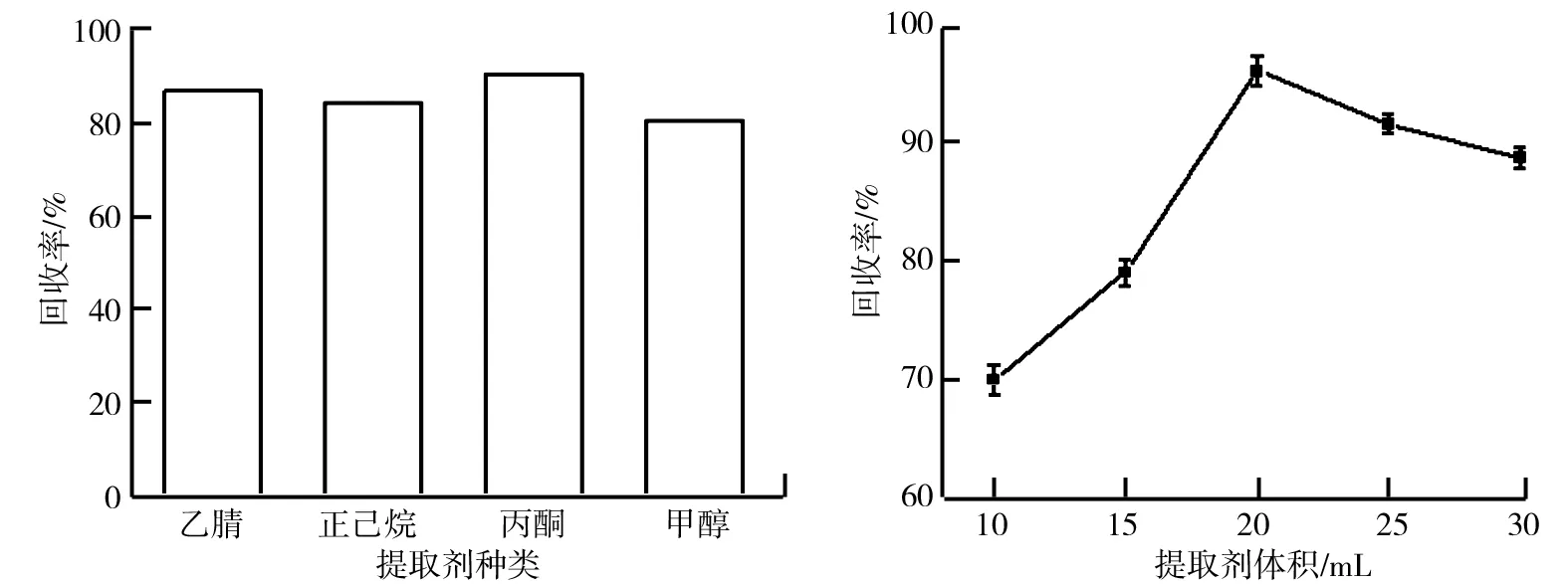
图1 提取剂对氟环唑回收率的影响 图2 提取剂体积对氟环唑回收率的影响
2.3 NaCl加入量的选择
在样品溶液中加入NaCl会降低待测物在水相中的溶解度、制约萃取剂在水中的溶解性,从而有利于对待测组分回收.NaCl质量对氟环唑回收率的影响如图3所示.由图3可知,在NaCl的用量逐渐增加时氟环唑的回收率先增加后降低,在NaCl的用量为0~0.8 g时,回收率呈线性增加,NaCl加到0.8 g时成为转折点,随着NaCl质量浓度增高导致萃取效果变差,回收率降低.因此选择0.8 g作为NaCl的最佳用量.
2.4 超声处理时间的选择
样品的前处理过程中,超声辅助萃取可以提高萃取效率.实验具体考察了不同的超声处理时间对氟环唑回收率的影响,结果如图4所示.由图4可知,超声处理时间由0 min到15 min时,萃取效果在提高,继续超声处理,其促进作用达到了饱和,可能是因为氟环唑见光易分解的特性,长时间暴露在日光中,有部分损失掉了,使得氟环唑的回收率开始下降,综合考虑超声时间为15 min时最佳.

图3 NaCl质量对氟环唑回收率的影响 图4 超声时间对氟环唑回收率的影响
2.5 洗脱液比例的优化
由于样品的基质较杂,合适的洗脱液可使目标物尽可能从柱中洗脱下来,同时减少杂质被洗脱下来,对比研究了不同体积比洗脱液的洗脱效果,结果如图5所示.由图5可知,氟环唑的回收率随着洗脱液体积比的减小先增高后降低,在体积比为7:3时回收率较高,可能是由于洗脱液的极性偏大或偏小,不利于目标物的洗脱净化,导致氟环唑的回收率较低.
2.6 固相萃取柱选择
样品中的基质成分复杂多样,必须经过净化处理,不同的萃取柱性能、效果不同,合适的萃取柱可降低检测器的杂峰干扰,提高回收率.为了最大限度地排除杂质离子的干扰,对比研究了不同种类的固相萃取柱的净化效果,结果如图6所示.由图6可知,Florlisil柱的净化效果最好.

图5 洗脱液比例对氟环唑回收率的影响 图6 萃取柱种类对氟环唑回收率的影响
2.7 标准曲线的绘制

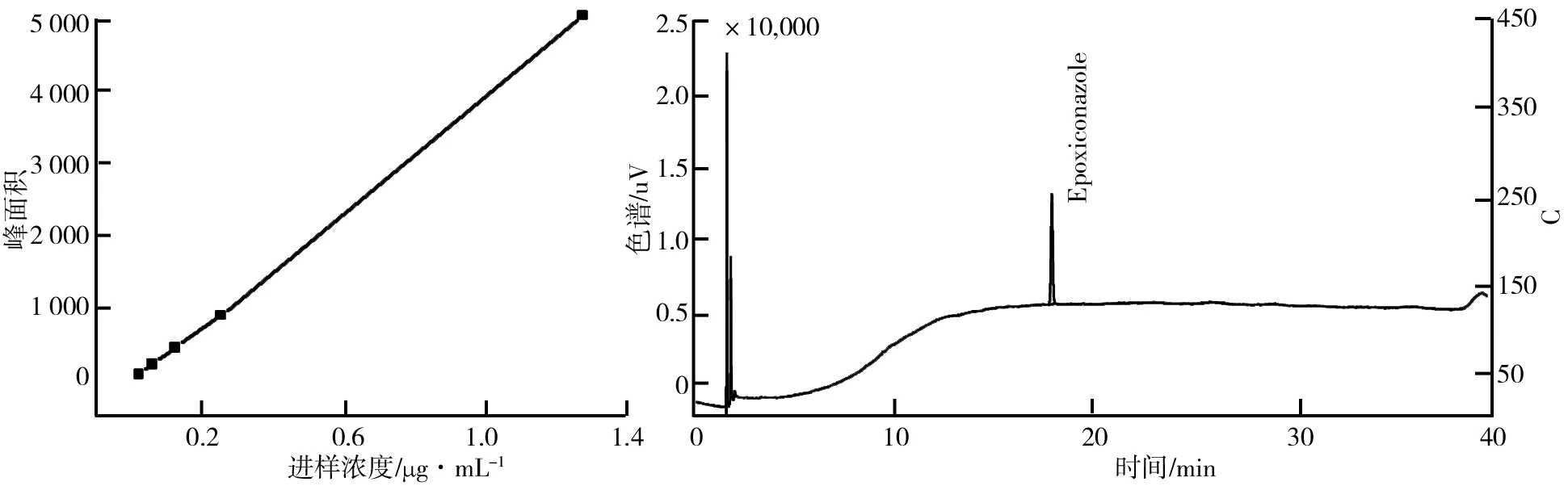
图7 氟环唑标准曲线 图8 氟环唑标准溶液气相色谱图(1.275 μg/mL)
2.8 响应面分析优化氟环唑的提取条件
(1)响应面试验因素水平的选择.实验根据以上单因素实验结果,选超声时间、氯化钠用量和提取剂体积为主要考察因素,以氟环唑的回收率为指标,设计3因素3水平响应面试验,选用Design-Expert 8.0软件中Box-Behnken作为响应面模型.实验的因素及水平如表1所示.

表1 响应面试验
(2)响应面实验设计及结果分析.以A(超声时间)、B(NaCl用量)、C(提取剂体积)为自变量,氟环唑的回收率为Y(响应值),以此进行17组分析试验,其中用以估算误差中心试验有5个.BBD的试验结果如表2所示.根据表2中试验的结果应用Design-Expert 8.0软件进行分析,3个自变量模型的方差分析结果如表3所示.由表3可知,模型的F=16.77,P=0.000 6<0.001,表明实验的二次模型是极显著的,在统计学上有意义.实验失拟项P=0.131 4>0.05,对模型有利,无失拟因素,数据中无异常点出现,因此可用于预测各因素与氟环唑回收率的关系.
由Design-Expert 8.0软件得出各个因素的效应图如图9、图10、图11所示.由图9、图10、图11可知,图形的表面有明显弯曲,可得各个因素对响应值Y是非线性的,A、B、C三个因素水平存在极值点.
(3)响应面回归模型的建立.结合Design-Expert软件计算,可得该响应面模型的回归方程如下:
R=-281.546 25+22.601 25A+205.528 12B+12.283 5C-3.275AB-2.7E-003AC-5.076 25BC-0.629 8A2-42.125B2-0.214 9C2
(4)各因素水平的优化.根据效应图绘制回归方程的3D响应面图,回归方程存在极值点.为了确证其最佳值,对方程取一阶偏导,整理可得:
22.601 25-3.275B-2.7E-003C-1.259 6A=0
205.528 12-3.275A-5.076 25C-48.25B=0
12.283 5-2.7E-003A-5.076 25B-0.425 8C=0
解方程组得A=13.02,B=0.75,C=19.65,代入响应面方程得到氟环唑的最大响应值是87.31.即在超声时间13 min,NaCl用量0.7 g,提取剂乙腈20 mL时,氟环唑的回收率高达87.31%.

表2 BBD的试验结果

表3 响应面试验的方差分析结果
P<0.05时,影响显著;P<0.01时,影响极显著,分别用*和**表示

图9 A和B对氟环唑回收率的影响 图10 A和C对氟环唑回收率的影响

图11 B和C对氟环唑回收率的影响
2.9 方法的重复性实验
准确称取茶叶样品,按上述方法进行测定,结果如表4所示.由表4可知,样品中氟环唑质量浓度的平均值是0.044 7 mg/kg,RSD为3.55%,方法重复性和精密度较好.
表4方法精密度实验
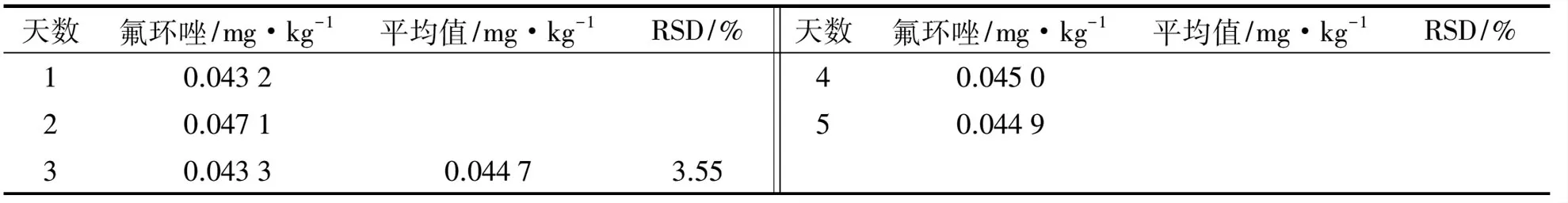
天数氟环唑/mg·kg-1平均值/mg·kg-1RSD/%10.043220.047130.04330.04473.55
2.10 方法的回收率实验
分别称取3份茶叶样品,在样品中分别加入0.02 mg/kg、0.05 mg/kg、0.1 mg/kg 3种质量浓度的氟环唑标准液,以最佳条件进行实验处理,结果如表5所示.由表5可知,氟环唑在茶叶中的添加回收率范围为86.38%~92.06%,平均回收率为89.32%,且变异系数范围为3.06%~5.64%,可见方法的回收率较好.茶叶粉中氟环唑的添加回收色谱图(加标水平为0.127 5 mg/kg)如图12所示.
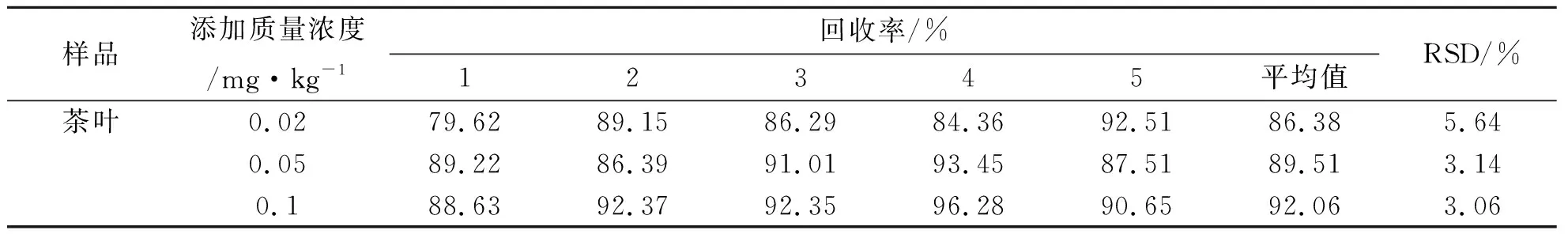
表5 方法的回收率实验

图12 氟环唑在茶叶中的添加回收色谱图
3 结论
SPE-GC测定茶叶中的氟环唑残留量的实验中,样品净化步骤采用Florlisil柱,应用Design-Expert 8.0优化样品预处理方法,得到最佳条件下回收率为87.31%,加标回收率在86.38%~92.06%之间,重复性实验RSD为3.55%,最低检出限为0.007 μg/mL.实验操作简单、快速、稳定,方法的精密度、重现性、灵敏度、回收率、线性关系良好,可用于大量样品的检测.
