IP方案与TP方案二线治疗小细胞肺癌的临床观察
2015-10-21孙永臣韩文杰
孙永臣 刘 军 杨 曦 韩文杰
(河南省商丘市第一人民医院肿瘤科,河南 商丘 476100)
IP方案与TP方案二线治疗小细胞肺癌的临床观察
孙永臣刘军杨曦韩文杰
(河南省商丘市第一人民医院肿瘤科,河南 商丘 476100)
目的 本研究为比较伊立替康联合顺铂(irinotecan plus cisplatin,IP)方案与紫杉醇联合顺铂(paclitaxel plus cisplatin,TP)方案二线治疗小细胞肺癌(SCLC)的近期疗效、无进展生存期及不良反应。方法 分析70例SCLC患者,随机分为两组,分别接受IP和TP方案的主治疗。要研究终点为无进展生存期(progression-free survival,PFS),客观反应率(response rate,RR)和不良反应。结果 IP组RR 68.6%,中位PFS为6.5个月;TP组RR 60.0%,中位PFS为4.6个月,两组PFS比较有统计学差异(P<0.05)。两组主要不良反应均为骨髓抑制和胃肠道反应,但骨髓抑制无统计学差异(P>0.05),IP组腹泻发生率高于TP组,两组比较差异具有统计学意义(P<0.05)。结论 IP方案二线治疗SCLC客观疗效与TP方案相当,但PFS优于TP组,不良反应可耐受。
伊立替康;紫杉醇;小细胞肺癌;化疗
小细胞肺癌(small cell lung cancer,SCLC)恶性程度高,预后差,生存期短,一线化疗后约80%的局限期及全部广泛期患者会在2年内复发或进展,需要二线化疗控制肿瘤进展,使得二线化疗在小细胞肺癌治疗中的地位非常重要,目前尚无标准的二线化疗方案。本研究中,我们比较了伊立替康联合顺铂与紫杉醇联合顺铂二线治疗小细胞肺癌患者的疗效、不良反应、无进展生存时间,以期探索更适合小细胞肺癌患者的二线化疗方案。
1 材料与方法
1.1临床资料:我院2008年1月至2013年6月期间收治的70例既往经过一线方案化疗后进展患者,均有包括术后病理、肺穿刺、纤维支气管镜活检病理明确小细胞肺癌病理诊断。患者中女性17例,男性53例;年龄35~76岁;局限期患者28例,广泛期患者42例。有符合RECIST疗效评价标准的可测量病灶,PS 0~2分,预计生存期>2个月,肝肾功能、心电图及血常规均未见明显异常,无症状的脑转移患者,依从性好。排除标准:妊娠期或哺乳期妇女,脑转移有症状,无法控制的胸腔积液,存在其他肿瘤病史。采用随机分组将患者分为伊立替康联合顺铂组(IP方案组,35例)和紫杉醇联合顺铂组(TP方案组,35例),两组一般资料的差异均无统计学意义(P>0.05)。
1.2治疗方案。IP组:伊立替康80 mg/m2,d1、d8天,静脉滴注;顺铂75 mg/m2,d1~3天静脉滴注,21 d一个周期;TP组:紫杉醇150 mg/m2,d1,DDP 75 mg/m2,d1~3天静脉滴注,21 d一个周期;伊立替康化疗前常规备有易蒙停和思密达,出现腹泻时服用。紫杉醇给药前12 h及6 h各口服地塞米松20 mg,化疗给予西咪替丁及异丙嗪应用。化疗前常规给予止吐及保护胃黏膜药物治疗应用,化疗前后定期复查血常规和肝功生化,出现消化道反应、肝功能异常及骨髓抑制等不良反应给予对症处理。
1.3评价标准:每化疗2个周期后应用256层螺旋CT评估疗效,末次化疗结束后每2个月复查CT评估疗效直至疾病进展,随访截止时间为2014年1月。客观疗效评价按RECIST实体瘤评价标准分为:完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD),以CR+PR计算有效率(RR)。疾病无进展生存期(PFS)为从患者化疗开始至CT确认为疾病进展的时间。毒性反应按WHO急性及亚急性毒性分级标准分为0~4级。
1.4统计学方法:采用SPSS18.0版统计软件处理。计数资料用χ2或Fisher确切概率法,用Kaplan-Meier绘制生存曲线。以P<0.05为差异有统计学意义。
2 结 果
2.1化疗完成情况及近期疗效:IP方案组共完成146个化疗周期,中位周期数4个;TP方组共完成153个化疗周期,中位周期数4个。所有患者均可评价近期疗效。IP方案组获CR 6例,PR 18例,SD 7例,PD 4例,RR为68.6%;TP方案组CR 7例,PR 14例,SD 8例,PD 6例,RR为60.0%;两组的RR差异无统计学意(P>0.05),见表1。

表1 IP组和TDP组患者的治疗客观反应表(例)
2.2不良反应:两组主要不良反应均为骨髓抑制和消化道道反应。但两组Ⅲ+Ⅳ度毒性反应均无统计学差异(P>0.05)。其中IP组腹泻发生率高于TP组(54.3% vs 14.3%),两组比较具有统计学差异(P<0.05)(表2)。
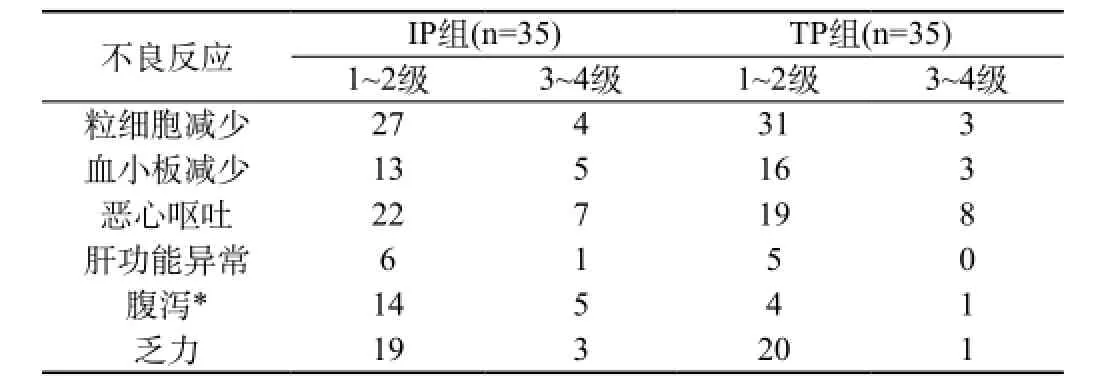
表2 IP组和TP组患者的不良反应表(例)
2.3无进展生存期:随访截止至2014年1月,所有患者均出现疾病进展。IP方案组的中位PFS为6.5个月,TP方案组中位PFS为4.6个月,组间差异有统计学意义(P=0.043)。见图l。
3 讨 论
小细胞肺癌(small-cell lung cancer,SCLC)约占所有肺癌的12%~15%[1],约1/3的患者在就诊时为局限期,2/3属广泛期。小细胞肺癌恶性程度高,生长迅速,对化疗敏感,一线化疗缓解率高,但是其高耐药率和复发率使其病死率居恶性肿瘤之首。大部分SCLC患者在化疗停止后3个月左右出现复发转移,常给予二线换药化疗控制肿瘤进展,延长生存期。
伊立替康(CPT-11)是喜树碱的衍生物,为DNA拓扑异构酶Ⅰ抑制剂,其与Topo Ⅰ-DNA形成的复合物结合,稳定此复合物,从而使断裂的DNA单链不能重新接合,阻止DNA复制及抑制RNA合成,为细胞周期S期特异性药物。CPT-11的抗瘤活性强,在SCLC的治疗中作用突出并且与依托泊苷及铂类无交叉耐药,目前CPT-11联合DDP联合使用具有协同效应。Noda等[2]在伊立替康联合顺铂的Ⅲ期临床试验中取得良好效果,根据此项试验日本批准IP为小细胞肺癌一线治疗方案。本研究中IP方案组获CR 6例,PR 18例,RR为68.6%;TP方案组CR 7例,PR 14例,RR为60.0%;两组的RR差异无统计学意(P>0.05)。但是IP方案组的中位PFS为6.5个月,TP方案组中位PFS为4.6个月,组间差异有统计学意义(P=0.043)。可见伊立替康二线治疗小细胞肺癌有一定的优势。两组骨髓抑制和恶心呕吐的不良反应相当,其中IP组腹泻发生率高于TP组(54.3% vs 14.3%),给予对症治疗后会在短期内缓解。与某些研究显示相似,腹泻为伊立替康主要的非血液学毒性,且为剂量限制性[3-4]。
伊立替康联合顺铂方案二线治疗SCLC的客观疗效与传统的紫杉醇二线方案相当,不良反应可控,无进展生存期方面有一定优势,值得临床应用。是否能够延长总生存期有待于临床进一步研究。
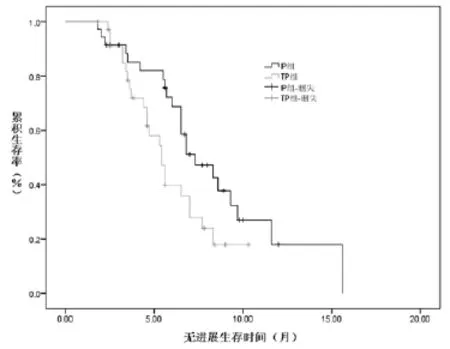
图1 IP组和TP组患者的无进展生存时间比较
[1] Govindan R,Page N,Morgensztern D,et a1.Changing epidemiology of small-cell lung cancer in the United States over the last 30years:Analysis of the Surveillance,Epidemiolngic and End-Results database[J].J Clin Oncol,2006,24(28):4539-4544.
[2] Noda K,Nishiwaki Y,Kawahara M,et a1.Irlnotecan plus cisplatin compared with etoposide plus ciaplatin for extensive small-cell lung cancer[J].N Engl J Med,2002,346(2):85-91.
[3] Schmittel A,Sebastian M,Fischer L,et al.A German multicenter,radomized phase Ⅲ trial comparing irinotecan-carboplatin with etopnoside-carboplatin as first-line therapy for extensive-disease small-cell lung cancer[J].Ann Oncol,2011,22(8): 1798-1804.
[4] 杨新杰,张卉,农靖颖,等.伊立替康或足叶乙甙联合顺铂方案一线治疗小细胞肺癌的临床随机对照研究[J].中国肿瘤临床,2012,39(13):923-926.
Clinical Study of IP and TP as Second-line Treatment for SCLC
SUN Yong-chen, LIU-Jun, YANG-Xi, HAN Wen-jie
(Department of Oncology, First People’s Hospital of Shangqiu, Shangqiu 476100, China)
Objective To compare the efficacy and toxicity of irinotecan plus etoposide (IP) with those of paclitaxel plus cisplatin (TP) as second-line treatments for small cell lung cancer (SCLC). Methods A total of 70 patients were randomly assigned into the IP arm and the TP arm. The primary endpoint was progression-free survival (PFS), response rate, and toxicity. Results The median PFS was 6.5 months in the IP arm and 4.6 months in the TP arm. Significant difference was observed (P<0.05). The response rate was 68.6% in the IP arm and 60.0% in the TP arm. No significant difference in response rate was observed between the two arms (P>0.05). The main common adverse reactions were myelosuppression and gastrointestinal response in both treatment arms. No significant difference in myelosuppression toxicity was observed between the arms (P>0.05). Diarrhea was significantly more frequent in the IP arm than in the TP arm (P<0.05). Conclusion The control rate of IP and TP as second-line therapy for SCLC are equivalent. Progression free survival was higher in the IP arm than TP arm, and adverse reactions can be tolerated.
Irinotecan; Paclitaxel; SCLC; Chemotherapy
R734.2
B
1671-8194(2015)09-0013-02
