宫颈癌CT引导的三维插植腔内后装放疗中膀胱壁、直肠壁受照剂量的评价
2014-07-14李小文高冬梅阿依努尔色义提
李小文, 高冬梅, 阿依努尔·色义提
(新疆医科大学附属肿瘤医院1妇科肿瘤放疗二病区, 2妇外五科, 乌鲁木齐 830011)
宫颈癌是妇科常见肿瘤。放射治疗是宫颈癌的重要治疗手段之一,约80%的患者可采用放射治疗或将放射治疗作为综合治疗手段之一[l]。体外加腔内后装治疗是局部晚期宫颈癌根治性放疗的标准模式,推荐总剂量为80~90 Gy[2],放疗效果满意。5年总生存率可达到65%。研究表明,宫颈癌是目前疗效较好的肿瘤之一[3]。但泌尿系统和消化道并发症一直是困扰放疗工作者的难题之一。随着定位设备、治疗计划系统及放疗设备和技术的不断更新,CT引导的三维插植高剂量率后装放疗(HDR-ISBT)得到了长足发展[4-5]。近距离放疗具有放射源周围局部剂量高、靶区外剂量下降梯度大的特点,插植后装近距离放疗由于在CT引导下精确置管、插针,定义肿瘤区、临床靶区、危及器官区及相应处方剂量,可对靶区尤其不规则靶区以精确高剂量照射[6-8]。降低正常器官受照剂量是减少放疗并发症的关键,而正确评价膀胱、直肠等正常器官的受照剂量更重要[9]。本研究旨在探讨宫颈癌CT引导的三维插植后装放疗计划设计中膀胱壁、直肠壁的受照剂量。
1 资料与方法
1.1临床资料选取新疆医科大学附属肿瘤医院2011年12月-2013年12月收治的45例首诊首治的宫颈癌根治性放射治疗患者,年龄28~72岁,平均(49.43±5.06)岁,中位年龄52岁。其中角化型鳞癌15例,非角化型鳞癌30例。按FIGO(2009年)分期标准,ⅡB期11例,Ⅲ期34例。通过随机数字表随机选择其中25例中晚期宫颈癌患者行体外三维适形调强放疗+CT引导的三维插植高剂量率后装放疗为试验组,同期行体外三维适形调强放疗+常规后装放疗的20例宫颈癌患者为对照组。经新疆医科大学附属肿瘤医院伦理学委员会的批准,患者治疗前均知情同意并签署了知情同意书。放疗前均经病理活检证实为宫颈癌,Karnofsky功能状态评分(KPS)均≥70分。两组临床资料差异无统计学意义(P>0.05),见表1。
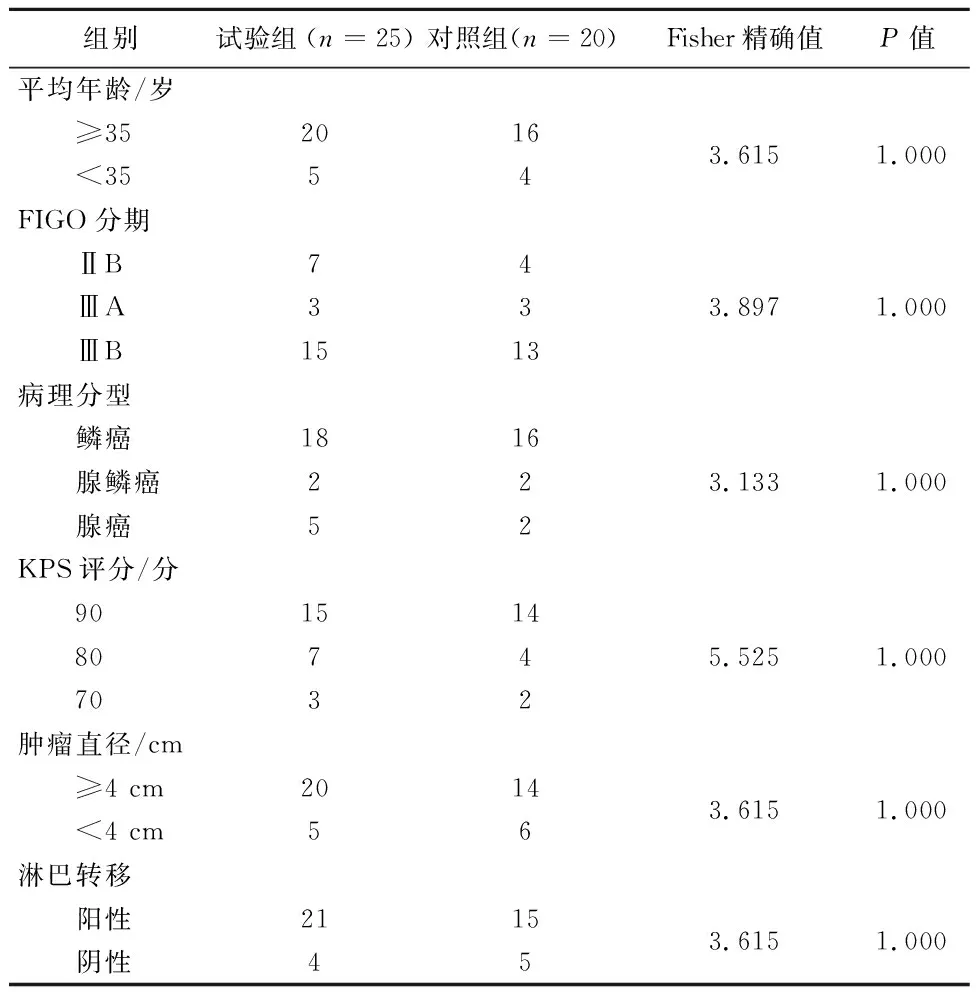
表1 45例宫颈癌的临床资料
1.2方法
1.2.1 CT模拟定位 患者于CT扫描前半小时排空膀胱后口服水800 mL,后憋尿以保证膀胱充盈,扫描前制作腹盆腔的体位固定膜,CT扫描同时静脉注射碘海醇100 mL进行影像对比增强。CT扫描范围自第1腰椎上缘至闭孔下缘,扫描层厚为0.5 cm,扫描数据图像经局域网传输至治疗计划系统工作站。
1.2.2 靶体积及危险器官的界定 制定三维计划前,逐层在CT层面勾画靶体积。GTV为淋巴结转移部位,CTV包括阴道上段1/2及宫体、宫旁、阴道旁组织和腹盆腔淋巴引流区域(包括腹主动脉下段、髂总、髂外、髂内、闭孔及骶前淋巴引流区)。计划靶区(planning target volume,PTV)由计划系统自动生成,分别在CTV上、下、前、后、左和右外扩1 cm,同时勾画临近的小肠、直肠、膀胱、乙状结肠、脊髓及双侧股骨头等危险器官(organs at risk,OAR)。
1.2.3 治疗计划的设计 均按照三维适形调强放疗(IMRT)治疗模式制定计划,计划的实施采用直线加速器,配备有动态多叶光栅准直器调节放射野的不规则形状。计划的PTV剂量均设定DT45~50 Gy,单次剂量1.8~2.0 Gy,选择能量为6 MV的X射线。区域淋巴结肿大给予同步加量DT至60~66 Gy。
1.2.4 CT引导的三维插植腔内近距离放疗 体外盆腹腔三维适形调强放疗照射完成处方剂量20~30 Gy后,加入CT引导的三维插植腔内高剂量率后装放疗。先根据临床检查、MR或CT等明确肿瘤范围,初步确定进针路径、深度、插植针数。常规消毒外阴、阴道,铺巾,膀胱内留置尿管,经宫颈管植入腔管,宫颈局部、阴道病灶区进针,初步插入金属插植针,飞利浦 CT-SIM下行CT扫描,明确针的位置及其与肿瘤、直肠和膀胱、乙状结肠的关系。调整针至合适位置后,用塑料扣固定,用碘纱填塞固定经阴道插植针,夹闭尿管,经尿管向膀胱注入生理盐水150 mL,使膀胱充盈,作CT平扫,图像经网络传至核通三维后装近距离计划系统,勾画高危临床靶区(HRCTV)及危及器官膀胱、直肠、乙状结肠。膀胱、直肠勾画壁层,厚度0.4 cm。用逆向计划系统调节每一针各点的剂量强度,形成适合靶区形状的剂量分布。以100%等剂量线包括全部高危临床靶区(HRCTV)为优秀方案,以90%等剂量线包括95%HRCTV为可接受方案。治疗前膀胱充盈以推开小肠,同时减少膀胱壁受照剂量体积,阴道内填塞纱布保护部分膀胱、直肠,插植针与后装机连接后,电脑执行优化方案实施治疗。后装治疗机进行腔内近距离后装放疗,每次靶区剂量D90为7 Gy,共放疗4次,总剂量为28 Gy,等效生物剂量36~40 Gy。每次均根据CT扫描结果重新设计治疗计划进行治疗。
1.2.5 常规后装近距离放疗 每周1次。膀胱内留置尿管,仅宫腔腔内置管后,夹闭尿管,经尿管向膀胱注入生理盐水150 mL,使膀胱充盈,也为CT引导勾画靶区及危及器官。靶区总剂量及疗程与CT引导的三维插植腔内近距离放疗相同。
1.2.6 同步放化疗 两组均在进行后装腔内放疗当日停止体外照射。所有患者自放疗开始,则每日进行阴道冲洗。在放射治疗期间同时给以每周顺铂每体表面积(DDP)30 mg,5 次。腔内后装放疗为高剂量率放疗,其放射源为铱源。
1.2.7 后装放疗计划对膀胱壁、直肠壁的受照剂量的评价 按照欧洲放疗协会(GEC ESTRO)(2006)建议[10],利用体积剂量直方图(DVH)分别评价CT引导的三维插植腔内后装和常规后装放疗计划膀胱壁、直肠壁的0.1、1、2、5 cm3和10 cm3等体积所受照射剂量。
1.3统计学处理应用SPSS 19.0统计软件,使用Fisher的精确检验及独立样本的t检验对各参数进行统计学分析。以P<0.05为差异有统计学意义。
2 结果
2.1CT引导的三维插植腔内后装放疗与常规后装放疗计划中膀胱壁的受照剂量比较CT引导的三维插植腔内后装计划中,膀胱壁的平均剂量在肿瘤直径<4 cm时,0.1、1、2、5 cm3和10 cm3分别为62.82、55.20、51.85、46.01 Gy 和40.26 Gy ;在肿瘤直径≥4 cm时,0.1、1、2、5 cm3和10 cm3分别为66.63、58.49、54.70、48.26 Gy和41.82 Gy。常规后装膀胱壁平均剂量在肿瘤直径<4 cm时,0.1、1、2、5 cm3和10 cm3分别为70.24、66.58、60.64、53.49 Gy和46.36 Gy;在肿瘤直径≥4 cm时,0.1、1、2、5 cm3和10 cm3分别为107.24、86.45、79.15、66.82 Gy和55.39 Gy。肿瘤直径<4 cm或≥4 cm时,两组膀胱壁受照剂量差异均有统计学意义(P<0.05),见表2。

表2 两组后装放疗计划中膀胱壁受照剂量比较(Gy, ±s)
2.2CT引导的三维插植腔内后装放疗与常规后装放疗计划中直肠壁的受照剂量比较CT引导的三维插植腔内后装计划中,直肠壁的平均剂量在肿瘤直径<4 cm时,0.1、1、2、5 cm3和10 cm3分别为59.98、52.96、48.63、40.20 Gy和30.74 Gy;在肿瘤直径≥4 cm时,0.1、1、2、5 cm3和10 cm3分别为58.74、49.12、45.59、39.53 Gy和32.85 Gy。常规后装直肠壁平均剂量在肿瘤直径<4 cm时,0.1、1、2、5 cm3和10 cm3分别为59.74、46.64、41.38、32.75 Gy和21.98 Gy;在肿瘤直径≥4 cm时,0.1、1、2、5 cm3和10 cm3分别为63.90、58.02、55.20、50.23 Gy和44.14 Gy。肿瘤直径<4 cm或≥4 cm时,两组直肠壁受照剂量差异均有统计学意义(P<0.05),见表3。
2.3CT引导的三维插植腔内后装放疗计划与常规后装放疗计划靶区体积横截面图像及DVH图通过CT引导,根据肿瘤的形态可调整插植针的位置,使高剂量区域的分布与治疗靶区高度适形,达到精确放疗,并可使膀胱和直肠受照剂量减少。而常规后装放疗对于肿瘤较大、偏心的、不规则的形态,其沿放射源同心圆的剂量分布及有限的照射范围,会导致靶区的漏照,或膀胱和直肠接收过多照射剂量,见图1~4。

表3 两组后装放疗计划中直肠壁受照剂量比较(Gy, ±s)
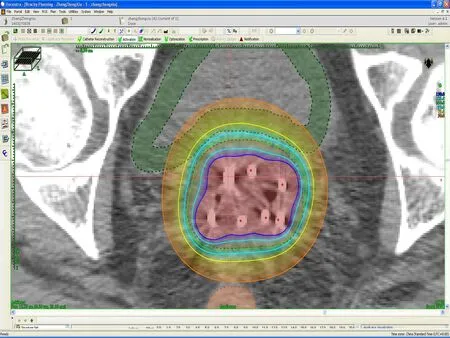
图1 CT引导的三维插植腔内后装放疗计划靶区体积横截面图像

图2 CT引导的三维插植腔内后装放疗计划剂量体积直方图

图3 CT引导的常规腔内后装放疗计划靶区体积横截面图像

图4 CT引导的常规腔内后装放疗计划剂量体积直方图
3 讨论
宫颈癌放疗中为了保护膀胱、小肠等重要器官,常需要患者治疗时充盈膀胱,这样可以降低膀胱等的受量[11-12]。但需要保护的实际上是膀胱壁,而不是整个充盈的膀胱。肖锋等[13]认为,在宫颈癌体外调强计划设计中,如果简单地用整个膀胱受量代替膀胱壁的受量,将会大大低估膀胱壁的真正受量,从而加大膀胱并发症的发生概率,对膀胱造成不必要的损伤。由于近距离腔内后装放疗时的放射源直接在肿瘤靶区照射,对局部病灶区域给予较高的剂量,靶区剂量参考点外剂量迅速下降,与距离的平方呈反比,可使靶区以外的正常组织如膀胱、直肠、乙状结肠等接受较低的剂量,这样可提高肿瘤的局控,对正常组织起到较好的保护作用,从而明显减少其毒副作用。但常规后装放疗单管置入腔内,对于肿瘤较大、偏心的、不规则的形态,其沿放射源同心圆的剂量分布及有限的照射范围,会导致靶区的漏照或正常组织接收过多照射剂量。而CT图像引导的核通三维组织间插植腔内后装近距离计划系统,各插植针可根据CTV等形态任意排列,相互间交叉、错位,不影响计划的优化,通过重建各针的三维位置,定义GTV、CTV及危及器官的位置及受量,使用逆向治疗计划系统优化各点的驻留时间,从而调节每一点的剂量,使合成的剂量与治疗的靶区高度适形,使肿瘤区受到高剂量的精确照射成为可能[14]。因此,Sharma等[15]认为组织间插植引导的后装放疗较传统后装放疗有明显的剂量学优势。有研究表明,与外照射调强放疗相比,CT引导的三维插植后装放疗肿瘤中心区剂量更高,膀胱、直肠充盈程度对剂量分布影响更小,而治疗体位、呼吸运动对盆腔剂量分布无影响[16]。后装治疗与外照射不同,按照(GYN) GEC ESTRO(2006)工作组的建议[10],当危及器官膀胱、直肠等器官只受到较小体积照射时,0.1、1、2 cm3甚至5、10 cm3等膀胱、直肠的体积可近似代表0.1、1、2、5 cm3和10 cm3膀胱壁的体积,所以可利用DVH图0.1、1、2、5 cm3和10 cm3等体积所受剂量评价膀胱受量,可用这些参数近似代替膀胱壁的受量。本研究对CT引导的三维插植后装放疗试验组与常规后装放疗对照组膀胱壁、直肠壁受量进行了比较,结果表明不论肿瘤直径<4 cm或≥4 cm,两组膀胱壁、直肠壁受照剂量差异均有统计学意义。试验组计划设计中膀胱壁、直肠壁所受剂量明显减少。
总之,在宫颈癌CT引导的三维插植腔内后装计划设计中,膀胱壁、直肠壁受量明显低于常规后装放疗。考虑根据肿瘤大小、范围、形态分布插植针与腔管,使肿瘤高剂量分布区与肿瘤形态高度适形,在达到精确放疗可能的同时,减少了膀胱、直肠等正常组织剂量的分布,可避免发生由常规后装单管放疗出现的沿放射源同心圆的剂量分布及有限的照射范围而导致靶区的漏照或直肠、膀胱接收过多照射剂量的可能性,从而可减少膀胱、直肠并发症的发生概率,降低对膀胱造成的不必要损伤。
参考文献:
[1] 麻富卯,张继东,王霞,等.宫颈癌术后不同因素对放疗疗效的影响[J].中华放射肿瘤学杂志,2006,15(2):120-122.
[2] Eifel PJ,Winter K, Morris M, et al. Pelvic irradiation with concurrent chemotherapy versus pelvic and para-aortic irradiation for high risk cervical cancer: An update of Radiation Therapy Oncology Group Trial (RTOG) 90-01[J]. Clin Oncol,2004,22:872-880.
[3] 林晓丹,周同冲,石兴源,等.同步放化疗治疗中晚期宫颈癌的临床分析及感染因素[J].中华医院感染学杂志,2011,21(18):3876-377.
[4] Akila N, Viswanathan AN, Carien L,et al. International brachytherapy practice patterns: A survey of the genecologic cancer intergroup(GCIG)[J].Radiat Oncol Biol Phys,2012,82(1): 250-255.
[5] Viswanathan AN, Erickson BA. Three-dimensional imaging in gynecologic brachytherapy:a survey of the American Brachytherapy Society [J]. Radiat Oncol Biol Phys ,2010,76:104-109.
[6] Viswanathan AN.The Frank Ellis Memorial lecture: the use of three dimensional imaging in gynaecological radiationtherapy [J].Clin Oncol,2008,20(1):1-5.
[7] Haie-Meder C,Potter R,van Limbergen E,et al.Recommendations from gynaecological (GYN)GEC-ESTRO working group(1):concepts and terms in 3D image based 3D treatment planning in cervix cancer brachytherapy with emphasis on MRI assessment of GTV and CTV[J].Radiother Oncol,2005,74:235-245.
[8] Tan LT,Coles CE,Hart C,et al.Clinical impact of computed tomography-based image-guided brachytherapy for cervix cancer using the tandem-ring applicator-the addenbrooke’s experience[J].Clin Oncol,2009,21:175-182.
[9] Baucal M,Babie J,Kuzmanovic Z.Rectal dosimetry in intracavitary applications of cervix carcinoma:Comparison of two methods [J].Arch Oncol,2002,10(4):253-259.
[10] Petter R,Haie-Meder C,van Limbergen E,et al.Recommendations from gynaecological(GYN)GEC ESTRO working group(1I):Concepts and terms in 3D image-based treatment planning in cervix cancer brachytherapy-3D dose volume parameters and aspects of 3D image-based anatomy,radiation physics,radiobiology[J].Radiother Oncol,2006,78(1):67-77.
[11] 叶伟军,曹新平,李爱菊,等.插植调强近距离放射治疗复发性宫颈癌的临床研究[J].中华肿瘤防治杂志,2009,16( 8):1427-1429.
[12] Cengiz M,Gurdalli S,Selek U, et al.Effect of bladder distension on dose distribution of intracavitary brachytherapy for cervical cancer:three-dimensional computed tomography plan evaluation[J].Radiat Oncol Biol Phys,2008,70(2):464-468.
[13] 肖锋,宋晖,魏丽春,等.宫颈癌调强放疗膀胱受照剂量的评价[J].中华肿瘤防治杂志,2011,18(6),463-465.
[14] Toita T, Kitagawa R, Hamano T, et al.Phase II study of concurrent chemoradiotherapy with high-dose-rate intracavitary brachytherapy in patients with locally advanced uterine cervical cancer: Efficacy and toxicity of a low cumulative radiation dose schedule[J].Gynaecol Oncol,2012,126,211-216.
[15] Sharma DN,Subramani V,Rath GK,et al.Interstitial brachytherapy guided intensity modulated radiation therapy in cervical carcinoma: a dosimetric study.Proceedings of the 49th annual ASTRO meeting[J].Int J Radioat Oncol Biol Phys,2007,69(3):731-732.
[16] Georg D,Kirsits C,Hillbrand M,et al.Image-guided radiotherapy for cervix cancer:High-tech external beam therapy versus high-tech brachytherapy[J].Int J Radioat Oncol Biol Phys,2008,71(4):1272-1278.
