鲤春病毒血症病毒糖蛋白的原核表达及单克隆抗体的制备
2014-02-15张家林李强叶仕根李华
张家林,李强,叶仕根,李华
(大连海洋大学 辽宁省海洋生物资源恢复与生境修复重点实验室,辽宁 大连116023)
鲤春病毒血症(Spring viremia of carp,SVC)是由鲤春病毒血症病毒(Spring viremia of carp virus,SVCV)引发的危害鲤科鱼类的一种急性、高致死性的传染病,目前在欧洲、美洲、亚洲广泛传播,现已造成了巨大的经济损失,世界动物卫生组织(World Organisation for Animal Health,OIE)已将其列为必须申报的疾病[1],中国在2008年颁布的动物疫病名录中将其列为一类动物疫病[2]。近年来,国内外很多学者致力于研究更加快速、准确地检测SVCV 的方法。中国应用较多的检测方法有套式RT-PCR、荧光定量PCR、LAMP等,相关免疫学检测方法尚未成熟[3]。而OIE 推荐的SVCV 检测方法是建立在单克隆抗体基础上的间接免疫荧光(IFA)和酶联免疫吸附试验(ELISA),其中单克隆抗体具有特异性强、灵敏度高、能够大量制备的特点,可应用于开发各种诊断试剂,具有广阔的应用前景[4],而传统的制备方法是用纯化病毒作为抗原制备单克隆抗体,但病毒纯化程序较为复杂且很难筛选出特定抗原表位的单克隆抗体。随着生物技术的不断发展,用重组蛋白制备特异性单克隆抗体已成为研究趋势。糖蛋白(G)位于SVCV 囊膜表面,是最主要的表面抗原,能够诱导引起鱼体产生中和抗体,参与病毒的感染[5]、免疫识别[6]和介导病毒内吞[7]等,可作为SVCV 免疫诊断的抗原,同时也是抗病毒药物作用的理想靶点。本研究中,选取并扩增鲤春病毒血症病毒(简称为鲤春病毒,下同)G 基因片段,原核重组表达了G 蛋白,继而制备了抗G 蛋白的单克隆抗体,并对单抗进行了初步鉴定,旨在为建立新型SVCV 免疫学诊断方法提供工具。
1 材料与方法
1.1 材料
1.1.1 病毒、质粒和菌株 SVCV 0504 毒株为辽宁省海洋生物资源恢复与生境修复重点实验室保存菌株。克隆载体pMD18 - T 购于TaKaRa(大连)公司,表达载体pET-28a(+)、大肠杆菌DH5α和BL21(DE3)感受态细胞由辽宁省海洋生物资源恢复与生境修复重点实验室保存。
1.1.2 工具酶、试剂和试验动物 rTaq 酶、DNA Marker 购自TaKaRa(大连)公司;抗His 单抗、质粒小提试剂盒、胶回收试剂盒购自天根生化科技有限公司;Bam H I 酶、Xho I 酶、T4DNA 连接酶、蛋白Marker 均购自Thermo Scientific 公司;His Bind Kits 购自Novagen 公司;胎牛血清、RPMI 1640 培养基、M199 培养基购于Hyclone 公司;HT、HAT、PEG1500、AP 标记羊抗鼠Ig和FITC标记羊抗鼠Ig 购自Sigma 公司;PCR 引物合成及DNA 测序由华大基因公司完成。6 ~8 周龄Balb/c小鼠购自大连医科大学SPF 实验动物中心,鲤春病毒阳性血清由北京检验检疫技术中心赠送。
小学生思维、理解能力有限,但对新鲜事物、动态事物、鲜艳的色彩和图案等具有强烈的好奇心和兴趣。因此,教师在借助微课进行课堂教学时,应紧紧抓住学生这一特征,将晦涩难懂的抽象知识,借助微课制作软件,以直观、间接的动态视频形式展示给学生,从而激发学生的探索兴趣,集中学生的注意力。
1.2 方法
1.2.1 鲤春病毒G 蛋白片段的扩增 采用Trizol法提取病毒总RNA,按照TaKaRa(大连)公司RNA 反转录试剂盒说明书进行反转录,以反转录得到的cDNA 产物作为模板。根据SVCV 0504 株G蛋白基因序列(GenBank:EU370915.1)设计扩增引物:F,5' TGGATCCTTTGTTCCATCTGGGC 3';R,5'GCTCGAGAGTTCCCCACCCACTG 3'。分别引入酶切位点Bam H I、Xho I,PCR 扩增G 基因片段(第21aa ~第463aa)。PCR 反应条件:94 ℃下预变性5 min;94 ℃下变性30 s,51.5 ℃下退火30 s,72 ℃下延伸1 min 30 s,共进行35 个循环;最后在72 ℃下再延伸10 min,终止反应。PCR 产物经10 g/L 琼脂糖凝胶电泳切胶回收后,克隆至pMD18 -T 载体中,将重组质粒pMD18 -T -G 转化至大肠杆菌DH5α 感受态细胞中,挑选阳性克隆送华大基因公司测序,验证插入的外源基因正确无误。
1.2.5 杂交瘤细胞的建立 以复性蛋白免疫Balb/c 小鼠,参考李强等[8]的方法进行细胞融合,杂交瘤培养上清液用间接ELISA 结合间接IFA 的方法进行检测。同时采用有限稀释法对阳性细胞株多次克隆,直至筛选结果为100%阳性止。
经Dot-ELISA 检测,MAb 1C5、MAb 2D5 的细胞培养上清液效价分别为1∶ 2560、1∶ 5120(图4);经Western-Blot 检测表明,两株单抗与G蛋白在相对分子质量为51 600 处结合(图5);分泌稳定性试验结果表明,两株杂交瘤细胞株体外连续培养30 d 后,可稳定分泌抗体(图6)。
由SVCV 引起的鲤春病毒血症严重威胁中国鲤科鱼类的养殖,而现阶段缺乏对SVCV 有效的治疗药物,及早检测、疫苗免疫等策略成为防控鲤春病毒血症最有效的途径。SVCV 主要结构蛋白包括核蛋白(N)、磷蛋白(P)、基质蛋白(M)、糖蛋白(G)、RNA 聚合酶(L),其中全长G 蛋白由509 个氨基酸组成,具有信号肽序列及跨膜结构域,是典型的跨膜糖蛋白[9-10],在病毒检测、DNA 疫苗构建上具有广阔的应用前景。随着分子生物学的发展,重组表达外源病毒蛋白已成为研究病毒蛋白的主要手段,鲤春病毒G 蛋白已在大肠杆菌、毕赤酵母和昆虫细胞中获得表达[11-13]。预试验中,构建的全长G 蛋白重组表达质粒在大肠杆菌中表达量过低,原因可能是全长G 蛋白含有较多疏水性氨基酸及大肠杆菌稀有密码子,影响了G 蛋白的表达。因此,本研究中在设计引物时去掉N 端信号肽及尾部疏水区,截取G 蛋白片段,成功地实现了G 蛋白的高效表达,这与张琳等[11]的研究结论一致。
1.2.2 重组G 蛋白表达质粒的构建 根据质粒小提试剂盒说明书提取pMD18 -T -G 及pET -28a(+)质粒,分别采用限制性内切酶Bam H I、Xho I 进行双酶切,酶切产物经胶回收后,用T4DNA连接酶于16 ℃下连接过夜,连接产物转化至大肠杆菌DH5α 感受态细胞中,挑选单菌落进行菌液PCR、双酶切和测序鉴定,将测序正确的重组质粒命名为pET -28a(+)-G。将重组表达质粒转化至大肠杆菌BL21(DE3)感受态细胞中。
间接IFA 检测方法的建立:在6 孔细胞培养板中进行EPC 细胞爬片,待接种病毒出现CPE 后倾去培养液,用体积分数为4%的多聚甲醛固定10 min,室温风干,用PBS 洗涤3次。以上述阳性杂交瘤细胞上清液为一抗,37 ℃下孵育1 h,再用PBS 洗涤3次,每次5 min,然后以FITC 标记羊抗鼠Ig(1∶ 100)为二抗,37 ℃下孵育45 min,再用PBS 洗涤后甘油封片,在荧光显微镜下观察。出现特异的亮绿色荧光者为阳性,反之判为阴性。同时设置未感染病毒EPC 细胞作为阴性对照,鲤春病毒阳性血清为阳性对照。
间接ELISA 检测方法的建立:以5 μg/mL 的复性蛋白作为检测原,按照李强等[8]的方法对融合细胞上清液进行间接ELISA 检测,设置阳性对照(免疫鼠血清)、阴性对照(空载体菌液)和空白对照(PBS),用酶标仪检测OD405nm值,将P/N≥2.1 时的杂交瘤上清液判定为阳性。
(2) 有关微网电能质量的关注点 微网内存在逆变器型微电源和旋转电机型微电源(微型燃气轮机)以及大量的非线性负载,可能会造成谐波污染、电压波动、电压(频率)闪变、环流等问题,所以微网的电能质量问题依然是未来微网的研究热点之一。
1.2.6 单克隆抗体的特性鉴定 收集细胞培养上清液,从1∶ 10 开始做二倍系列稀释,采用Dot -ELISA 法测定抗体效价;表达鲤春病毒G 蛋白pET-28a -G,经诱导后进行SDS - PAGE,湿法转印后,用杂交瘤细胞上清液进行Western - Blot抗体检测;将阳性率达100%的细胞株每隔3 d 连续培养30 d,取培养的上清液进行间接ELISA 检测。
2 结果
2.1 G 基因片段的扩增及重组表达质粒的构建
重组表达菌株经IPTG 诱导后,可表达相对分子质量为51 600 左右的融合蛋白(图2 泳道3),而空载体诱导全菌、未诱导全菌无相应蛋白条带。裂解试验说明,重组表达的G 蛋白主要以包涵体形式存在(图2 泳道4、5)。经优化条件(0.4 mmol/L IPTG,37 ℃下孵育5 h)后大量表达,制备包涵体并采用亲和层析柱纯化(图2 泳道6),通过尿素梯度透析复性和Western -Blot 检测表明,融合蛋白与抗His 单抗特异性结合,条带大小与预测结果相一致(图2 泳道7),证实了目的蛋白成功表达。用Image J 软件检测SDS - PAGE图谱,结果表明,复性蛋白纯度达到90%。用BCA 蛋白定量试剂盒检测,蛋白浓度约为1.0 mg/mL。
有研究者认为《苏北女人》中的女主角令人想起女娲补天的神话故事,我非常赞同。女娲的两个伟大创举是造人和补天。柳采莲一生养育了四个孩子,两次到石宕里采石、筑屋补屋,恰与之形成对应关系。养育孩子就是“造人”的隐喻,采石、筑屋可以视作“补天”的隐喻。在远古神话中,“四极废,九州裂,天不兼覆,地不周载,火爁焱而不灭,水浩洋而不息,于是女娲炼无色石以补苍天”[3]284。柳采莲们的行为是否可看作对现代性的“爁焱”大火造成的“天”之“裂隙”的象征性补救呢?

图1 鲤春病毒G 基因片段扩增Fig.1 Amplification of spring viremia of carp virus(SVCV)G gene fragment
2.2 重组蛋白的表达及纯化
RT-PCR 扩增后得到1326 bp 的特异性条带,与预期大小相符,将pET -28a(+)质粒与pMD 18 -T -G 质粒经双酶切后连接,构建重组表达质粒,命名为pET-28a-G。经双酶切鉴定表明,已在pET-28a(+)质粒中插入了一段约1326 bp的序列(图1),结合测序结果证明,重组表达载体构建正确无误。
2.3 杂交瘤细胞株的建立
采用间接ELISA 法筛选出11 株阳性杂交瘤细胞株,经有限稀释法克隆后收集培养上清液,同时制备病毒感染的EPC 细胞爬片,采用间接IFA 法进一步筛选出两株能与病毒反应的杂交瘤细胞株,分别命名为1C5、2D5(图3)。
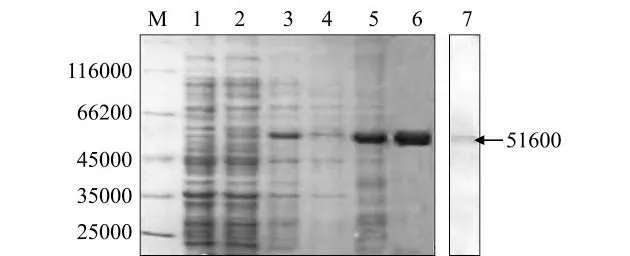
图2 重组G 蛋白的表达Fig.2 Expression of recombinant G protein
2.4 单克隆抗体的特性分析
1.2.3 重组G 蛋白的表达及SDS -PAGE 分析挑取单菌落接种于含Kan+(40 μg/mL)的LB 培养基中,37 ℃下震荡培养过夜。以1∶ 100 比例转接至5 mL 新鲜培养基中,在37 ℃恒温培养箱中培养至细菌对数生长期,加入IPTG 至终浓度为1 mmol/L 后继续培养5 h,制样进行SDS -PAGE 电泳,分析蛋白的表达形式,并设置空载体诱导全菌和未诱导全菌为对照。同时采用湿法转印,用1%BSA 于4 ℃下封闭过夜,用PBST 洗涤3次,每次5 min,加入用0.01 mol/L PBS 稀释的抗His 单抗(1∶ 1000),37 ℃下孵育1 h;用PBST 洗涤3次,每次5 min,加入用0.01 mol/L PBS 稀释的羊抗鼠Ig(1∶ 3000),37 ℃下孵育45 min;再用PBST 洗涤3次,每次5 min,最后加入NBT - BCIP 显色液,以双蒸水终止反应。
魏乐村:斗渠长度由2 170 m变为2 605 m,比原设计增加435 m,1-1农渠长度由850 m变为1 300 m,1-2农渠长度由820 m变为700 m,1-3农渠长度由930 m变为1 700 m,1-4农渠长度由980 m变为2 410 m,1-5农渠长度由990 m变为1 200 m,变更后农渠总长比原设计增加2 740 m。
3 讨论
1.2.4 包涵体的纯化及复性在筛选出的最佳诱导条件(0.4 mmoL/L IPTG,37 ℃下孵育5 h)下大量表达重组表达菌,将其超声破碎后进行漂洗、洗涤、变性,变性蛋白按照Invitrogen His - Bind Kits 说明书进行亲和层析纯化。调整蛋白浓度至1 mg/mL,分别在含4、3、2、1、0.5 moL/L 尿素的复性缓冲液(50 mmol/L Tris,0.5 mmol/L EDTA,50 mmol/L NaCl,10%甘油,1%精氨酸,pH 8.0)中进行梯度透析复性,每6 h 更换1次透析液,最后在Tris-HCl 缓冲液中透析过夜。采用SDS -PAGE 电泳检测复性蛋白的纯度,用BCA 蛋白定量试剂盒测定蛋白浓度。
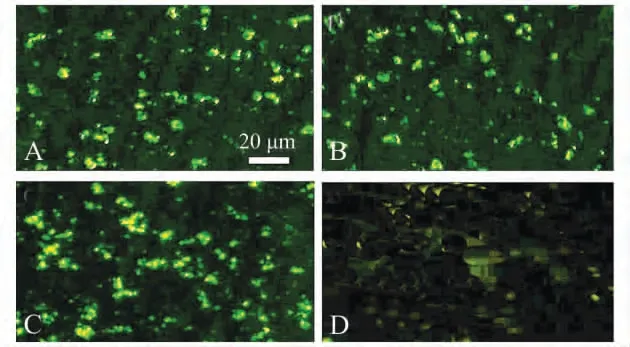
图3 间接IFA 检测结果Fig.3 Dection results of indirect immunofluorescence analysis(IFA)

图4 单克隆抗体效价的测定Fig.4 Determination of 2 MAbs titer by Dot-enzyme-linked immunosorbent assay(Dot-ELISA)

图5 单克隆抗体的特异性分析Fig.5 Specificity analysis of MAbs
pET-28a 原核表达载体功能强大,表达产物携带His 标签,可采用亲和层析法进行纯化。本研究中构建重组表达质粒pET -28a -G 时,同时转化大肠杆菌BL21,经诱导,表达产物浓度在1 mg/mL 左右,但主要以包涵体形式存在。通常载体、宿主、外源基因和诱导条件等是影响外源蛋白可溶性表达的主要因素,本研究中曾更换携带GST 标签的pGS -21a(+)表达载体,更换E.coli Rosseta表达菌株,筛选表达条件(即固定其他因子,对单个因子进行不同温度、不同IPTG 浓度和不同诱导时间表达),均未明显提高上清液表达量,较多的疏水性氨基酸与稀有密码子成为G 蛋白的可溶表达瓶颈。

图6 分泌稳定性测定Fig.6 Secreting stability analysis of MAb 1C5 and MAb 2D5
包涵体经复性后可恢复部分抗原性,杨振慧[14]制备了包涵体形式的SVCV-G 蛋白,割胶回收后免疫新西兰大白兔,经Western -Blot 检测表明,制备的兔抗血清与细胞培养的SVCV 发生特异性反应,这是本研究中利用包涵体形式蛋白制备单克隆抗体的理论依据。
科室学术例会是培养研究生科研水平的一种重要手段,其主要内容是工作汇报,实验交流和科学问题探讨[6]。还可以利用研究课题方向相近的特点,在有限范围内建立课题小组。通过课题组定期组会制度对研究生文献检索能力进行培养和考核。对于刚入学或刚进实验室的研究生,主要汇报所查阅的文献,通过相互的交流和讨论,确定研究生的具体课题方向;对于高年级研究生,则着重汇报自己课题的进展情况以及遇到的问题,通过查阅文献如何解决[7]。
张朋等[15]利用纯化病毒制备抗鲤春病毒单克隆抗体,经Western -Blot 检测表明,制备的单抗主要识别SVCV N 蛋白,这可能与N 蛋白是病毒粒子中含量最丰富的蛋白有关。若用全病毒抗原制备单克隆抗体,难以筛选出与鲤春病毒G 蛋白反应的单抗,而本研究中以重组蛋白制备抗SVCV G 蛋白的单抗,则无需进行复杂的病毒纯化。为保证筛选结果的准确性,本研究中建立了间接ELISA 结合间接IFA 的筛选方法,前者可一次性处理大批样品以缩小筛选范围,后者可确保具有特异性的单抗与病毒反应。结果表明,本研究中成功筛选出两株阳性的杂交瘤细胞株,经Western -Blot 检测表明,两株单抗能与SVCV G 蛋白反应,具有良好的特异性。
苏霍姆林斯基说过:“教育的全部奥妙就在于爱儿童。”陶行之先生也说过:“捧着一颗心来,不带半根草去。”因此,爱是一种力量、一种品质,是教育成功的秘诀。在德育工作中,爱是基础,爱是本质,爱是师德的核心,爱是教师最基本的行为准则和道德准则。在德育工作中,如何让学生在师爱中快乐学习、健康成长、全面发展呢?
本研究中,采用大肠杆菌原核表达系统地实现了鲤春病毒G 蛋白的高效表达,经包涵体洗涤、亲和层析纯化后,采用尿素浓度梯度复性,首次以重组蛋白制备出抗鲤春病毒G 蛋白的单克隆抗体,为进一步建立新型SVCV 快速检测方法提供了技术支持。
[1]付峰,刘荭.鲤春病毒血症病毒(SVCV)的研究进展[J].中国水产科学,2006,13(2):328 -334.
[2]王姝,张利峰,徐立蒲.鲤春病毒核酸检测方法研究进展[J].检验检疫学刊,2012,22(3):49 -51.
[3]吕文雪,孟庆峰.淡水鱼病毒性疾病的研究进展[J].中国农学通报,2012,28(8):77 -81.
[4]刘萍,陈苗苗,刘学荣.单克隆抗体研究进展[J].中国畜牧兽医,2012,39(1):67 -70.
[5]Jorgensen P E V,Olesen N J,Ahne W,et al.SVCV and PFR viruses:serological examination of 22 isolates indicates close relationship between the two fish rhabdoviruses[C]//Viruses of Lower Vertebrates.Berlin:Springer,1989:349 -366.
[6]刘荭,付峰,黄倢.鲤春病毒血症病毒中国分离株糖蛋白基因和氨基酸序列的初步解析[J].中国病毒学,2005,20(6):647-651.
[7]Padhi A,Verghese B.Detecting positively selected codons in the glycoprotein of spring viremia of carp virus(SVCV)isolates from the USA and China[J].J Fish Dis,2008,31:785 -791.
[8]李强,迟刚,李莹,等.仿刺参体腔细胞单克隆抗体的制备及特性分析[J].大连海洋大学学报,2010,25(6):542 -546.
[9]孟思妤,孟长明.鲤春病毒血症(spring viremia of carp,SVC)的研究现状[J].渔业致富指南,2010(3):66 -67.
[10]Ahne W,Bjorklund H,Essbauer S,et al.Spring viremia of carp(SVC)[J].Dis Aquat Organ,2002,52:261 -272.
[11]张琳,丁雅苓,陈建民,等.中国鲤鱼春病毒血症毒株糖蛋白基因的亚克隆表达与纯化[J].中国兽医杂志,2011,47(7):10 -12.
[12]付峰,刘荭.鲤春病毒血症病毒的克隆及其在毕赤酵母中的初步表达[J].海洋水产研究,2007,28(4):72 -76.
[13]Huang F T,Li Q,Cui X X,et al.Characterization of spring viremia of carp virus glycoprotein expressed by recombinant baculovirus[J].Pak Vet J,2012,32(3):334 -338.
[14]杨振慧.鲤春病毒血症病毒外膜蛋白G和基质蛋白M 的原核表达及多克隆抗体的制备[D].福州:福建师范大学,2011.
[15]张朋,刘荭,陈孝煊.鲤春病毒血症病毒单克隆抗体的制备及其特性鉴定[J].中国预防兽医学报,2011,33(4):305 -308.
