叔丁基亚胺四氯合钽(Ⅱ)阴离子配合物[IPrH]+[tBuN=TaCl4(py)]-的合成与表征
2013-11-09张冬腾祝英英罗光明
张冬腾 祝英英 罗光明 蔡 琥
叔丁基亚胺四氯合钽(Ⅱ)阴离子配合物[IPrH]+[tBuN=TaCl4(py)]-的合成与表征
张冬腾 祝英英 罗光明 蔡 琥*
(南昌大学化学系,南昌 330031)
[tBuN=TaCl3(py)2]和氮杂环卡宾(IPr=1,3-bis(2,6-diisoproylphenyl)imidazol-2-ylidene)的反应得到预料之外的叔丁基亚胺四氯合钽(Ⅱ)阴离子配合物[IPrH]+[tBuN=TaCl4(py)]-(1)。利用核磁共振波谱,红外吸收光谱,荧光光谱,元素分析和X-Ray单晶衍射对配合物1的结构进行了表征。X-射线单晶衍射分析表明,Ta(V)中心与4个氯和2个分别来自亚胺和吡啶配体的氮原子以八面体构型配位。
亚胺;氮杂环卡宾;钽化合物;荧光
亚胺配体可以通过金属-氮的π键稳定高价态的前过渡金属化合物[1-2],这类化合物因其在诸如烯烃的复分解反应等均相催化方面的应用,引起广泛的关注[3]。另一方面,氮杂环卡宾(NHC)作为一个很强的σ电子给体,能与过渡金属形成稳定的配合物,近年来,氮杂环卡宾与后过渡金属的配合物因在C-C偶联反应、C-N键的生成、烯烃复分解反应、硅氢加成反应等有机反应中的高催化活性日益引起人们的重视[4-18]。由于稳定性的原因,对N-杂环卡宾金属配合物的研究主要集中在低价态的后过渡金属,而对高价态的前过渡金属N-杂环卡宾配合物的研究则相对较少[19-26]。因此,在前过渡金属氮杂环卡宾配合物的合成中引入亚胺基团以得到稳定的NHC配合物具有重要的实际意义[24,27]。本文利用NHC(IPr)和钽(Ⅱ)的亚胺化合物tBuN=TaCl3(py)2反应期望得到稳定的钽(Ⅱ)氮杂环卡宾配合物,得到一个意料之外的结构独特的叔丁基亚胺四氯合钽(Ⅱ)阴离子与咪唑盐阳离子的配合物 [IPrH]+[tBuN=TaCl4(py)]-(1),并用核磁共振波谱,元素分析和X射线单晶衍射对配合物1进行了表征。
1 实验部分
1.1试 剂
IPr[28-29]和tBuN=TaCl3(py)2[30]均按文献方法合成;其它试剂均为国药分析纯,甲苯溶剂在氮气保护下与钾和二苯甲酮蒸馏制得,CH2Cl2溶剂则在氮气保护下与CaH2一起蒸馏制得。
1.2 测试仪器
Bruker AV600型核磁共振仪(溶剂CD2Cl2,无内标),Scimitar 2000(Varian)红外光谱仪(KBr固体压片),Hitachi F-4500,Hitachi F-4600型荧光光谱仪,Bruker Smart Apex-Ⅱ CCD单晶衍射仪,Elementar Vario ELⅢ元素分析仪。
1.3 化合物1的合成
将氮杂环卡宾(IPr)(0.389 g,1.0 mmol)与钽(Ⅱ)亚胺 化 合 物tBuN=TaCl3(py)2(0.517 g,1.0 mmol)在Schlenk烧瓶中混合,在-40℃下加入30 mL甲苯并搅拌30 min,然后缓慢升温至0℃,继续搅拌过夜,过滤得到固体,固体用甲苯洗3次后,加入15 mL二氯甲烷溶解,浓缩,放入冰箱中冷冻,得到黄绿色的晶体 0.402 g,产率:48.5%,合成路线如 Scheme 1所示。
1H NMR(600 MHz,CD2Cl2):δ 9.20(s,1H,NCHN),9.15(d,J=4.1 Hz,2H,o-py),7.74(s,2H,NCH=),7.69(d,J=7.6 Hz,2H,p-C6H3)),7.63(t,J=7.8 Hz,1H,ppy),7.40(d,J=7.9 Hz,4H,m-C6H3),7.28~7.23(m,2H,m-py),5.33(s,4H,CH2Cl2),2.39(m,J=6.8 Hz,4H,CHMe2),1.27(d,J=6.8 Hz,12H,CH(CH3)2),1.22(d,J=6.9 Hz,12H,CH(CH3)2),1.19(s,9H,C(CH3)3)。13C NMR(150 MHz,CD2Cl2):δ 152.15(o-pyC),145.4(ipso-C6H3),140.8(p-pyC),137.3(o-C6H3),132.7(NCHN),130.1(p-C6H3),126.4(m-C6H3),125.3(m-pyC),125.2(NCH=),65.1(CMe3),54.24(CH2Cl2),32.00(C(CH3)3),29.6(CHMe2),24.6(CH(CH3)2),24.1(CH(CH3)2);IR(KBr 固体压片,ν/cm-1):3 376(w),2 964(s),2 876(w),1 639(m),1 531(s),1478(m),1380(m),1 334(m),1 208(m),807(s),761(s),671(m),618(w),438(m);元素分析(括号内为计算值)[IPrH]+[tBuN=TaCl4]-:C 48.02(47.52);H 6.34(5.92);N 4.36(4.37)。
1.5 晶体结构的测定
单晶均采用Bruker Smart Apex-ⅡCCD单晶衍射仪收集数据,在(296±2)K时,用经过石墨单色器单色化 Mo Kα(λ=0.071 073 nm)射线,选取大小为0.16 mm×0.13 mm×0.12 mm 的 单 晶 用于 X-射 线衍射分析, 在 1.43°≤θ≤26.00°的范围内共收集33 208个衍射数据,其中含8 851个独立衍射数据,74 27 个可观测衍射数据 I>2σ(I)。
晶体结构用SHELXS-97程序由直接法解出。用理论加氢法获得氢原子在晶胞中的位置。用SHELXL-97程序对所有非氢原子的坐标及其各向异性参数进行了全矩阵最小二乘法修正。


表1 配合物1的晶体学数据Table 1 Crystal Structure Parameters of complex 1

表2 配合物1的部分键长及主要键角Table 2 Selected bond distance(nm)and bond angles(°)of complex 1
配合物1晶体属于单斜晶系,空间群:P21/n,a=1.136 0(2)nm,b=1.991 7(4)nm,c=2.0424(4)nm,β=93.46°,V=4.612 65(163)nm3,Z=4,Dc=1.486 57 g·cm-3,F(000)=2 080,残差因子 R1=0.050 8,wR2=0.098 0。配合物1的晶体学数据见表1,主要键长键角列于表2。
CCDC:873803。
2 结果与讨论
本文期望利用NHC(IPr)和钽(Ⅱ)的亚胺化合物tBuN=TaCl3(py)2反应得到稳定的钽(Ⅱ)氮杂环卡宾亚胺配合物,却得到一个意料之外的叔丁基亚胺四氯合钽(Ⅱ)阴离子与咪唑盐阳离子通过静电作用结合在一起的配合物 [IPrH]+[tBuN=TaCl4(py)]-(1),其形成机理尚不清楚,可能的原因是由于NHC(IPr)配体具有较大的空间位阻,与钽(Ⅱ)中心形成配位比较困难,体系中存在的痕量HCl易与NHC(IPr)发生反应形成盐酸盐,其游离的氯离子进而取代tBuN=TaCl3(py)2中的一个吡啶分子(py)形成化合物1。1H和13C核磁波谱分析结果与单晶X-ray衍射分析所得到的分子结构是一致的,元素分析结果(C 48.02;H 6.34;N 4.36)与失去一个吡啶分子 (py)得到的化合物[IPrH]+[tBuN=TaCl4]-的计算值 (C 47.52;H 5.92;N 4.37)一致,这是由于化合物1中吡啶与金属中心的作用比较弱,在真空封管的过程中容易失去所致。
2.1 配合物的晶体结构
配合物1的分子结构图见图1(略去晶体中含有的2个CH2Cl2的溶剂分子)。从化合物1的晶体结构可以看出该配合物由咪唑阳离子和叔丁基亚胺四氯合钽(Ⅱ)阴离子两部分构成,Ta(Ⅱ)中心与4个氯和2个分别来自亚胺和吡啶配体的氮原子(N2、N1)构成扭曲的八面体构型。[tBuN=TaCl4py]-中Ta(Ⅱ)与亚胺氮原子的键长(Ta(1)-N(2),0.176 6(4)nm)以及Ta(Ⅱ)与吡啶氮原子的键长(Ta(1)-N(1),0.2460(4)nm)均略长于tBuN=TaCl3(py)2[30]中相应的Ta-N键长(0.174 5(5)nm,0.245 2(5)nm)。 Ta-Cl的平均键长为0.242 1 nm也略长于tBuN=TaCl3(py)2中的Ta-Cl平均键长(0.238 5 nm)。由于咪唑阳离子[IPrH]+的存在,使得化合物 1 中的 Ta(1)-N(2)-C(8)键角(170.5(4)°)较tBuN=TaCl3(py)2中相应的的Ta-N-C键角(175.50(5)°)小。化合物1中4个Cl原子近乎处在同一平面上,Cl(1)-Ta(1)-Cl(2),Cl(1)-Ta(1)-Cl(3),Cl(2)-Ta(1)-Cl(4)的平均键角为89.40°比靠近咪唑阳离子[IPrH]+的Cl(3)-Ta(1)-Cl(4)(87.52(4)°)更接近于直角,且来自亚胺配体的氮原子N2与Ta和Cl形成的N(2)-Ta(1)-Cl的平均键角(>90°)大于来自吡啶配体的氮原子N1与Ta 和 Cl形成的 N(1)-Ta(1)-Cl的平均键角(<90°),形成略似伞形的结构。Ta(Ⅱ)中心与来自亚胺和吡啶配体的氮原子之间的N(1)-Ta(1)-N(2)角度177.28(15)°大于tBuN=TaCl3(py)2的174.1(2)°,近似于直线。图2为化合物1的晶胞堆积图,从中可以看出阴离子[tBuN=TaCl4(py)]-中的吡啶环平面相互间几乎平行。
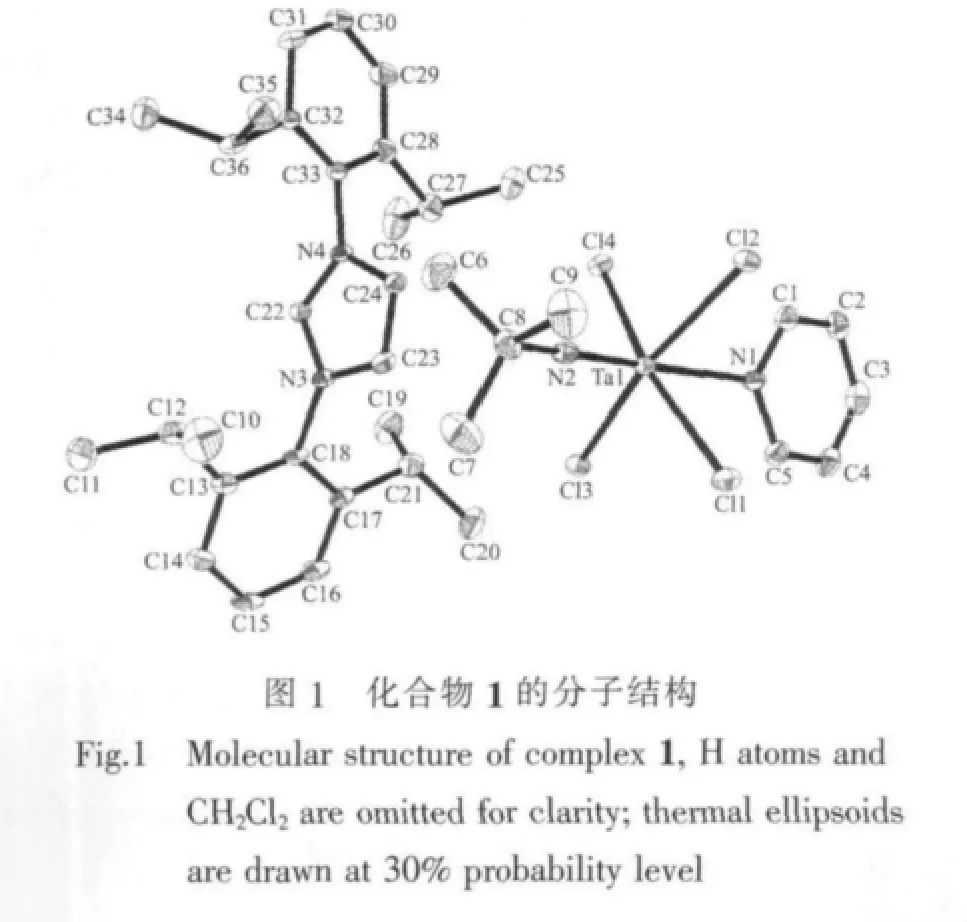

2.2 荧光性质
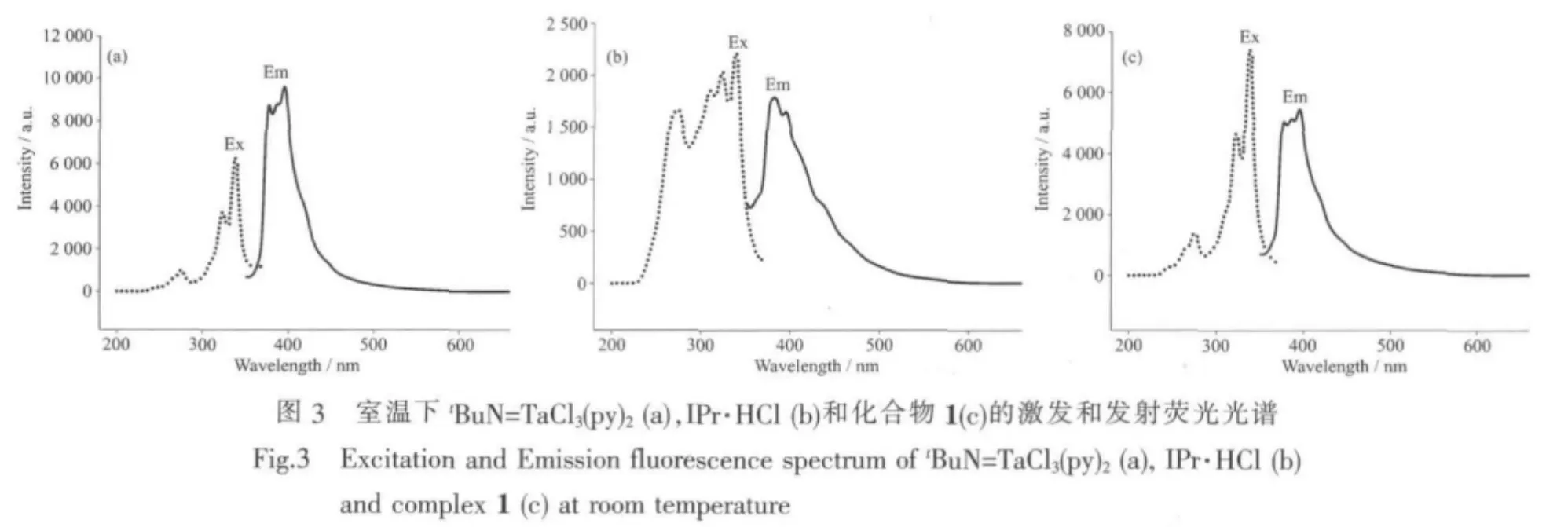
化合物1、tBuN=TaCl3(py)2以及氮杂环卡宾盐酸盐(IPr·HCl)配体的二氯甲烷溶液在室温下的荧光激发和发射谱如图3所示,氮杂环卡宾盐酸盐(IPr·HCl)配体在激发波长为340 nm时显示相对较弱的荧光发射峰(λmax=380 nm)(图 3(b));当激发波长为340 nm时,化合物1显示出与tBuN=TaCl3(py)2基本相同但强度有所减弱的荧光发射 (λmax=395 nm),这可以归属为钽(Ⅱ)与亚胺形成的离域πMN与钽的非键轨道之间的迁移(πMN→nM)[27]。由于在化合物1的晶体结构中 [IPrH]+基团与Ta(Ⅱ)中心之间只存在离子间的较弱静电作用而且本身荧光很弱,导致对化合物1荧光发射基本没有影响。另外,由于吡啶配体与πMN的作用很弱,因此吡啶配体数目的减少并没有对化合物1的荧光发射产生什么影响。
[1]Nugent W A,Mayer J M.Metal-Ligand Multiple Bonds.New York:Wiley,1988.
[2]Wigley D E.Progress in Inorganic Chemistry:Vol.42.New York:Wiley,1994:239-482
[3]Miguel G,Carlos G,Mannuel G,et al.Dalton Trans.,2011,40:2797-2804
[4]Ragone F,Poater A,Cavallo L,J.Am.Chem.Soc.,2010,132:4249-4258
[5]Gonzalez D C,Savariar E N,Thayumanavan S.J.Am.Chem.Soc.,2009,131:7708-7716
[6]Marion N,Nolan S P.Acc.Chem.Res.,2008,41:1440-1449
[7]Würtz S,Glorius F.Acc.Chem.Res.,2008,41:1523-1533
[8]Xi Z,Liu B,Chen W.J.Org.Chem.,2008,73:3954-3957
[9]Arrowsmith M,Hill M S,Kociok-Kohn G.Organometallics,2009,28:1730-1738
[10]John A,Ghosh P.Dalton Trans.,2010,39:7183-7260
[11]WANG Zhi-Guo(王志国),BIAN Qing-Quan(边清泉),HUANG Bao-Mei(黄宝美),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2012,28:191-194
[12]CHEN Chao(陈超),QIU Hua-Yu(邱化玉),LIU Ai-Ling(刘爱玲),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2011,27:1423-1430
[13]Melaimi M,Soleilhavoup M,Bertrand G.Angew.Chem.,Int.Ed.,2010,49:8810-8849
[14]Markó I E,Stérin S,Buisine O,et al.Science,2002,298:204-206
[15]Markó I E,Michaud G,Berthon-Gelloz G,et al.Adv.Synth.Catal.,2004,346:1429-1434
[16]Mas-Marza E,Sanau M,Peris E.Inorg.Chem.,2005,44:9961-9967
[17]Dragutan V,Dragutan I,Delaude L,et al.Coord.Chem.Rev.,2007,251:765-794
[18]Kandepi V V K M,Cardoso J M S,Peris E,et al.Organometallics,2010,29:2777-2782
[19]Jain K R,Herrmann W A,Kühn F E.Curr.Org.Chem.,2008,12:1468-1478
[20]Herrmann W Α, Öfele K,Elison M,et al.J.Organomet.Chem.,1994,480:C7-C9
[21]Kuhn N,Kratz T,Bläser D,et al.Inorg.Chim.Acta,1995,238:179-181
[22]Abernethy C D,Codd G M,Spicer M D,et al.J.Am.Chem.Soc.,2003,125:1128-1129
[23]Shukla P,Johnson J Α,Vidovic D,et al.Chem.Commun.,2004:360-361
[24]Lorber C,Vendier L.Dalton Trans.,2009,35:6972-6984
[25]Romain C,Miqueu K,Sotiropoulos J M,et al.Angew.Chem.Inter.Ed.,2010,49:2198-2201
[26]Spencer L P,Beddle C,Hall M B,et al.J.Am.Chem.Soc.,2006,128:12531-12543
[27]Willams D S,Korolev A V.Inorg.Chem.,1998,37:3809-3819
[28]Hintermann L,Beilstein J.Organomet.Chem.,2007,3:1-5
[29]Jafarpour L,Stevens E D,Nolan S P.J.Organomet.Chem.,2000,606:49-54
[30]Chiu H T,Chuang S H,Tsai C E,et al.Polyhedron,1998,17:2187-2190
Synthesis and Characterization of Tert-butylimido Tetra-chloro Tantalum(Ⅱ)Anion Complex[IPrH]+[tBuN=TaCl4(py)]-
ZHANG Dong-Teng ZHU Ying-Ying LUO Guang-Ming CAI Hu*
(Department of Chemistry,Nanchang University,Nanchang 330031,China)
[IPrH]+[tBuN=TaCl4(py)]-(1)(IPr=1,3-bis(2,6-diisoproylphenyl)imidazol-2-ylidene)was obtained unexpectedly by the reaction oftBuN=TaCl3(py)2and IPr.Complex 1 was structurally characterized by NMR,IR,fluorescence spectra,elemental analysis and single-crystal X-ray diffraction.The crystal structure of 1 shows that the Ta(Ⅱ)center is octahedrally coordinated by four chlorides and two nitrogen atoms from imido and pyridyl ligands,respectively.CCDC:873803.
imido complex;N-heterocyclic-carbene;Ta complex;luminescence
O614.51+3
A
1001-4861(2013)05-0953-05
10.3969/j.issn.1001-4861.2013.00.162
2012-04-18。收修改稿日期:2013-02-24。
国家自然科学基金(No.20861007)和江西省教育厅基金(No.GJJ08026)资助项目。
*通讯联系人。 E-mail:caihu@ncu.edu.cn;Tel:0791-88109568
