L-鸟氨酸-阿司匹林复合盐结晶工艺研究
2013-10-30熊洋黄志旭朱超张建万红贵
熊洋,黄志旭,朱超,张建,万红贵
(南京工业大学生物与制药工程学院,江苏 南京,210009)
L-鸟氨酸是一种非蛋白氨基酸,有很多重要的生理功能,其中最重要的作用是参与尿素循环,另外,它还能保护肝脏、刺激生长激素的分泌、改善睡眠、缓解疲劳、调节脂质代谢等[1]。近年,随着L-鸟氨酸的保健及医药功能的逐渐被发掘,人们对它的研究及新产品的开发逐渐产生了浓厚的兴趣,并取得了一定的成果:含L-鸟氨酸的20AA 复方氨基酸制剂不仅能保护肝脏、激发病态下肝脏活力,而且与大剂量VitB6 联合使用能有效治疗多器官功能障碍引起的大出血[2];L-鸟氨酸-门冬氨酸复合盐能治疗肝性脑病、肝炎以及保护肝脏[3-4];L-鸟氨酸苯乙酸盐能有效的降低鸟氨酸循环障碍患者体内的血氨浓度[5-6];鸟氨酸α-酮戊二酸盐是很好的临床营养剂,能促进外科创伤病人的恢复,改善慢性营养不良,改善免疫功能等[7];鸟氨酸柠檬酸盐可以改善食品和饮料的口味[8];此外,L-鸟氨酸与药物形成的复合盐能改善药物在理化性质上的缺陷,如鸟氨酸阿魏酸盐[9]、奥扎格雷鸟氨酸盐[10]等的稳定性或水溶性较成盐前好。研究表明,L-鸟氨酸复合盐不仅能改善某些药物的稳定性及水溶性,而且能起到联合使用相互增强药效的作用。因此,开发L-鸟氨酸复合盐具有很高的实用价值。
本文涉及的L-鸟氨酸-阿司匹林复合盐(L-ornithine-aspirin compound salt,以下简称“LOA”)是将L-鸟氨酸与阿司匹林以离子键结合形成的结晶产物,与临床上广泛使用的赖氨匹林相似,能有效改善阿司匹林的水溶性、稳定性。而L-鸟氨酸能够促进血脂代谢[1,11]、保护肝脏,这将有利于LOA 用于心脑血管疾病的预防与治疗,降低服用阿司匹林引起的肝毒性以及出血症风险。目前人们对阿司匹林的精氨酸盐以及赖氨酸盐研究较多,生产工艺也比较成熟,而关于LOA 制备工艺的研究较少。而结晶过程是LOA 制备工艺中的核心所在,本研究的目的是介绍一种制备结晶型LOA 的方法,并研究了其结晶过程,重点探讨了晶种和溶析剂流加情况对结晶质量的影响。
1 材料与方法
1.1 实验材料
L-鸟氨酸盐酸盐 实验室自制;阿司匹林、乙醇、氨水均为分析纯试剂。
BT00 -300M 恒流泵,保定兰格恒流泵有限公司;RE-52AA 旋转蒸发器,上海亚荣生化仪器厂;SHB-III 循环水式多用真空泵,郑州长城科工贸有限公司;PHS-3C pH 计,海三信仪表厂;JJ-1 精密增力电动搅拌器,常州国华电器有限公司;MasterSizer 2000激光粒度仪,英国马尔文仪器有限公司;leica DM 1000 显微镜,德国莱卡公司。
1.2 测定方法
1.2.1 产品纯度测定方法
以LOA 样品中的鸟氨酸含量计算产品的纯度,其中L-鸟氨酸含量测定方法见参考文献[12]。产品纯度计算公式:

式中:ms—样品总质量,g;mc—样品中实际测得的鸟氨酸的质量,g。
1.2.2 阿斯匹林含量测定方法
[13]。
1.2.3 普通光学显微镜样品处理方法
取少许样品于载玻片上,滴加2 ~3 滴无水乙醇在样品上,放在光学显微镜下观察且拍照,放大倍数为64 倍。
1.2.4 粒度分布测定方法
采用MasterSizer 2000 激光粒度分析仪测定样品粒度。
1.3 实验方法
1.3.1L-鸟氨酸盐酸盐的脱盐
将30 g 的L-鸟氨酸盐酸盐溶解在1 000 mL 水中,调节pH 到2.0,流过强酸性阳离子交换柱,L-鸟氨酸会与树脂结合,而Cl-并不在树脂上保留,而是随着上柱液流出柱子。用300 mL 水冲洗柱子,洗去树脂间隙中的Cl-等杂质,再用400 mL 的浓度为2 mol/L 的氨水洗脱,浓缩除氨,得到游离的L-鸟氨酸水溶液。
1.3.2 LOA 粗品的制备
25℃下,取500 mL 浓度为53 g/L 的游离L-鸟氨酸,减压浓缩10 倍,立即加入150 mL 无水乙醇,搅拌下,将上述L-鸟氨酸的乙醇溶液缓缓加入480 mL 浓度为75 g/L 的阿司匹林乙醇溶液。得到L-鸟氨酸-阿司匹林的白色沉淀,过滤,干燥得L-鸟氨酸-阿司匹林盐粗品。
1.3.3 LOA 溶解度的测定
维持恒定温度,溶剂配比以及搅拌速率,让溶剂与过量的LOA 经过一定时间的混合使其趋于溶解平衡,混合液离心后取上清液,测定其中鸟氨酸的浓度,换算成LOA 的质量即该条件下的溶解度。具体实验步骤为:配制乙醇与水的混合溶剂,将体系中乙醇的比例记为r,调整混合溶剂中乙醇与水的比例,使r值分别为:100%、95%、90%、85%、80%、75%、70%、65%、60%;分别加入过量的LOA,搅拌,溶解平衡后,取上清液,样品用0.25μm 微孔滤膜过滤,滤液稀释后,测定浓度。
1.3.4 LOA 的结晶
LOA 的间歇结晶过程按照溶析剂加入的量可以分成5 个阶段,如图1 所示。
取60 mL 浓度约为600 g/L 的LOA 加入结晶器,在适宜恒定的速度下搅拌;25℃下,恒流泵匀速流加乙醇,调整乙醇与LOA 溶液的体积比,添加晶种(将结晶质量较好的LOA 样品过标准筛,保藏备用,其中本实验采用125 目的晶种),搅拌养晶2 h;第III、IV阶段分别调整乙醇的滴加速率,使体系维持适宜的过饱和度,以适应晶体的生长;当乙醇与LOA 溶液的比例达到4∶1 时,停止流加乙醇,搅拌养晶,并降温到10℃;真空抽滤,无水乙醇洗晶3 次,干燥,得到结晶样品。
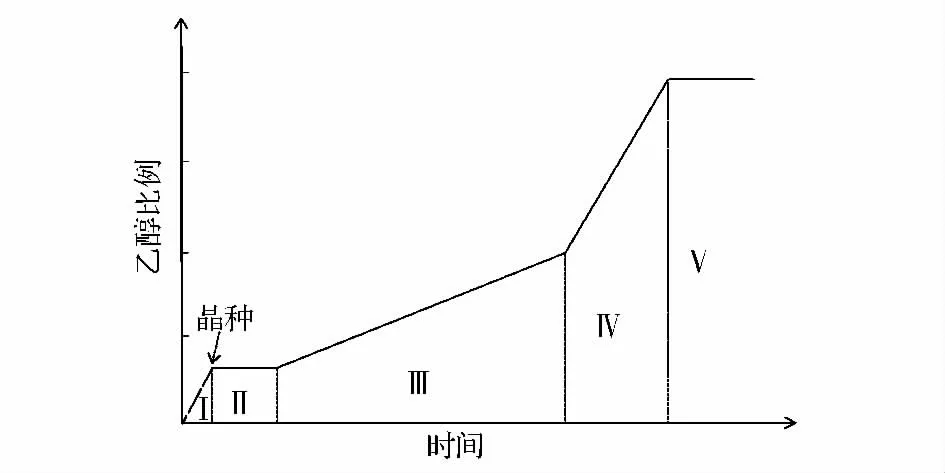
图1 溶析结晶过程示意图Fig.1 Schematic for dilution crystallization
2 结果与讨论
2.1 不同体积比的乙醇/水体系中LOA 的溶解
图2 为25℃下不同配比的乙醇/水体系中LOA的溶解度曲线。
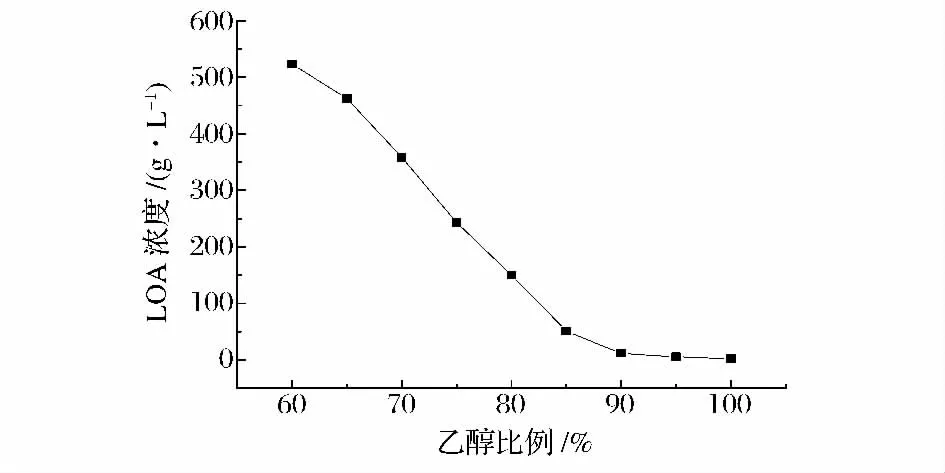
图2 25℃时不同配比的乙醇/水体系中LOA 的溶解度曲线Fig.2 Solubility of LOA at different ethanol/water ratio in 25℃
在溶析结晶第I 阶段,向60 mL 浓度约为600 g/L 的LOA 溶液中快速流加45 mL 的乙醇,体系中乙醇的比例从0 增加到60%,此时LOA 的溶解度为523 g/L,则此时体系的过饱和度约为ΔC=77 g/L。
在溶析结晶第III 阶段,继续慢速滴加75 mL 乙醇,体系中乙醇的比例为80%,而LOA 的溶解度由523 g/L 降低到150 g/L,流加单位体积的乙醇引起的溶解度改变较大,因此为得到质量较高的结晶产物,需要控制此阶段乙醇的滴加速率,以维持体系的过饱和度。
在溶析结晶第IV 阶段,较快速度流加120 mL 乙醇,体系中乙醇的比例为89%,LOA 的溶解度由150 g/L 降低到20 g/L。
显然60% <r<80%时,单位体积乙醇形成的过饱和度较大。从理论上分析,假设在结晶过程中晶体生长速率不变,那么在第III 阶段的乙醇流加速率应该最小,以保持体系保持合理的过饱和度,避免引发爆发成核。而为了提高生产效率,则在第I 和第IV阶段可以适当加快乙醇流加速率。
2.2 添加晶种的优化研究
在结晶的过程中,向体系加入少量的晶种有利于抑制一次成核并维持适量的二次成核,以提高产品质量。通过控制乙醇加入量,使LOA 溶液达到一定的过饱和度,考察晶种添加时机、晶种添加量对结晶的影响。
2.2.1 晶种添加时机对结晶的影响
取60 mL 浓度约为600 g/L 的LOA 溶液,25℃下,向体系中流加无水乙醇,当V(乙醇)∶V(LOA 溶液)分别为0.6、0.8、1.0、1.2 时,加入晶种。考察晶种加入时机对结晶的影响,实验结果如表1 所示。
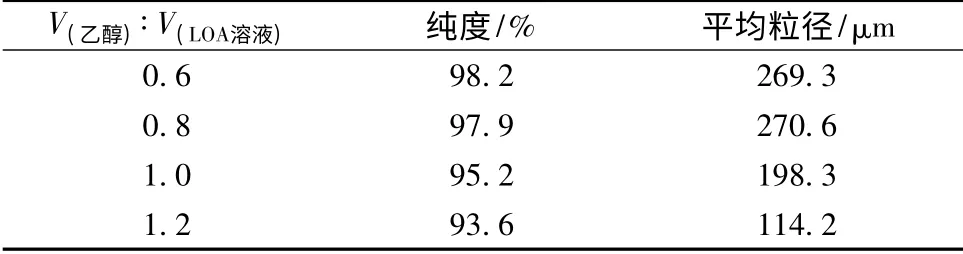
表1 晶种加入时机对结晶的影响Table 1 The influence of addition time of crystal seeds to crystal
实验结果表明,若在V(乙醇)∶V(LOA溶液)>0.8 时加入晶种,最终结晶产品细小且产品纯度较低,主要是因为溶液的过饱和度较大,越过介稳区,进入不稳区,造成初级均相成核,瞬间产生大量的晶核;V(乙醇)∶V(LOA溶液)为0.6、0.8 时加入晶种,结晶颗粒较大、产品纯度较高,说明加入晶种时溶液形成的过饱和度不高,并且加入晶种会及时降低过饱和度,避免形成初级均相成核现象。然而,过早加入晶种作用不大,故本研究选定V(乙醇)∶V(LOA溶液)=0.8 时,为最佳晶种添加时机。
2.2.2 晶种添加量对结晶的影响
取60 mL 浓度约为600 g/L 的LOA 溶液,25℃下,向体系中流加无水乙醇,当V(乙醇)∶V(LOA溶液)=0.8时,分别加入大小为125 目的(约115 μm)晶种。考察0%、2%、4%、6%的晶种加入量对结晶的影响,实验结果如表2 所示,不同晶种加入量对应的晶体显微照片如图3 所示。

图3 不同晶种添加量得到的晶体照片(64 倍)Fig.3 The picture of crystal with different addition amount of crystal seed (64 times)
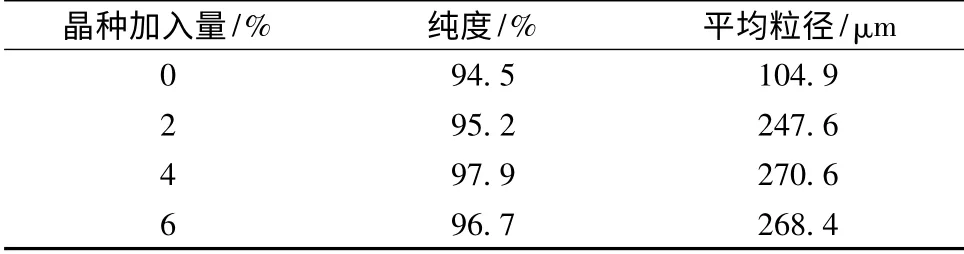
表2 晶种添加量对结晶的影响Table 2 Effect of crystal seeds amount on crystallization
实验结果表明,不添加晶种时,LOA 晶体平均粒径较小,且产品纯度低。这主要是因为不添加晶种时,初级均相成核现象严重,易爆发成核,导致晶核数量过多,同时过饱和度也会因此降低较多,使晶体生长动力不足;2%的晶种添加量时,提供的晶体数量少,结晶面积不够大,而体系的过饱和度较大,易产生初级均相成核,瞬间产生大量的晶核,导致LOA 颗粒细小、产品质量差;4%、6%的晶种添加量时,逐渐增大的晶种量,增加了结晶表面积,确保了结晶颗粒在介稳区内生长,产品平均粒度增大,细晶减少,在4%的晶种添加量时,平均粒度最大,纯度最高;6%的晶种添加量,晶体粒度较4%的晶种添加量时小,产品中存在少量细晶,可能是因为晶种数量过大,这虽然能够控制结晶过程在介稳区内进行,但是过多的晶种会增加晶体与晶体、晶体与搅拌桨、晶体与罐壁的碰撞机会,而且在过饱和度不变的条件下过多的晶种会导致晶体生长推动力下降。故选择4%的晶种添加量为最优值。
2.3 溶析剂流加速率的优化研究
2.3.1 第III 阶段乙醇流加速率对结晶的影响
取60 mL 浓度约为600 g/L 的LOA 溶液,25℃下,向体系中流加无水乙醇,当V(乙醇)∶V(LOA溶液)=0.8时,加入4%的晶种,搅拌养晶2 h,控制第III 阶段乙醇流加时间分别为:120 min、240 min、360 min,而第III 阶段共需要流加75 mL 乙醇,则对应的乙醇流加速率分别为:0.63 mL/min、0.31 mL/min、0.21 mL/min。
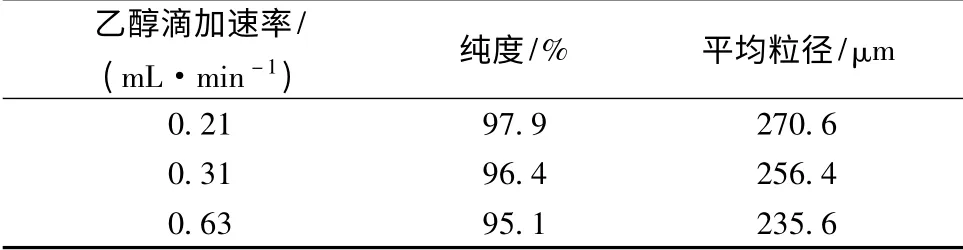
表3 乙醇滴加速率对结晶的影响Table 3 The influence of feeding rate of ethanol to crystal

图4 不同乙醇滴加速率的晶体照片(64 倍)Fig.4 The picture of crystal with different feeding rate of ethanol (64 times)
在结晶第III 阶段流加乙醇时间长短意味着结晶体系中LOA 的过饱和度不同。由粒径分布图和晶体照片可以看出,若以0.63 mL/min 流加乙醇,时间较短,体系中LOA 的浓度增值大于结晶速率,过饱和度不断增加,出现均相成核的机会增多,因此形成的晶体颗粒细小[14]。在0.21 mL/min 的流速下碎晶较少并且粒度分布均匀。但如果过度延长结晶时间,则可能会因晶体之间、晶体与搅拌桨叶之间的碰撞增加而形成细晶。故选择0.21 mL/min 为乙醇最佳流加速率。
2.3.2 第IV 阶段乙醇流加速度对结晶的影响
取60 mL 浓度约为600 g/L 的LOA 溶液,25℃下,向体系中流加无水乙醇,当V(乙醇)∶V(LOA溶液)=0.8时,加入4%的晶种,搅拌养晶2 h,控制第III 阶段乙醇流加速率为0.21 mL/min。第IV 阶段共需要流加120 mL 乙醇,控制流加时间分别为90 min、150 min、210 min,对应的流速分别为1.3 mL/min、0.8 mL/min、0.57 mL/min,考察第IV 阶段乙醇流加速率不同对结晶的影响。
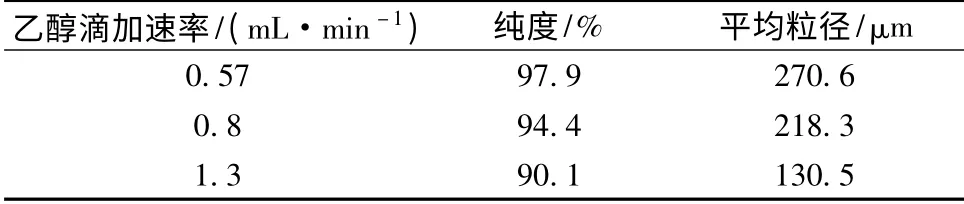
表4 第IV 阶段乙醇滴加速率对结晶的影响Table 4 The influence of ethanol velocity of flow to crystal at stage IV
实验结果表明,第IV 阶段乙醇流加速率为1.3 mL/min、0.8 mL/min 时,结晶产物中细小晶体较多,产品纯度也较低,主要是因为乙醇流加速率过快,导致过饱和度太大,而晶体生长速率相对较小,来不及消耗产生的过饱和度。而流加速率过低,不利于提高生产效率,故最佳流加速率选择为0.57 mL/min。
3 结论
本文介绍了L-鸟氨酸-阿司匹林复合盐的制备方法,重点讨论了其溶析结晶过程。由于在结晶的过程中,向体系加入少量的晶种有利于抑制一次成核并维持适量的二次成核,可以提高产品质量。因此,文章重点讨论了晶种加入时机以及加入量对结晶的影响。另外,根据乙醇流加量的不同将结晶过程分成了5 个阶段,重点研究了对结晶影响较大的第III、IV 阶段乙醇流加速率的不同对结晶的影响。结果表明,LOA的最优溶析结晶工艺为:取60 mL 浓度约为600 g/L的LOA 溶液,25℃下,向体系中快速流加无水乙醇,当V(乙醇)∶V(LOA溶液)=0.8 时,加入4%的晶种,搅拌养晶2 h;控制第III 阶段乙醇流加速率为0.21mL/min,维持6 h;然后加大乙醇流加速率至0.5 mL/min,维持3.5 h;最后搅拌养晶2 h,并将体系温度逐渐降至10℃。最终产品纯度为97.9%,平均粒径为270.6 μm。
参 考 文 献
[1] Chromiak J A,Antonio J. Use of amino acids as growth
hormone-releasing agents by athletes[J]. Nutrition,2002,18(7):657 -661.
[2] 岳茂兴,万红贵等. 用于治疗因凝血障碍而出血的药物组合物及其用途:中国,WO/016408 A1[P],2012.
[3] Ahmad I,Khan A A,Alam A,et al.L-Ornithine-L-aspartate infusion efficacy in hepatic encephalopathy[J]. Journal of the College of Physicians and Surgeons Pakistan,2008,18 (11):684 -687.
[4] 李晖. 门冬氨酸-鸟氨酸联用治疗肝性脑病[J]. 医药论坛杂志,2006(23):44 -45.
[5] Anderson K,Behling J.L-ornithine phenylacetate and methods of making thereof:US,WO/115055[P],2010.
[6] Oria M,Romero-Giménez J. Ornithine phenylacetate prevents disturbances of motor-evoked potentials induced by intestinal blood in rats with portacaval anastomosis[J].Journal of Hepatology,2012,56(1):109 -114.
[7] Coudray-Lucas C,Le Bever H. Ornithine[alpha]-ketoglutarate improves wound healing in severe burn patients:A prospective randomized double-blind trial versus isonitrogenous controls[J]. Critical Care Medicine,2000,28(6):1772 -1776
[8] Murata H,Yamamoto Y. Crystal ofL-Ornithine-Citric Acid Salt:Japan,US 2008/0015386[P],2008.
[9] 黄振华. 阿魏酸的氨基酸盐:中国,CN101195570[P],2008.
[10] 王东凯. 奥扎格雷鸟氨酸盐及其注射剂型:中国,CN1847228[P],2006.
[11] Sugino T,Shirai T,Kajimoto Y,et al.L-Ornithine supplementation attenuates physical fatigue in healthy volunteers by modulating lipid and amino acid metabolism[J].Nutr. Res,2008(28):738 -43
[12] 叶慧. HPLC—ELSD 法测定发酵液中L-鸟氨酸的含量[J]. 氨基酸和生物资源,2007,29(1):77 -79
[13] 庄舒翔,吴雨川. HPLC 法测定阿司匹林片的含量[J]. 中国药师杂志,2007,10(6):611 -612
[14] 王正伟,张建华等. 谷氨酸间歇等电结晶研究Ⅰ:调酸速率的控制[J]. 食品与发酵工业,2009,35(9):1-5.
