参麦注射液上市后安全性再评价研究*
2013-10-22张珏
张 珏
(天津市河西医院,天津 300202)
中药注射剂是以中医药理论为指导,采用现代科学技术和方法,从中药中提取有效物质制成的注射剂,相对其他中药剂型具有药效快、疗效确切等特点[1],近年来发展迅速,临床应用广泛。自2005年以来,一系列中药注射剂安全事件的出现引起了全社会的极大关注,对中药注射剂的安全性提出了质疑。中药注射剂的不良反应事件几乎涉及了目前所有在用的品种。本院参与天津市药品不良反应监测中心组织的参麦注射液上市后安全性再评价工作,为临床合理使用中药注射剂提供参考。
1 资料与方法
1.1 资料 2009年7月—2010年10月间在本院住院使用参麦注射液的患者200例,其中心内科86例,神经内科42例,血液科72例,病种分为冠心病、心衰、心绞痛、脑动脉硬化和急性白血病等。
1.2 方法 200例病例均给予参麦注射液50 m l,溶媒为5%葡萄糖注射液250 ml(或250 ml氯化钠注射液),静脉输注,1次/d,7~14 d为一疗程。
1.3 不良反应或不良反应事件监测方法 从用药开始至用药后15 d内为观察期。首先在给药后的30 min内进行密切观察,观测有无不良反应的发生,30 min 后进行定期检查,时间段为 1 h、2 h、5 h、12 h、24 h、48 h、5 d、10 d 和 15 d,并填写筛查表。记录疑似为参麦注射液不良反应的病例。15 d后停止主动观察,但对病人主动汇报仍继续接受。
2 结果
通过临床观察记录,在溶媒为5%250 ml葡萄糖注射液的164例病例和溶媒为250 ml氯化钠注射液的36例病例中,均未发现药源性不良反应。
2.1 观察对象的基本情况 见表1和表2。

表1 观察对象年龄分布

表2 观察对象性别分布
2.2 用药情况 见表3~5。
表3 用药疗程情况

表4 所用溶媒比例

表5 停用药情况
2.3 ADR观察结果 见表6。
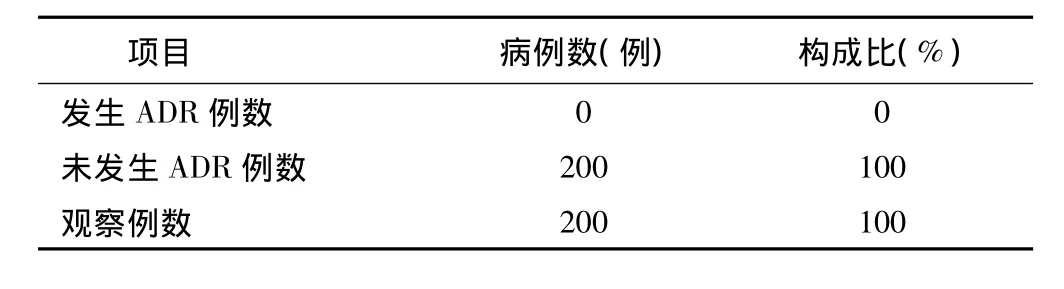
项目 病例数(例) 构成比(%)发生ADR例数00未发生ADR例数 200 100观察例数200 100
3 讨论
参麦注射液的主要成分为红参、麦冬,辅料为聚山梨酯80、亚硫酸氢钠。其功能为益气固脱,养阴生津,生脉。临床主要用于治疗气阴两虚型之休克、冠心病、心绞痛、心肌梗死、心力衰竭、慢性肺心病、病毒性心肌炎及增强肿瘤化疗药物疗效、调节肌体免疫力等。参麦注射液的临床疗效已经得到证实,其不良反应主要表现以过敏反应和输液反应为主,严重过敏性反应主要有过敏性休克和呼吸困难;偶有患者谷丙转氨酶升高;少数患者有口干、口渴与舌燥;此外,还可能引起皮肤、呼吸系统、心脏和消化系统等相关不良反应。在此基础上,对正大青春宝药业生产的第三代参麦注射液的安全性进行了再评价。参麦注射液中含有人参皂苷,是人参的主要活性成分。人参并无毒性,但用之不当或配伍不适则可引起不良反应,主要是导致延脑的呼吸及循环中枢陷入麻痹,临床表现为胸闷、气促、面部潮红,偶见皮疹和休克。
本院入选病例均为排除了过敏体质及药物过敏病例,用药剂量、适应证及给药间隔、给药速度等均以药品说明书为准。
中药注射液成分复杂,其中未除尽的动植物蛋白和鞣质等杂质极易引起变态反应;此外药物本身在生产或储存中也可产生新的杂质,以及临床不合理配伍、配制操作过程中污染等因素都可诱发中药注射液的不良反应。中药注射液的不良反应占所有中药不良反应发生率的75%甚至更高[2]。
本次研究是针对正大青春宝药业生产的参麦注射液进行的上市后安全性再评价,由于不良反应均发生在开始输液的2~5 min内,因此参麦注射液的不良反应为速发型,在对其输液后30 min内进行密切观察以及在随后的时间段中未发现有不良反应出现,证明正大青春宝药业生产的参麦注射液在本院的临床使用中是安全的。药品上市后的安全性再评价能够弥补药品上市前评价的不足,在广泛的人群使用中所发现迟发的不良反应和药物相互作用,可为临床合理用药提供依据。
1 周文燕,刘滔滔.中药注射剂不良反应分析[J].中药新药与临床药理,1997,8(1):52
2 叶爱琴,王建平.中药注射剂的不良反应与上市后再评价[J].医药导报,2006,12(25)12:1338
