新型锂离子电池组导电带耐腐蚀性能研究
2024-04-12楚翊婷王凯凤刘艾佳宋振兴韩建波金楠淏
楚翊婷,王凯凤,刘艾佳,陈 可,宋振兴,韩建波,金楠淏
(1.天津科技大学 化工与材料学院,天津 300457; 2.天津科技大学 理学院,天津 300457:3. 天津科技大学 人工智能学院,天津 300457; 4.天津工业大学 物理科学与技术学院,天津 300387
锂离子电池由于具有能量密度高、循环寿命长、无记忆效应等突出优点,已成为汽车动力电池的发展的一个主要方向[1]。锂电池被广泛应用于移动电子设备、电动汽车等领域[2]。锂离子电池组装为电池组需要导电带进行连接,要求导电带具有接触电阻低、导电性好、钎焊性好等优点。因此,导电带在整个电池系统中扮演着至关重要的作用。
锂电池导电带的腐蚀问题是制约锂电池性能和寿命的重要因素之一。锂电池导电带大多使用镍带、铜带或镀镍钢带,文献中对于上述材料的性能研究较多,如王云鹏等[3]研究了铜带电沉积镍层性能,杨娟丽等[4]研究了的镍带退火均匀性,严平等[5]研究了提高镍带强度的方法,Hongli Suo等[6]研究了高纯镍带的拉伸性能,刘奉英等[7]、梁旭等[8]学者研究了镀镍钢带的拉伸性能,但是对镍带、铜带或镀镍钢带的耐腐蚀性能研究较少。
表面修饰是对器件进行保护性防护的一种重要方式,如柳宇等[9]在太阳能电池性能的提升中研究了表面修饰的作用,同时导电聚苯胺(PANI)原料廉价易得、合成方法简单且环境友好,逐渐成为人们研究的热点[10],如徐海东等[11]在导电聚苯胺缓蚀剂的改性方法中研究了导电聚苯胺作为缓蚀剂的应用,牛丽丽等[12]在聚苯胺导电水凝胶的制备与表征中研究了导电聚苯胺作为水凝胶的制备。本文为提高导电带耐腐蚀性能,通过对镍带进行电沉积处理,使镍带表面形成聚苯胺复合石墨烯镀层,能大幅提高其耐腐蚀性能且不影响其钎焊性,并研究对比了电沉积不同时间的导电带在3.5% NaCl溶液中的耐腐蚀性能。
1 试验方法
称量0.93 g苯胺单体、4.90 g浓硫酸及4 g石墨烯,加入100 mL蒸馏水中,经超声振荡至白色絮状沉淀消失[13]。将镍带作为阳极浸入上述溶液进行电沉积,对电极为铂电极,沉积电压1.2 V。由于电沉积时间过长,所受应力不均匀,导致镀层过厚而脱落,所以电沉积时间分别选择1 min、3 min、5 min。然后依次用无水乙醇和去离子水进行清洗后作为试样备用。
浸泡实验在室温条件下进行,将试样浸入3.5%NaCl溶液,每24 h拍照记录试样的腐蚀过程。利用TESCAN5130SB扫描电子显微镜观测镀层表面形貌。采用CHI660E电化学工作站(上海辰华)及三电极系统进行阳极极化曲线和电化学阻抗谱(EIS)测试。其中待测试样为工作电极,钌钛电极网为辅助电极,饱和甘汞电极(SCE)为参比电极[14]。阳极极化扫描速率为10 mV·s-1。交流阻抗频率范围为10-2Hz~105Hz。
2 结果与讨论
2.1 扫描电镜观察
用电镜分别观察聚苯胺涂层与添加了石墨烯的电镀5 min的聚苯胺-石墨烯复合镀层,结果见图1。

图1 聚苯胺涂层与聚苯胺-石墨烯镀层的SEM照片Fig.1 SEM photograph of polyaniline coating with polyaniline-graphene coating
添加石墨烯后的电镀5 min聚苯胺-石墨烯复合镀层可以明显观察石墨烯褶皱,聚苯胺与石墨烯融合均匀,镀层致密,未见明显缝隙,基体基本被覆盖,石墨烯能隔绝基体与外界接触。
2.2 浸泡腐蚀试验
在3.5% NaCl溶液中,电沉积时间分别为1 min、3 min、5 min的试样的浸泡腐蚀试验结果照片见图2。

图2 镍带试样在盐水中浸泡7 d的表面变化Fig.2 Surface change of nickel strip specimens immersed in salt water for 7 days
由图2可知,无镀层的试样在3.5% NaCl环境下快速发生锈蚀,2 d后部分发生腐蚀,并且随着浸泡时间的延长,试样腐蚀程度急速加剧。在3.5%NaCl溶液中,镀覆聚苯胺改性镍带腐蚀进程较缓,浸泡5 d后开始发生局部点蚀,7 d后点蚀面积增加,但相比无镀层试样腐蚀面积大大减小[15]。对比电沉积1 min、3 min、5 min的试样腐蚀情况,观察可得:电沉积时间为5 min的试样腐蚀程度较低,耐腐蚀性能优于电沉积时间为1 min、3 min的试样。这是由于聚苯胺镀层越厚,使试样表面形成的阳极氧化膜越平整、结构更加致密,能够更好地保护试样,防止NaCl向试样内部渗透,使其耐腐蚀性能更优。但电沉积时间不可过长,会导致所受应力不均匀,镀层过厚而脱落。
2.3 电化学测试
2.3.1 阳极极化曲线
电沉积时间分别为:1 min、3 min、5 min的试样与未电沉积的试样在3.5% NaCl溶液中的阳极极化曲线,见图3。对阳极极化曲线数据进行拟合,电沉积不同时间的试样的自腐蚀电位Ecorr和腐蚀电流密度jcorr值,列于表1。
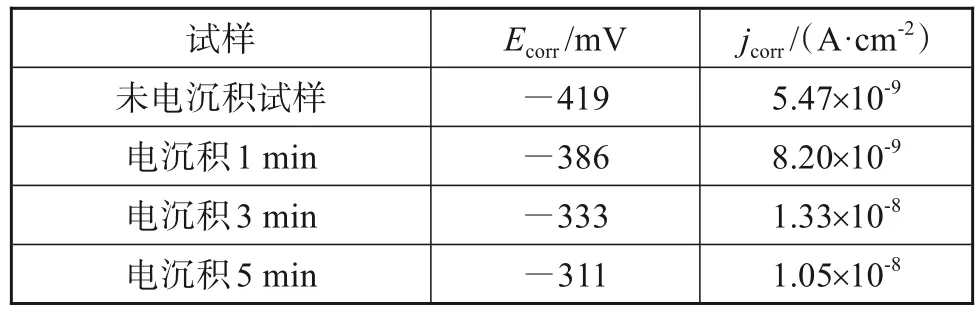
表1 试样在3.5% NaCl溶液中阳极极化曲线拟合数据Tab.1 Data fitted to the anodic polarization curves in 3.5% NaCl solution

图3 电沉积不同时间的镀覆聚苯胺镍带的阳极极化曲线Fig.3 Anodic polarization curves of coated PANI bands at different times of electrodeposition
阳极极化曲线是表征材料表面腐蚀特性的常用方法,通常自腐蚀电位越低、自腐蚀电流越高,说明该表面越容易被腐蚀。由图可知,电沉积聚苯胺试样与未电沉积试样相比,自腐蚀电位明显减小,表明聚苯胺镀层对试样起到了一定的保护作用。且随着电沉积时间的不断增长,镀覆聚苯胺镍带自腐蚀电位明显增加,与电沉积1 min试样相比,电沉积3 min和5 min聚苯胺的试样自腐蚀电位分别由-386 mV正移至-333 mV和-311 mV,腐蚀速率显著降低,且电沉积时间为5 min的镍带耐腐蚀性能更优。
2.3.2 交流阻抗试验
为了进一步探究试样的耐腐蚀性能,在3.5%NaCl溶液中进行了交流阻抗谱图的测试,图4为电沉积不同时间的镀覆聚苯胺镍带的Nyquist图。由图4可知,4条交流阻抗曲线都呈单一容抗弧,电沉积聚苯胺试样的容抗弧半径明显大于未电沉积试样的容抗弧半径。
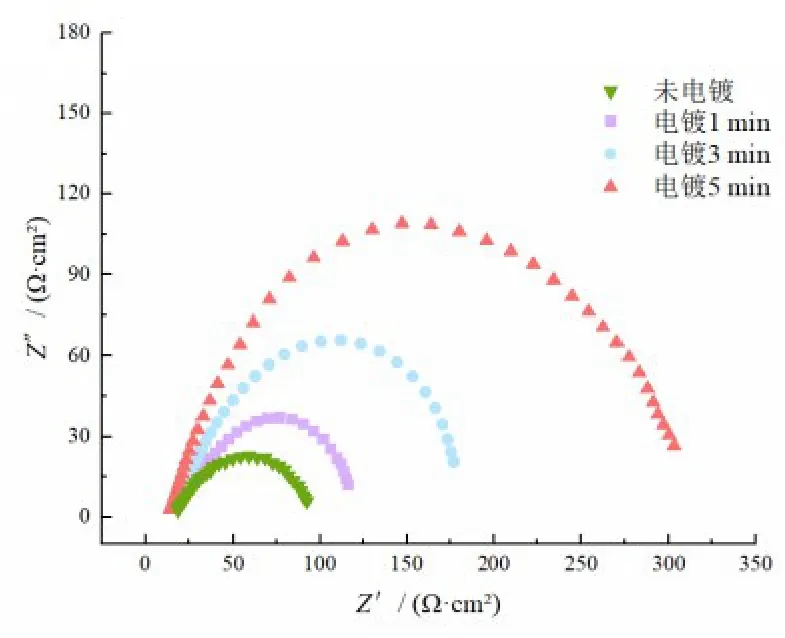
图4 电沉积不同时长聚苯胺的Nyquist图Fig.4 Nyquist plot of plating polyaniline at different times
通过交流阻抗谱及在腐蚀介质中的电化学体系特征,利用Zview软件进行电路拟合并解析电化学参数,交流阻抗谱等效电路如图5所示,RΩ为工作电极(试样)和参比电极(饱和甘汞电极)之间的溶液电阻;Rct为电荷转移电阻,为交流阻抗曲线半圆直径,结合公式Z=RΩ+[16],可知该参数反映腐蚀速率快慢,即Rct越大腐蚀过程中发生电荷转移越困难,试样腐蚀速率越慢,耐腐蚀性能越优异[17]。试验过程中腐蚀介质相同,不同时间测定RΩ值变化不大,可忽略RΩ对腐蚀过程的影响[18]。
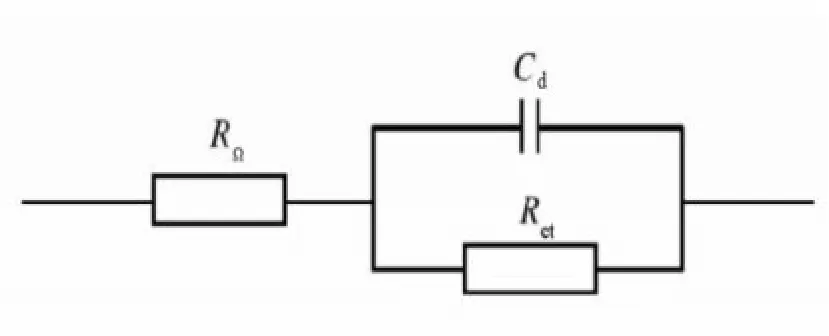
图5 交流阻抗谱的等效电路Fig.5 Equivalent circuit for the AC impedance spectrum
交流阻抗谱的拟合结果如表2所示,随着电沉积时间从1 min增加到5 min,试样的镀层厚度逐渐增厚,容抗弧半径逐渐增大,电荷转移电阻明显提高,当电沉积时间为1 min时,聚苯胺镀层电荷转移电阻为116.70 Ω·cm2,当电沉积时间为5 min时,聚苯胺镀层具有最大的容抗弧和最高的电荷转移电阻265.90 Ω·cm2,电荷转移电阻与电沉积1 min时相比提高了约149.20 Ω·cm2。这是由于聚苯胺镀层使试样表面形成较平整、结构致密的阳极氧化膜[19-20],阻碍腐蚀介质向试样内部渗透,表面发生电荷转移更困难,从而延缓了试样腐蚀的发展。上述规律与极化曲线测试结果得到相互印证。
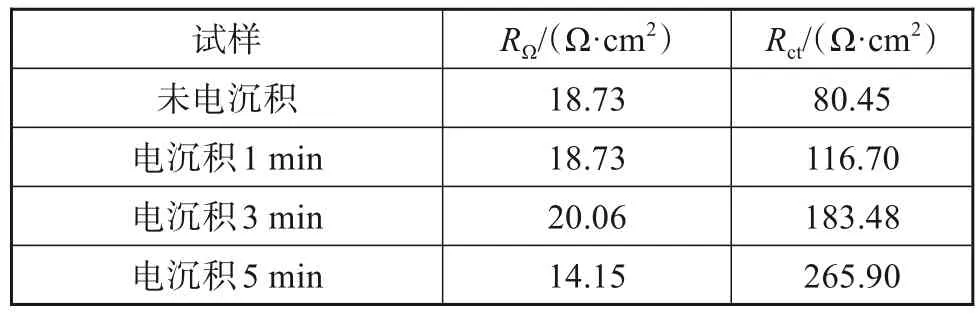
表2 3.5% NaCl溶液中样品的电化学阻抗谱拟合参数Tab.2 The electrochemical impedance spectral fitting parameters of the samples in 3.5% NaCl solution
3 结 论
本文利用恒电压法对镍带电沉积聚苯胺-石墨烯镀层,在3.5% NaCl溶液中进行浸泡腐蚀实验,并运用电化学工作站进行阳极极化和交流阻抗试验,对试样进行耐腐蚀性能的研究。
从电镜图可得添加石墨烯后的聚苯胺-石墨烯复合镀层致密,基体基本被覆盖;经浸泡腐蚀试验可看出镀覆聚苯胺改性镍带相比无镀层试样腐蚀面积大大减小;由阳极极化实验可得,电沉积5 min聚苯胺的试样比电沉积1 min、3 min试样自腐蚀电位均有提高;由交流阻抗实验可得,电沉积时间为5 min时,聚苯胺镀层具有最大的容抗弧和最高的电荷转移电阻,电荷转移电阻与电沉积1 min时相比提高了约149.20 Ω·cm2。实验表明聚苯胺镀层使镍带的耐腐蚀性能增强,且电沉积时间为5 min的试样耐腐蚀性能最好。
