HPLC法多成分含量测定结合化学计量学评价上清丸中大黄的质量
2024-01-08肖琳婧秦学玲金蒙付兴情龙琴张赟华
肖琳婧 秦学玲 金蒙 付兴情 龙琴 张赟华


基金项目:国家药品抽检项目(No.国药监药管[2022]1号)。
作者简介:
肖琳婧(1987—),女,白族,硕士,主管药师,研究方向为中药质量标准研究。E-mail:xiaolinjing1@126.com
通信作者:
张赟华(1977—),男,彝族,本科,副主任药师,研究方向为中药质量标准研究。 E-mail:33683185@qq.com
【摘 要】
目的:建立HPLC的方法测定上清丸中大黄的游离蒽醌(芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素)的含量,结合主成分分析方法,对市售上清丸中大黄(酒炒)的质量进行评价。方法:采用月旭Xtimate-C18(4.6 mm×250 mm,5 μm)色谱柱;流动相为乙腈-0.1%磷酸,梯度洗脱,检测波长为254 nm;流速为1 mL/min;柱温为30 ℃;进样量为10 μL。结果:103批上清丸大黄中游离蒽醌类成分含量相差较大,5种成分线性良好(0.9996≤r≤1.0000),平均加样回收率96.91%~101.40%(RSD值为0.6%~2.2%),通过主成分成分对上清丸(大蜜丸、水丸)中大黄(酒炒)质量进行综合评价,大蜜丸中大黄(酒炒)质量排名靠前的是来自A,C、F、G企业的样品,大黄(酒炒)质量较差是B、D、E、I企业生产的样品。上清丸(水丸)中,L、M企业各批次样品游离蒽醌的量较N企业高,说明L、M企業上清丸中大黄(酒炒)的质量较N企业好。结论:该分析方法简单可行,具有良好精密度、重复性和稳定性为上清丸中大黄(酒炒)质量评价提供参考。
【关键词】 上清丸;高效液相色谱法;游离蒽醌;主成分分析
【中图分类号】R284.1 【文献标志码】 A 【文章编号】1007-8517(2023)20-0028-10
DOI:10.3969/j.issn.1007-8517.2023.20.zgmzmjyyzz202320008
Quality Evaluation of Shangqing Pills by HPLC Coupled with Chemometrics
XIAO Linjing QIN Xuelin JIN Meng FU Xingqing LONG Qin ZHANG Yunhua*
Yunnan Institute for Food and Drug Control, Kunming 650106, China
Abstract:
Objective To establish simultaneous determination method of five anthraquinones(aloe-emodin, rhein, emodin, chrysophanol and physcion)in Shangqing Pills by HPLC. Methods Separation was performed on a Xtimate-C18 column (250 mm×4.6 mm, 5 μm) and the mobile phase was acetonitrile-0.1% phosphoric acid with gradient elution. The flow rate at 1 mL/min, the column temperature at 30 ℃, the detection wavelength at 254 nm, and the injection volume was 10 μL. Results The contents of five anthraquinones in the 103 batches of Shangqing pills were significantly different. There was a good linear relationships of five compoments in Shangqing Pills, with average recoveries of 96.91%-101.40% (RSD 0.6%-2.2%). Comprehensive evaluation of Shangqing pills by principal components analysis (PCA). The top companies in the comprehensive ranking of Shangqing big honeyed pills were A、C、H and G companies, and the lower ranking wereB、D、E and I companies. In Shangqing pills (water pills), the amount of free anthraquinone in samples from L and M were higher than that of N. Conclusion The analytical method is simple and feasible, with good precision, repeatability and stability. The method can provide a reference for the quality evaluation of Shangqing Pills.
Keywords:
Shangqing Pills; HPLC; Free Anthraquinones; Principal Components Analysis (PCA)
上清丸来源于《丹溪心法》“朱丹溪方上清散加减”[1],但与现行处方一致的上清丸最先记载于《北京市中药成方选集》[2]。上清丸现标准收载于卫生部药品标准中药成方制剂第十册,标准编号为 WS3-B-1878-95,标准收载大蜜丸和水丸两种剂型,后增加水蜜丸的规格。上清丸由菊花、薄荷、川芎、白芷、荆芥、防风、桔梗、连翘、栀子、黄芩(酒炒)、黄柏(酒炒)及大黄(酒炒)十二味药材组成。主要有清热散风、解毒通便的功效。临床上常用于头晕耳鸣、目赤、鼻流黄涕、口舌生疮、牙龈肿痛、大便秘结[3]。大黄为处方中的君药,用量约占处方量的五分之一,其主要活性成分为芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚等蒽醌类化合物。大黄蒽醌类成分仅占大黄成分的3%~5%,但具有较强的泻下、消炎、抗菌作用,是评价大黄药材以及含大黄制剂质量的指标成分[4-8]。上清丸现行质量标准仅对大黄进行显微鉴别。文献[9-11]报道,采用HPLC方法可对上清丸中的欧前胡素、黄芩苷、绿原酸及大黄中总蒽醌进行含量测定,但上清丸中大黄(酒炒)游离蒽醌含量测定未见报道。大黄(酒炒)后结合性蒽醌减少30%~50%,而游离蒽醌的量大幅提升,为评价大黄(酒炒)的质量,有必要建立其游离蒽醌的测定方法。
上清丸包括大蜜丸、水丸、水蜜丸三种剂型。三种剂型处方量相同,制法不同,具体制法如下:以上12味药材共530g,其中每100g粉末加炼蜜180g制成大蜜丸,每100g粉末加炼蜜40g制成水蜜丸,以水泛丸制成水丸。由于加入的辅料的量不同,造成不同剂型每克上清丸中含的大黄(酒炒)的量不同。为综合评价市售上清丸中大黄(酒炒)的质量,本实验采用了HPLC测定了103批样品中大黄中游离蒽醌类成分的含量,运用化学计量学的方法进行主成分分析,实现上清丸大黄(酒炒)质量科学、系统的控制。
1 仪器与试药
1.1 仪器 岛津LC-20A高效液相色谱仪;赛多利斯 BS224S电子天平;赛多利斯SECURA225D电子天平。
1.2 试药 芦荟大黄素对照品(批号:110795-201308,来源:中国食品药品检定研究院,含量以97.8%计);大黄酸对照品(批号:110757-201607,来源:中国食品药品检定研究院,含量以99.3%计,);大黄素对照品(批号:110756-201913,来源:中国食品药品检定研究院,含量以96.0%计);大黄酚对照品(批号:110796-201621,来源:中国食品药品检定研究院, 含量以 99.2%计);大黄素甲醚对照品(批号:110758-201415,来源:中国食品药品检定研究院,含量以 99.1%計)。乙腈为色谱纯(默克公司),水为纯化水,甲醇、乙醇、磷酸等其他试剂均为分析纯。
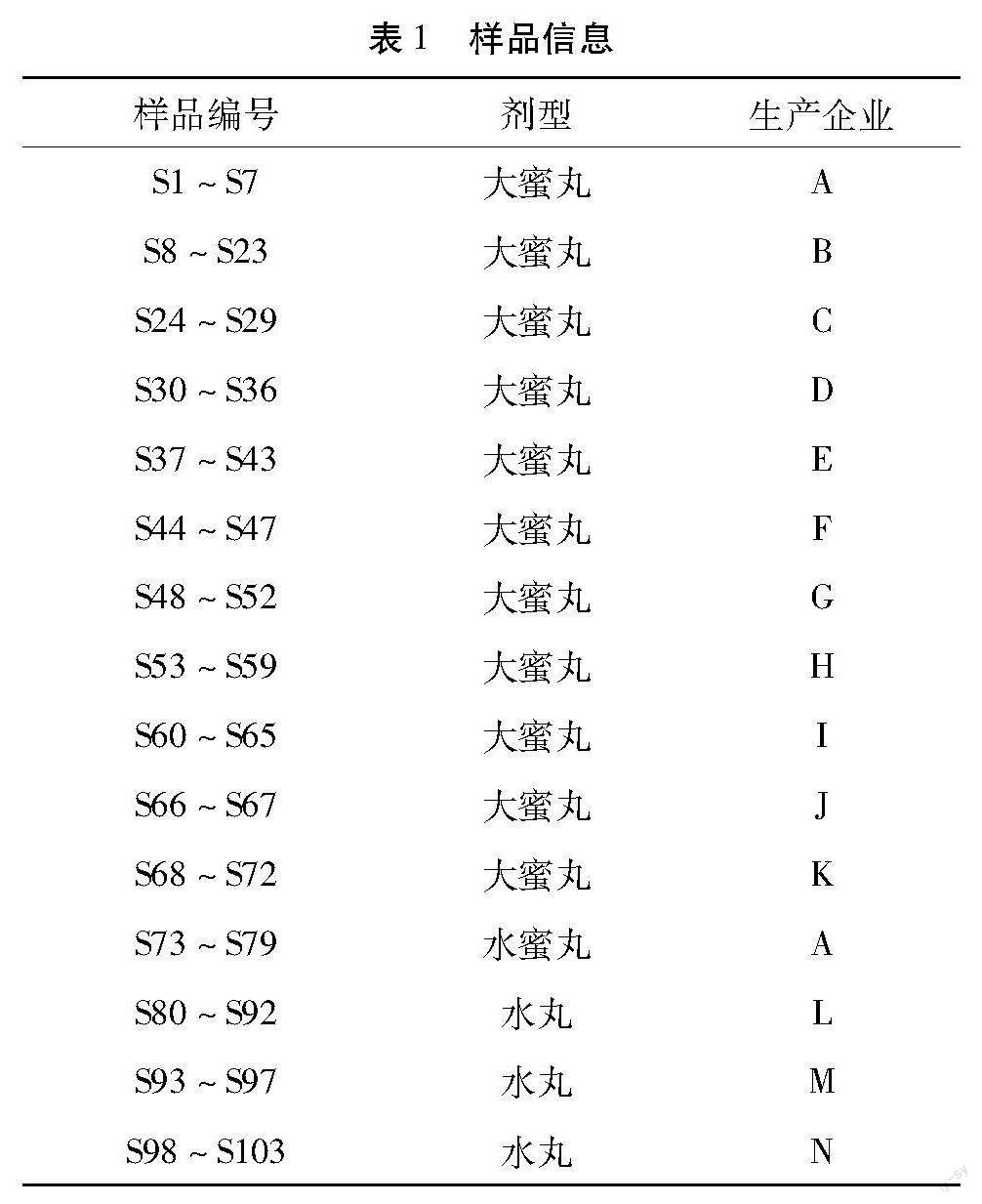
1.3 样品 方法学考察用的样品:上清丸(水蜜丸,批号:A12003,广州白云山陈李济药厂有限公司生产),其余103批次上清丸样品来源于14家生产企业,由于样品来源国家专项抽验,涉及数据保密,生产企业由A~N代替。具体信息见表1。
2 方法与结果
2.1 色谱条件 采用月旭Xtimate-C18色谱柱(4.6 mm×250 mm,5μm),以乙腈为流动相A,以0.1%磷酸为流动相B,梯度洗脱,流速为1 mL/min,柱温30℃,检测波长为254 nm。理论板数按大黄素峰计算应不低于3000。见表2。
2.2 溶液的制备
2.2.1 对照品溶液的制备 分别取芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚对照品适量,精密称定,加甲醇分别制成每1 mL含芦荟大黄素10μg、大黄酸8μg 、大黄素8μg、大黄酚40μg,大黄素甲醚10μg的混合溶液,即得。
2.2.2 供试品溶液的制备 取本品重量差异项下大蜜丸,剪碎,精密称定,取约2 g;取水丸或水蜜丸适量,研细,取约1 g,置具塞三角锥形瓶中,精密加入甲醇20 mL,称定重量,加热回流45 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.2.3 阴性供试品溶液的制备 按处方比例,在实验室模拟工艺,分别配制缺大黄细粉,分别取约1 g,同供试品溶液制备,即得阴性供试品溶液。
2.3 方法学考察
2.3.1 专属性试验 按“2.2.1、2.2.2、2.2.3”项下制备的对照品溶液、供试品溶液和阴性供试品,在上述试验条件下,采用紫外检测器检测,测定,记录色谱图,如图1。结果表明上述液相色谱条件下,供试品溶液色谱中呈现与对照品保留时间相同的色谱峰,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚与相邻色谱峰的分离度大于1.5,理论理论板数以大黄素峰计均不低于3000,阴性供试品在相应位置处未见色谱峰,表明其他药味不干扰5种待测成分的测定,方法专属性良好。
2.3.2 线性关系考察 精密称定取芦荟大黄素对照品10mg、大黄酸对照品8mg、大黄素对照品8mg、大黄酚对照品20mg、芦荟大黄素对照品10mg置于50 mL量瓶中,用甲醇溶解定容至刻度,摇匀,得芦荟大黄素母液(C=200μg/mL)、大黄酸母液(C=160μg/mL)、大黄素母液(C=160μg/mL)、大黄酚母液(C=400μg/mL)、大黄素甲醚母液(C=200μg/mL)精密吸取5 mL、5 mL、2 mL、1 mL、1 mL置于10 mL、50 mL、50 mL、100 mL、250 mL容量瓶中,加甲醇稀释定容至刻度,摇匀,即得系列线性溶液。精密吸取上述线性对照品溶液各10 μL,分别注入高效液相色谱仪中,按上述色谱条件进行测定。以各成分进样量为横坐标,相应峰面积为纵坐标,绘制标准曲线,计算回归方程,线性测定数据、回归方程及相关系数见表3。
2.3.3 精密度試验 取混合对照品适量,按上述方法制备,连续6次测定,测得芦荟大黄素、大黄酸苷、大黄素、大黄酚、大黄素甲醚的峰面积RSD(n=6)分别为0.3%、0.5%、0.7%、0.3%、0.5%,仪器的精密度良好。
2.3.4 稳定性试验 取上清丸(水蜜丸,批号:A12003,广州白云山陈李济药厂有限公司生产)同一供试品溶液,按“2.1”项下色谱条件分别进样,分别在0 h、4 h、8 h、12 h、20 h、24 h各进样一次,测定各组分的峰面积,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的峰面积RSD (n=6) 分别为0.9%、0.9%、0.5%、0.9%、1.0%,样品溶液在24 h内基本稳定。
2.3.5 重复性试验 取上清丸(水蜜丸,批号:A12003,广州白云山陈李济药厂有限公司生产)按“2.2.2”项下操作,平行提取 6 份,测得结果见表4,表明该方法重复性良好。
2.3.6 加样回收试验 分别精密称6份样品(批号:A12003) 0.5 g,采用加样回收试验方法,分别按下表精密加入5种对照品溶液,计算回收率和RSD见表5。
2.4 含量测定 取上清丸103批,按照2.2.2项下方法制备供试品溶液,各精密吸取10 μL,注入HPLC中,采用外标法计算各成分的含量,结果见表6。
由于不同剂型上清丸中每克样品大黄(酒炒)的量不同,对相同剂型不同企业不同批次的样品进行分析。
通过BM SPSS 18.0对不同企业生产的72批次上清丸(大蜜丸)游离蒽醌的含量进行显著性分析,结果见表7。上清丸(大蜜丸)A、C、F、G企业各批次样品游离蒽醌的量整体较高,上清丸中大黄(酒炒)质量整体较好;D、E、I企业各批次样品游离蒽醌的量均较低,上清丸中大黄(酒炒)质量整体较差,如A企业生产的大蜜丸游离蒽醌的量与其余B、D、E、I、K企业有显著性差异。
通过BM SPSS 18.0对不同企业生产的 72批次上清丸(水丸)游离蒽醌的含量进行显著性分析,结果见表8。上清丸(水丸)中,L、M企业各批次样品游离蒽醌的量较N企业高,说明L、M企业上清丸中大黄(酒炒)的质量较N企业好,L、M企业生产水丸游离蒽醌的量与N企业间有显著性差异。
2.5 化学计量学分析
2.5.1 主成分分析及综合评价[12-15] 采用IBM SPSS 18.0 和SIMCA 12.0软件对不同企业不同批次上清丸大黄中游离蒽醌类成分的量进行主成分分析。
将103批次不同剂型的上清丸样品导入IBM SPSS 18.0、SIMCA 12.0分析软件,根据表9,显示前2个主成分累积方差贡献率分别为95.39%,选取前2个主成分进行主成分分析。PCA 得分图如图2,不同剂型的上清丸在得分图中可以大致区分,红色为大蜜丸、紫色为水丸、绿色为水丸,但部分大蜜丸和水蜜丸之间存在交叉。
7批次水蜜丸为A厂家独家生产,因水蜜丸样本量较少未做主成分分析。将72批次上清丸(大蜜丸)、24批次上清丸(水丸)大黄中5个蒽醌类成分导入SPSS 18.0软件。
上清丸(大蜜丸、水丸)KMO统计量分别为0.663、0.524,大于最低标准0.5;Bartlett球型检验结果为0.000,P<0.001,说明该数据适合做因子分析,根据表10、11分别显示前2个主成分特征值均大于1,累积方差贡献率分别为94.63%、92.14%,选取前2个主成分进行主成分分析。
SIMCA 12.0 分析软件得到上清丸(大蜜丸、水丸)PCA 得分图,如图3、图4所示。
通过上清丸大蜜丸PCA得分图,结合上清丸中游离蒽醌的总量,72批上清丸(大蜜丸)样品大致可分为2组,说明不同生产企业生产的上清丸(大蜜丸)的质量存在差异,红色部分上清丸大蜜丸大黄(酒炒)质量较好,主要来自A、C、F、G企业,绿色部分大黄(酒炒)质量较差,主要由B、D、E、I企业生产。
24批上清丸(水丸)样品大致可分为3组,结合游离蒽醌的总量,红色部分为上清丸中大黄(酒炒)质量较好,N企业生产的上清丸均在绿色部分,大黄(酒炒)质量较差。
3 讨论
本研究比较了不同提取溶剂(90%甲醇、70%甲醇、70%乙醇、甲醇),不同提取方式(超声30 min、加热回流30 min),不同回流时间(30 min、45 min、60 min),最终确定最佳提取条件是甲醇加热回流提取45 min。此条件提取较完全,通过上述色谱条件,可以较好地测定上清丸大黄(酒炒)中游离蒽醌的含量。
本实验在筛选流动相时,通过对乙腈-水、甲醇-水的运行,筛选出乙腈-水系统优于甲醇-水系统,但大黄酸色谱峰出现了拖尾现象,进而以乙腈-0.1%磷酸水溶液为流动相,同时测定上清丸中游离蒽醌的含量。结果发现,以乙腈-0.1%磷酸水溶液为流动相梯度洗脱时,供试品中5个蒽醌类成分可达到基线分离,峰型较好,并且干扰较少,出峰时间适中,故选取此条件为流动相。
通过测定103批上清丸大黄中游离蒽醌的含量,按剂型对不同企业的样品中游离蒽醌的含量进行比较,上清丸(大蜜丸)中A、C、F、G企业各批次样品游离蒽醌的量整体较高,大黄(酒炒)质量整体较好;D、E、I企业各批次样品游离蒽醌的量均较低,大黄(酒炒)质量整体较差。上清丸(水丸)中,L、M企业样品游离蒽醌的量整体较N企业高,L、M企业上清丸中大黄(酒炒)的质量较N企业好。
进一步建立PCA模型,对不同剂型的上清丸进行主成分分析,大蜜丸、水蜜丸、水丸可大致区分,但部分批次大蜜丸和水蜜丸存在交叉。分析存在交叉的原因,根据不同剂型的上清丸制法,每克大蜜丸、水蜜丸、水丸中大黄的量分别为0.08 g、0.16 g、0.22 g,水蜜丸、水丸每克大黄的量分别为大蜜丸的2倍和3倍,如用品质相同的大黄投料,水蜜丸中大黄的游离蒽醌的量应为大蜜丸的2倍,但部分批次上清丸(大蜜丸)投料的大黄(酒炒)质量较好,游离蒽醌的量达到1mg/g以上,与水蜜丸中游离蒽醌的量相当。
综上,本实验采用多成分含量测定结合化学计量学市售上清丸中大黄(酒炒)的质量进行评价,为综合评价上清丸中大黄的质量提供依据。
参考文献
[1]
朱丹溪. 丹溪心法 [M]. 北京: 中国中医药出版社, 2008: 215.
[2]北京市公共卫生局. 北京市中药成方选集 [M]. 北京: 人民卫生出版社, 1961: 62.
[3]中华人民共和国药典委员会. 中华人民共和国卫生部药品标准: 中药成方制剂 第十册 [S]. 北京: 中华人民共和国卫生部, 1995: 8.
[4]国家药典委员会. 中华人民共和国药典一部 [S].北京:中国医药科技出版社, 2020:24-25.
[5]周浓. 实用临床中成药学 [M]. 北京: 中国中医药出版社, 2010: 42-43.
[6]李鑫楠, 黄毅岚, 张丹. RP -HPLC 测定熊胆降热丸中的5种大黄蒽醌类化合物 [J]. 华西药学杂志, 2002, 22(6): 697-698.
[7]高亮亮, 许旭东, 南海江, 等. 唐古特大黄化学成分研究 [ J]. 中草药, 2011, 42(3): 443.
[8]姚仲青. HPLC 法同时测定黄连上清丸中大黄素、大黄酚、大黄素 甲醚的含量[ J]. 中草药, 2001, 32(8): 699 -700.
[9]范贤标. 上清丸中欧前胡素和异欧前胡素含量的同时测定 [J]. 海峡药学, 2019, 31(12): 86-88.
[10]周遠雄, 陈繁华. 高效液相色谱-可变波长检测法用于上清丸的质量标准提高 [J]. 中国医药科学, 2018, 8(9): 53-55.
[11]黄敏, 陆石英, 叶萍. HPLC法测定上清丸中芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的含量 [J]. 中药材, 2013, 36(7): 1174-1176.
[12]刘慧, 肖金超, 张庆捷, 等. 金骨莲胶囊HPLC指纹图谱及化学模式识别研究 [J]. 中草药, 2021, 52(14): 4185-4192.
[13]周霖, 孙志, 薛文华, 等. 基于UPLC指纹图谱结合化学模式识别的丹灯通脑软胶囊质量控制研究[J]. 中国中药杂志, 2018, 43(16): 3279-3284.
[14]肖会敏, 杨旭, 黄新文, 等. 基于 HPLC指纹图谱及多成分含量的化学模式识别法评价小血藤质量[J]. 西北药学, 2022, 37(5): 1-7.
[15]关丽文, 高鑫磊, 杨天明. 基于HPLC多指标含量测定及化学计量学的养正消积胶囊质量评价[J]. 西北药学, 2022, 37(3): 26-33.
(收稿日期:2023-01-10 编辑:刘 斌)
