高效液相色谱法用于丙酸睾酮注射液的含量测定
2016-12-28徐文峰徐硕马捷
徐文峰+徐硕+马捷
[摘要] 目的 应用高效液相色谱(HPLC)建立丙酸睾酮注射液中丙酸睾酮的含量测定方法。 方法 采用Alltima C18色谱柱(4.6 mm×150 mm,5 μm),以甲醇-水(80∶20,v/v)为流动相,流速1.0 mL/min,检测波长241 nm,进样体积10 μL为色谱条件建立丙酸睾酮注射液含量测定方法,考察方法的线性、精密度、稳定性及加样回收率情况,并用药典方法验证该方法含量测定结果。 结果 在本方法中,丙酸睾酮的线性良好,相关系数(r)为0.9999,线性范围为120.86~282.01 μg/mL;精密度和稳定性良好,RSD均小于1.0%;丙酸睾酮的平均加样回收率良好,为100.1%(n = 9);运用该方法测得四个批号丙酸睾酮注射液的含量分别为标示量的99.5%、97.6%、98.4%、97.1%,相同批号样品药典方法含量测定结果为98.2%、98.5%、97.3%、95.9%,说明该方法与药典方法测定结果一致。 结论 该方法准确、简单、快速,可用于测定丙酸睾酮注射液中丙酸睾酮的含量。
[关键词] 高效液相色谱法;丙酸睾酮注射液;含量测定
[中图分类号] R927.2 [文献标识码] A [文章编号] 1673-7210(2016)10(c)-0134-04
[Abstract] Objective To establish a content determination method for testosterone propionate in Testosterone Propionate Injection using high performance liquid chromatography (HPLC). Methods An Alltima C18 column (4.6 mm×150 mm, 5 μm) was used for the separation with methanol: purified water (80∶20, v/v) as the mobile phase at the flow rate of 1.0 mL/min with 241 nm as the detection wavelength and 10 μL as the injection volume. The linearity, precisions, stability and spiked recovery of the established method were inspected and the determination results of this method were verified using the method in Chinese Pharmacopoeia. Results The method showed good linearity with correlation coefficient of 0.9999 for testosterone propionate in the linear range 120.86-282.01 μg/mL. The precisions and stability were satisfactory with the relative standard deviations (RSD) below 1.0%. The average spiked recovery of testosterone propionate was 100.1% (n = 9). The determination results of four batches of Testosterone Propionate Injection were 99.5%, 97.6%, 98.4% and 97.1% using this method. The contents of the same four batches of Testosterone Propionate Injection were 98.2%, 98.5%, 97.3% and 95.9% measured by the method in Chinese Pharmacopoeia, which suggested that the determination results of this method were consistent with the method of Chinese Pharmacopoeia. Conclusion The established method is accurate, simple and fast, and can be used for determination of testosterone propionate in Testosterone Propionate Injection.
[Key words] HPLC; Testosterone propionate injection; Determination
丙酸睾酮是人工合成的睾酮类雄性激素药物(化学结构式见图1),具有较强的生理活性,药理学研究表明丙酸睾酮能抑制双氧水诱导泪腺上皮细胞的凋亡,影响缺氧缺血性脑损伤新生大鼠海马、皮层胶质原纤维酸性蛋白的表达,影响大肠杆菌解旋酶结构和功能,影响大鼠胸腺细胞凋亡及胸腺中B淋巴细胞瘤-2基因的表达,拮抗促凋亡基因的表达等[1-9]。临床研究表明丙酸睾酮能促进男性器官及副性征的发育、成熟。大剂量时有对抗雌性激素作用,抑制子宫内膜生长及卵巢、垂体功能,还有促进蛋白质合成及骨质形成等作用[10]。注射液是丙酸睾酮唯一一种药物剂型,被《中国药典》2015年版二部收载,主要有1 mL∶10 mg,1 mL∶25 mg,1 mL∶50 mg,1 mL∶100 mg四种规格[11]。丙酸睾酮注射液临床适应证为原发性或继发性男性性功能减低;男性青春期发育迟缓;绝经后女性晚期乳腺癌姑息性治疗等。根据国家食品药品监督管理总局网站的最新数据显示,全国共六家企业生产丙酸睾酮注射液,分别为上海通用药业股份有限公司、天津金耀药业有限公司、广州白云山明兴制药有限公司、远大医药(中国)有限公司、河南科伦药业有限公司及福州海王福药制药有限公司。《中国药典》2015年版中丙酸睾酮注射液含量测定的前处理环节复杂,采用了提取、复溶、离心等方法,整个过程操作繁琐,影响因素较多[11]。结合文献[12-20],本实验改进了丙酸睾酮注射液含量测定中供试品的前处理方法,简化了药典方法中复杂的前处理环节,收到了满意的效果。
1 仪器与试药
1.1 仪器
Agilent 1260液相色谱系统,配有G1311C四元梯度泵,G1329B自动进样器,G1316A柱温箱,G4212B DAD检测器(Agilent Technologies,美国);Mettler XP-205电子天平(Mettler Toledo,瑞士);KQ-800KDE超声仪(昆山市超声仪器有限公司);Milli-Q超纯水处理系统(Millipore,美国)。
1.2 试药
甲醇(色谱纯,批号:155175,Fisher公司);实验室用水为超纯水;丙酸睾酮对照品(批号:100008-201206,中国食品药品检定研究院,纯度:99.8%);丙酸睾酮注射液(规格:1 mL∶25 mg;产品批号:1507111、 1411171;天津金耀药业有限公司)。丙酸睾酮注射液(规格:1 mL∶25 mg;产品批号:130609, 121202;上海通用药业股份有限公司);注射用大豆油(产品批号:150709;中航(铁岭)药业股份有限公司)。
2 方法与结果
2.1 色谱条件
色谱柱:Alltima C18色谱柱(4.6 mm×150 mm,5 μm);流动相:甲醇: 纯水(80∶20,v/v);流速:1.0 mL/min;检测波长241 nm;进样体积:10 μL;柱温为室温。进样前,所用溶液均用0.22 μm孔径尼龙滤膜过滤。
2.2 对照品溶液的制备
精密称定丙酸睾酮对照品约200 mg于100 mL容量瓶中,加甲醇适量,超声使溶解,用甲醇定容至刻度,摇匀,即为丙酸睾酮储备液(2.0 mg/mL)。精密量取丙酸睾酮储备液1.5、2.0、2.5、3.0、3.5 mL于25 mL容量瓶中,加甲醇定容,摇匀,获得丙酸睾酮浓度均约为120、160、200、240、280 μg/mL的对照品溶液。中间浓度的对照品溶液作为含量测定用的对照品溶液。
2.3 供试品溶液及阴性对照溶液的制备
精密量取本品2 mL(约相当于丙酸睾酮50 mg),置50 mL容量瓶中,用甲醇分数次洗涤移液管内壁,洗液并入容量瓶中,加甲醇适量,超声30 min,甲醇定容至刻度,摇匀,精密量取5 mL,置25 mL容量瓶中,用甲醇稀释至刻度,摇匀,作为供试品溶液。精密量取注射用大豆油2 mL,按上述方法操作,即得阴性对照溶液。
2.4 专属性实验和系统适应性实验
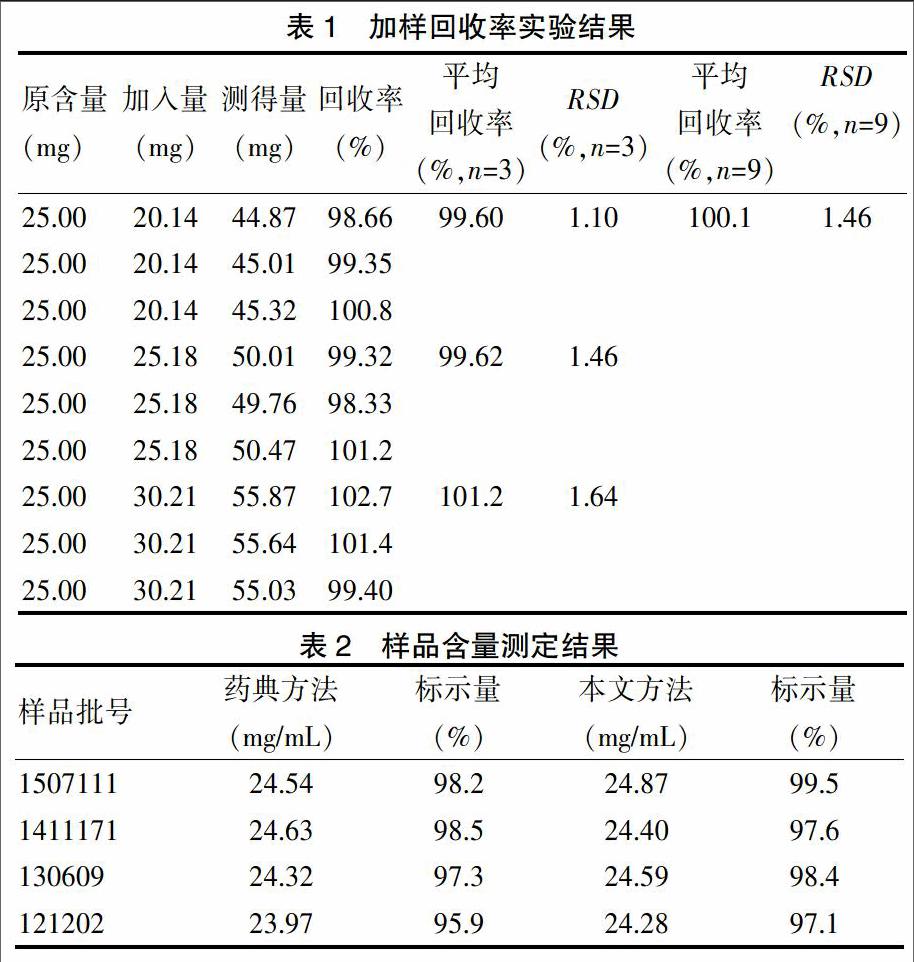
分别对阴性对照溶液、对照品溶液和供试品溶液进样分析,考察样品中辅料对丙酸睾酮定量的干扰。根据图2显示:样品中辅料不干扰丙酸睾酮的测定。理论板数按丙酸睾酮计算不低于4000。
2.5 线性和灵敏度
对“2.2”项不同浓度的对照品溶液分别进样,以峰面积为纵坐标,浓度(μg/mL)为横坐标作标准曲线。得到丙酸睾酮的线性方程为Y =27.6083X-9.8635,线性相关系数(r)为0.9999,线性范围120.86~282.01 μg/mL,说明方法在该范围内,线性相关性良好。
将对照品溶液用甲醇逐级稀释后,以信噪比(S/N)约为3.0时的浓度为最低检测限(LOD),S/N约为10.0时的浓度为最低定量限(LOQ),测得丙酸睾酮的LOD和LOQ分别为0.013、0.032 μg/mL。
2.6 精密度试验
对中间浓度的对照品溶液连续进样6次,对照品溶液中丙酸睾酮峰面积的RSD(n = 6)为0.18%,说明仪器精密度良好。
2.7 重复性试验
对批号1507111的丙酸睾酮注射液独立制备供试品溶液6份,分别进样分析,计算得到丙酸睾酮含量的RSD(n = 6)为0.56%,说明方法的重复性良好。
2.8 加样回收率试验
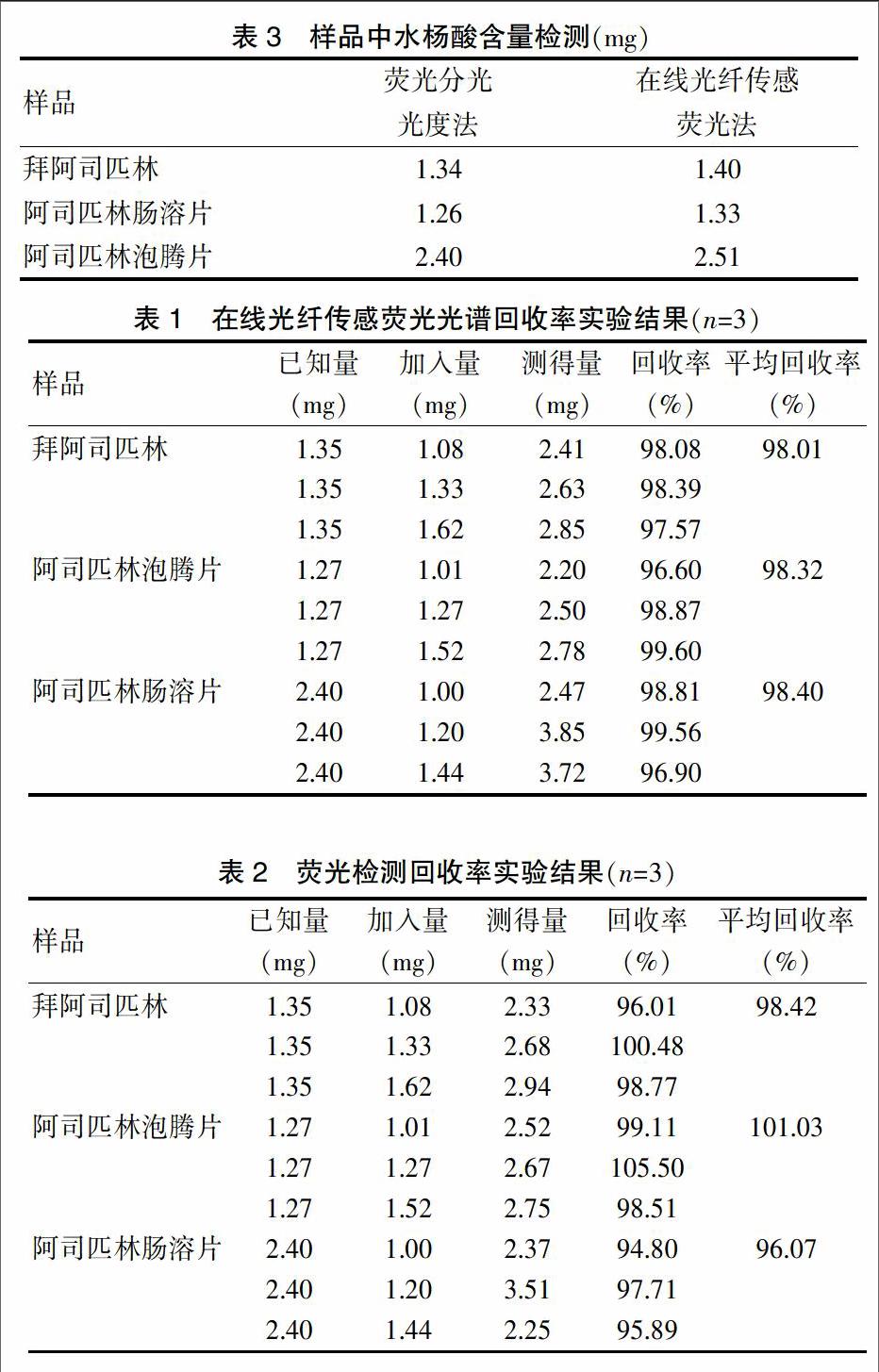
精密量取丙酸睾酮注射液1 mL(约相当于丙酸睾酮25 mg),置50 mL容量瓶中,用甲醇分数次洗涤移液管内壁,洗液并入容量瓶中,分别精密加入丙酸睾酮储备液10.0、12.5、15.0 mL,加甲醇适量,超声30 min,甲醇定容至刻度,摇匀,精密量取5 mL,置25 mL容量瓶中,用甲醇稀释至刻度,摇匀,过滤。每个浓度制备3份样品,共9份样品。进样测定,计算加样回收率和RSD,结果显示,丙酸睾酮的平均加样回收率为100.1%(n=9),RSD为1.46%(n=9),表明方法的加样回收率良好。见表1。
2.9 稳定性试验
对批号1507111的供试品溶液分别于0、2、4、8、12、24 h进样分析,计算得到24 h内丙酸睾酮色谱峰面积RSD(n = 6)为0.27%,表明供试品溶液在24 h内稳定性良好。
2.10 样品含量测定
应用本研究建立的方法及《中国药典》方法[11]对批号为1507111、1411171(天津金耀药业有限公司)、130609、121202(上海通用药业股份有限公司)的丙酸睾酮注射液进行含量测定,每个样品制备2份,取平均值。测定结果显示该方法与药典方法含量测定结果一致,说明方法准确可靠,可用于丙酸睾酮注射液的含量测定。见表2。
3 讨论
3.1 提取过程更简便
药典方法选择乙醚作为提取溶剂,需要将乙醚水浴挥散后甲醇复溶提取物,并需要通过多次振摇后离心的方式去除溶解在乙醚而不溶于甲醇的辅料成分[11],操作相对繁琐;本实验采用甲醇直接超声提取丙酸睾酮,操作简单,尽可能减少操作中引入的误差及减少辅料中的成分对丙酸睾酮含量测定时的干扰。
3.2 实验过程更快捷
药典方法需要用甲醇振摇4次(5、5、5、3 mL)复溶丙酸睾酮乙醚提取物,每次需振摇10 min,之后还需离心15 min,处理一份样品共计100 min[11]。本实验超声提取一份样品仅需30 min,方法更快捷。
3.3 含量测定结果准确可靠
本实验在保证丙酸睾酮注射液供试品的取样量(约相当于丙酸睾酮50 mg),稀释倍数(250倍),对照品溶液浓度(200 μg/mL),流动相的选择(甲醇-水,80∶20),检测波长(241 nm),丙酸睾酮峰的保留时间(约12 min)均与药典方法一致的前提下,对供试品前处理方法加以优化,保证测试结果只受样品前处理方法的影响。结果显示该方法与药典方法含量测定结果一致,说明方法准确可靠,可用于丙酸睾酮注射液的含量测定。
[参考文献]
[1] 沙翔垠,罗春云,宋莉,等.雌二醇及丙酸睾酮对H2O2诱导泪腺上皮细胞凋亡的抑制作用[J].中华实验眼科杂志,2011,29(12):1082-1086.
[2] 刘曼玲,李占魁.丙酸睾酮对HIBD新生大鼠海马、皮层GFAP表达的影响及其意义[J].中国妇幼保健,2011,26(31):4907-4911.
[3] 段丽霞,许厚强,陈祥,等.丙酸睾酮对大肠杆菌RecQ解旋酶结构和功能的影响[J].中国药理学通报,2011,27(4):467-472.
[4] 崔春红,殷彦君,王东.丙酸睾酮对大鼠胸腺细胞凋亡及胸腺中Bcl-2、Bax表达的影响[J].四川解剖学杂志,2010, 18(3):17-19.
[5] 李世佳,戎成婷,韩俊岭,等.不同剂量丙酸睾酮对半去势小鼠生精功能的影响[J].中国男科学杂志,2012(10): 21-24.
[6] 邵磊,李昇刚,孙振平,等.丙酸睾酮注射液对小鼠精子畸形的影响[J].齐鲁药事,2012,31(10):573.
[7] 邵磊,李昇刚,孙振平,等.丙酸睾酮注射液对大鼠的长期毒性[J].药学研究,2013,32(2):74-76.
[8] 李娜.丙酸睾酮治疗小鼠自身免疫性卵巢早衰及其机制的研究[D].长沙:中南大学,2011.
[9] 李洪蛟,陈树雄,蒋彦文,等.丙酸睾酮对小鼠睾丸NT-3和NT-4表达的影响[J].吉林农业大学学报,2016,38(2):203-207.
[10] 岂春晓.丙酸睾酮改变大鼠发育早起的旷场行为及中脑DA能神经元在旷场行为改变中的参与[D].石家庄:河北医科大学,2014.
[11] 国家药典委员会.中国药典[S].二部.北京:中国医药科技出版社,2015:150.
[12] 周筠,余敏灵,魏长勇,等.高效液相色谱法测定丙酸睾酮注射液的含量[J].现代医药卫生,2013,29(12):1811-1812.
[13] 李锡晶.复方丙酸睾酮乳膏的研究[D].天津:天津医科大学,2010.
[14] 程俊,余佩佩,顾华,等.高效液相色谱-二极管阵列/荧光检测器串联法同时测定化妆品中8种性激素[J].分析试验室,2016,35(1):112-116.
[15] 林芳,李涛,耿庆光,等.超高效液相色谱-二极管阵列检测器法快速测定保健食品中违法添加的14种性功能药物[J].食品科学,2014,35(4):163-169.
[16] 顾炳仁,许奇,缪刚.UPLC同时测定中成药及保健品中非法添加12种激素成分[J].药物分析杂志,2010,30(11):2185-2187.
[17] 冯碧敏,叶云,张昊.丙酸睾酮擦剂的制备与含量测定[J].中国药业,2012,21(1):38-39.
[18] 王桂英,杨湘君,杨新建.高效液相色谱法测定复方丙睾凝胶剂中丙酸睾酮的含量[J].天津药学,2015,27(3):7-8.
[19] 孟舒,杨立群,李淼,等.丙酸睾酮在不同介质中平衡溶解度和表观油水分配系数的HPLC法测定[J].时珍国医国药,2012,23(1):171-172.
[20] 周艳飞.高效液相色谱法测定黄体酮、丙酸睾酮及苯甲酸雌二醇含量[J].中国兽药杂志,2003,37(12):19-21.
(收稿日期:2016-07-10 本文编辑:赵鲁枫)
