替诺福韦与产后联合免疫阻断HBV母婴传播的有效性及安全性
2023-04-12吴飞霞孙立琪董晓晖张弦张彬
吴飞霞 孙立琪 董晓晖 张弦 张彬
[摘 要] 目的:观察HBV高病毒载量孕妇服用替诺福韦(TDF)与产后新生儿乙肝免疫球蛋白(hepatitis B immune globulin,HBIG)、乙肝疫苗联合免疫阻断慢性乙型肝炎病毒(hepatitis B virus,HBV)母婴传播的有效性和安全性。方法:慢性HBV感染(HBsAg阳性)孕妇100例,根据血清HBV DNA水平分为高病毒载量组(≥5.30 lg IU/mL)21例,低病毒载量组(<5.30 lg IU/mL,但高于检测下限)28例和低于检测下限组(<1.70 lg IU/mL)51例。高病毒载量组孕妇在妊娠28周至分娩结束前予以TDF抗HBV治疗;所有婴儿在出生12小时内完成乙肝免疫球蛋白和乙肝疫苗联合免疫,其后按计划接种乙肝疫苗。比较3组HBV母婴传播阻断效果,观察TDF用药的安全性。结果:高病毒载量组分娩前HBV DNA 4.61(3.96,5.86)lg IU/ mL明显低于用药前7.98(7.75,8.12)lg IU/mL,差异有统计学意义(P<0.05)。高病毒载量组有1例婴儿在7月龄发生HBV感染,HBV母婴传播阻断失败率4.7%,而低病毒载量组和低于检测下限组婴儿未发生产后HBV感染,3组阻断失败率比较,差异无统计学意义(P>0.05)。分娩前3组ALT水平比较,差异无统计学意义(P>0.05)。3组孕妇剖宫产率、胎膜早破、妊娠期糖尿病、妊娠期高血压、产后出血等并发症发生率比较,差异均无统计学意义(P>0.05)。3组均无胎儿窘迫、先天畸形及低体重儿,3组间新生儿出生体重、胎龄和5 min Apgar评分比较,差异均无统计学意义(P>0.05)。结论:高HBV DNA载量孕妇服用替诺福韦,联合新生儿乙肝疫苗和乙肝免疫球蛋白联合免疫,可有效阻断HBV母婴传播,安全性良好。
[关键词] 慢性乙型肝炎;高HBV病毒载量;母婴阻断;替诺福韦;免疫预防
[中图分类号] R512.6+2 [文献标志码] B [DOI] 10.19767/j.cnki.32-1412.2023.06.005
2016年5月世界卫生组织提出到2030年消除包括乙型肝炎病毒(hepatitis B virus,HBV)和丙型肝炎病毒性肝炎目标[1]。由于乙型肝炎疫苗的广泛接种,新感染HBV患者数量有所减少。然而,HBV传播的主要途经是妊娠期和围产期的母婴传播(mother-to-child transmission,MTCT)[2],90%~95%胎儿、婴儿感染HBV后可转为慢性HBV感染,因此预防HBV母婴传播,是降低慢性乙型肝炎(chronic hepatitis B,CHB)发病率的重要措施。
为贯彻落实《“健康中国2030”规划纲要》、《中国妇女发展纲要(2021-2030年)》和《中国儿童发展纲要(2021-2030年)》,响应世界卫生组织消除乙肝母婴传播的倡议,保护母亲和儿童的健康权益,中国国家卫健委提出到2025年在国家层面实现消除母婴传播,使HBV的MTCT率下降至1%以下。在中国MTCT是HBV传播的主要途径,文献报道乙型肝炎e抗原(hepatitis B e antigen,HBeAg)阳性母亲所生婴儿中,90%以上发生慢性HBV感染(CHB)[3-4]。乙型肝炎免疫球蛋白(hepatitis B immune globulin,HBIG)和HBV疫苗的联合免疫预防将MTCT率从90%降至10%~20%[5-7];HBV高病毒载量者孕晚期加用替诺福韦(TDF)能更好减少MTCT,但孕期使用核苷类似物抗HBV治疗对母婴可能存在一定不良反应。本文对2018年1月—12月在南通大学附属医院产检并完成分娩的慢性HBV感染母亲及所生婴儿进行回顾性研究,观察TDF与产后新生儿HBIG、乙肝疫苗联合免疫阻断HBV母婴传播的有效性和安全性。
1 资料与方法
1.1 一般资料 慢性HBV感染孕产妇100例,根据妊娠28周时血清HBV DNA水平分为高病毒载量组(≥5.30 lg IU/mL)21例,低病毒载量组28例(<5.30 lg IU/mL,但高于检测下限),低于检测下限组(<1.70 lg IU)51例[8]。高病毒载量组平均年龄29.67±4.53岁,平均孕期38.86±1.11周,丙氨酸转氨酶(ALT)7.98(7.75,8.12)U/L;低病毒载量组平均年龄30.32±4.68岁,平均孕期38.54±1.17周,ALT 15.50(12,20)U/L;低于检测下限组平均年龄31.39±3.74岁,平均孕期38.59±1.10周,ALT 15(10,20)U/L;3组孕妇平均年龄、平均孕周、ALT水平比较,差异均无统计学意义(P>0.05)。纳入标准:(1)母亲为慢性HBV感染者(HBsAg阳性>6个月);(2)单胎妊娠;(3)治疗依从性好;(4)同意产后婴幼儿按时复查两对半定量评估母嬰阻断效果;(5)自愿参加本研究并签署知情同意书。排除标准:(1)合并酒精性肝炎、药物性肝炎、脂肪性肝炎、自身免疫性肝炎、肝硬化等;(2)合并其他病毒感染或不明原因导致的肝功能损害;(3)不能配合随访者。
1.2 母婴阻断实施方案 所有临床诊疗行为参照《乙型肝炎母婴阻断临床管理流程》[9]和《AASLD 2018乙型肝炎指南》[10]。高病毒载量组孕妇于孕28周口服TDF片(成都倍特药业股份有限公司,国药准字 H20203610)0.3 g,每日1次,分娩后停药。3组新生儿出生后12小时内完成乙肝疫苗和HBIG联合免疫,在新生儿大腿前部外侧肌肉或上臂三角肌内接种重组酵母乙肝疫苗(深圳康泰生物制品股份有限公司,国药准字S20110026)10 μg/0.5 mL,在对侧相应部位注射HBIG(成都蓉生药业有限责任公司,国药准字 S20013033)100 IU,在1月龄和6月龄时分别接种相同剂量第2针和第3针乙肝疫苗。
1.3 检测方法 乙肝两对半定量采用美国Abbott公司i2000微粒子化学发光免疫分析系统及其配套試剂检测。采用实时荧光定量聚合酶链反应(poly-merase chain reaction,PCR)检测血清HBV DNA(检测下限为1.70 lg IU),按试剂盒(上海科华生物工程股份有限公司)说明书操作。
1.4 观察指标 (1)HBV母婴传播阻断效果:包括分娩时孕妇血清HBV DNA水平以及7个月龄时婴儿HBV感染率。(2)TDF用药安全性:产妇安全性评估主要包括围产期不良事件和并发症以及丙氨酸氨基转移酶(ALT)升高,婴儿安全性评估主要包括胎儿窘迫、先天畸形、低体重儿和5 min Apgar评分。
1.5 统计学处理 应用SPSS 25.0统计学软件进行数据分析。计数资料以频数和百分率表示,组间比较采用χ2检验或Fisher精确检验;符合正态分布的计量资料以x±s表示,组间比较采用t检验;非正态分布的计量资料以M(Q1,Q3)表示,组间比较采用K-W秩和检验。
2 结 果
2.1 HBV母婴传播阻断效果 高病毒载量组孕妇分娩前血清HBV DNA 4.61(3.96,5.86)lg IU/mL,显著低于TDF用药前7.98(7.75,8.12)lg IU/ mL,差异有统计学意义(P<0.05)。3组新生儿均完成全部免疫预防,7月龄时高病毒载量组1例婴儿发生HBV感染,阻断成功率95.24%,失败率4.76%,而低病毒载量组及低于检测下限组无婴儿感染,阻断失败率为0,组间比较差异无统计学意义(P>0.05)。
2.2 替诺福韦用药安全性
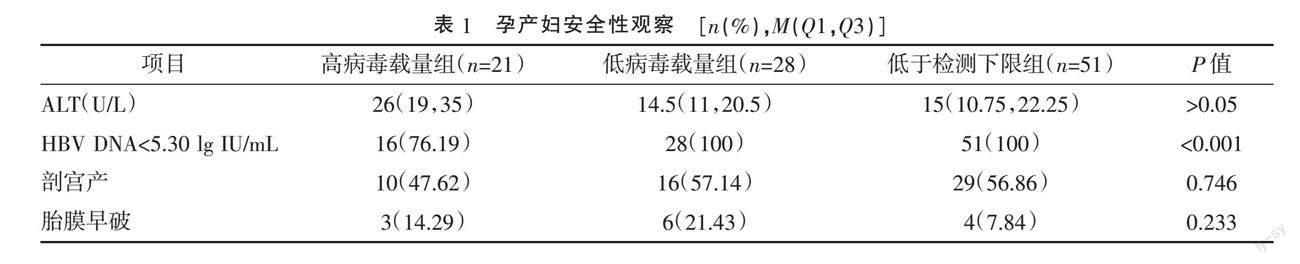
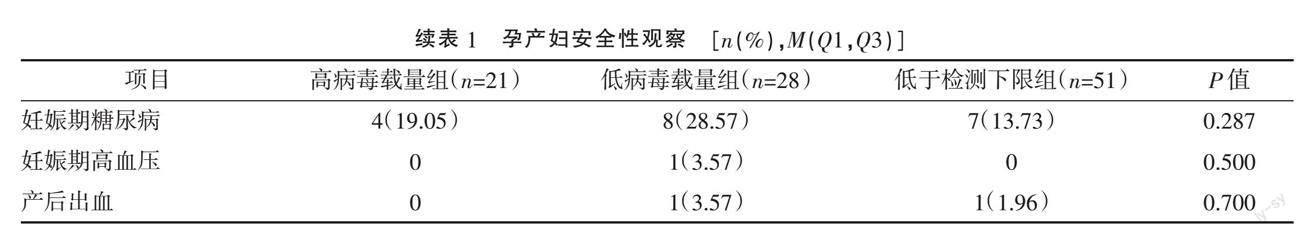
2.2.1 孕产妇安全性:分娩前高病毒载量组血清HBV DNA水平仍高于其他两组,低病毒载量组HBV DNA水平高于低于检测下限组,差异均有统计学意义(P<0.001)。3组间ALT水平比较,差异无统计学意义(P>0.05)。3组孕妇剖宫产率、胎膜早破、妊娠期糖尿病、妊娠期高血压、产后出血等并发症发生率比较,差异均无统计学意义(P>0.05)。见表1。
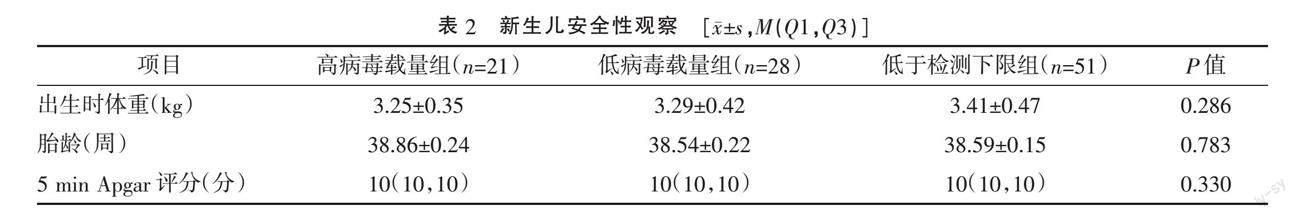
2.2.2 新生儿安全性:3组均无胎儿窘迫、先天畸形及低体重儿,3组间新生儿出生体重、胎龄和5 min Apgar评分比较,差异均无统计学意义(P>0.05)。见表2。
3 讨 论
母婴传播是我国乙型肝炎的主要传播途径之一,是导致慢性HBV感染的主要原因[11]。乙型肝炎疫苗和乙型肝炎免疫球蛋白联合免疫可降低HBV母婴传播,但完成联合免疫后仍有5%~10%新生儿感染HBV,而妊娠晚期孕妇HBV高病毒载量是导致联合免疫阻断失败的主要原因[12-13]。因此,国内外多个权威指南推荐高病毒载量孕妇在妊娠中晚期口服核苷(酸)类似物降低HBV DNA水平,以期阻断HBV母婴传播[14],《中国乙型肝炎病毒母婴传播防治指南》推荐的首选药物是富马酸替诺福韦二吡呋酯[15-16]。
HBV高病毒载量孕妇于妊娠中晚期(孕24~28周)应用TDF结合标准的婴儿HBV免疫预防,预防MTCT的成功率为99%[16]。本研究回顾性分析100例HBsAg阳性孕妇,显示95%孕妇分娩前HBV DNA水平<5.30 lg IU/mL;其中高病毒载量组76.19%孕妇在分娩前HBV DNA水平<5.30 lg IU/mL,仅1例HBV高病毒载量组孕妇出现母婴垂直传播,提示妊娠28周时HBV病毒载量超过5.30 lg IU/mL孕妇是发生HBV母婴垂直传播高危人群。本研究中HBV高病毒载量组孕妇在孕28周启动TDF抗HBV治疗,分娩后12小时内完成新生儿乙肝疫苗和乙肝免疫球蛋白联合免疫,从而明显降低MTCT的发生,与文献[17]报道TDF预防MTCT的效果一致。
本研究发现高病毒载量组孕妇对TDF耐受性良好,未出现妊娠期高血压和产后出血,仅4例妊娠期糖尿病,3例胎膜早破,并发症与其他两组比较,差异无统计学意义(P>0.05)。有2例孕妇在TDF治疗期间ALT升高,1例ALT为194 U/L,另1例为168 U/L,产后均恢复正常。高病毒载量组新生儿平均胎龄为38.86±0.24周,5 min Apgar评分10(10,10)分,也未出现胎儿窘迫、先天性缺陷及低体重儿,与其他两组的差异无统计学意义(P>0.05)。
综上所述,HBV高病毒载量孕妇在妊娠28周服用替诺福韦,联合新生儿免疫治疗可有效降低母婴传播的风险,安全性良好。
[参考文献]
[1] COOKE G S,ANDRIEUX-MEYER I,APPLEGATE T L,et al. Accelerating the elimination of viral hepatitis:a Lancet Gastroenterology & Hepatology Commission[J]. Lancet Gastroenterol Hepatol,2019,4(2):135-184.
[2] PAN C Q,ZHANG J X. Natural history and clinical consequences of hepatitis B virus infection[J]. Int J Med Sci,2005,2(1):36-40.
[3] WANG F S,FAN J G,ZHANG Z,et al. The global burden of liver disease: the major impact of China[J]. Hepatology,2014,60(6):2099-2108.
[4] JING W Z,LIU J,LIU M. Eliminating mother-to-child transmission of HBV: progress and challenges in China[J]. Front Med,2020,14(1):21-29.
[5] GREENUP A J,TAN P K,NGUYEN V,et al. Efficacy and safety of tenofovir disoproxil fumarate in pregnancy to prevent perinatal transmission of hepatitis B virus[J]. J Hepatol,2014,61(3):502-507.
[6] CHEN H L,LEE C N,CHANG C H,et al. Efficacy of maternal tenofovir disoproxil fumarate in interrupting mother-to-infant transmission of hepatitis B virus[J]. Hepatology,2015,
62(3):375-386.
[7] PAN C Q,DUAN Z,DAI E,et al. Tenofovir to prevent hepatitis B transmission in mothers with high viral load[J]. N Engl J Med,2016,374(24):2324-2334.
[8] 中国肝炎防治基金会,中华医学会感染病学分会,中华医学会肝病学分会.阻断乙型肝炎病毒母婴传播临床管理流程(2021年)[J]. 临床肝胆病杂志,2021,37(3):527-531.
[9] 中国肝炎防治基金会,中华医学会感染病学分会,中华医学会肝病学分会. 乙型肝炎母婴阻断临床管理流程[J]. 临床肝胆病杂志,2017,33(7):1214-1217.
[10] TERRAULT N A,LOK A S F,MCMAHON B J,et al. Update on prevention,diagnosis,and treatment of chronic hepatitis B: AASLD 2018 hepatitis B guidance[J]. Hepatology,2018,67(4):1560-1599.
[11] INDOLFI G,EASTERBROOK P,DUSHEIKO G,et al. Hepatitis B virus infection in children and adolescents[J].Lancet Gastroenterol Hepatol,2019,4(6):466-476.
[12] DING Y,SHENG Q J,MA L,et al. Chronic HBV infection among pregnant women and their infants in Shenyang,China[J]. Virol J,2013,10:17.
[13] KANG W,LI Q,SHEN L,et al. Risk factors related to the failure of prevention of hepatitis B virus Mother-to-Child transmission in Yunnan,China[J]. Vaccine,2017,35(4):605-609.
[14] 中華医学会感染病学分会,中华医学会肝病学分会. 慢性乙型肝炎防治指南(2019年版)[J]. 中华肝脏病杂志,2019,27(12): 938-961.
[15] 中华医学会感染病学分会,GRADE中国中心. 中国乙型肝炎病毒母婴传播防治指南(2019年版)[J]. 中华传染病杂志,2019,37(7):388-396.
[16] 中华医学会肝病学分会. 感染乙型肝炎病毒的育龄女性临床管理共识[J]. 中华肝脏病杂志,2018,26(3):204-208.
[17] CHEN H L,LEE C N,CHANG C H,et al. Efficacy of maternal tenofovir disoproxil fumarate in interrupting mother-to-infant transmission of hepatitis B virus[J]. Hepatology,2015,62(2):375-386.
[收稿日期] 2023-10-03
(本文编辑 缪宏建)
