ZnO/g-C3N4复合光催化剂的制备及光催化还原U(Ⅵ)
2022-10-24刘岳林谢水波葛玉杰刘迎九
雷 铭,刘岳林,谢水波,2*,葛玉杰,刘迎九
(1 南华大学 土木工程学院,湖南 衡阳 421001;2 南华大学污染控制与资源化技术湖南省重点实验室,湖南 衡阳 421001;3 湖南工业大学 土木工程学院,湖南 株洲 412007)

众多的半导体之中,ZnO是一种非常适合用于改性g-C3N4的材料。ZnO作为一种n型半导体材料,制备成本低廉、安全无毒害,且其导带(CB)电位高于g-C3N4,因此在复合后位于g-C3N4导带上的电子会迁移到ZnO的导带上,从而有效改善g-C3N4电子-空穴对复合率过高的缺点。Lv等[13]采用化学沉积法将ZnO粒子负载在g-C3N4上,得到的ZnO/g-C3N4表现出较好的光催化活性。He等[14]采用浸渍复合法合成了ZnO/g-C3N4复合光催化剂,能够高效光催化还原CO2。本工作以ZnO和三聚氰胺为原料,采用热聚合法制备ZnO/g-C3N4复合材料。用SEM,XPS,XRD,PL,UV-Vis等表征手段对材料的表面形貌、元素组成、光催化性能等进行测试,探讨其对溶液中U(Ⅵ)的还原性能,为其在含铀废水处理领域的实际应用提供理论基础。
1 实验
1.1 试剂与仪器
ZnO,天津市天力试剂有限公司,分析纯;三聚氰胺,天津市科密欧化学试剂有限公司,分析纯;模拟含铀废水采用GBW04201 U3O8标准品配制而成;实验室用水均为蒸馏水;光催化反应仪GG-GHX-V,上海桂戈实业有限公司。
1.2 复合型光催化剂的制备
1.2.1 g-C3N4的制备
将5 g三聚氰胺置于100 mL坩埚中,在马弗炉中以550 ℃煅烧2 h,待其冷却至室温后充分研磨,得到的淡黄色固体粉末即为g-C3N4。
1.2.2 ZnO/g-C3N4的制备
将5 g三聚氰胺与0.5 g ZnO加入80 mL蒸馏水中,剧烈搅拌30 min后蒸干。将得到的白色粉末充分研磨,置于100 mL坩埚中,在马弗炉中550 ℃下煅烧2 h后取出,待其冷却至室温后充分研磨,得到的淡黄色固体粉末即为ZnO与g-C3N4的质量比为1∶10的ZnO/g-C3N4复合材料(ZnO/g-C3N4(0.1))。依此方法通过调整ZnO含量分别获得1∶20,1∶5不同配比的复合材料ZnO/g-C3N4(0.05),ZnO/g-C3N4(0.2)。
1.3 光催化还原U(Ⅵ)的实验
整个实验在光催化反应仪中进行,用500 W未加滤光片的氙灯作为光源来模拟太阳光。光催化反应仪中配有石英冷阱内冷却循环水系统,用于吸收氙灯散发的热量,保证反应在恒温条件下进行。底部配有磁力搅拌器,可以使光催化剂悬浮在溶液中,与溶液中的U(Ⅵ)充分接触。在试管中依次加入10 mg/L的铀溶液20 mL、0.5 g/L的光催化剂和2 mL甲醇作为空穴掩蔽剂。将其置于反应仪中,先在黑暗条件下反应30 min,然后开灯反应30 min,反应全过程通入N2,使其在无氧条件下进行。反应完毕后取出试管中的溶液进行离心,收集溶液的上清液,用分光光度法测定溶液中U(Ⅵ)的剩余浓度。
1.4 反应后材料收集
将反应后的溶液进行离心,收集溶液中的材料后用去离子水洗涤3次,将其置于60 ℃的真空干燥箱中烘干至恒重,然后重复使用。
1.5 性能测试与表征
利用D/max-2400e X射线衍射仪(XRD)对样品物相组成进行分析,实验条件为Cu靶,扫描速率为4(°)·min-1;利用JSM-6701F型场发射扫描电子显微镜(SEM)对样品形貌进行观察;利用ESCALAB250电子光谱仪对样品进行XPS分析;利用Lambda850型双光束紫外-可见分光光度计(UV-Vis)分析产物的光吸收特性和禁带宽度。
2 结果与讨论
2.1 XRD分析
图1为g-C3N4,ZnO及ZnO/g-C3N4(0.1)的XRD谱图。从g-C3N4谱图中可以看出,在13.1°处出现的衍射峰代表g-C3N4的(001)面,表明g-C3N4内部三嗪环的存在。在27.4°处的衍射峰则代表材料中的共轭芳香化合物。ZnO中处于31.7°,34.3°,36.1°,47.4°,56.5°,62.8°,66.4°,68.0°和69.2°[15]处的衍射峰符合六方纤锌结构的ZnO衍射峰特征。以上特征峰均出现在复合材料ZnO/g-C3N4中,且复合材料中没有出现新的晶相,说明复合材料由g-C3N4和ZnO两种物质构成。
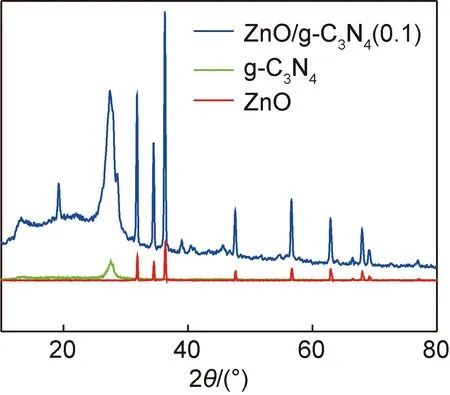
图1 ZnO,g-C3N4及ZnO/g-C3N4(0.1)的XRD谱图Fig.1 XRD patterns of ZnO,g-C3N4 and ZnO/g-C3N4(0.1)
2.2 SEM分析
图2为ZnO,g-C3N4及ZnO/g-C3N4(0.1)的扫描电镜图。由图2(a)可知,ZnO的表面结构为非常规则的六方体纳米棒状结构。图2(b)中g-C3N4呈无规则的块状结构,大小分布不均,表面存在大量孔隙,十分松散。复合后的ZnO/g-C3N4材料形貌(如图2(c))与纯g-C3N4相比,材料表面出现许多棒状结构。这可能是ZnO与g-C3N4经过高温煅烧后发生相互作用,前者成功嵌入g-C3N4中,说明两种材料不是简单的物理复合,而是形成了一种紧密的结构。

图2 ZnO(a),g-C3N4(b)及ZnO/g-C3N4(0.1)(c)的SEM图Fig.2 SEM images of ZnO(a),g-C3N4(b) and ZnO/g-C3N4(0.1)(c)
2.3 XPS分析


图3 ZnO/g-C3N4(0.1)的XPS谱图 (a)Zn2p;(b)O1s;(c)C1s;(d)N1sFig.3 XPS spectra of ZnO/g-C3N4 (0.1) (a)Zn2p;(b)O1s;(c)C1s;(d)N1s
2.4 UV-Vis分析
图4为ZnO,g-C3N4和ZnO/g-C3N4(0.1)样品的UV-Vis DRS谱图和带隙计算图。如图4(a)所示,与纯ZnO相比,复合材料的吸收边缘出现明显的红移,表现出更强的可见光吸收能力,在400~500 nm范围内有明显的吸收增强。利用Tauc-Plot法:(αhv)1/n=A(hv-Eg),作hv对应(αhv)1/n的谱图(图4(b))。其中α,h,v分别为半导体的吸收系数、普朗克常数和光子频率;A,n均为常数,当材料为直接半导体时,n=1/2,若为间接性半导体,则n=2;Eg为禁带宽度[16]。由于ZnO和g-C3N4均属于直接型半导体[17],所以n=1/2。通过图4(b)中的3条切线截距[18],求得ZnO,g-C3N4和ZnO/g-C3N4(0.1)的禁带宽度约为3.20,2.67 eV和2.30 eV。可以看出,复合材料的带隙能较单体材料有所降低,更容易被可见光所激发,从而增强对可见光的利用率,有效提高材料的光催化性能。
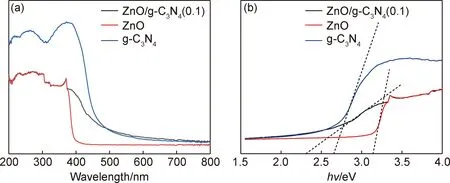
图4 ZnO,g-C3N4及ZnO/g-C3N4(0.1)的UV-Vis DRS谱图(a)和带隙计算图(b)Fig.4 UV-Vis DRS spectra(a) and estimated band gap(b) of ZnO,g-C3N4 and ZnO/g-C3N4(0.1)
2.5 PL光谱分析
光生电子-空穴对过高的复合率是影响大部分单一材料光催化性能的主要原因,本工作采用光致发光光谱(PL)来测定材料光生电子与空穴的分离能力。PL光谱的强度越高,则光生电子与空穴的复合率越高,光催化性能越差。在325 nm的激发波长下,ZnO,g-C3N4及ZnO/g-C3N4(0.1)的PL光谱如图5所示。显然,单纯的ZnO材料光电子对分离效率十分优秀。同时,复合材料的PL强度明显小于单纯的g-C3N4材料,介于g-C3N4与ZnO之间,说明ZnO与g-C3N4成功复合形成异质结,有效降低复合材料光生电子与空穴的复合率,提高电子传递的效率,显著提升材料的光催化性能。

图5 ZnO,g-C3N4及ZnO/g-C3N4(0.1)的PL谱图Fig.5 PL spectra of ZnO,g-C3N4 and ZnO/g-C3N4(0.1)
2.6 光催化还原U(Ⅵ)的性能研究
2.6.1 光照下不同材料对U(Ⅵ)的还原效果
本工作中U(Ⅵ)溶液初始浓度为10 mg/L,光催化剂的投加量为0.5 g/L,pH=5。图6为不同光催化剂在整个反应过程中去除U(Ⅵ)的效果及在模拟伪一级动力学下的光降解反应速率。由图6(a)可知,纯g-C3N4的去除率仅为32%。而在与ZnO复合后,材料对U(Ⅵ)的去除率得到明显提高,其中,ZnO/g-C3N4(0.1)去除率最高,达到97%。单纯的ZnO在反应中也显示出相当高的去除率,达到98%。
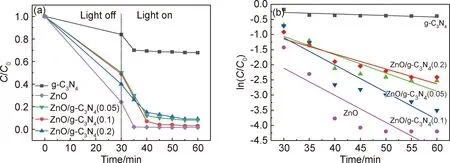
图6 不同光催化剂去除U(Ⅵ)的效果(a)及反应速率常数(b)Fig.6 Removal performance of U(Ⅵ) of different photocatalysts(a) and the reaction rate constant(b)
由于电子-空穴对复合率较高,纯g-C3N4材料对U(Ⅵ)的还原效果非常不理想。材料成功复合后,随着光电子对分离效率的提升,去除率也得到显著提高。然而,随着复合材料中ZnO含量的进一步增加,U(Ⅵ)的去除率反而降低,这可能是因为过量的ZnO引起了团聚,导致材料表面活性位点减少。实验同时显示,单纯ZnO对U(Ⅵ)的去除率十分优秀。根据暗反应结果,这可能是因为ZnO本身对U(Ⅵ)有较高的吸附率[19],可以通过物理吸附去除溶液中的U(Ⅵ)。
根据图6(a)作出不同光催化剂还原U(Ⅵ)的模拟伪一级动力学模型(图6(b)),结果显示,在复合材料中ZnO/g-C3N4(0.1)的反应速率最高,反应速率常数k=0.09 min-1,是纯g-C3N4反应速率常数(k=0.005 min-1)的18倍。
表1列举了复合型光催化剂的一些参数,其中大部分材料采用氙灯(Xe)作为光源来模拟太阳光,少部分使用金卤灯(MHI)、汞灯(Hg)。光催化性能方面,ZnO/g-C3N4的禁带宽度小于S-g-C3N4[20]和锐钛矿型TiO2[21],但大于CuO/BiFeO3[5],Sn-In2S3[22],Bi2O3-Bi2WO6[23]。更小的禁带宽度代表更低的激发阈值,意味着材料更容易被激发,光谱吸收范围更广。同时ZnO/g-C3N4的反应速率较为优秀,高于Bi2O3-Bi2WO6,锐钛矿型TiO2,Sn-In2S3和CuO/BiFeO3,与S-g-C3N4相同。这可能是由于,ZnO与g-C3N4复合后提高了材料对U(Ⅵ)的吸附能力,使被还原的对象能够更好与材料表面的活性位点相结合,提高光催化反应速率。目前本材料对于高浓度含铀废水的还原还缺乏相关研究,去除效果尚不明确。综合来看,对中低浓度的铀溶液来说,ZnO/g-C3N4有着优秀的光催化性能,能够很好地从溶液中还原U(Ⅵ)。
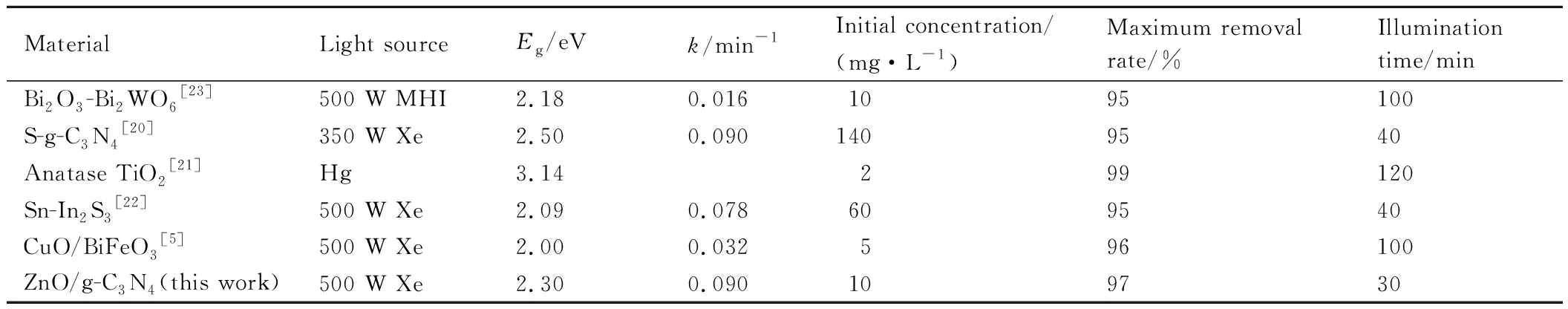
表1 不同光催化剂还原U(Ⅵ)比较Table 1 Comparison of different photocatalysts on U(Ⅵ) reduction
2.6.2 溶液初始pH值对光催化还原U(Ⅵ)的影响
溶液的初始pH值会影响铀酰离子的存在形态,对光催化还原的效果有着很显著的影响。图7为不同pH值下ZnO/g-C3N4(0.1)去除U(Ⅵ)的效果。本工作中U(Ⅵ)的初始浓度为10 mg/L,催化剂投加量为0.5 g/L,溶液pH值分别为3,4,5,6,7。随着pH值从3上升到5,光催化还原U(Ⅵ)的效果得到明显提升,在pH=5时效果最佳,去除率达到97%。而随着pH值的继续上升,去除率反而下降,当pH=7时,去除率下降到51.5%。

图7 不同pH值下ZnO/g-C3N4(0.1)去除U(Ⅵ)的效果Fig.7 Removal performance of U(Ⅵ) by ZnO/g-C3N4(0.1) at different pH values
当溶液中pH≤3时,铀酰离子主要以UO22+的形式存在,在强酸性溶液中,高浓度的H+会与UO22+竞争催化剂表面的活性位点,这直接影响催化剂还原的效率。而在pH≥7的溶液中,铀酰离子会逐渐水解成各种阴离子铀基络合离子,甚至形成沉淀,同样会影响催化剂对U(Ⅵ)的还原。综上所述,催化剂的最佳值为pH=5。
2.6.3 光催化还原U(Ⅵ)的机理探究

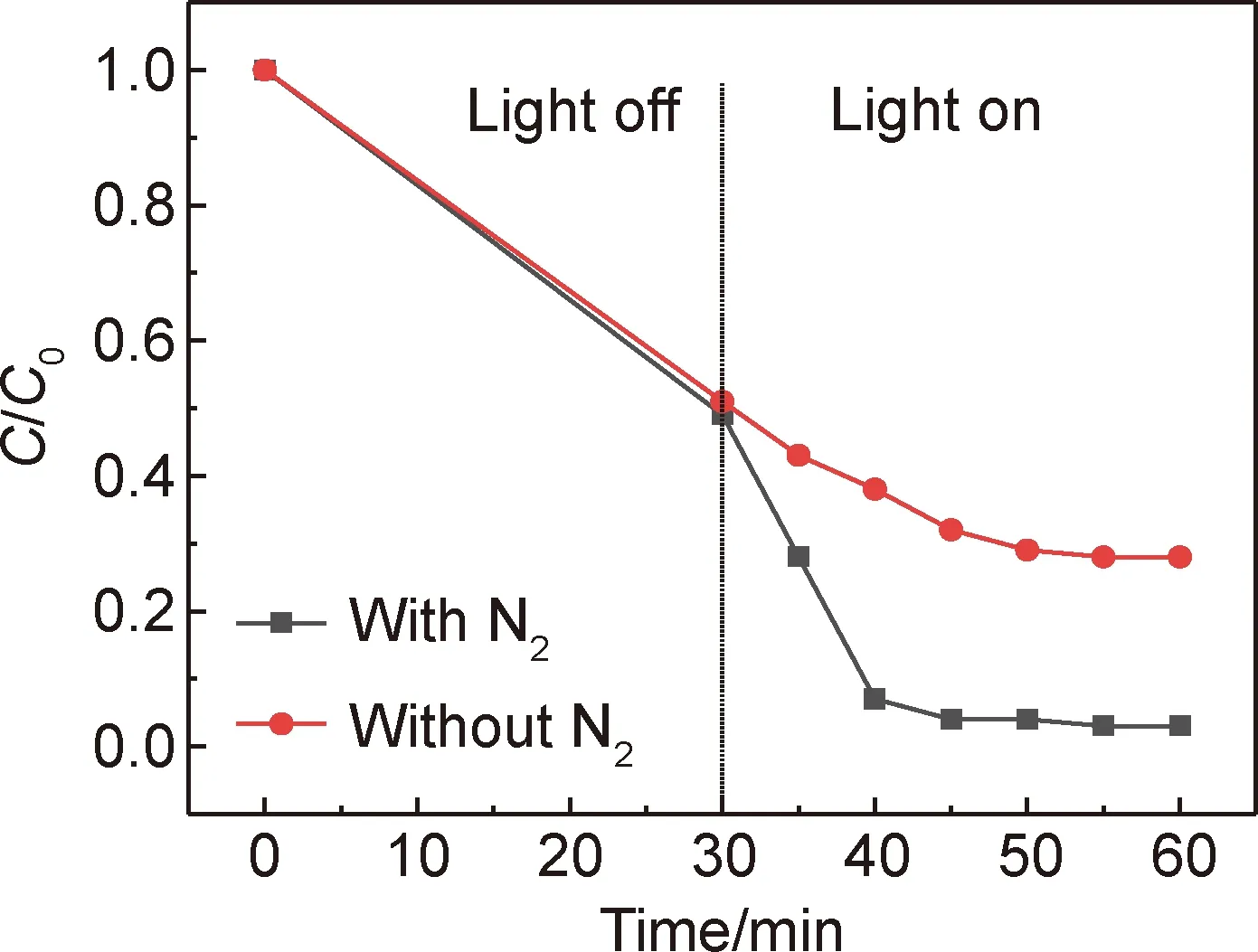
图8 N2对ZnO/g-C3N4(0.1)光催化还原U(Ⅵ)效果的影响Fig.8 Effect of N2 on the photocatalytic reduction performance of U(Ⅵ) over the ZnO/g-C3N4(0.1)
对光催化反应后的ZnO/g-C3N4(0.1)材料表面的U4f进行XPS表征测试,结果如图9所示。U4f中结合能为381.9 eV和392.7 eV对应的是U(Ⅵ),结合能为380.9 eV和391.8 eV的特征峰则代表U(Ⅳ)。表明光催化反应成功将部分U(Ⅵ)还原为U(Ⅳ),两者共存于催化剂的表面。
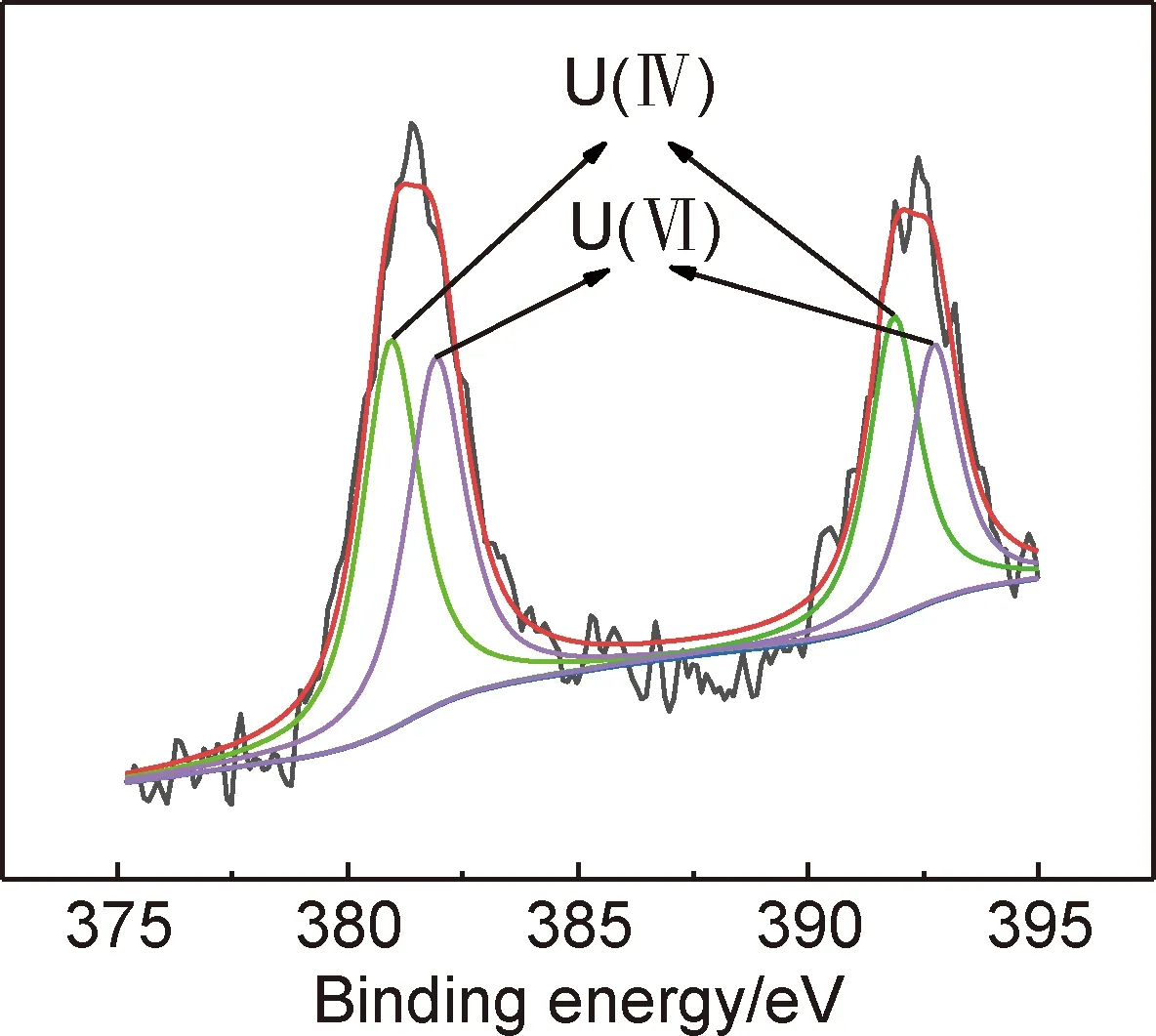
图9 ZnO/g-C3N4(0.1)光催化还原U(Ⅵ)后表面的U4f XPS谱图Fig.9 XPS spectra of U4f for the surface of ZnO/g-C3N4(0.1) after U(Ⅵ) photoreduction experiment
基于上述研究,对光催化还原U(Ⅵ)的机理进行推测,如图10所示。当复合材料被大于其带隙能的可见光照射时,被激发产生光生电子e-和空穴h+,光生电子由价带(VB)迁移到导带(CB)。而g-C3N4导带电势更负于ZnO的导带电势,因此位于g-C3N4导带上的e-会迁移到ZnO的导带上,通过这一过程能够有效降低光催化剂电子-空穴对的复合率,提高光催化性能。ZnO价带上的空穴具有一定的氧化能力,能与溶液中的水反应生成羟基自由基(OH·)。而导带上的e-则将溶液中的U(Ⅵ)还原成U(Ⅳ)。g-C3N4价带上的空穴由于比羟基自由基的电位更负,不会与水发生氧化反应,而会将作为空穴掩蔽剂的甲醇氧化为CO2和H2O。

图10 ZnO/g-C3N4在光照下还原U(Ⅵ)的机理示意图Fig.10 Photoreduction mechanism diagram of U(Ⅵ) over ZnO/g-C3N4 under solar light irradiation
2.6.4 光催化剂的稳定性和再利用能力
评判催化剂的一个重要标准便是其稳定性与可重复利用性。本实验将反应后的催化剂重新收集、洗涤、烘干并重复利用,如图11所示。经过4次重复利用后,光催化还原的效率仍能达到83%左右,说明催化剂具有良好的稳定性与循环利用能力。
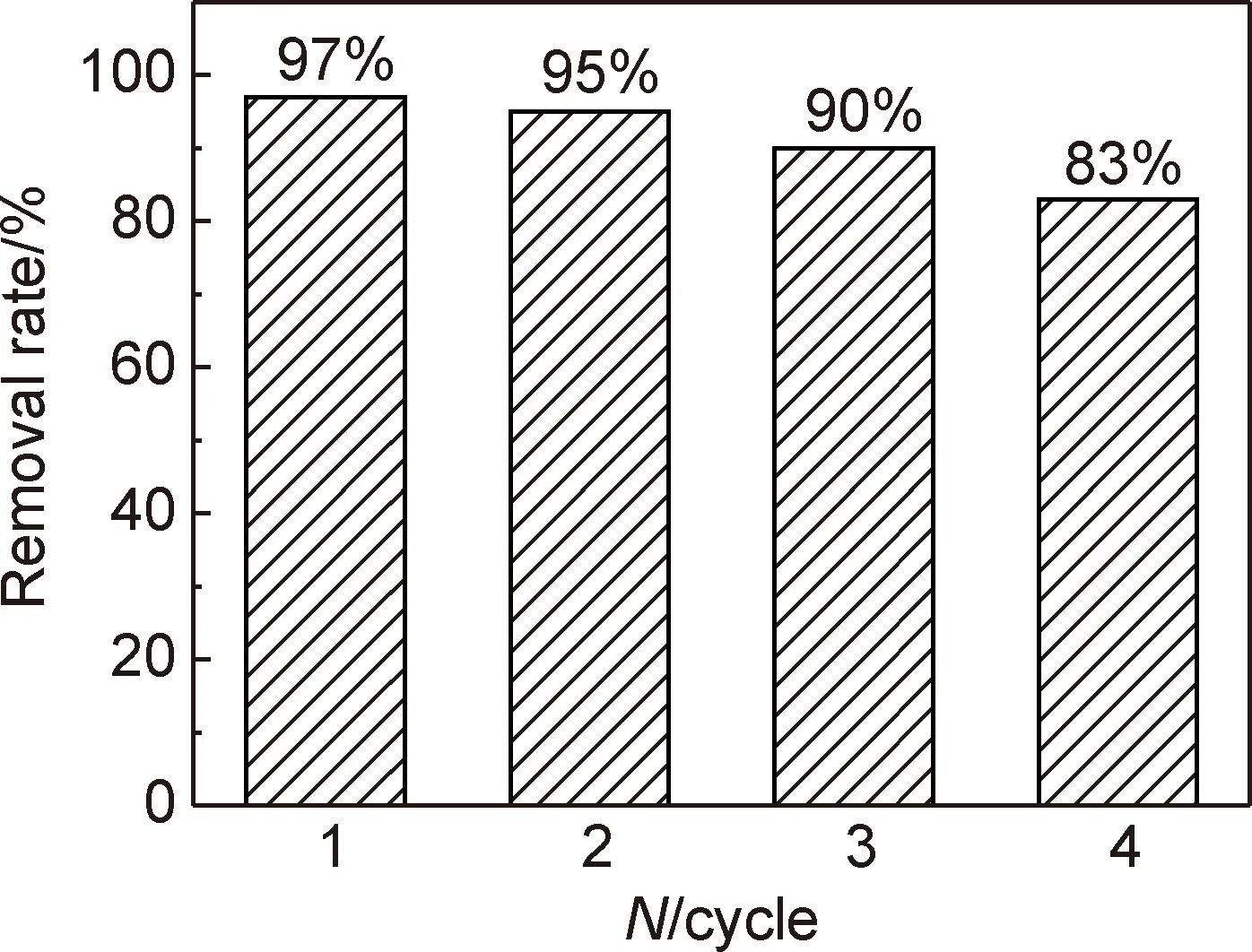
图11 ZnO/g-C3N4(0.1)光催化还原U(Ⅵ)的循环实验Fig.11 Cycle experiments of the photoreduction of U(Ⅵ) over ZnO/g-C3N4(0.1)
3 结论
(1)复合后纳米棒状的ZnO可以嵌入g-C3N4,结合紧密。通过在g-C3N4上负载适量的ZnO,能有效抑制光生电子-空穴对的复合,提高可见光响应能力,增强光催化活性。
(2)复合型光催化剂对U(Ⅵ)表现出很高的光催化活性。当pH=5、U(Ⅵ)溶液初始浓度为10 mg/L时,经30 min光照后ZnO/g-C3N4对U(Ⅵ)的去除率达到97%。ZnO/g-C3N4(0.1)具有良好的重复利用性,循环利用4次后仍对溶液中的U(Ⅵ)有83%的去除率。
(3)ZnO/g-C3N4复合型光催化剂能够将U(Ⅵ)还原为U(Ⅳ),主要是光生电子e-的作用。两种材料的复合有利于电子的快速传导,增强电子-空穴对的分离效率,提高对U(Ⅵ)的还原性能。
