新冠疫苗接种后罹患成人Blaschko皮炎一例
2022-08-20林维茹陈声利刘国艳
左 墨 林维茹 陈声利 刘国艳
1山东第一医科大学附属皮肤病医院(山东省皮肤病医院),山东省皮肤病性病防治研究所,山东济南,250022;2潍坊医学院,山东潍坊,261000
成人Blaschko皮炎亦称为获得性Blaschko皮炎或复发性自愈性Blaschko皮炎是一种获得性、自限性的炎症性皮肤病,以沿着单侧Blaschko线分布皮疹为特点。很少见于成人,皮疹主要见于四肢,偶尔也见于躯干或头皮。我科诊治1例由新冠疫苗引发的药源性成人Blaschko皮炎患者,现报道如下。
临床资料患者,女,30岁。因“右腹部及右下肢多发丘疹45天”来诊。45天前患者反复感冒,后始于右侧下肢出现散在丘疹,瘙痒明显,后皮疹逐渐增多呈线状,30天前腹部右侧出现丘疹,逐渐增多,呈带状分布,未予治疗。追问病史,患者发病前1个月曾注射新冠疫苗第一针(发病前30天)及第二针(发病前15天)。患者发病以来无发热,既往无高血压、糖尿病及心脏病等慢性病史,无银屑病史。体格检查:系统查体未见异常。皮肤科检查:右侧腹部可见米粒大红色丘疹,群集带状分布。右下肢可见米粒至黄豆大炎性丘疹,呈线状分布(图1)。
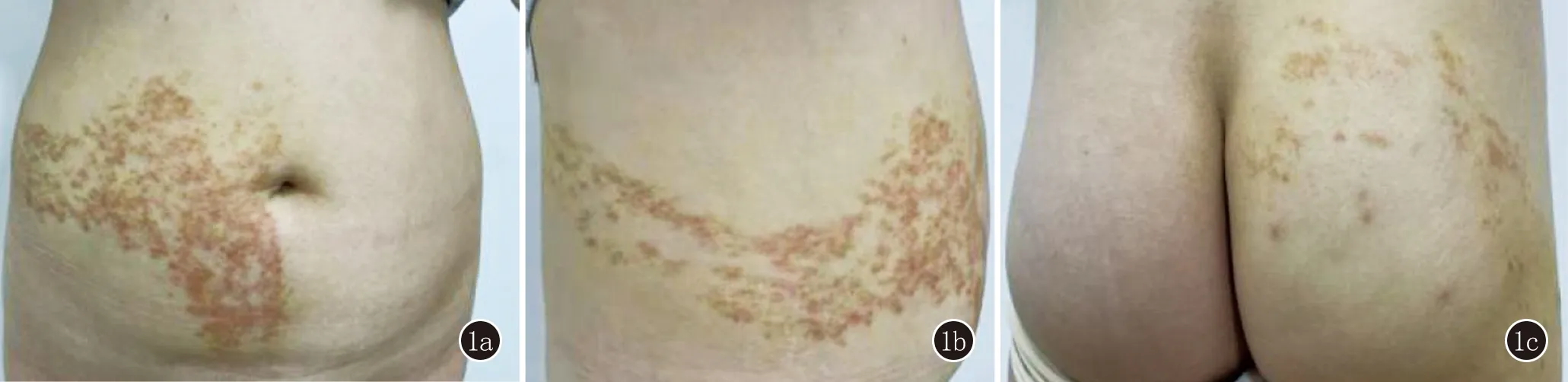
图1 1a、1b:右侧腹部可见米粒大红色丘疹,群集带状分布;1c:右下肢可见米粒至黄豆大炎性丘疹,呈线状分布
实验室检查:血常规及肝肾功未见明显异常。皮肤镜(图2):淡红色背景下可见点状、小球状血管结构,散在黄白色鳞屑,未见明显白色网纹样结构及色素沉着。
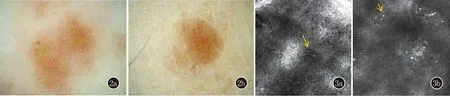
图2 淡红色背景下可见点状、小球状血管结构,散在黄白色鳞屑,未见明显白色网纹样结构及色素沉着。淡红色背景下可见点状、小球状血管结构,散在黄白色鳞屑,未见明显白色网纹样结构及色素沉着 图3 皮损处皮损区角化过度,表皮增厚,棘层水肿,基底层局部液化变性,真皮浅层单一核细胞及嗜色素细胞浸润(黄色箭头)
皮肤CT(图3):(腹部、下肢)皮损处角化过度,表皮增厚,棘层水肿,灶性基底层局部液化变性,真皮浅层单一核细胞及嗜色素细胞浸润。
组织病理示:(腹部)表皮角化过度,角化不全,棘层轻度增厚,细胞间水肿,真皮浅层淋巴细胞和嗜酸粒细胞浸润(图4)。
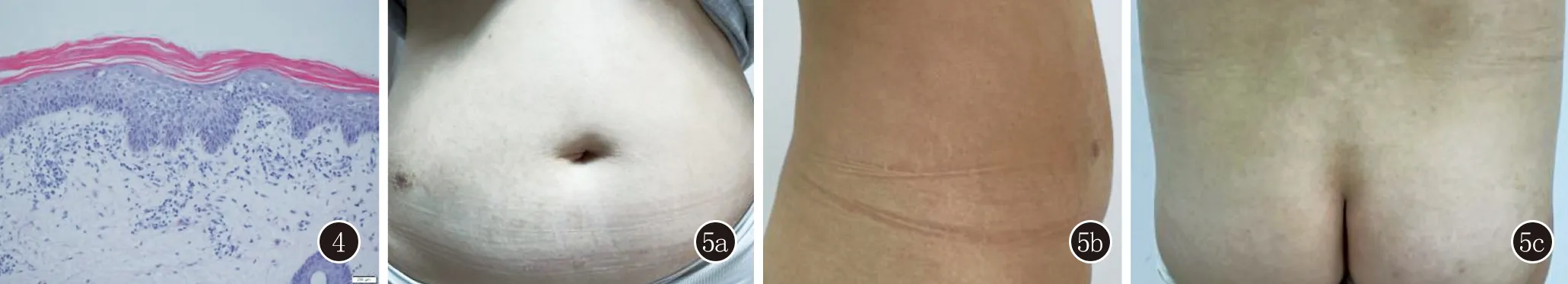
图4 表皮角化过度,角化不全,棘层轻度增厚,局部基底液化变性,细胞间水肿,真皮浅层淋巴细胞和嗜酸粒细胞浸润(HE,×200) 图5 腹部及下肢未见明显皮疹
诊断:成人Blaschko皮炎。治疗:给予口服荆蒡颗粒10 g/d(主要成分为荆芥、防风、牛蒡子等)、雷公藤多苷片60 mg/d,外用硅油乳膏、复方醋酸曲安奈德软膏后,患者皮疹较前缓解,21天后复诊,皮疹消退(图5),未见其他不适。
讨论成人Blaschko皮炎是一种少见的皮肤病,一般起病突然,多发生于成年人[1]。皮肤组织病理以海绵水肿性皮炎为特点,可见界限皮炎改变。成人Blaschko皮炎由1990年Grosshans和Marot[2]首次报道并命名,其特征性表现为沿着单侧Blaschko线分布的瘙痒性红斑、丘疹和丘疱疹,多线型且条带较宽。Blaschko线被认为是由胚胎发育过程中皮肤细胞的迁移所决定的,反映了正常细胞和突变细胞间的界限,这被称为皮肤的“镶嵌现象”。遵循Blaschko线分布的疾病的分布特点被认为是由遗传嵌合体引起的,这是由X连锁疾病的裂解、零星条件下的合子后体细胞突变和配子半染色单体突变引起的[3]。成人Blaschko皮炎发病机制尚不明确,目前认为可能是机体在一些外界刺激下,编码皮肤抗原决定簇的基因发生嵌合并克隆表达,导致免疫耐受丧失,引发了沿Blaschko线分布的 T 细胞阶段的皮肤炎症反应,从而导致沿Blaschko线分布的皮炎。本病在应激及精神紧张等诱因可使皮疹加重,有自愈倾向,多数能自行消退,但较易复发,目前疗效比较肯定的是系统使用糖皮质激素。
Taieb等[4]曾提出线状苔藓与成人Blaschko皮炎为同一病谱的两种疾病。亦有学者认为线状苔藓与获得性Blaschko皮炎为同一种疾病,发生在成人者为获得性Blaschko皮炎,发生在儿童者为线状苔藓[3]。一些作者通过强调其不同的临床特征、组织病理学结果和自然病史来区分成人Blaschko皮炎和线状苔藓,组织学上,成人Blaschko皮炎的特征是主要海绵水肿样皮炎,而非苔藓样变。本例患者为成年女性,组织病理表现提示海绵水肿性皮炎改变,未见小汗腺等附属器受累,临床表现为丘疹性瘙痒性皮损、呈线状、带状分布,根据Grosshans标准[2],符合成人Blaschko皮炎诊断。
随着预防疾病的疫苗种类增多,接种范围增大,有关疫苗的皮肤反应的报道也逐渐增多。国内现有的新冠疫苗主要为灭活疫苗,2021年我国报道了1例由灭活新冠疫苗诱发的药物超敏反应综合征[5],其发病机制尚不明确。国外新冠疫苗主要为mRNA疫苗,现已报道数例因其引起的急性泛发性发疹性脓疱病、大疱性类天疱疮、史蒂文斯-约翰逊综合征等[6,7]。Ohsawa[8]认为,m-RNA疫苗(如辉瑞疫苗)接种后所引起的皮疹机制为:1)病毒蛋白可能在疫苗接种后的2天内表达;2)患者可能曾感染过冠状病毒(传统冠状病毒或新型冠状病毒),其病毒蛋白可能是与mRNA疫苗编码的冠状病毒发生交叉反应的抗原;3)mRNA疫苗引起的突发性免疫反应与SARS-CoV-2感染相似。同时Larson等[9]发现,接种新冠疫苗可能会恶化先前存在的皮肤病,例如扁平苔藓、单纯疱疹病毒感染的红斑、特应性皮炎、银屑病和荨麻疹血管炎,而大多数这些反应发生在接受mRNA辉瑞生物科技疫苗的患者中,目前与疫苗性质是否相关仍需进一步研究。国内外现均未见关于新冠疫苗引起的成人Blaschko皮炎的病例报道。作者于Pubmed数据库以“blaschkitis”及“adult blaschkitis”为关键词进行文献检索,共发现2篇与药物相关引起的成人Blaschko皮炎,分别为甲硝唑及赛妥珠单抗引起的病例[10,11]。现针对疫苗引起的Blaschko皮炎相关疾病发病机制已经被提出[12],在疫苗的作用下,角质形成细胞上的共享表位和疫苗中的病毒蛋白之间发生交叉反应。因此,这些沿着Blaschko线分布的异常的角质形成细胞发生改变,从而暂时打破了先前的免疫系统耐受性,并触发了细胞毒性T细胞的细胞介导的攻击。该病例为我们首次报道新冠疫苗注射后引起的成人Blaschko皮炎。本例患者于接种新冠疫苗30天后出现皮疹,且无其他明显诱因及病因,无其他既往疾病史,故考虑该患者的皮肤表现可能与新冠疫苗的注射相关。经过治疗后皮疹全部消退,目前仍在随访中。
