脊柱骨纤维性结构不良的外科治疗:一项单中心回顾性研究
2022-06-30徐启明徐海荣崔丽嘉李远单华超黄真马珂牛晓辉
徐启明,徐海荣,崔丽嘉,李远,单华超,黄真,马珂,牛晓辉
骨纤维性结构不良(fibrous dysplasia),又称骨纤维异常增殖症,是由于骨形成机制异常导致的正常骨结构被不成熟骨组织及纤维结缔组织替代[1,2],导致疼痛、骨折、功能障碍及骨骼畸形等。骨纤维性结构不良约占所有原发性骨肿瘤的7%[3],主要累及肋骨、股骨及胫骨等部位。根据发病部位的数量,该病分为单骨型骨纤维性结构不良和多骨型骨纤维性结构不良,其中单骨型骨纤维性结构不良约占所有报道病例的70%。多骨型骨纤维性结构不良,如伴有皮肤咖啡牛奶斑及内分泌异常(常表现为性早熟),则称之为麦丘恩-奥尔布赖特综合征(McCune-Albright syndrome)。该综合征的病因是GNAS基因的体细胞突变,不具有遗传性[4]。骨纤维性结构不良是一种难以治愈的疾病,以药物治疗为主[4,5]。对于出现骨折及骨骼畸形的病例,可进行手术治疗[6]。
脊柱骨纤维性结构不良仅占所有骨纤维性结构不良病例的2.0%~4.7%[7],相关报道仅有数十例[8-18],因此关于脊柱骨纤维性结构不良的相关治疗策略尚存争议。脊柱骨纤维性结构不良邻近脊髓及神经根,局部膨胀性生长容易累及神经,如发生局部骨折容易导致脊柱不稳定或畸形,均增加了该疾病的治疗难度。
脊柱骨纤维性结构不良的治疗方案包括单纯活检明确病理诊断并定期复查[15]、手术刮除或切除[17]、椎体成形术[12,14]及药物治疗。本研究回顾性分析1999年3月至2020年11月就诊于北京积水潭医院的脊柱骨纤维性结构不良患者的病历资料,旨在探讨脊柱骨纤维性结构不良的诊断要点及治疗策略的选择,为不同病情的脊柱骨纤维性结构不良患者制定个性化的治疗方案,以减少对脊柱稳定性的破坏,降低复发率。
1 资料与方法
病例纳入标准:①脊柱增强CT显示典型的溶骨性病变伴膨胀性生长,边缘硬化区域,伴或不伴病理性骨折,②活检和/或手术标本病理诊断证实为骨纤维性结构不良。排除标准:术后失随访及随访时间不足1年的患者。
本研究回顾分析1999年3月至2020年11月就诊于北京积水潭医院的脊柱骨纤维性结构不良患者的病历资料。详细查看患者病历、手术记录、影像学及病理报告,使用Frankel评分系统评估神经功能情况,记录患者性别、年龄、发病时间、影像学特征、临床症状、肿瘤的位置、病理诊断、手术方式,并采用电话随访或门诊随访形式,收集患者术后症状缓解情况及病灶有无复发。本研究获北京积水潭医院伦理委员会批准,征得患者知情同意,并签署知情同意书。
术前穿刺活检术均在CT引导下或术中ISO-C计算机辅助导航定位下进行,使用直径为9G的穿刺活检针,到达病灶中央及边缘反复切刮,并使用注射针筒负压抽吸标本。
手术治疗脊柱骨纤维性结构不良的适应证包括:持续性疼痛、神经症状、病理性骨折、脊柱不稳。采取的手术方式包括病灶刮除术、切除术、经皮椎体成形术;固定方式包括钢丝固定、椎弓根螺钉固定、椎体钢板螺钉固定;重建方式包括自体植骨融合术、骨水泥填充术。
2 结果
本研究共纳入7例脊柱骨纤维性结构不良患者,其中男4 例,女3 例,年龄21~46 岁,平均32.3 岁(表1)。以单纯脊柱区域疼痛症状发病者4例,以脊柱区域疼痛合并肢体神经症状发病者3例(Frankle分级均为D 级)。多骨型骨纤维性结构不良3 例,单骨型骨纤维性结构不良4 例。在脊柱骨纤维性结构不良病变中,累及颈椎者2例,均无病理性骨折;累及胸椎者2 例,均发生病理性骨折;累及腰椎者3 例,2 例发生病理性骨折。2 例伴发脊柱外骨纤维性结构不良的病例,均累及肋骨,其中1 例发生病理性骨折。共2例患者伴有脊柱畸形,其中1例为病变位于腰椎的脊柱侧凸,1例为病变位于颈椎的斜颈畸形。

表1 本研究7例患者的人口学特征、手术信息及随访情况
4 例接受术前穿刺活检术的患者中,2 例明确病理诊断为骨纤维性结构不良,1例部分符合骨纤维性结构不良的病理特征但未明确诊断,1例未观察到肿瘤细胞。所有7 例患者均接受手术治疗:病灶切除术、病灶刮除术各3例,经皮椎体成形术1例;固定方式:钢丝固定术、椎弓根螺钉固定术、椎体接骨板螺钉固定术各1例;重建方式:自体骨植骨融合术、骨水泥填充术各2例。
所有患者在术后均获得疼痛症状及肢体神经症状的缓解,无手术并发症,术后病理诊断均明确为骨纤维性结构不良,其中有1例患者合并动脉瘤样骨囊肿。脊柱侧凸及斜颈畸形未获得显著改善。平均随访时间为13.3年(6~22年)。
3 讨论
近20 年来,文献报道的脊柱骨纤维性结构不良仅有二十余例(表2)。既往文献中脊柱单骨型及多骨型骨纤维性结构不良在男女群体中的发病率疾病一致,且多好发于30~40 岁人群[17]。其中,脊柱多骨型骨纤维性结构不良具有更高的病理骨折、脊柱畸形及神经功能障碍的风险,而脊柱单骨型骨纤维发育不良出现上述并发症的风险较低,多数仅呈现颈肩或腰背部疼痛[18]。本研究所纳入病例平均起病年龄21~46 岁,男女比例相当,主要症状为脊柱区域疼痛,部分合并肢体神经症状,与文献报道一致。
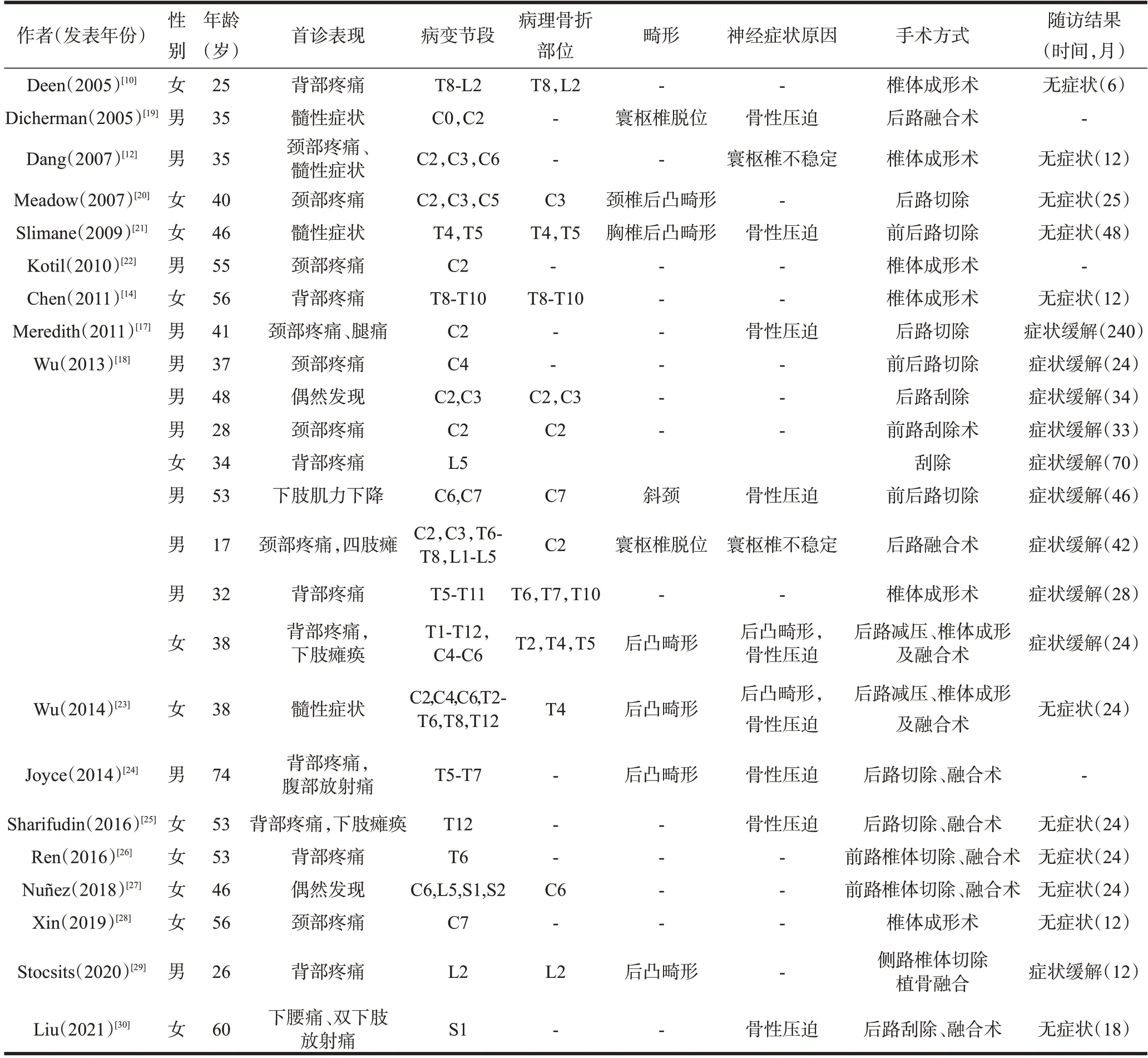
表2 近20年文献报道中脊柱骨纤维性结构不良患者的详细信息
骨纤维性结构不良在X 线片上可表现为平滑而均质的骨病变,可呈透亮影,也可呈硬化影[31]。但由于脊柱的解剖结构复杂,上述特征在脊柱骨纤维性结构不良中并不典型。在本研究的脊柱骨纤维性结构不良患者中,X 线片除显示椎体压缩性骨折外,无明确提示意义。骨纤维性结构不良在CT 上表现为磨玻璃样不透明影或均质的硬化影,可伴边界清晰完好的膨胀性生长及边缘硬化区域,伴或不伴病理性骨折[32,33]。在本研究中,脊柱骨纤维性结构不良患者在CT 上均表现为溶骨性病变,或伴有病理性骨折。MRI在骨纤维性结构不良与其他骨肿瘤的鉴别诊断方面并无优势,这是因为不同骨纤维性结构不良的MRI 表现存在较大变异。因此,对于脊柱骨纤维性结构不良,我们更推荐用CT判断病变性质及范围。骨纤维性结构不良在全身骨显像上呈现骨代谢活跃病灶,如病例6、7的全身骨显像提示患者同时具有脊柱及肋骨的异常浓聚,因此全身骨显像对判断单骨型或多骨型骨纤维性结构不良有重要意义。
骨纤维性结构不良的病理结构显示为大片的纤维基质及散在分布的未成熟骨小梁,其外形呈不规则弯曲状[34]。其外周无成骨细胞带,需和牙骨质骨化性纤维瘤鉴别;在10%的病例中有软骨岛形成,需和软骨肉瘤相鉴别。骨纤维性结构不良的影像学表现和其病理结构密切相关[35]。如果病灶中纤维基质占主要成分,则影像学表现为透亮影;如病灶中骨小梁占主要成分,则影像学表现为致密影。本研究纳入病例的病变在CT上表现以溶骨性病变为主,可能与病理以纤维基质占主要成分相关。
治疗前的活检手术对脊柱骨纤维性结构不良的确诊至关重要。在本组病例中,病例1、2因就诊时间久远,当时未行穿刺活检;病例7 因病变累及右第六肋导致病理性骨折,肋骨切除术后已获得骨纤维性结构不良病理诊断,在椎体成形术的同时进行了脊柱穿刺活检术;其余4 例病例均在术前采取CT 引导下的经皮穿刺活检术。以往文献报道该方法对于脊柱骨纤维性结构不良的诊断具有较高的安全性及确诊率[36,37]。如果穿刺活检标本可见纤维基质和骨小梁等典型成分,则可诊断为骨纤维性结构不良病变[36]。然而本组病例的活检病理确诊率并不理想,可能因为每个活检术者对病灶的结构及位置理解程度不一样,未必能够穿刺到上述全部的典型病变组织。如病例6中,活检病理仅见正常的骨髓组织。因此建议在脊柱骨纤维性结构不良穿刺活检前,需做精细的术前设计,才可能穿刺到典型的病变组织。此外,有报道认为穿刺针的粗细可以影响确诊率,较粗的穿刺针比较细的穿刺针更容易获取足量的病变标本,进而提高确诊率[18]。然而我们认为选择更粗的穿刺针,在提高确诊率的同时,是否存在潜在骨折及神经损伤的风险,尚需更深入的研究。
本研究的病例7,T12 椎体术后病理诊断为骨纤维性结构不良合并动脉瘤样骨囊肿。骨纤维性结构不良合并动脉瘤样骨囊肿是极为罕见的疾病,既往共有三十余例报道,病灶分布于颅骨、颌面骨、肋骨、髂骨、股骨及桡骨等部位[38]。Lomasney 等[39]在2003年首次报道了脊柱骨纤维性结构不良合并动脉瘤样骨囊肿,此后无相关报道。骨纤维性结构不良合并动脉瘤样骨囊肿的发病机制有待进一步研究。
对于脊柱骨纤维性结构不良患者,如出现神经症状、病理性骨折合并脊柱不稳定或脊柱畸形者,我们推荐手术治疗。脊柱骨纤维性结构不良的手术治疗方案包括单纯活检明确病理诊断并定期随诊[15],手术刮除或切除术[17]、椎体成形术[12,14]。其中,如需行多节段病灶切除、前方椎体切除或椎间隙切除范围较大者,则可能影响术后脊柱稳定性,我们推荐病灶切除或刮除后,使用前路椎体钢板或后路椎弓根螺钉内固定手术,并使用植骨材料重建骨缺损(病例1~3)。尽管有些学者提倡彻底清除病灶以防止复发及恶变[9],然而彻底清除病灶也伴随更大的神经损伤风险,且有些多骨型病灶无法切除。如病例1中的病灶范围过大(图1),已累及椎板及椎体,引起颈椎不稳、脊髓压迫,导致神经症状,因此该病例的手术目的是切除脊髓后方病灶,解除脊髓压迫,植骨融合维持脊柱稳定性。对于前方病灶,由于病变范围广、手术风险大,未予以完全切除,术后多年随访病灶无进展,症状无复发。此外,对于脊柱附件病灶切除或刮除者,及椎体小范围病灶刮除对脊柱稳定性影响较小者,则可选择单纯病灶切除或刮除术,并根据实际情况判断是否选用骨水泥重建骨缺损(病例4~6)。
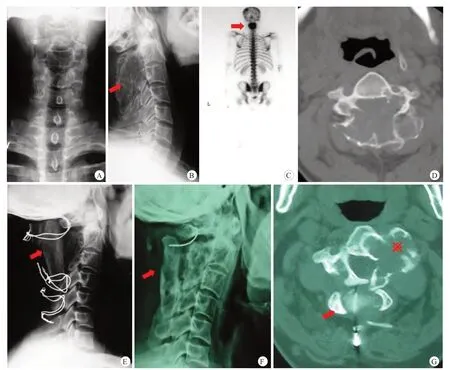
图1 病例1,男,40岁,因C2-C3骨纤维性结构不良行后路肿瘤切除、椎板减压、自体骨植骨融合术
对于单纯的椎体压缩骨折病例,我们尝试使用椎体成形骨水泥填充术并得到良好疗效(病例7,图2)。在既往文献报道中,有数例脊柱骨纤维性结构不良患者接受椎体成形术[10,12,14,18,22,28],这些患者均获得了良好的疗效,且无骨水泥相关并发症的记录。随访显示疼痛症状缓解,脊柱畸形得到较好的控制。这是因为骨水泥可以提供坚强的支撑作用,并能显著缓解疼痛。此外,骨纤维性结构不良病灶具有一定的溶骨特性,而骨水泥比植骨材料能更好的阻止骨吸收及骨溶解[17]。因此,对于单纯椎体压缩骨折的骨纤维性结构不良患者,我们认为在充分评估术前CT 明确椎体后侧皮质完好,无骨水泥渗漏风险的前提下,可谨慎选择经皮椎体成形术。然而,我们不推荐过度追求使用球囊扩张恢复椎体高度,因为过度撑开可能导致病灶周围的硬化带缺损,从而引起骨水泥泄漏。

图2 病例7,女,35岁,因T12-L3骨纤维性结构不良行经皮T12穿刺活检、椎体成形术
对于无神经症状、无病理性骨折或脊柱不稳定的脊柱骨纤维性结构不良患者,在明确诊断的前提下可接受药物治疗[4]。双膦酸盐被推荐运用于VAS疼痛评分大于3分的骨纤维性结构不良患者[4]。该类药物对骨痛有显著缓解作用,但影像学改善及长期效果并不明确[40-42]。地舒单抗是一种可以和位于破骨细胞及其前体细胞表面的RANK配体结合的单克隆抗体,可以抑制破骨细胞形成、功能及存活周期,从而抑制骨破坏及骨丢失[43]。近年来,地舒单抗在控制骨纤维性结构不良引起的骨痛及骨膨胀性病变方面获得成功[5],该药物最初被运用于骨巨细胞瘤的治疗,而骨纤维性结构不良周围的骨膨胀性病变被认为和破骨细胞活性增高有关,因此也被用于骨纤维性结构不良的治疗。然而关于该药物的长期疗效及副作用,仍缺少大宗、长期病例随访研究。
本研究对7 例脊柱骨纤维性结构不良患者的临床特征、手术方式、病理及术后转归进行了详细分析。本研究随访时间长,病例资料齐全,针对脊柱骨纤维性结构不良的影像学特征、术前活检、手术方式及骨重建方式等提出了经验总结。
本研究的不足之处是病例数量较少。脊柱骨纤维性结构不良为罕见的脊柱肿瘤,我们试图通过文献回顾的方式,分析其疾病特点及治疗方案的利弊,以弥补本研究的不足。后续仍需积累更多的病例进行深入研究。
4 结论
脊柱骨纤维性结构不良具有多样的临床表现。对于出现病理性骨折、脊柱不稳或神经症状的患者,建议手术治疗。根据病情为每个患者提供个性化的手术方案,有助于缓解疼痛、解除神经压迫、维持脊柱稳定性、重建骨性结构,并降低术后复发,增加患者获益。
【利益冲突】所有作者均声明不存在利益冲突
