β-FeOOH改性蒙脱土复合过氧化氢对罗丹明B的降解
2022-05-18陈修栋张义焕张浩东盛冬河吴嘉伟刘金杭占昌朝
陈修栋,张义焕,张浩东,盛冬河,吴嘉伟,刘金杭,严 平,占昌朝
(1.九江学院化学化工学院,江西九江 332005;2.江西省生态化工工程技术研究中心)
水资源的污染是一个日益严重的问题,印染废水作为几种较难处理的废水之一,废水存在成分复杂、色度深、毒性大、可生化性差、pH、温度、排放量波动大等问题[1]。印染废水一般利用物理、化学、生物等方法处理。传统的物理法及其生物处理法反应时间长、运行成本高对特殊染料具有选择性,不适合分散染料等。化学法可能会引入新的杂质,并且生成难以降解的物质。因此,利用高级氧化技术处理印染废水越来越受到人们的重视。
Fenton 法作为高级氧化技术的主流技术之一,其原理是Fe2+和H2O2混合发生系列反应,生成大量强氧化性的·OH。Fenton 法具有降解彻底、无二次污染、停留时间短等优势。但是传统的Fenton 法具有H2O2消耗大、铁源回收困难、反应不易控制等问题[2-3]。另外反应在酸性条件下进行,对废水的酸化和中和处理成本较高也是影响Fenton法广泛应用的阻碍[4-5]。将Fenton 法与其他方法联合应用为这种方法带来了新思路。
中国具有丰富的蒙脱土资源,由于蒙脱土具有层间离子可交换性、可膨胀性以及酸性可调节性和吸附性能,且储量丰富、价格低廉,许多学者把它作为处理印染废水的重点研究对象[6-7]。本文利用蒙脱土负载β-FeOOH 辅助类Fenton 试剂处理印染污水,望能找到一种新的印染废水处理方式,能够改良Fenton法,提高降解废水效率。
1 实验部分
1.1 试剂和仪器
蒙脱土(MMT)、NaCl、FeCl3、Na2CO3、H2O2、NaOH、HCl溶液、玫瑰红B,均为分析纯;去离子水,自制。
PHS-3C型pH计;BS224S型电子天平;721型可见分光光度计;JSM-6700F 型场发射扫描电子显微镜(SEM);激光拉曼光谱测试仪(Raman)。
1.2 实验方法
1.2.1 蒙脱土的改性
将4 g 蒙脱土(MMT)和200 mL 2mol/L NaCl 溶液混合后加热至80 ℃搅拌1.5 h得到钠基化蒙脱土,密封备用。在高速搅拌下,取一定量的Na2CO3溶液,缓慢滴入FeCl3溶液n(OH-)/n(Fe3+)=2.5(氢氧根的物质的量是溶液加入Na2CO3后计算溶液pH得到的),继续搅拌1 h,然后在90 ℃水热老化4.5 h,在高速搅拌下将一定量的蒙脱土粉末n(Fe3+)/m(MMT)=xmmol/g 缓慢加入上述制得的含铁溶液中,继续搅拌1.5 h,用蒸馏水洗涤至无Cl-为止(用1%的AgNO3溶液检验),烘干粉碎,制得β-FeOOH-MMT(x),密封备用。
1.2.2 RhB的降解
在50 mL烧杯中加入一定初始pH、质量浓度为20 mg/L 的RhB 模拟废水10 mL,然后依次加入一定体积的30%H2O2和一定质量的β-FeOOH-MMT(x)。搅拌处理一定时间,将悬浊液放入离心管内,在3 500 r/min条件下离心20 min。取上层清液,用可见分光光度计在RhB 最大吸收波长(λ=554 nm)处测定吸光度,用去除率表征RhB的降解效果。
2 结果与讨论
2.1 SEM分析
蒙脱土和钠基化蒙脱土的扫描电子显微镜照片见图1。由图1a 可知,在改性前蒙脱土为致密的片层晶体颗粒,表面结构平坦光滑。由图1b 可见,钠基化后的蒙脱土结构发生明显改变,颗粒形貌变得蓬松,而盐溶液中的阳离子可以与蒙脱土层间的阳离子发生离子交换,说明Na+进入层间,使得蒙脱土变的疏松。

图1 蒙脱土(a)和钠基化蒙脱土的SEM照片(b)Fig.1 SEM images of montmorillonite(a)and sodiumbased montmorillonite(b)
对不同的β-FeOOH-MMT(2.5)、β-FeOOHMMT(3.5)和β-FeOOH-MMT(4.5)进行SEM 表征以分析不同比例对β-FeOOH-MMT(x)表面结构的影响,结果如图2所示。从图2可知,样品中β-FeOOHMMT(x)呈现片状结构,但制备时加入的β-FeOOH量不同,表面粗糙度也不同,其中x=2.5时最为光滑,x=4.5时表面较为粗糙,x=3.5时最为粗糙。

图2 β-FeOOH-MMT(x)的SEM照片Fig.2 SEM images of β-FeOOH-MMT(x)
图3 为蒙脱土、钠基化蒙脱土、β-FeOOH-MMT(2.5)、β-FeOOH-MMT(3.5)和β-FeOOH-MMT(4.5)的拉曼光谱图。由图3可见,在2 400~2 600 cm-1处从下往上,相对峰强度降低,因而羟基基团的红外效果增强,所以说明了FeOOH 的含量增加;在400~500 cm-1的指纹区从下往上,相对强度降低,可知MMT的含量降低。

图3 蒙脱土、钠基化蒙脱土、β-FeOOH-MMT(2.5)、β-FeOOH-MMT(3.5)和β-FeOOH-MMT(4.5)的拉曼光谱图Fig.3 Raman spectra of montmorillonite,sodium-based mont-morillonite,β-FeOOH-MMT(2.5),β-FeOOH-MMT(3.5)and β-FeOOH-MMT(4.5)
2.2 MMT、钠基化蒙脱土对RhB的降解
RhB模拟废水的标准曲线见图4。MMT和钠基化蒙脱土对RhB模拟废水去除率的影响见图5。由图5 可知,在同一时间内钠基化蒙脱土的吸附效果比MMT 的吸附效果更高。这可能是因为钠基蒙脱土具有更好的膨胀性[8]和更大的空隙,这与MMT、钠基化蒙脱土的SEM 照片结果一致。因而将蒙脱土钠基化改性,再制备β-FeOOH-MMT(x)。
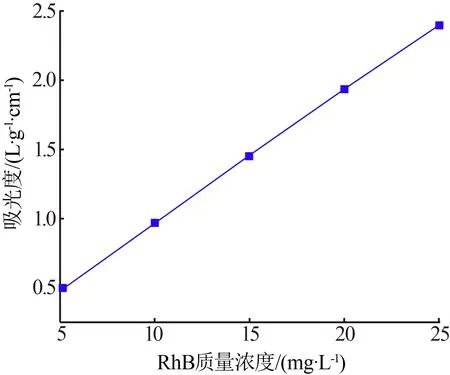
图4 RhB模拟废水标准曲线Fig.4 Standard curve of rhodamine B simulated wastewater
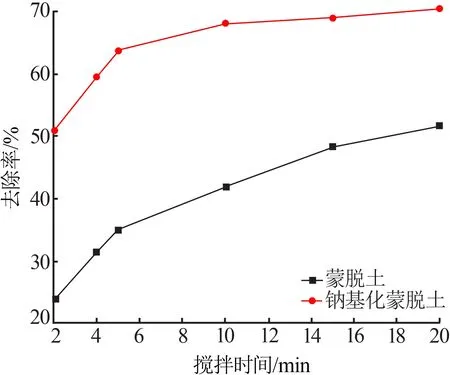
图5 蒙脱土、钠基化蒙脱土对罗丹明B去除率Fig.5 Removal rate of rhodamine B by montmorillonite and sodium-based montmorillonite
2.3 n(Fe)/m(MMT)对RhB的去除率的影响
在反应温度为25 ℃、n(H2O2)∶n(Fe)=10∶1、pH=5.2、搅拌时间为10 min 的情况下,改变x的数值以时间为变量测定β-FeOOH-MMT(x)对RhB 的去除率,结果见图6。由图6 可以看出,当x=2.5 时,对模拟废水的去除率最弱,但x增加后FeOOH 增多,活性位点增加,·OH 的浓度升高,式(2)~(4)[9-10]向右移动,使得RhB 的去除率增强。但随着x的增加,x=4.5 时,对RhB 的去除率反而降低,这可能是因为FeOOH 增多,活性位点增加,·OH 的浓度继续升高,发生了式(5)~(6)[11-12]反应,反而不利于·OH和RhB 反应。
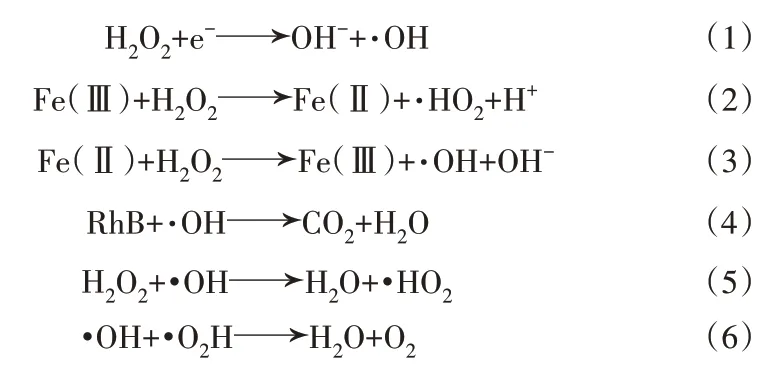

图6 x值与去除率的关系图Fig.6 Relationship between x and removal rate
2.4 搅拌时间对RhB的去除效果影响
在反应温度25 ℃、n(H2O2)∶n(Fe)=10 的条件下,搅拌时间对RhB模拟废水的去除率影响见图7。由图7 看出,在0~10 min 去除率提升很明显,在10~20 min RhB模拟废水去除率基本没有变化。综合考虑,选用搅拌时间为10 min,此时RhB去除率可达到78.56%。

图7 搅拌时间对RhB去除率的影响Fig.7 Effect of stirring time on RhB removal rate
2.5 H2O2与Fe 的物质的量比对RhB 模拟废水的去除效果的影响
在罗丹明B初始质量浓度为20 mg/L、x=3.5、pH=5.2、搅拌10 min 条件下,改变n(H2O2)∶n(Fe)探究罗丹明B 的去除效果,结果见图8。由图8 可见,n(H2O2)∶n(Fe)从0 增加到50 时RhB 的去除效率不断增高,在n(H2O2)∶n(Fe)=50 时去除率可达到89.3%,这可能与发生了式(2)~(4)反应有关。随着n(H2O2)∶n(Fe)继续增加,RhB的去除效果反而逐步降低,这可能是因为n(H2O2)增加,导致局部H2O2浓度增加,促进H2O2分解为·HO2[13-14],·HO2的浓度增大反而发生了式(5)~(6)的副反应,使得RhB 的去除效果降低。故选用n(H2O2)∶n(Fe)=50为最佳。
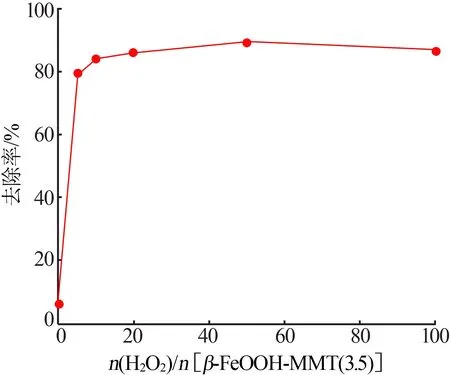
图8 n(H2O2)∶n(Fe)对罗丹明B的去除效果的影响Fig.8 Effect of n(H2O2)∶n(Fe)on the removal effect of rhodamine B
2.6 pH对罗丹明B的去除效果的影响
在罗丹明B初始质量浓度为20 mg/L、n(H2O2)∶n(Fe)=50、x=3.5、搅拌时间为10 min 条件下,改变pH,探究罗丹明B 的去除效果,结果见图9。由图9可知,当pH 从7 降低至5.2(初始pH)时,去除率升高。但pH 从5.2 降至4 时RhB 的去除率却降低了,可能发生了式(7)反应,使得FeOOH结构被破坏,但当pH 进一步降低时,发生了式(2)~(3)[15]反应,使得去除率进一步升高,式(7)达到95.91%。但如果应用强酸性条件处理废水,则在废水排放之前需要多次调节pH,增加处理成本,因而选用pH=5.2(自然条件)最为合适。
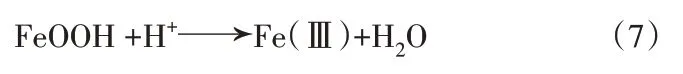
2.7 不同处理方法的比较
在反应温度为25 ℃、初始pH=5.2、x=3.5、n(H2O2)∶n(Fe)=50条件下,处理方法对RhB的去除率的影响见图10。由图10可知,单独β-FeOOH-MMT(3.5)对RhB的去除效率和单独H2O2的降解效率都较低,β-FeOOH-MMT(3.5)和H2O2协同作用对RhB 的去除率提升十分明显,说明β-FeOOH-MMT(3.5)和H2O2有着很强的协同作用。
采用表观一级反应动力学方程ln(ρ0/ρt)=kt(ρ0和ρt分别为初始及t时刻的RhB的质量浓度,mg/L;k为表观动力学常数,min-1;t为时间,min)对图10 的数据进行线性拟合可得到表1。
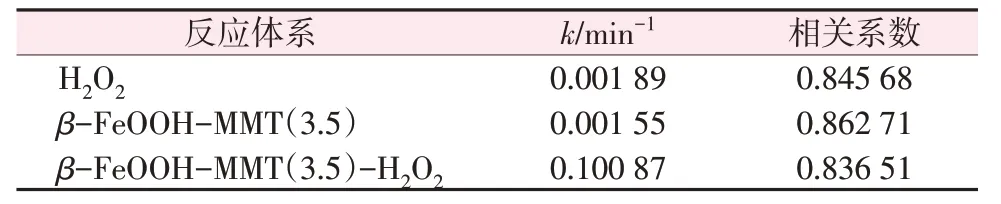
表1 不同反应体系的表观体系常数Table 1 Apparent system constants of different reaction systems
β-FeOOH-MMT(3.5)与H2O2反应体系的协同作用可用速率常数增强因子f表示[15],见式(8)。式中,k[β-FeOOH-MMT(3.5)-H2O2]、k[β-FeOOHMMT(3.5)]、k(H2O2)分别为3 种反应体系的表观速率常数。

由数据可以推算出f=29.32,因此可知β-FeOOHMMT(3.5)-H2O2体系的协同作用是非常明显的。
3 结论
1)β-FeOOH-MMT(3.5)-H2O2体系对降解RhB模拟废水产生了明显的协同效应,在β-FeOOHMMT(x=3.5)用量为2 g/L、n(H2O2)∶n(Fe)=50、pH=5.2 条件下搅拌10 min 较佳处理工艺下,20 mg/L罗丹明B 去除率可达到89.3%。2)β-FeOOHMMT(3.5)-H2O2体系较为符合一级动力学,速率增强因子可到达29.32。3)推测了可能的降解机理:H2O2在FeOOH 的催化下生成了·OH 进攻RhB 大分子从而降解RhB染料废水。
