钠离子电池正极材料Na3V2(PO4)3研究进展
2022-05-18周英杰侯敏杰杨冬荣戴永年
东 鹏,周英杰,侯敏杰,杨冬荣,戴永年,3,梁 风,3
(1.昆明理工大学真空冶金国家工程实验室,云南昆明 650093;2.昆明理工大学云南省有色金属真空冶金重点实验室;3.昆明理工大学省部共建复杂有色金属资源清洁利用国家重点实验室)
在“碳达峰、碳中和”国家战略目标的驱动下,储能技术作为支撑新型电力系统的重要技术和基础装备,其规模化发展已成为必然趋势。其中,可充电金属离子电池被认为是解决日益增长的高能量密度化学电源需求的最有效方法,在过去的20 a,成熟的锂离子电池(LIB)技术已广泛应用于人们的日常生活,成为电动汽车和便携式电子设备的理想电源。然而,在锂资源匮乏和储能成本降低的双重因素影响下,LIB 已经难以支撑电动汽车和电网储能两大产业的需求,因此加速了其他替代电池的发展,如钠离子电池、钾离子电池、镁离子电池和钙离子电池等[1-2]。
钠与锂为同主族元素,二者物化性质相近。与锂相比,钠资源丰富、成本低廉、环境友好。因此,钠离子电池(SIBs)被普遍认为是大规模储能应用中最有前景的候选电池之一[3]。然而,由于Na的相对原子质量较大、标准电化学电位较低、离子半径较大,导致Na+的扩散速率迟缓,造成SIBs 能量和功率密度相对较低。因此,开发高性能正极材料对提高SIBs能量密度、循环寿命、倍率性能及加速其商业化应用起着关键作用[4-5]。
在充/放电过程中,电池正极材料需要进行可逆的氧化还原反应和有效的传质,必须具有合适的化学性质(热稳定性、氧化稳定性、还原稳定性)和物理结构(比表面积、孔隙度、电子导电性)。2002 年,UEBOU 课题组[6]首次用具有NASICON 结构的NVP作为SIBs的正极材料,其优越的离子扩散速率实现了Na+的自由嵌入/脱出,使其具有稳定的钠容量。然而,由于NVP电子导电性差以及在钠离子脱嵌过程中显著的体积变化、晶格应力的积累和材料表面缝隙的产生,导致SIBs 容量衰减以及副反应产生,限制了NVP的商业化应用。近年来,新的制备方法和先进的表征技术得到迅速发展,对NVP的学术研究日趋活跃,在发展先进的NVP 正极材料和Na+插层化学方面取得了重大突破如图1 所示,为进一步提高NVP 的能量密度、倍率性能、循环寿命等电化学性能提供了新的机会。

图1 NVP正极材料发展史[7-13]Fig.1 Development history of NVP cathode materials[7-13]
本文首先综述了NVP正极材料的储钠机理、制备方法的最新进展;然后,总结了NVP 正极材料的先进改性手段,重点评价了不同改性方法对本征结构、电子导电性、体积效应等的影响规律;最后,展望了NVP正极材料未来发展的关键挑战和研究方向。
1 NVP的结构及其电化学储能机理介绍
NVP 是由3 个PO4四面体和2 个VO6八面体组成,通过共用氧原子进行链接,成为聚阴离子体[V2(PO4)3],并在c轴方向通过PO4与相同聚阴离子体相连。其中存在两类不同氧环境的Na+位于该晶体的空隙或通道中,一类是六配位环境位于八面体位置的容钠位(6b),定义为Na(1)位,每个单元包含1个Na(1)位;另一类是八配位环境位于四面体位置的容钠位(18e),定义为Na(2)位,每个单元包含3个Na(2)位,如图2a 所示[14]。NVP 中V4+/V3+和V3+/V2+电对分别产生3.4 V 和1.6 V(vs.Na+/Na)的工作电压,其理论容量达到176 mA·h/g。但部分Na(1)起到支撑晶格的作用,一旦脱出就无法进一步嵌入,因此可逆容量主要由Na(2)贡献,对应的理论容量为117.6 mA·h/g[15],虽然NVP可以提供两种Na+的脱嵌位点,但由于多面体电负性较大,使电子转移通道受阻,造成电导率较低。
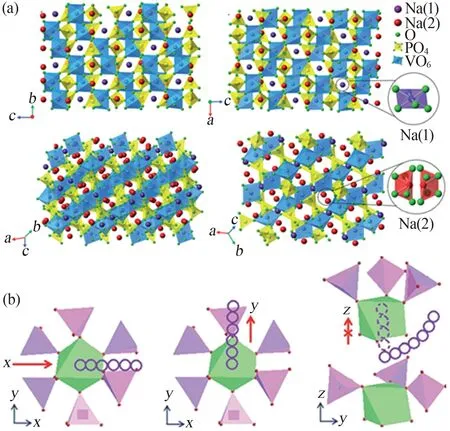
图2 NVP的结构示意图(a);NVP中沿x、y和弯曲z轴方向的离子迁移机制图(b)[11,14]Fig.2 Structure diagram of NVP(a);The ion migration scheme diagram along x,y and bending directions in NVP(b)[11,14]
如图2b所示,利用第一性原理计算迁移活化能得到3种可能存在的迁移路径:第一种机制是Na+在两个PO4四面体之间的间隙沿x方向迁移;第二种机制是Na+沿y方向穿过PO4四面体和VO6八面体间隙;第三种机制是Na+通过八面体曲折进入相邻的PO4四面体和VO6八面体通道。通过扩散路径计算3 种机制的迁移活化能分别为0.090 4、0.117 74、2.438 eV,表明Na+主要沿着x方向和y方向进行迁移[11]。
2 NVP的制备方法
不同制备方法会导致NVP 产物在结构、形貌、粒径、比表面积等方面的差异,对其可逆容量、循环效率、电子以及离子电导率有着显著影响。目前,制备NVP 的研究热点主要集中在固相法、溶胶-凝胶法和水热法[16]。
2.1 固相法
固相法(Solid phase method)是将固相原料(钠源、钒源、磷源等)按特定比例进行球磨混合和细化,在高温下经过元素扩散、反应成核、晶体生长等过程得到NVP。
VAN 等[17]采用一步固相法成功地制备了纯相NVP,NVP 的TEM 和SEM 表征见图3a~3b。由图可知,其形状不规则、部分颗粒聚集形成更大的次级颗粒,平均直径约为50 nm;纯相NVP 在0.1C 时,可逆容量仅为83.71 mA·h/g。SUN等[18]通过高能球磨结合固相法制备出非化学计量比的Na3-3xV2+x(PO4)3@C(x=0~0.1)纳米复合材料。实验证实,当x=0.05 时,复合材料的性能最为优异,即使在20C 下仍然能提供92.3 mA·h/g(理论可逆容量的79%)的可观可逆容量,循环500次后仍然能够保持初始容量的95%,其电化学性能的显著提高归因于内阻的降低和Na+扩散速率的提高。KLEE等[19]通过优化球磨时间(10~24 h)制备NVP@C,结果表明,球磨24 h 与球磨0 h和10 h相比团聚明显减少、纯度更高、结晶度更好,且由于活性物质周围碳导电相的均匀分散以及NVP@C粒径的有效减小保证了快速的动力学传输,所以具有优异的倍率性能,如图3e~3j 所示。球磨24 h 的NVP@C在10C下循环100次后容量为111 mA·h/g。

图3 NVP样品不同分辨率的SEM照片(a~b);NVP样品不同分辨率的TEM照片(c~d);NVP-BM 0 h(e),NVP-BM 10 h(f),NVP-BM 24 h(g)的TEM照片;NVP-BM 0 h(h),NVP-BM 10 h(i),NVP-BM 24 h(j)的SEM照片[17,19]Fig.3 SEM images of NVP samples with different resolutions(a~b);TEM images of NVP samples with different resolutions(c~d);TEM images of(e)NVP-BM 0 h,(f)NVP-BM 10 h,and(g)NVP-BM 24 h;SEM images of(h)NVP-BM 0 h,(i)NVP-BM 10 h,and(j)NVP-BM 24 h[17,19]
固相法具有反应条件可控、成本低、操作过程简单且易于大规模工业化生产等优势。但固相反应各组分原子和离子受到晶体内聚力影响不能像在液相或气相反应中自由地迁移,使反应物扩散不充分导致产物NVP形貌不规则,且颗粒会随着烧结温度的升高和时间的延长而发生熔联长大(NVP 粒径一般大于1 μm),具有较差的倍率性能和循环性能。
2.2 溶胶-凝胶法
溶胶-凝胶法(Sol-gel method)是将可溶性钒源、钠源、磷源依次按特定步骤溶于溶剂中,经充分搅拌均匀、溶解、缩聚等过程形成溶胶,通过干燥得到前驱体,进而在一定的温度下煅烧得到NVP。
LUO 等[20]通过正交实验对溶胶-凝胶法制备NVP@C 的工艺参数进行优化,图4a 为实验过程的示意图。结果表明,在800 ℃时,NVP@C 团聚现象减少,二次颗粒尺寸减小到5 μm且具有微小孔状结构(见图4b~4e)。在0.2C 下,首次循环时容量为106.7 mA·h/g,经 过100次循环后可逆容量为104.5 mA·h/g,仅比初始容量损失2.5%。此外,结构的优化使NVP@C 表现出更好的倍率性能以及相同倍率下的最高放电容量,即使在20C的高倍率下,放电容量也超过90 mA·h/g,如图4f~4g 所示。TIAN等[21]利用溶胶-凝胶法成功地将K/Co均匀地掺杂到NVP@C 中。掺杂后的K0.1Co0.05-NVP@C 在1C 下初始可逆容量为100.9 mA·h/g,循环500次后可逆容量可保持在71 mA·h/g;在10C 下可逆容量可达98.8 mA·h/g,循环400 次后容量保持率可达75.9%,表现出优异的循环性能和倍率性能。WANG 等[22]采用溶胶-凝胶法制备的具有三维互联多孔骨架的NVP@C 具有较大的比表面积,平均孔径为20 nm。由于NVP@C 具有纳米级尺寸的3D 多孔框架的支撑,使其具有出色的倍率性能和容量保持率,在192C 下放电容量为75.8 mA·h/g,在1 C 循环800 次后容量保持率可达98.4%。
基于系统的涌现理论对企业价值共创体系价值创造能力进行评价具有合理性和优越性。这样的评价能够从系统整体的角度评价价值共创体系的优劣,更适用于当前的复杂环境,体现企业价值共创体系价值创造能力的敏捷适应性。
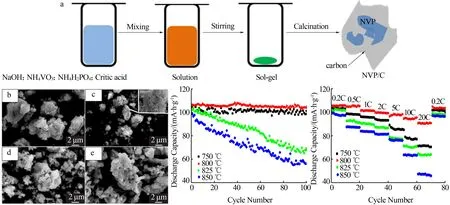
图4 NVP@C制备过程及不同煅烧温度下的SEM照片和电化学性能[20]Fig.4 Preparation process,SEM images and electrochemical properties of NVP@C at different calcination temperature[20]
溶胶-凝胶法可将原料在短时间实现反应物之间分子水平上的混合,前驱体在发生化学反应时扩散尺度可以达到纳米水平,致使产物NVP的形貌为均匀的球状颗粒(粒径为0.5~1.5 μm)、比表面积相对较大。但该方法工艺复杂、处理周期长,由溶胶到粉体需要消耗大量时间和能量,不利于工业化生产[23]。
2.3 水热法
水热法(Hydrothermal method)是将原料(可溶性钒源、钠源、磷源)充分混合均匀再移至反应釜中,在高温高压环境下进行水热反应,完成后经洗涤、干燥、煅烧处理等工艺得到NVP。
LI 等[24]使用水热法制成多孔纳米片层NVP@C(NVP@C-P),其形貌呈纳米层状且厚度为20~50 nm,直径为200~500 nm,图5a~5c为NVP@C-P制备过程示意图及SEM照片。结果表明,由于多孔纳米片层结构增加了离子/电子传输速率,缩短了离子/电子传输的扩散路径,且制备的NVP@C-P 具有高的结晶度,这些特性的协同使得NVP@C-P具有出色的倍率性能和超长的循环稳定性能,在0.2、100C下可逆容量分别为117、76.5 mA·h/g,在50C循环10 000次后容量保持率为82.6%。RUAN 等[25]探索了水热时间(10~30 h)对NVP@C形貌的影响,最终在20 h得到结晶度较高的3D 菊花状结构的NVP@C,纳米片平均厚度为20~30 nm,如图5d 所示。该结构通过降低Na+传输过程中的能量消耗提高了离子传输效率,并且表面的碳涂层可以显著提高整体电子电导率,其在5C下循环300次后容量保持率为98%。

图5 NVP@C-P的制备过程示意图及SEM照片[24-25]Fig.5 Schematic diagram of the preparation process and SEM images of NVP@C-P[24-25]
相对于其他制备方法,水热法制备的NVP具有晶粒生长完全、粒径小(一般在200 nm 左右)、颗粒二次生长减少、分散性好、可以实现多种形貌调控(如菊花状、空心微球状、片层状等)等优势。并且NVP 经过形貌调控可以提供连续电子/离子迁移通道,大比表面积有利于电极与电解质接触且纳米级的晶粒尺寸显著缩短了Na+扩散路径,从而提高了离子迁移率。但其缺点在于水热条件不易控制、成本较高、产量较低[26-27]。
3 NVP改性方法
NVP 内部丰富的孔道有助于Na+快速且可逆地扩散[28-29],所以具有很高的理论能量密度和库伦效率。目前,针对电子电导率低、体积效应和循环稳定性差的缺点[30],主要的改进方法有碳包覆、金属离子掺杂和晶体纳米化。
3.1 碳包覆
使用碳材料对NVP 进行包覆提高导电性作为一种常用的改性手段已被广泛报道,通过将碳源(有机碳源或者无机碳源)引入前驱体,在惰性气氛下通过高温热解在NVP 的晶体表面包覆一层非晶碳薄层来形成导电网络,使NVP正极材料的电导率极大提高并且可以优化电极和电解液之间的兼容性,同时在晶粒表面沉积的碳还能有效防止材料在高温煅烧和退火过程中的过度生长和团聚现象[31]。
SI 等[32]通过固相法以乙炔作为碳源制备NVP@C,结果表明,产物含有尺寸为1~2 μm 的不规则颗粒,且存在孔隙和薄膜,如图6a~6b所示。用王水清除NVP 粒子后形成一层连续且均匀的非晶态碳薄膜(厚度为10 nm),该膜与NVP 粒子紧密结合,不仅使电子具有连续的传导路径,而且NVP在Na+脱嵌过程中的晶体结构较为稳定使其表现出较好的循环性能,在1C下循环300次后具有83.7 mA·h/g的充电容量和82.1 mA·h/g 的放电容量,库仑效率为98%(见图6c~6d)。LIU等[33]通过固相法将3种不同有机碳源(葡萄糖、蔗糖和可溶性淀粉)包覆NVP进行对比。结果表明,用可溶性淀粉作为碳源得到的NVP@C在1C下可逆容量为100 mA·h/g,循环1 000次后容量保持率为82.8%,即使在40C 下可逆容量也可高达72 mA·h/g。出色的循环稳定性能得益于可溶性淀粉衍生的三维互联碳网络抑制了NVP 粒子的过度生长和聚集,缩短了电子传输路径,改善了转移动力学,减小了体积效应。CHANG 等[34]用石墨烯对NVP进行碳包覆,由于石墨烯具有三维导电结构框架,所以在1C 下可逆容量为114.6 mA·h/g,即使在30C 下可逆容量也高达89.7 mA·h/g。为进一步提高石墨烯包覆NVP 的电化学性能,ZENG 等[35]首次对包覆在NVP 表面的石墨烯进行硼元素掺杂得到纳米球状的BG-Na3V2(PO4)3@C,该结构可以提高Na+的扩散效率和电子传导效率,使其在10C下可逆容量高达94.7 mA·h/g,并在循环100 次后容量保持率为96.4%,如图6e~6f所示。

图6 样品NVP@C的形貌表征(a~d);Na3V2(PO4)3@C和BG-Na3V2(PO4)3@C的电化学性能(e~f)[32,35]Fig.6 Morphology characterization of sample NVP@C(a~d);electrochemical performance ofNa3V2(PO4)3@C and BG-Na3V2(PO4)3@C(e~f)[32,35]
3.2 杂原子掺杂
利用金属离子掺杂(K+、Mg2+、Al3+、Mn3+、Ti4+和Ni2+等)的方法可以提高NVP 本体离子导电率和电子电导率,其中部分元素掺杂之后可作为惰性组分不参与电化学反应,起到稳定结构、改善材料电子导电性、扩宽Na+传输通道、缩短Na+传输路径等作用,从而有效提高NVP的电化学性能[36]。
ZHU等[37]通过溶胶-凝胶法结合冷冻干燥将K+和Ca2+对Na+位点进行共同取代,最佳掺杂成分为Na2.79K0.07Ca0.07V2(PO4)3@C,在0.1C、1C 和10C 下可逆容量分别为110.2、92.7和83.6 mA·h/g。其中在10C下循环150 次后容量保持率为83%,如图7a 所示。出色的倍率性能得益于杂原子掺杂使得晶胞体积增大,拓宽了Na+的传输通道。LIU等[38]采用Nb5+掺杂对NVP 的晶体结构进行优化,如图7b 所示,包覆的碳纳米壳可以构筑电子导电网络,缓冲Na+脱嵌过程中体积的畸变。此外,引入的Nb5+可以调节晶体参数,产生更多的Na 空位,进一步促进Na+的传输。当Nb 质量分数为0.2%时,表现出较好的倍率性能和高倍率下的循环稳定性,在50C 下可稳定循环1 600 次以上,容量衰减率仅为0.011%,如图7c~7e所示。GU 等[39]首次制备了钛掺杂的纳米NVP@C,结果表明,掺杂的金属钛离子可以提高NVP的本征电导率,且包覆碳层可减少Na+脱嵌过程中体积变化[40],使Na2.9V1.9Ti0.1(PO4)3@C 在5C 时容量高达106.3 mA·h/g,在10C 循环200 次后容量仍保持在95.8 mA·h/g。
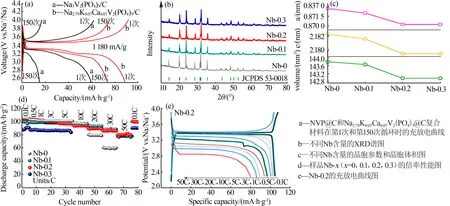
图7 NVP@C和Na2.79K0.07Ca0.07V2(PO4)3@C复合材料的电化学性能和结构表征参数[37-38]Fig.7 Electrochemical performance and structural characterization parameters of NVP@C and Na2.79K0.07Ca0.07V2(PO4)3@C[37-38]
金属离子掺杂拓宽了NVP中Na+迁移通道并且使Na+脱嵌过程中的体积效应受到一定的限制,在提高电子/离子电导率的同时增强了NVP 晶体结构的稳定性。最后,对金属离子掺杂工作进行了总结,如表2所示。
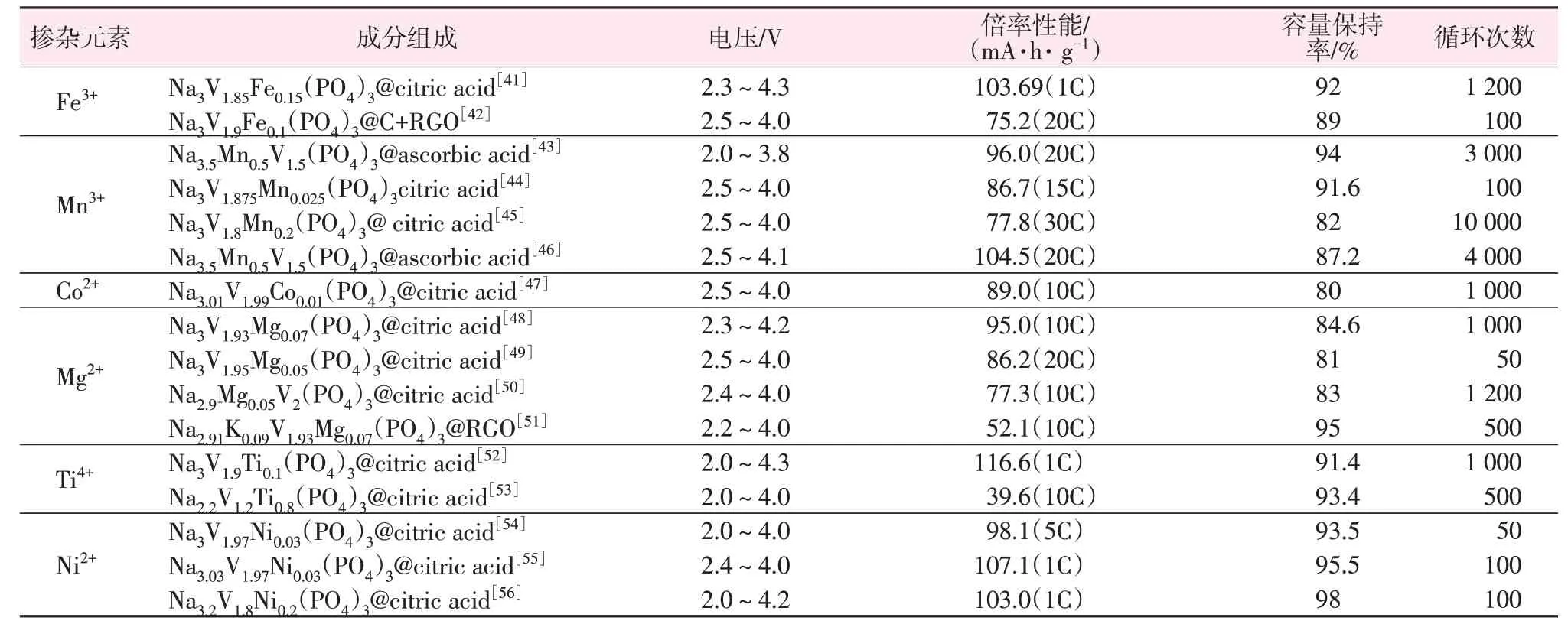
表2 不同元素掺杂NVP的性能对比[41-56]Table 2 Performance comparison of NVP doped with different elements[41-56]
3.3 晶体纳米化
晶体纳米化通过构建纳米级三维形貌来增加NVP 的比表面积,例如,构造出的纳米级多孔结构,使得电解液与NVP的兼容性更好,从而提高其电子导电率和Na+电导率[57-58]。利用溶胶-凝胶法、静电纺丝法等可制备出纳米化的NVP材料。
YANG 等[59]利用溶胶-凝胶法结合干燥喷雾法成功制备了球形多孔碳包覆的NVP粒子如图8a~8c所示,粒径尺寸为1~3 μm,由于该结构不仅可以缩短Na+的传输路径,而且能吸收更多的电解液,提高离子电导率,在10C下具有101 mA·h/g的可逆容量,在200C 具有60 mA·h/g 的可逆容量,表现出优异的倍率性能。YANG等[60]采用静电纺丝工艺将NVP纳米颗粒嵌入到碳纳米纤维中,得到碳纳米纤维复合材料(NVP-CNF),如图8d~8e 所示。CNF 为负载的NVP 提供了连续的电子转移通道,且纳米孔隙会储存更多的电解液加快离子传输,在0.1C 下得到112.5 mA·h/g(理论可逆容量的96%)的可观可逆容量,在1C 下循环300 次后,容量保持率为93%。GUO 等[61]采用乙二醇(软模板)和热解法制备了抗团聚碳包覆的NVP(Agg-r-NVP@C),其平面尺寸为100~150 nm,表面碳涂层厚度为3~7 nm,纳米片间距促进了电解液对Agg-r-NVP@C 表面的润湿和渗透,加速了Na+和电子的快速传输,使其在200C和300C超高倍率下,分别获得71.2、56.2 mA·h/g放电容量,且在200C 下循环20 000 次时容量保持率为83.3%,表现出非常出色的倍率性能和超稳定的循环性能。
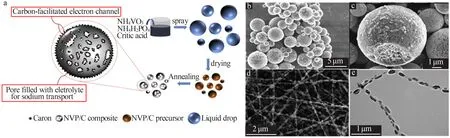
图8 NVP@C的合成流程图(a);(b)和(c)NVP@C空心球的SEM照片;(d)和(e)不同倍率下NVP-CNF的SEM照片[59-60]Fig.8 Synthesis diagram of NVP@C(a);(b)and(c)SEM images of NVP@C hollow spheres;(d)and(e)SEM images of NVP-CNF at different magnification[59-60]
4 总结与展望
SIBs 相较于LIB 具有原材料储量丰富、价格低廉等优势,在大规模储能领域存在广阔的应用前景。NASICON结构NVP正极材料独特的3D连续网络通道和开放晶体框架结构为Na+的迁移提供了良好的扩散路径和储钠空间,为高能量密度SIBs的开发提供了新的途径。本文综述了近年来NVP 正极材料的储钠机理、制备和改性的研究进展,认为NVP 正极材料的体积效应、低比容量和电子导电率是限制其发展的主要因素。
目前,NVP 正极材料的制备方法主要有固相法、溶胶-凝胶法和水热法。其中,固相法具有反应条件可控、成本低、操作过程简单、易于大规模工业化生产等优势。然而,由于烧结产物的晶粒过度生长和粒径分布不均匀制约了其进一步发展。溶胶-凝胶法和水热法制备的NVP 具有纯度高、分散性好、颗粒均匀且形貌可控制的优势,但是存在工艺复杂、处理周期长、能耗高、产量低等缺点。
碳包覆、金属离子掺杂、晶粒纳米化已经广泛用于提高NVP正极材料的容量和电子导电率。然而,碳纳米管或石墨烯的引入虽然为NVP 正极材料构筑了连续电子通路,却增加了生产成本,失去了SIBs工业化的核心优势;杂原子掺杂起到稳定结构和改善材料电子导电率等效果,却不可避免地降低了NVP 正极材料的工作电压和理论容量;此外,纳米级的活性材料比微米级的活性材料具有更低的振实密度,这表明纳米级的电极材料具有更低的体积能量密度。因此,在不损害现有SIBs固有优点的前提下,开发合适的NVP正极材料制备和改性方法是非常有必要的。
随着SIBs的发展,通过静电纺丝、喷雾干燥法、模板法等新型技术定制化制备NVP 正极材料有望显著提高电池容量、充放电速率和循环寿命等电化学性能;结合原位表征技术(如原位XRD、原位扫描透射X射线显微镜、原位TEM、冷冻电镜和电化学相场模型等先进的模拟技术)构建电化学反应机理和内部结构退化过程,了解相变行为与过电位和尺寸依赖性,实现高稳定性NVP 正极材料的设计,助力SIBs的商业化应用。此外,为了更好地将NVP正极材料应用于SIBs,还需要做以下工作:
1)由于电解液高压分解的限制,NVP 正极材料的工作电压一般低于4.6 V(vs.Na/Na+),开发不易分解、低成本、易处理的电解液对NVP 正极材料的实际应用具有重要意义;
2)传统的黏结剂对NVP 正极材料和集流体的黏附性有限,充放电循环过程中活性材料脱落和粉碎是电池容量降低的主要原因,通过原子层沉积、水热反应实现活性材料与集流体的一体化生长,是提高SIBs电化学性能和循环寿命的有效途径;
3)为实现粒度分布均匀、纯度高、形貌可控的NVP 正极材料规模化生产,需要开发一种简单、低成本的合成方法;
4)通过高通量计算和实验获得大量NVP 正极材料的晶体结构、电子分布等相关性质,指导新型SIBs的设计;
5)多学科交叉合作,在材料、封装设计、充放电监测等方面同步优化,加速高能量密度SIBs的开发应用。
