亚硫酸处理碱减量废水的研究及回收利用
2021-05-25张书良杜小玉
郭 提,张书良,杜小玉
(河南工业大学 环境工程学院,河南 郑州 450001)
1 碱减量废水的水质特点
1.1 废水中的污染物
废水中有机物的含量较高,主要污染物包括对苯二甲酸钠,EG和氢氧化钠。废水中对苯二甲酸钠的含量为60%~70%[1],是碱减量废水的特征污染物。
1.2 废水的COD高
因为碱减量加工过程的废水中含有EG,TADS和少量其他聚合物,所以废水呈高COD的特征。其CODcr一般在20000 mg/L左右,有时甚至能超过100000 mg/L[2]。印染废水与碱减量废水混合后COD浓度能达到2000~3000 mg/L以上,其中含5%~10%的不可生物降解的COD[3]。通常选择采用酸析法、活性炭吸附法、膜分离技术等方法处置碱减量废水,可以很好地达到去除废水中COD的目的。
1.3 废水的pH值高
在碱减量工艺操作过程中,为保证减量率,通常采用间歇式或连续式处理工艺对碱液进行多次利用,减量处理后的大量碱液将会留在碱减量废水中,使得废水呈现pH值高的特征,可高达13.0以上[4]。废水的pH值过大,会对后续的生物化学处理过程产生严重影响,所以处置前要先降低废水的pH值。
1.4 废水的可生化性差
碱减量废水的BOD5/CODcr值一般在0.4~0.5之间。如果碱减量废水的COD含量超过混合废水COD含量的20%时,废水的可生化性会很差;BOD5/CODcr达到0.2以下,很难进行生化处理[5]。一般情况下,碱减量废水中的大部分有机物很难被微生物分解利用,所以污染物去除率较低,废水的可生化差。
2 碱减量废水处理技术的国内外研究现状
2.1 酸析法
利用酸析法处置碱减量废水,操作简单方便,并且能回收废水中的大部分TA,从而使废水的COD大幅度下降,既可以实现清洁生产,又能回收利用资源。酸析法对废水中的TA去除率一般在70%~99%左右,COD的去除率一般在50%~90%之间[6]。但是利用酸析法回收对苯二甲酸过程中需要消耗大量的H2SO4,处理费用比较高。而且酸析法产生的沉淀颗粒细小,回收的TA纯度较低[4]。
2.2 碱析法
采用碱析法处理减减量废水,就是向废水中投加氯化钙,使对苯二甲酸以不溶性的对苯二甲酸钙盐析出,从而实现对苯二甲酸与废水的分离[7]。与酸析法比较,使用碱析法处理碱减量废水,其中对苯二甲酸的去除率提高,并且得到的对苯二甲酸钙粒径较大,沉淀性能较好,便于分离回收。但是碱析法的处置费用较高,且最终回收的对苯二甲酸钙没有利用价值[5]。
2.3 膜分离技术
膜分离技术利用膜的吸附和扩散作用对废水中的污染物进行选择性的过滤,从而去除废水中的污染物,并且可以回收对苯二甲酸,实现了碱液的回用。超滤-纳滤组合膜分离技术处理废水,能很好地达到回收利用对苯二甲酸、降低废水COD的目的。但是膜分离技术仅适用于低浓度的碱减量废水。
2.4 好氧生物处理法
现在对于碱减量废水的处理,采用的好氧生物处理法主要有活性污泥法和生物膜法。
采用好氧生物法处理碱减量废水,处理过程中容易出现污泥膨胀的现象[8]。碱减量废水水质水量变化大,COD高,水中含有除TA之外的其他不易降解的污染物,致使活性污泥在运行过程中产生很多问题。比如活性污泥的抗冲击负荷能力差,会产生大量活性物质,容易造成二次污染[5]。
生物膜法,其抗冲击负荷能力强,产生的活性污泥量少,避免了产生活性污泥膨胀,可使TA的生物降解率大大提高。由于印染行业的产水具有水量大和水质变化复杂的特点,而该种方法仅适用于处理水量较小的印染废水,具有一定的局限性。
2.5 厌氧生物处理法
现在对于碱减量废水的处理主要采用的厌氧活性污泥法是上流式厌氧污泥床法(UASB)。UASB产泥率低,可处理高浓度的有机废水。该方法具有COD去除率高,容积负荷大,反应器结构简单和操作方便的优点,是一种使用价值很大的碱减量废水处理方法。但是采用UASB处置碱减量废水时[9],厌氧生物处理法启动时间较长,可能需要几个月,操作不方便。
综上所述,在现有的众多碱减量废水处理方法中,每种方法都有自己的使用条件和优缺点,并不能真正有效处理和回收利用碱减量废水[10]。
全新奥迪A8L的强大绝非这千余字的文章所能深入描述,但它的豪华,它的质感,它的科技和它所代表的豪华旗舰面对未来所展现出的领先理念都是令人印象深刻的。奥迪用全新A8L强大的产品力和前瞻的视野给予“突破科技,启迪未来”这句口号奉上了一个完美的印证。
3 实验原理与方法
3.1 实验原理
在碱减量废水中加入H2SO3,把pH值调至2.0~4.0,使TA析出,实现与废水分离。在碱减量废水中加入H2SO3后发生反应:
C8H4Na2O4+H2SO3→C8H6O4↓+Na2SO3
(1)
TA为难溶性物质,可通过过滤分离除去。剩余产物主要为Na2SO3,再向废水中加入CaO,两者反应生成NaOH和CaSO3,NaOH可通过膜分离的方法分离出来,并可用于对涤纶织物的水解;CaSO3经过加热干馏的方法可分解为CaO和SO2,CaO可再次用于Na2SO3的处理;SO2则可与H2O反应生成H2SO3,重新用于TADS的酸析反应。理论上该反应系统可循环运行,极大地降低了碱减量废水的处理成本。
3.2 碱减量废水的制备方案
实验时,碱减量废水可采用化学方法制备。本实验按碱减量废水的COD值为20000.0 mg/L,pH值为12.0~14.0的指标配制废水。经过实际测定,在室温为20 ℃的条件下,碱减量废水的COD值为20553.5 mg/L,pH值为13.2。
3.3 亚硫酸的制备及应用
利用SO2气体溶于水来制备H2SO3。SO2在常温下为无色有刺激性气味的气体,有毒,易溶于水(约为1∶40)。由于SO2是一种主要的大气污染物,对环境和人体具有危害性,所以该实验选择在通风橱中进行。
实验室通常采用无水亚硫酸钠与浓硫酸发生反应的方法反应制备SO2气体,即
Na2SO3+H2SO4→Na2SO4+SO2(g)+H2O
(2)
实验开始时,在一个250 mL的三相圆底烧瓶中放入无水亚硫酸钠,然后将浓硫酸逐量加入烧瓶里,立即发生剧烈反应,产生SO2气体。即
2NaOH+SO2→Na2SO3+H2O
(3)
C8H4Na2O4+H2SO3→C8H6O4↓+Na2SO3
(4)
酸析得到的TA为难溶性物质,并且颗粒较大,可通过过滤的方法分离除去。此工艺回收的TA纯度较高,同时H2SO3的制备方法简单,极大地降低了碱减量废水的处理成本[11]。
3.4 碱减量废水处理产物的回收利用
本实验中碱减量废水的剩余产物主要为Na2SO3,向废水中加入CaO,反应生成NaOH和CaSO3,NaOH可通过膜分离的方法分离出来,并可用于对涤纶织物的水解;CaSO3经过加热干馏的方法可分解为CaO和SO2,可重复利用(图1)。
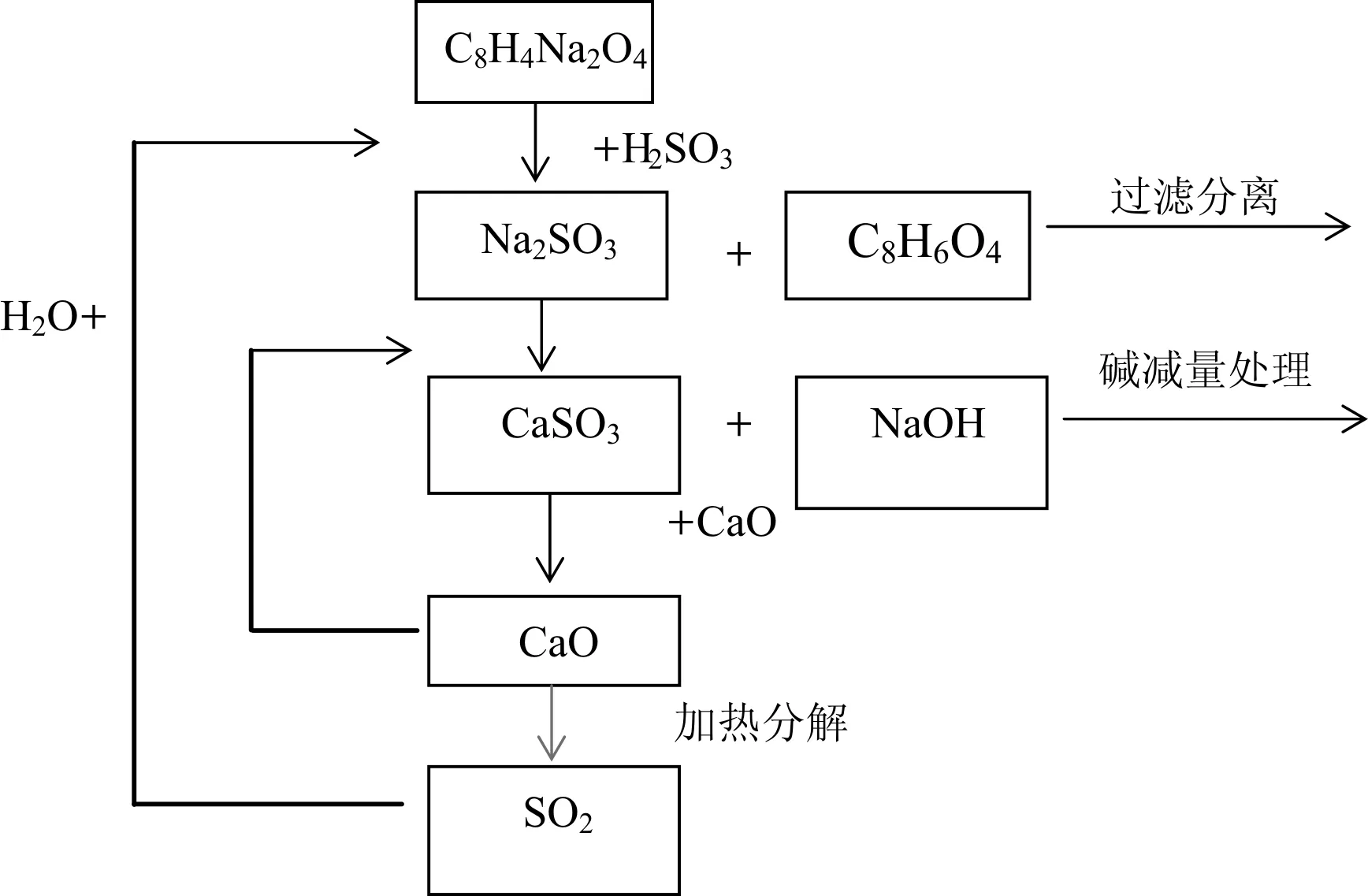
图1 碱减量废水的回收利用流程
4 实验结果与分析
实验时,取无水Na2SO3和浓H2SO4快速加入烧瓶中,制备SO2气体。将生成的SO2气体通入碱减量废水中。每隔一定时间取样,测定废水的pH值、COD,反应至水样的pH值小于3.0时即可停止。经过滤之后收集生成的对苯二甲酸,烘干之后称TA的质量;将反应后的废水放入恒温水浴锅中,设定温度为60~70 ℃,逐量向废水中加入CaO,并不断搅拌,反应至废水pH值为10.0左右时停止加入,测COD。过滤废水,将滤渣烘干,称量生成的CaSO3的质量。
4.1 碱减量废水的处理过程
实验一:70.0 g无水Na2SO3+130.0 mL浓H2SO4+400.0 mL碱减量废水+3.7 g CaO。
COD和pH值随着反应时间变化如表1和图2所示。

表1 实验数据
经计算,实验过程中,加入CaO之后碱减量废水的pH值为10.9,COD值为1801.2 mg/L。反应生成的对苯二甲酸质量为4.7 g,生成的CaSO3质量为6.2 g。
由于配制碱减量废水时,使用的对苯二甲酸质量为14.0 g,反应生成TA的质量为4.8 g,所以对苯二甲酸的回收率为34.3%。
实验二:100.0 g无水Na2SO3+160.0 mL浓H2SO4+400.0 mL碱减量废水+3.2 g CaO。
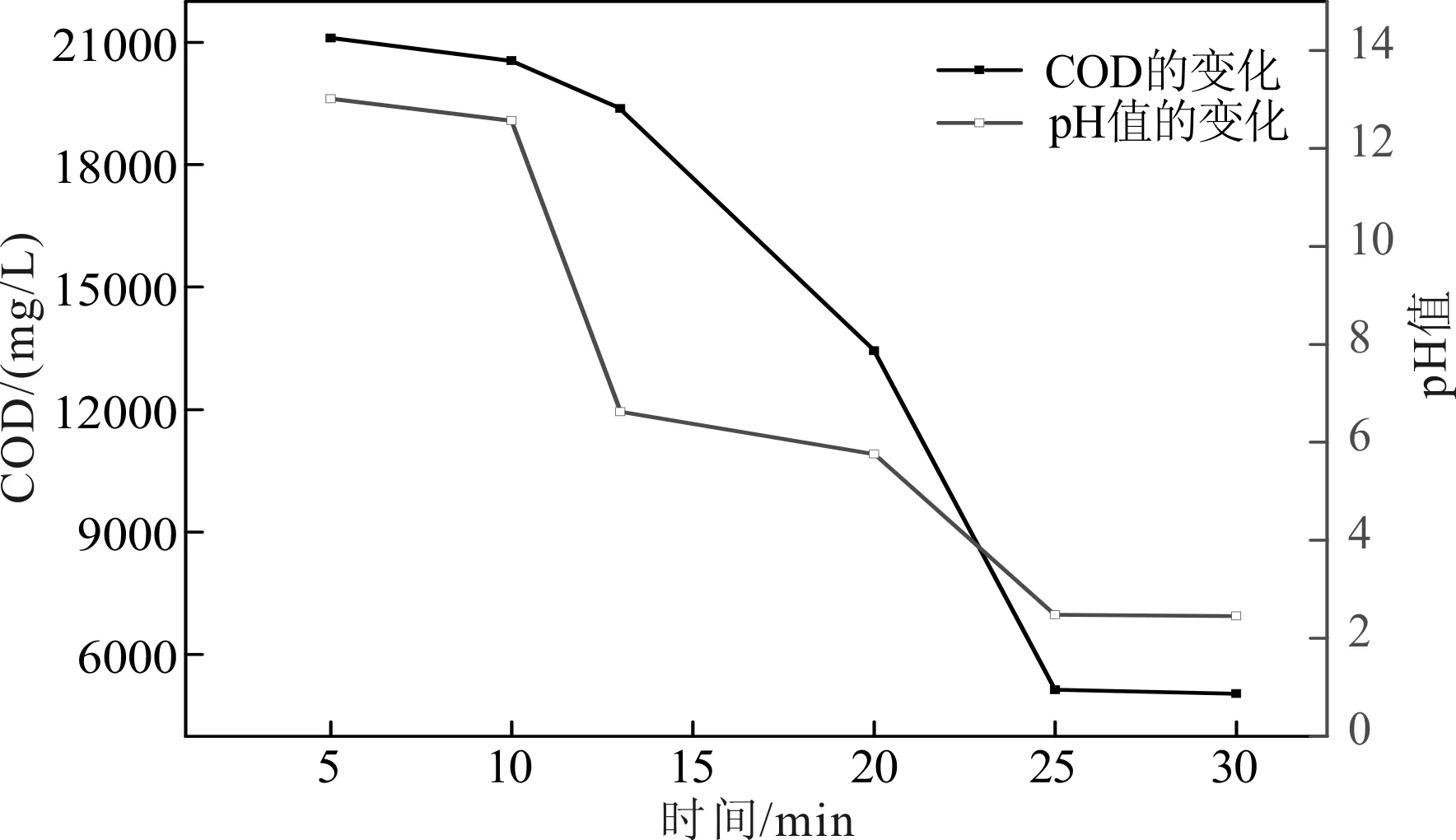
图2 COD和pH随反应时间的变化
COD和pH值随着反应时间变化如表2和图3。
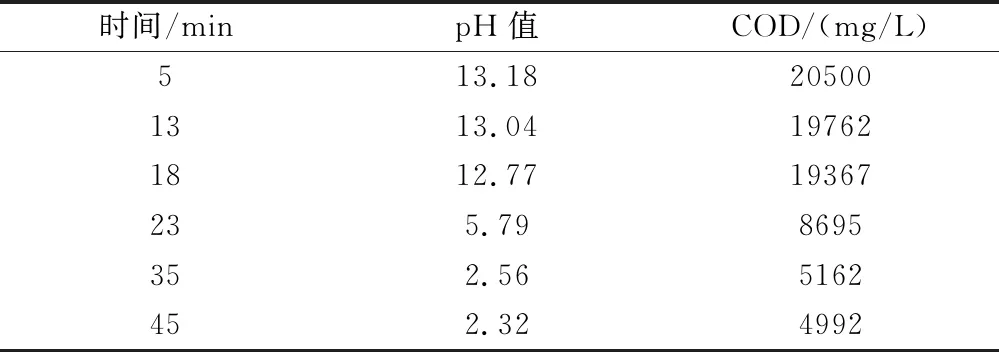
表2 实验数据

图3 COD和pH随反应时间的变化
经计算,实验过程中,加入CaO之后碱减量废水的pH值为13.3,COD值为1184.6 mg/L。
由于配制碱减量废水时,使用的对苯二甲酸质量为14.0 g,反应生成TA的质量为4.0 g,所以对苯二甲酸的回收率为28.6%。
实验三:150.0 g Na2SO3+270.0 mL浓H2SO4+400.0 mL碱减量废水+3.8 g CaO。
COD和pH随着反应时间变化如表3和图4所示。

表3 实验数据
经计算,实验过程中,加入CaO之后碱减量废水的pH值为10.6,COD值为1461.3 mg/L。反应生成的对苯二甲酸质量为6.8 g,生成的CaSO3质量为5.8 g。

图4 COD和pH随反应时间的变化
由于配制碱减量废水时,使用的对苯二甲酸质量为14.0 g,反应生成的TA质量为6.9 g,所以对苯二甲酸的回收率为49.3%。
4.2 碱减量废水的回收利用结果
称取10.0 g该反应生成的CaSO3放入管式炉中进行热分解,在最佳热解条件下,即1100 ℃下,燃烧60 min,主要生成物为CaO和SO2。将生成的SO2回收并用于碱减量废水的处理,得到了对苯二甲酸,质量为1.6 g;经过滤后再加入CaO,可重新获得CaSO3,质量为2.1 g。
通过实验可以得到结果:利用H2SO3处理碱减量废水,其生成的产物CaSO3,经过热分解和回收,得到的CaO和SO2可重新用于废水的处理。但是实验中得到的CaO和SO2的百分比较低,还有待于进一步研究。
5 结论
实验通过向纯水中加入对苯二甲酸和氢氧化钠模拟碱减量废水;将无水Na2SO3和浓H2SO4快速加入烧瓶中的方法,制备SO2气体。将生成的SO2气体通入碱减量废水中,即加入H2SO3,使其发生反应,回收利用对苯二甲酸、SO2、CaO等产物,其中对苯二甲酸的回收率可达到49.4%。利用H2SO3处理碱减量废水,其生成的产物CaSO3,经过分解和提纯,得到的CaO和SO2可重新用于废水的处理,大大将低了废水的处理成本,能有效地处理和回收利用碱减量废水。该方法在达到碱减量废水的处理标准的同时,做到了环保经济,是一种非常具有应用前景的碱减量废水处置方法[12]。
