羧肽酶G2在大鼠体内的组织分布及排泄
2022-03-31吴卓娜朱鲲鹏顾若兰孟志云朱晓霞窦桂芳
吴卓娜,朱鲲鹏,顾若兰,孟志云,甘 慧,朱晓霞,李 俭,窦桂芳
(1.军事科学院军事医学研究院辐射医学研究所,北京 100850;2.中国人民武装警察部队特色医学中心,天津 300162)
羧肽酶 G2(carboxypeptidase G2,CPG2)是用基因重组技术从假单胞菌获得的甲氨蝶呤(methotrexate,MTX)解毒剂,特异性地作用于MTX游离羧基端的谷氨酸,可快速、持久、大量地将MTX转化为非活性代谢产物,降低大剂量MTX在临床肿瘤治疗中的风险[1-5]。基础研究和临床试验均显示,CPG2迅速降低体内MTX浓度,不通过生物膜转运,对进入肿瘤细胞内的MTX的抗肿瘤活性影响较小,安全性良好。目前,美国FDA已批准其作为MTX的解毒药上市[6-8]。
本研究采用同位素示踪法对国产的CPG2进行[125I]标记(即[125I]CPG2),并对其在大鼠体内的药动学、组织分布和排泄进行研究,为临床研究及临床用药提供数据支撑。
1 材料与方法
1.1 药物、试剂和主要仪器
重组CPG2冻干粉针剂(批号:20110803,每支3.50 mg,活性1500 U),重庆科润生物医药研发有限公司;三氯醋酸(trichloroacetic acid,TCA,批号:20110-919,每瓶500 mL),国药集团化学试剂有限公司;BCA蛋白分析测定试剂盒(批号:TC263614,每盒10 mg),美国Thermo公司;[125I]CPG2(每瓶1 mL,放射性1mCi),由北京福瑞生物工程公司标记并纯化。
高效液相色谱仪(LC-20AT),日本岛津公司;γ计数仪(Wallac 1470),美国PerkinElmerTM公司;高效液相色谱仪自动分步收集器(BS-100A),上海沪西分析仪器厂;酶标仪(EIX800),美国Bio-Tek公司;凝胶色谱柱(TSK-GEL G2000,规格:300 mm×7.8 mm,5 μm),日本东芝公司。
1.2 动物
Wistar大鼠36只,雌雄各半,体重180~220 g,购自军事医学研究院实验动物中心,动物生产许可证号:SCXK(京)2007-004,实验动物饲养许可证号:SYXK(军)2007-004。动物饲养环境符合实验动物福利伦理委员会要求,大鼠自由饮水摄食,在室温24~26℃、湿度55%~65%、明暗交替12 h(7∶00-19∶00照明)的环境下适应性饲养1周。
1.3 [125l]CPG2的纯度和蛋白含量测定
用高效液相色谱法鉴定[125I]CPG2的纯度,洗脱液为 0.01 mol·L-1磷酸缓冲液,pH 7.4,流速1.0 mL·min-1。用分步收集器收集洗脱液,每0.5 min收集1管,用γ计数仪测定每管的放射性。用BCA试剂盒测定其蛋白含量,96孔板每孔加25 μL系列标准牛血清白蛋白(0.031~2.0 g·L-1)及[125I]CPG2,然后加入200 μL BCA混匀,37℃置30 min,用酶标仪测定其在570 nm处的吸光度值,绘制标准曲线,加权最小二乘法(1/X2)计算[125I]CPG2的蛋白含量。
1.4 [125l]CPG2在大鼠体内药动学
6只Wistar大鼠,雌雄各半,尾静脉推注[125I]CPG2 700 μg·kg-1,放射剂量936.88 kBq·kg-1,饲以标准大鼠饲料,自由饮水。给药前及给药后0.08,0.5,1,2,4,14和24 h经眼眶静脉采血,8000×g离心10 min取血清,加入等体积的20%TCA进行酸沉,然后5000×g离心5 min,弃上清,测定酸沉物的放射性。根据血清中酸沉物放射性计算不同时间点的药物浓度,再根据药物浓度-时间曲线,计算[125I]CPG2在大鼠体内的药动学参数。
1.5 [125l]CPG2在大鼠体内组织分布
18只Wistar大鼠,雌雄各半,随机分为3组(0.5,6和24 h组),尾静脉推注[125I]CPG2 700 μg·kg-1,放射剂量936.88 kBq·kg-1。分别于推注结束后0.5,6和24 h取全血,并将大鼠安乐死,取肝、肾、脾、肺、肾上腺、睾丸、卵巢、子宫、输卵管、输精管、心脏、胰腺、胸腺、小肠、小肠内容物、脂肪、膀胱、胃、胃内容物、大肠、大肠内容物、骨骼、骨骼肌、皮肤、骨髓、脑和眼球,共28种组织或体液、内容物及全血样本。组织和内容物分别称重,剪碎;血液离心,取血清。各处理后的样本加入等重量的20%TCA沉淀蛋白,5000×g离心5 min,弃上清,测定酸沉物的放射性,并计算同一时间点相同组织的平均放射性。
1.6 粪-尿和胆汁排泄实验
Wistar大鼠6只,雌雄各半,尾静脉推注[125I]CPG2 700 μg·kg-1(放射剂量936.88 kBq·kg-1)后单独饲养于代谢笼内,饲以标准大鼠饲料,自由饮水。给药前和给药后5,8,15,24,41,50,73,102,159,190,211,230和286 h收集尿液和粪便,记录体积或重量,测定其放射性。
Wistar大鼠6只,雌雄各半,麻醉后行胆管插管手术。待大鼠清醒后,尾静脉推注[125I]CPG2 700 μg·kg-1,放射剂量936.88 kBq·kg-1,给药后5,8,15和24 h收集胆汁,记录体积,测定其放射性。
1.7 统计学分析
使用计算机程序Microsoft Excel和Microcal Origin进行数据处理和制图。采用WinNorlin 5.2的非房室模型计算药动学参数。
2 结果
2.1 [125l]CPG2的纯度和蛋白含量
[125I]CPG2经TSK-GEL G2000凝胶过滤色谱分离后得到一个放射性主峰,该主峰在相同条件下与未标记的CPG2的洗脱保留体积一致,表明洗脱出的放射性主峰为[125I]CPG2,且放射性主峰的放射量占总放射量的95.06%。放射性主峰流分用BCA试剂盒测得蛋白浓度为840 mg·L-1,换算得到比活性为13.87 GBq·g-1,放化纯度为97.8%,满足实验要求。
2.2 [125l]CPG2在大鼠体内的药动学参数
大鼠静脉推注[125I]CPG2 700 μg·kg-1后平均血药浓度-时间变化曲线见图1。药-时曲线下面积AUC 为(27 792±6896)μg·h·L-1,峰浓度Cmax为(16 894±1809)μg·L-1,清除率CL为(0.026±0.005)L·h-1·kg-1,表观分布容积Vd为(0.16±0.04)L·kg-1,半衰期t1/2为(4.2±0.6)h。
2.3 [125l]CPG2在大鼠体内组织分布
大鼠静脉注射[125I]CPG2 700 μg·kg-1后,不同时间点不同组织、内容物及血清的平均放射性见表1。实验结果显示,[125I]CPG2主要分布在血清中,其次为血流丰富的组织及代谢和排泄器官,如肝、肾和胃内容物,在脑、肌肉和脂肪中较低,表明药物不易进入脂肪和肌肉组织,不易透过血脑屏障。给药24 h后[125I]CPG2在泌尿排泄系统内浓度较高,说明其主要通过肾排泄。
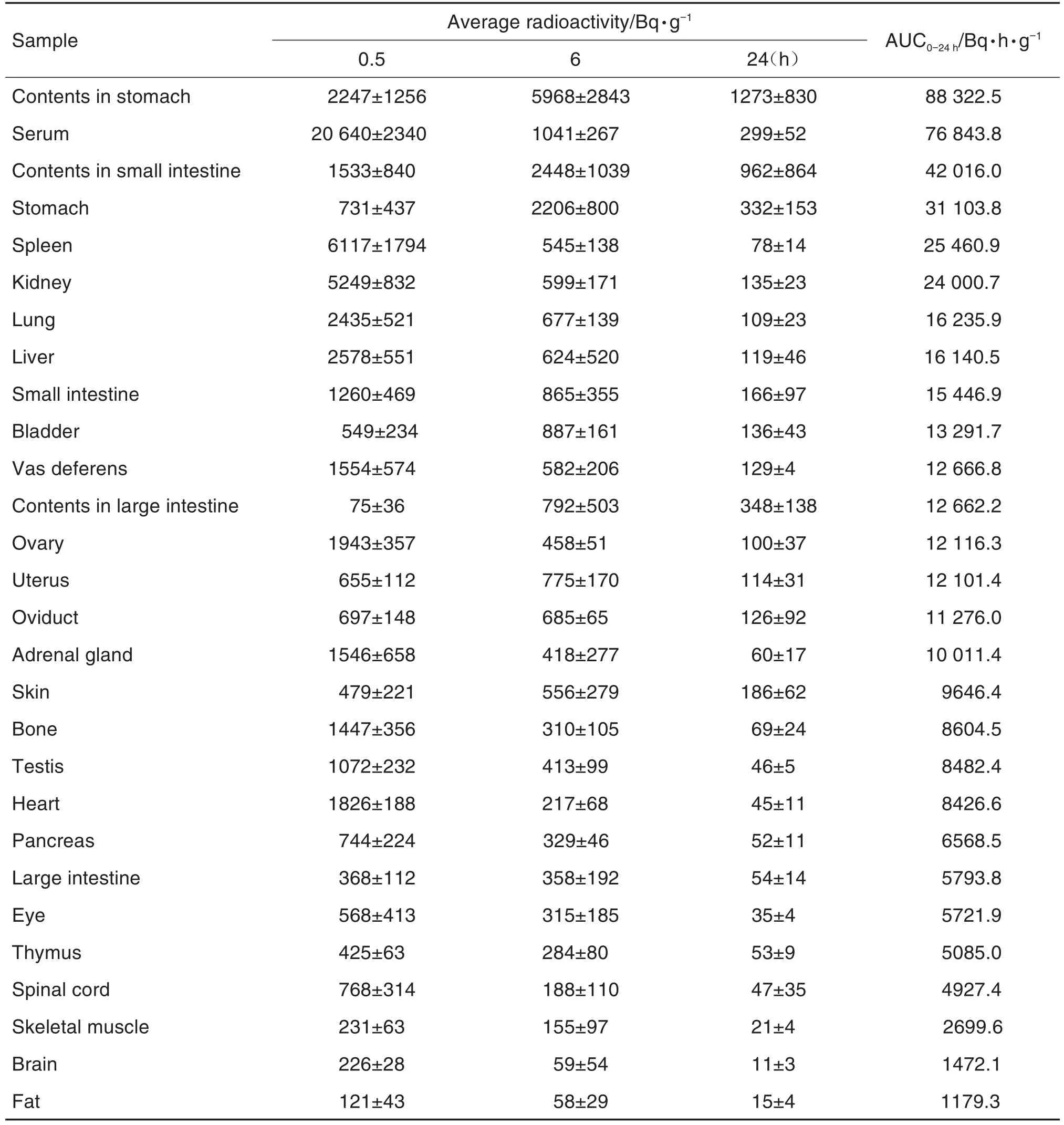
Tab.1 Average radioactivity in different tissues,body fluids and contents of digestive tract at different time points after intravenous injection of[125l]CPG2 in rats
2.4 [125l]CPG2在大鼠体内的排泄
大鼠静脉注射[125I]CPG2 700 μg·kg-1后286 h内粪便、尿液和胆汁的平均累积排泄量见表2。给药后286 h内,从尿液中回收到给药量的(84±4)%,从粪便中回收到给药量的(3.00±0.78)%,粪尿合计(87±4)%。给药后24 h内,从胆汁中回收到给药量的(7.77±0.54)%。

Tab.2 Average cumulative excretion of[125l]CPG2 in feces,urine and bile of rats after intravenous injection of[125l]CPG2
3 讨论
本研究应用同位素示踪法探究了[125I]CPG2在大鼠体内的药动学、组织分布和排泄的特点。大鼠尾静脉推注[125I]CPG2后,于不同时间取大鼠组织、内容物及全血,通过γ计数仪测定TCA可沉淀部分的放射性。TCA可沉淀部分是相对分子质量较大的蛋白质,近似代表原形药物CPG2,因此用TCA沉淀部分的放射性统计分析各组织、内容物及血清中CPG2的含量。大鼠尾静脉推注[125I]CPG2后,放射性主要分布在血清中,其次为血流丰富的组织及代谢和排泄的器官,如肝、肾及胃肠道等。[125I]CPG2在脑组织中浓度较低,表明其不易透过血脑屏障;给药后6和24 h,[125I]CPG2在泌尿排泄系统内的浓度较高,推测CPG2可能通过肾排泄。[125I]CPG2在脂肪、肌肉中的放射性含量较低,表明该蛋白不易进入脂肪、肌肉等组织。[125I]CPG2在胃内容物中浓度比较高,可能与标记方法有关。[125I]需要标记到CPG2的酪氨酸上,酪氨酸是碱性氨基酸,胃液为酸性环境,代谢后的125I-酪氨酸或蛋白片断可能通过胃壁分泌,导致在胃肠道内有较高的放射性分布。[125I]CPG2在大鼠体内的排泄研究表明,药物主要从尿液中排泄,少量从粪便中排泄,70%的放射性在给药后24 h内已经排泄,给药后41~286 h的排泄较缓慢,286 h时排泄≥80%。粪便和尿液中的放射性主要是[125I]CPG2的降解产物。
本研究结果可为制定CPG2的临床给药方案提供参考依据,同时也可为其他药物的药动学及组织分布和排泄研究提供借鉴。
