住院2型糖尿病患者皮下胰岛素泵降糖后血糖波动的影响因素分析*
2022-03-15刘晴晴孙殿静侯丽萍荣义华
刘晴晴,孙殿静,侯丽萍,徐 怡,荣义华
(衡水市人民医院/哈励逊国际和平医院内分泌科,河北衡水 053000)
住院2型糖尿病患者因院外血糖控制差在入院后往往给予皮下胰岛素泵强化降糖,在血糖达标后予以撤泵并改为皮下胰岛素注射方案,但在诊疗过程中发现患者的血糖波动情况不一,究竟是哪些因素影响了血糖波动从而最终影响临床疗效需要进一步探讨。血糖波动也称血糖变异性,近年来受到极高的重视。目前学界已认识到,只用糖化血红蛋白(HbA1c)、空腹血糖(FBG)、餐后血糖(PPG)、低血糖事件等无法全面解释糖尿病并发症的发生、发展。MONNIER等[1]提出血糖波动是独立于HbA1c、FBG、PPG之外的血糖变化信息。以往研究多以动态血糖监测系统(continuous glucose monitoring system,CGMS)提供的血糖变异指标来比较不同降糖方案、胰岛β细胞功能、生活方式等因素对血糖波动的影响[2-5],但由于CGMS成本较高、操作相对复杂,不易普及。我国于2017年制订了《糖尿病患者血糖波动管理专家共识》[6](以下简称共识),其中提出了由自我血糖监测(self-monitoring of blood glucose,SMBG)来计算日内血糖变异指标,包括血糖水平的标准差(standarddeviation of blood glucose,SDBG)、餐后血糖波动幅度(postprandial glucoseexcursion,PPGE)、最大血糖波动幅度(largest amplitudeof glycemic excursions,LAGE)。本研究选用了由SMBG计算得出的血糖变异指标来代表血糖波动情况。其中,由于PPGE与CGMS的血糖波动指标具有良好的相关性,又是影响糖尿病并发症发生、发展的重要因素[7],故本研究着重分析影响PPGE的因素,以指导临床医生更早地发现或改善这些因素从而提高临床治疗效果。
1 资料与方法
1.1 一般资料
选取2018年11月至2020年6月于本院内分泌科住院的2型糖尿病患者165例。诊断标准:糖尿病诊断符合1999年世界卫生组织糖尿病诊断标准。入组标准:院外应用≥2种降糖药物且经过饮食控制及运动血糖仍控制不佳[FBG≥9.0 mmol/L,餐后2 h血糖(2 h PG)≥11.0 mmol/L]的2型糖尿病患者。排除标准:(1)已知对胰岛素过敏者;(2)合并糖尿病酮症酸中毒、高血糖高渗状态者;(3)合并严重糖尿病慢性并发症者;(4)合并肝肾功能不全、心力衰竭、感染者等。剔除标准:(1)撤皮下胰岛素泵改为皮下胰岛素治疗后住院时间小于4 d者;(2)住院血糖监测次数小于7次/天者。患者均签署知情同意书,本研究经本院伦理委员会审核批准。
1.2 方法
1.2.1胰岛素泵治疗和撤泵后的胰岛素治疗
入选患者均给予糖尿病饮食,进行糖尿病知识宣教、运动指导,入院当天开始停用院外降糖药物,给予皮下胰岛素泵(美国美敦力公司712E型)持续皮下输注(continuous subcutaneous insulin infusion,CSII)门冬胰岛素注射液(丹麦诺和诺德公司)强化治疗。起始剂量按0.4~0.6 IU·kg-1·d-1计算,根据院外血糖情况、口服降糖药种类等适当增减总量的10%。其中全天量的50%为基础量,剩下50%为三餐前负荷量。依据SMBG指标调整胰岛素泵用量,并根据不同患者的血糖监测情况选择联合二甲双胍肠溶胶囊(每粒0.5 g,每天3次)或阿卡波糖片(每片50 mg或100 mg,3次/天)。其余种类口服降糖药物本研究不予以加入。血糖达到预期值予以撤泵,预期血糖为FBG 5.0~8.0 mmol/L,2 h PG 7.0~10.0 mmol/L。临床住院2型糖尿病患者在皮下胰岛素泵强化降糖后多给予“三短一长”或预混胰岛素多次皮下注射两个方案,不同治疗方案对血糖波动是否会产生影响亦需明确。在撤皮下胰岛素泵后,96例患者给予地特胰岛素注射液(丹麦诺和诺德公司)+门冬胰岛素注射液,三餐时皮下注射(Det+Asp);69例患者给予门冬胰岛素30注射液(丹麦诺和诺德公司),2次/天,早晚餐时皮下注射(Asp30)。分配到Det+Asp治疗的患者三餐时门冬胰岛素用量与撤泵时餐时负荷量等量转换,地特胰岛素用量与基础量等量转换。分配到Asp30治疗的患者门冬胰岛素30注射液早餐前剂量=[CSII早餐前剂量+(6:00-18:00的基础量)+CSII午餐前量];晚餐前剂量=[CSII晚餐前剂量+(18:00-6:00基础量)][8]。转换后依据血糖调整胰岛素用量。
1.2.2研究分组
撤泵后所有入组患者皮下胰岛素注射3 d,依据撤泵后第4天的aPPGE将患者分为两组,界值为2.2 mmol/L,<2.2 mmol/L为组1,≥2.2 mmol/L为组2[7]。
1.2.3观察指标
记录两组患者性别、年龄、病程、体重指数(BMI)、谷氨酸氨基转移酶(ALT)、丙氨酸氨基转移酶(AST)、血清肌酐(Scr)、总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、糖化清蛋白比值(glycosylated albumin ratio,GAR)、HbA1c(高效液相色谱法)、FPG、空腹C肽、联合口服降糖药物(二甲双胍、阿卡波糖)等指标。记录每日多点指尖血糖:三餐前、三餐后2 h、睡前血糖。胰岛素抵抗指数(HOMA-IR)=1.5+FBG×空腹C肽/2 800,胰岛功能指数(HOMA-β)= 0.27×空腹C肽/(FBG-3.5)[9]。记录撤泵当日及撤泵后第4天的日内血糖变异指标(SDBG、PPGE、LAGE)、当日胰岛素总量(total insulin,Tins)及当日最小血糖数值(minimum blood glucose,minGlu),其中SDBG为1天内多点血糖的标准差,PPGE为三餐后2 h的血糖与其相应餐前血糖差值绝对值的平均值,LAGE为日内最大和最小血糖值之差[2]。撤泵当日的血糖变异指标标记为bSDBG、bPPGE、bLAGE,Tins标记为bTins,当日minGlu标记为bminGlu;给予撤泵后第4天的血糖变异指标标记为aSDBG、aPPGE、aLAGE,Tins简写为aTins,minGlu标记为aminGlu。日内多点血糖由稳豪倍优型血糖仪(强生医疗器械有限公司)测定。
1.3 统计学处理

2 结 果
2.1 两组患者一般临床资料比较
根据aPPGE将患者分为两组,其中组1有74例(aPPGE<2.2 mmol/L),组2有91例(aPPGE≥2.2 mmol/L)。两组患者年龄、性别、病程、BMI、ALT、AST、TC、TG、HDL-C、LDL-C、Scr、HbA1c水平及GAR、bTins、bminGlu比较,差异均无统计学意义(P>0.05);组2患者HOMA-IR明显高于组1(Z=-2.046,P=0.041),Lg(HOMA-β)明显低于组1(Z=3.295,P=0.001);两组患者口服药物构成、应用胰岛素种类构成比较,差异均无统计学意义(P>0.05),见表1。
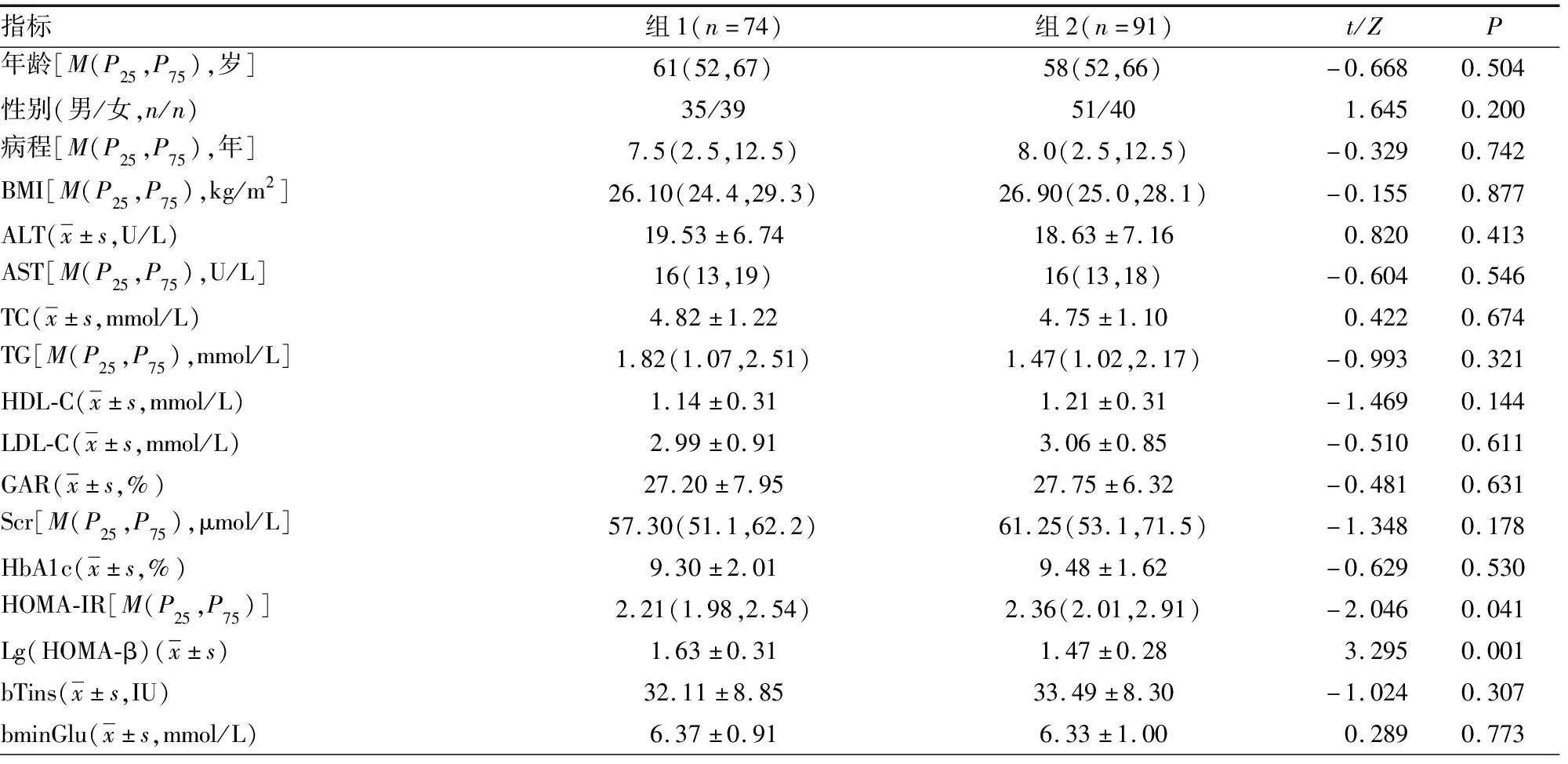
表1 两组患者一般临床资料比较
2.2 两组患者各时间点血糖变异指标、胰岛素及最小血糖比较
组2患者撤泵当日bSDBG、bPPGE、bLAGE高于组1,差异均有统计学意义(P<0.05),见表2。组2撤泵后第4天aSDBG、aPPGE、aLAGE高于组1,aminGlu低于组1,差异均有统计学意义(P<0.05),两组aTins无明显差异(P>0.05),见表3。

表2 两组间患者撤泵当日血糖变异指标比较(mmol/L)

表3 两组间患者撤泵后第4天血糖变异指标、胰岛素及最小血糖比较
2.3 aPPGE与其他变量的相关性分析
aPPGE与年龄、病程、BMI、ALT、AST、TC、TG、HDL-C、LDL-C、GAR、Scr、HbA1c、HOMA-IR、bminGlu、bTins均无明显相关性(P>0.05),与Lg(Homa-β)呈负相关(r=-0.166,P=0.034),与bSDBG、bPPGE、bLAGE呈正相关(r=0.243,P=0.002;r=0.209,P=0.008;r=0.186,P=0.018),见表4。

表4 aPPGE与其他变量的相关性分析
2.4 aPPGE影响因素的logistic回归分析
以aPPGE是否小于2.2 mmol/L为因变量(aPPGE<2.2 mmol/L=0,aPPGE≥2.2 mmol/L=1),将可能影响aPPGE的因素:Lg(HOMA-β)、HOMA-IR、bSDBG、bPPGE、bLAGE引入logistic回归模型,其中Lg(Homa-β)、Homa-IR、bSDBG、bPPGE、bLAGE为连续性变量,采用向前LR回归方法分析,以α<0.05为入选标准,最终进入方程的自变量为Lg(HOMA-β)、HOMA-IR、bSDBG,其中Lg(HOMA-β)为减少aPPGE波动的保护性因素[OR(95%CI):0.043(0.009,0.193),P<0.001],HOMA-IR、bSDBG为aPPGE波动的危险因素[OR(95%CI):4.650(2.071,10.440),P<0.001;OR(95%CI):4.013(1.653,9.747),P=0.002],见表5。

表5 aPPGE影响因素的logistic回归分析
3 讨 论
近年来对血糖波动即血糖变异的认识逐渐加深[10-12]。学者认识到控制血糖已不再仅仅是HbA1c、FBG、PPG达标及减少低血糖事件的发生频率,因为即使有着良好的HbA1c控制也可能发生糖尿病并发症[13-14]。现用来评估血糖波动的监测方法主要为CGMS和SMBG,其中由CGMS获得的平均血糖波动幅度(mean amplitude of glycemic excursion,MAGE)已被公认为评估血糖波动的“金标准”。此外,共识中提出SMBG与动态血糖有较好的相关性,且国内外均有研究证实相关结论[15-16]。本研究采用了由SMBG计算出的日内血糖变异指标来反映血糖波动。ROSENSTOCK等[17]将PPGE<2.2 mmol/L作为截点进行研究。急性PPGE峰值引起的氧化应激可造成大血管损伤[18],并可能加重心血管疾病[19]。WANG等[20]研究结果显示,MAGE与PPGE具有良好的相关性。另有研究同样证实,MAGE与PPGE及午餐后与晚餐后点血糖水平均呈明显正相关[21]。由此可见,PPGE无论在糖尿病并发症影响方面还是在评估血糖变异方面的作用不容忽视。
本研究结果显示,住院2型糖尿病患者撤泵后PPG波动的主要影响因素是胰岛β细胞功能、胰岛素抵抗及撤泵时的bSDBG。其中胰岛素抵抗、bSDBG为血糖波动的危险因素,而相对好的胰岛β细胞功能是减少PPG波动的保护因素。周淑晶[22]研究发现,MAGE与HOMA-IR呈正相关(r=0.405,P<0.05),与HOMA-β呈负相关(r=-0.526,P<0.05)。PENG等[23]研究亦得到相似结果。另外,撤泵时的血糖波动程度亦不容忽视,本研究显示以SDBG最为明显。本研究中撤泵时血糖预期目标为FBG 5~8 mmol/L、PPG 7~10 mmol/L,由此可见撤泵时仅参考FBG、PPG是不够的,还需结合撤泵当日的SDBG,尤其在患者同时有胰岛素抵抗、相对较差的胰岛β细胞功能时,可以适当延长佩戴皮下胰岛素泵的时间来减少撤泵后的血糖波动问题。区洪炎等[24]研究结果示,1周胰岛素强化治疗可促进胰岛β细胞休整,其中CSII亚组血糖达标更快。WANG等[25]研究发现,随着降糖治疗的进行,在解除持续高血糖对胰岛β细胞的损伤后,已经发生去分化现象的胰岛β细胞,可以从分化的其他类型细胞重新变为具有正常胰岛β细胞功能的细胞。
本研究未发现撤泵后不同胰岛素降糖方案及联合口服药情况(本研究仅限于二甲双胍或阿卡波糖)对血糖波动的影响。从口服药物构成比可看出二甲双胍肠溶胶囊(0.5 g,每天3次)联合口服阿卡波糖片(50 mg,每天3次)者与未口服二甲双胍肠溶胶囊但口服阿卡波糖片(50 mg,每天3次)者所占比例最大,在两组中分别各占55.4%、20.3%与50.5%、23.1%。国外糖尿病PPG管理指南中提到几种药效学上优先降低PPG的药物[26]:α糖苷酶抑制剂、二肽基肽酶-4(DDP-4)抑制剂、格列奈类、短效磺脲类、胰升糖素样多肽-1(GLP-1)类似物、短效人胰岛素/速效胰岛素类似物、预混人胰岛素/胰岛素类似物。另有研究报道,阿卡波糖可减少PPG的漂移[27]。故临床上应该重视相关药物的应用以减少血糖波动。
综上所述,本文主要以住院2型糖尿病患者皮下胰岛素泵强化降糖之后的短期治疗作为研究阶段,探讨了影响PPG波动的因素。结果显示,PPG波动主要受胰岛β细胞功能、胰岛素抵抗及撤泵时的bSDBG的影响,对于胰岛素抵抗明显、胰岛β细胞功能相对差的患者,可延长佩戴皮下胰岛素泵时间,进一步改善胰岛β细胞功能,减少胰岛素抵抗,使撤泵后血糖控制得以保障。
