硫酸溶液中O,O'-二(对甲苯基)二硫代磷酸三乙醇铵对Q235钢的缓蚀性能研究
2021-11-05王成端曾小彤樊成武
赖 川,王成端,桂 骁,曾小彤,庞 然,樊成武
(1.四川文理学院a化学化工学院,b国家城市污水处理及资源化工程技术研究中心川东分中心,四川 达州 635000;2.达州市生态环境科学研究院,四川 达州 635000;3.四川四众玄武岩纤维技术研发有限公司,四川 达州 635000;4.达州市质量技术监督检验测试中心,四川 达州 635000)
引 言
Q235钢因其机械强度好、成本低、易于加工等优点,在化工、油气田生产、金属加工、海洋工程、建材等多个行业中有广泛应用。因Q235钢在使用过程中存在生锈的突出问题,所以往往需要用盐酸、硫酸、硝酸等酸性溶液进行除锈、除垢和清洗,但由于酸性溶液具有腐蚀性,所以在除锈和除垢的同时还会造成Q235钢基体腐蚀[1-5]。基体腐蚀不仅会造成资源浪费,还可能造成安全隐患甚至引发灾难性后果,因此如何有效减缓Q235钢酸洗过程中基体腐蚀具有重大意义[6-8]。
在众多的减缓金属酸洗腐蚀技术中,使用缓蚀剂是最简单、成本最低、效果最好的方法之一[4-6,9]。不同类型的缓蚀剂中,有机缓蚀剂通常表现出卓越的缓蚀性能,这主要得益于其分子结构中往往含有N、O、S等高电子云密度的杂原子,它们较强的供电子能力有利于有机缓蚀剂分子在金属表面吸附成膜[3,6,8,10]。为此,本文将合成分子结构中同时包含N、O、S和P 4种杂原子的O,O'-二(对甲苯基)二硫代磷酸三乙醇铵盐(TADPD),并采用动电位极化曲线法和失重法评价缓蚀剂在H2SO4溶液中对Q235钢的缓蚀性能。
1 试验部分
1.1 试剂与仪器
试剂:五硫化二磷(P2S5,化学纯)、对甲苯酚(分析纯)、三乙醇胺(分析纯)、甲苯(分析纯)、丙酮(分析纯)、石油醚(60 ℃~90 ℃)、乙醚(分析纯)、氢氧化钠(分析纯)、浓硫酸(H2SO4,98%),所用试剂均购买于成都市科隆化学品有限公司,且试剂使用前均未作进一步纯化。
仪器:CHI760D 电化学工作站(上海辰华仪器有限公司)。
1.2 缓蚀剂合成
缓蚀剂合成过程参照文献[8,11-12],其具体原理如 图1 所 示。 首 先 称 取22.20 g P2S5(0.10 mol)于250 mL 三口烧瓶中,然后加入40 mL 甲苯作为溶剂。再用恒压漏斗在30 min 内逐滴滴加43.20 g 对甲苯酚(C7H7OH,0.40 mol,用80 mL 甲苯溶解),全部滴加后,缓慢升温至甲苯回流状态,持续回流反应至溶液体系澄清透明(约4.5 h)。反应结束后,用活性炭脱色、抽滤,并静置冷却。将冷液在搅拌条件下滴加29.80 g 三乙醇胺(C6H15NO3,0.20 mol),随反应进行可看到大量白色沉淀生成,静置过夜,减压抽滤,用石油醚洗涤2 次~3 次,烘干得到粗产品。粗产品用丙酮/石油醚混合溶剂重结晶,真空烘干得59.70 g白色晶体粉末O,O' -二(对甲苯基)二硫代磷酸盐(TADPD,MTADPD= 459),产率为65.03%。
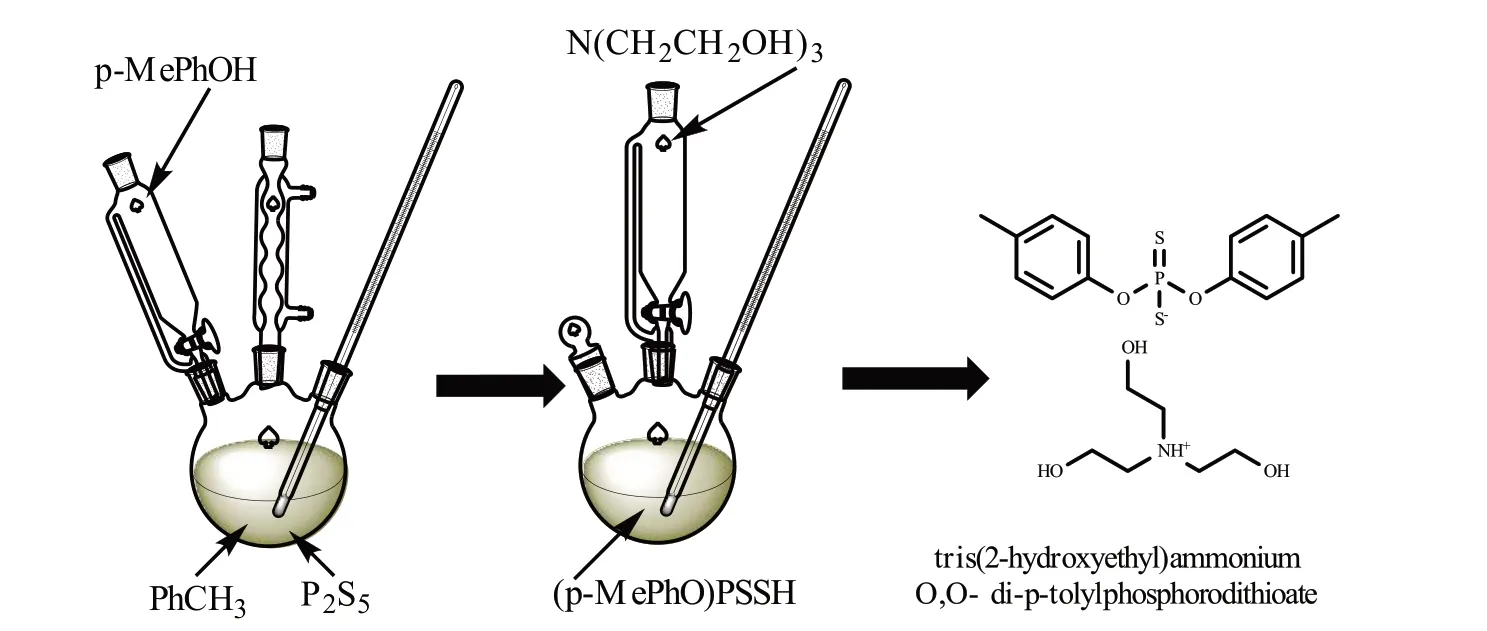
图1 缓蚀剂O,O'-二(对甲苯基)二硫代磷酸三乙醇铵的合成
1.3 试片与电极
试片:市售Q235 钢切割成25 mm × 30 mm × 5 mm规格,其元素含量为:0.21% C,0.44% Si,0.39% Mn,0.01% P,0.01% S,其余为Fe。试片使用前,表面统一用120#~1600#金相砂纸分级逐步打磨,然后用蒸馏水在超声条件下清洗干净,丙酮脱脂,最后用无水乙醇清洗后,冷风吹干,密封好置于干燥器中备用。
电极:市售Q235钢加工成圆柱状(Φ 1.0 cm),用聚四氟乙烯封装作为工作电极(工作面积0.785 cm2),电化学测试(动电位极化曲线测试)前用金相砂纸将电极逐级打磨(360#~1500#),去离子水冲洗,丙酮和乙醇清洗,吹干待用;镭磁217型饱和甘汞电极(SCE)作为参比电极,自制铂片电极作为辅助电极。
1.4 缓蚀性能评价
以电化学法进行缓蚀性能评价[13-14]:采用动电位极化曲线法评价缓蚀剂(TADPD)浓度及腐蚀体系温度、硫酸浓度和静置时间对缓蚀性能的影响。动电位极化曲线测试时电位极化范围为-0.25 V ~+0.25 V(相对于开路电位),扫描速度为0.5 mV/s。每组实验重复3 次。缓蚀率(IEPPM%)由式(1)计算得到:
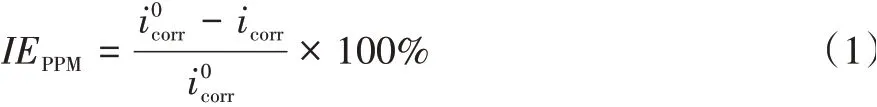
其中:i0corr与icorr分别为无TADPD 缓蚀剂和有TADPD 缓蚀剂时Q235钢在H2SO4溶液中腐蚀所得腐蚀电流密度(μA ⋅cm-2)。
失重法评价缓蚀性能[15-16]:为了选用不同方法共同验证实验结果,采用失重法研究TADPD 缓蚀剂在H2SO4溶液中对Q235 钢的腐蚀抑制效果,同时分析了TADPD 在Q235 钢表面的吸附行为。腐蚀速率(vinh)和缓蚀率(IEW%)分别由式(2)与式(3)计算得到:

其中:m0和mi分别为腐蚀试片腐蚀前后的质量(mg),S和t 分别为腐蚀试片表面积(cm2)和腐蚀时间(h),v0和vinh分别为不加TADPD 缓蚀剂和添加TADPD 缓蚀剂时腐蚀试片在H2SO4溶液中的腐蚀速率。
2 实验结果与讨论
2.1 动电位极化曲线法
采用动电位极化曲线法评价TADPD 缓蚀剂在30 ℃件下1.0 mol/L H2SO4溶液中对Q235 钢的缓蚀性能。当1.0 mol/L H2SO4溶液中TADPD 浓度不同时所得动电位极化曲线如图2 所示,对应电化学参数(包含缓 蚀 率,IEPPM%)列 于 表1。 从 图2 和 表1 可 知,1.0 mol/L H2SO4溶液中存在TADPD 时Q235 电极的腐蚀电流密度icorr与空白溶液中(1.0 mol/L H2SO4溶液不含缓蚀剂)Q235 电极的腐蚀电流密度i0corr相比,呈现急剧下降趋势,当缓蚀剂浓度达到250 mg ⋅L-1,其腐蚀电流密度从2903.44 μA·cm-2下降至27.63 μA·cm-2。腐蚀电流密度下降是由于缓蚀剂TADPD 分子中杂原子所带孤对电子与Q235 钢表面Fe 原子空轨道有效结合,使TADPD 分子吸附在Q235 钢表面形成保护层,很好地减少了H2SO4体系中H+与Q235 钢基体表面Fe 原子发生反应,进而起到减缓腐蚀作用。由图2和表1数据可发现,随TADPD浓度升高,腐蚀电流密度(icorr)和腐蚀电位(E)的绝对值逐渐降低。这是由于腐蚀电流密度和腐蚀电位与缓蚀剂吸附情况有关,缓蚀剂吸附成膜致密性越好,腐蚀电流密度也就越小,相应地缓蚀效果越好。30 ℃条 件 下1.0 mol/L H2SO4溶液中TADPD 浓 度 为250 mg·L-1时,缓蚀率IEPPM为99.05%。这表明TADPD具有非常好的缓蚀效果,是一种性能优异的缓蚀剂。
此外,从图2 可以看出随TADPD 浓度不断增加,极化曲线阴极和阳极斜率变化趋势基本一致;而由表1 可知,当TADPD 浓度从50 mg·L-1增加至250 mg·L-1时,相对应的腐蚀电位(E)绝对值变化远小于85 mV。因此,二者均表明TADPD是一种混合型缓蚀剂[13,16]。
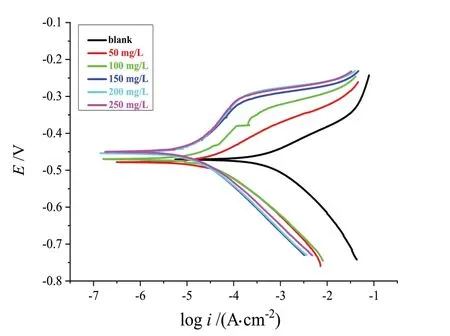
图2 30 ℃条件下1.0 mol/L H2SO4溶液中缓蚀剂TADPD浓度不同时所得Q235钢动电位极化曲线

表1 30 ℃条件下1.0 mol/L H2SO4溶液中缓蚀剂TADPD浓度不同时所得相应电化学参数
2.2 失重法
2.2.1 TADPD浓度对缓蚀性能的影响
失重法所得30 ℃条件下1.0 mol/L H2SO4中缓蚀剂TADPD 浓度(c,mg·L-1)与缓蚀率(IEW,%)和缓蚀速度(v, g·m-2·h-1)关系如图3所示。由图3曲线变化趋势可知,随TADPD 浓度增大,腐蚀速率先逐渐减小后基本趋于平稳,缓蚀率先逐渐增大后基本趋于平稳。曲线如此变化主要是由于随TADPD 浓度逐渐增大,TADPD 在Q235 钢表面吸附逐渐致密,形成的致密保护层将起到很好的腐蚀抑制作用;曲线趋于平稳主要是由于TADPD在Q235 钢表面吸附逐渐达到饱和。从图3 可以看出,当TADPD 浓度为从50 mg·L-1上升至250 mg·L-1时,腐蚀速率从14.41g·m-2·h-1下降至0.13 g·m-2·h-1,其缓蚀率从68.17% 上升至99.70%,这很好地验证了动电位极化曲线测试结果,二者共同印证了TADPD 是一种缓蚀效果优异的新型缓蚀剂。
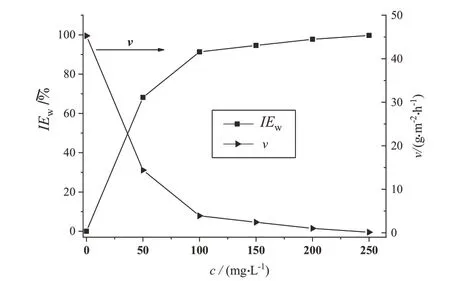
图3 30 ℃条件下1.0 mol/L H2SO4溶液中TADPD浓度与腐蚀速率和缓蚀率的关系
2.2.2 吸附行为研究
基于图3 的失重法数据,选用不同的吸附等温模型对TADPD 在1.0 mol/L H2SO4溶液中于Q235 钢的吸附行为进行研究。研究发现TADPD 在1.0 mol/L H2SO4溶液中于Q235钢表面的吸附符合Langmuir吸附等温模型。Langmuir方程表达式为:


其中:c 为TADPD 浓度(mg ⋅L-1),Ka为吸附过程的平衡常数,θ为表面覆盖度[16-17]。
Langmuir 吸附等温模型拟合关系曲线如图4 所示。由图4 可知,回归系数(R2)为0.9972和c 呈现良好的线性关系说明TADPD 在1.0 mol/L H2SO4溶液中于Q235钢表面的吸附符合Langmuir等温模型。另外,吸附自由能(ΔG0ads)是考察缓蚀剂吸附自发性的重要参数,可以通过式(6)与式(7)计算得到。其中MTADPD是TADPD 的分子质量,R 和T 分别为气体常数(8.314 J/(mol·K))和测试温度(K)。
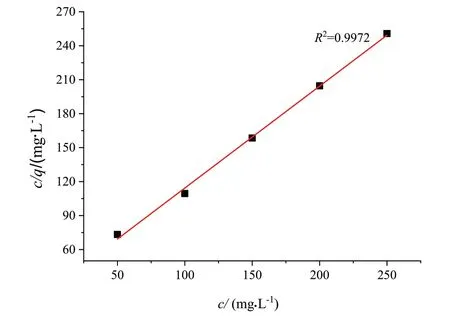
图4 Langmuir吸附等温模型拟合关系曲线
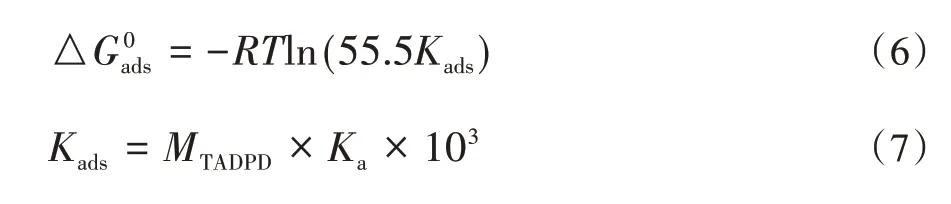
基于式(6)与式(7),结合等温吸附拟合结果,可以计算得到TADPD在Q235钢表面的吸附自由能(ΔG0ads)并列于表2。根据文献[18-19],ΔG0ads小于-20 kJ·mol-1时,缓蚀剂在金属表面的吸附属于物理吸附类型。由表2数据可知,30 ℃条件下1.0 mol/L H2SO4溶液中TADPD的吸附ΔG0ads值为-34.94 kJ·mol-1,在-40 kJ·mol-1~-20 kJ·mol-1之间,这表明TADPD 在Q235 钢表面的吸附类型为物理与化学混合吸附类型[18-20]。

表2 Langmuir吸附拟合参数及吸附自由能
2.3 缓蚀性能影响因素探究
为探究腐蚀体系温度(T,℃)、酸浓度(cH,mol·L-1)和静置时间(t,h)对TADPD 缓蚀性能影响,选用动电位极化曲线法评价TADPD 浓度为200 mg·L-1条件下H2SO4溶液中Q235 钢的缓蚀率,结果如图5 所示。从图5(a)可以看出,温度对TADPD 的缓蚀性能有明显影响。当温度从10 ℃上升到70 ℃时,缓蚀率(IEPPM,%)从98.92% 下降至54.33%,尤其是当腐蚀体系温度超过40 ℃之后,随腐蚀温度上升缓蚀率出现明显下降。腐蚀体系的缓蚀率随温度升高而下降,主要是由于温度上升导致TADPD 在Q235 钢表面的吸附减弱和脱附增强,致使TADPD在Q235钢表面的保护层遭到破坏。
硫酸浓度(cH,mol·L-1)对TADPD 缓蚀性能的影响如图5(b)所示,从图中不难发现,随着酸浓度增加,缓蚀率呈下降趋势。当H2SO4浓度从0.1mol·L-1上升到4.0 mol·L-1时,缓蚀率从99.57% 下降到64.06%。而且当H2SO4浓度从2.0 mol·L-1增加到4.0 mol·L-1时,缓蚀率随H+的增加而急剧下降。缓蚀率随H2SO4浓度增加而降低主要是由于腐蚀液中H+含量随H2SO4浓度增加而增加,这将致使单位时间内与Q235 表面Fe 原子发生腐蚀反应增多,产生的H2量增大,从而导致缓蚀率降低。从图5(c)可以看出,静置时间对缓蚀效果的影响较小,当静置时间从0 h 增加至144 h 时,缓蚀率始终维持在96%~97% 之间基本未发生变化,这说明TADPD 在H2SO4中具有很好的稳定性,可作为长效缓蚀剂。
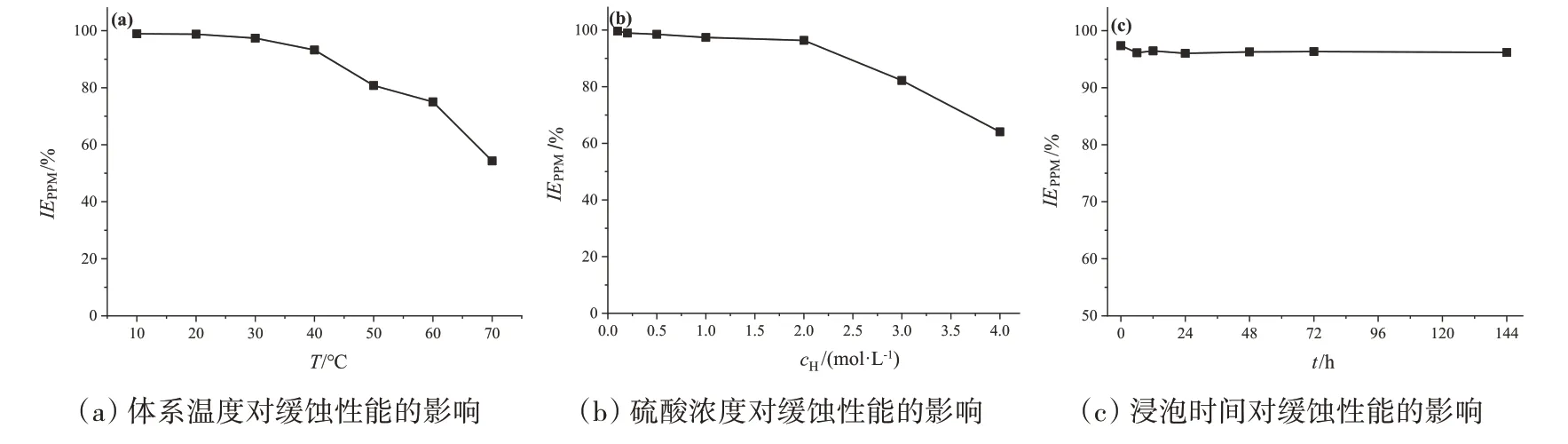
图5 TADPD浓度为200 mg·L-1时腐蚀体系温度、硫酸浓度和浸泡时间对缓蚀性能的影响
3 结束语
本文成功合成了缓蚀性能优异的O,O' -二(对甲苯基)二硫代磷酸三乙醇铵盐(TADPD),TADPD 是一种混合型缓蚀剂,其最高缓蚀率可高达99.05%,TADPD 在Q235 钢表面的吸附符合Langmuir 吸附等温模型;TADPD 的缓蚀率随其浓度升高而增加,随腐蚀体系温度上升和H2SO4浓度增大而下降,受静置时间影响较小,是一种性能优异的酸洗缓蚀剂。
