索磷布韦/维帕他韦治疗慢性丙型肝炎疗效及安全性分析
2021-09-27周毅骏金巧菲刘惠敏
项 波 周毅骏 金巧菲 刘惠敏
亚洲地区约有1000 万人感染慢性丙型肝炎病毒(hepatitis C virus,HCV),中国及东南亚地区总体流行率在0.1%~1.1%[1]。中国最常见的基因分型(GT)为1b 型(约占57%),3b 型相对罕见(约占7%),4型、5 型未见报道[2]。基于上述流行病学特征及GT 情况,世界卫生组织(World Health Organization,WHO)在2018 年提出,新一代直接抗病毒药物(direct acting antivirals,DAAs)要符合全员治疗(treat all)、检测简单(test simple)、治疗简单(treat simple)的“3T”要求,从而最终达到消除丙肝的目的[3]。2018 年12 月,索磷布韦/维帕他韦在中国正式上市。索磷布韦是非结构蛋白(non-structural,NS)5B 抑制剂,可直接抑制HCV 病毒复制。维帕他韦是NS5A 抑制剂,而NS5A 是HCV 复制过程中的必需蛋白。全球注册的临床研究显示,12 周疗程的索磷布韦/维帕他韦显示出良好的耐受性及极高的持续病毒学应答(sustained virologic response,SVR)率,适用于所有GT-1、2、3、6 型的HCV 感染者,无论有无肝硬化、是否经治[4]。因此,索磷布韦/维帕他韦是中国丙型肝炎防治指南(2019 年版)[5]推荐的一线首选治疗药物。本研究对索磷布韦/维帕他韦治疗的23例慢性丙型肝炎患者临床资料进行回顾性分析。
1 资料与方法
1.1 一般资料 回顾性分析2019 年1 月1 日—2019 年12 月31 日在杭州市西溪医院肝病中心门诊及住院使用索磷布韦/维帕他韦治疗的慢性丙型肝炎患者23例。本研究获杭州市西溪医院伦理委员会审核通过,伦理审批号:2020 年(科)伦审第29 号。
1.2 纳入及排除标准 纳入标准:(1)年龄18~80岁;(2)参照丙型肝炎防治指南(2019 年版)[5]确诊为慢性丙型肝炎,包括丙肝相关肝硬化患者;肝硬化的界定标准参照肝纤维化诊断及治疗共识(2019 年)[6],肝脏瞬时弹性测定≥14.6kPa 或客观影像学检查发现肝硬化者均考虑存在肝硬化,再根据childturcotte-pugh(CTP)分级标准分为A 级(代偿期肝硬化)、B~C 级(失代偿期肝硬化);(3)使用索磷布韦/维帕他韦(400mg/100mg)口服,1 片/天,治疗12 周。排除标准:(1)有明显心、脑、肺、肾、造血系统等严重疾病及功能障碍;(2)临床资料不全影响疗效判断;(3)血肌酐清除率≤30mL/min、妊娠、吸毒或同性恋者;(4)依从性差者,包括自行中断服药、服药不规范、服药不连续等。
1.3 研究方案 所有慢性丙型肝炎及代偿期肝硬化患者均服用索磷布韦/维帕他韦(400mg/100mg)治疗12 周,索磷布韦/维帕他韦(400mg/100mg)片为美国Gilead Sciences Ireland UC 产品(批号JX20170309)。分别于治疗第4、12 周及治疗结束后12 周进行随访,检测HCV RNA 水平。
1.4 HCV RNA 及其基因型检测方法 HCV 基因分型检测采用一代测序(试剂为中山大学达安基因股份有限公司产品)。高灵敏度HCV RNA 定量检测采用荧光PCR 法(试剂为湖南圣湘公司产品),PCR 检测仪器型号:ABI3500XL,均按说明书操作。
1.5 疗效评价(1)病毒学应答:评估快速病毒学应答(rapid virologic response,RVR):抗病毒治疗4 周时血清HCV RNA 低于检测下限(<1.18logIU/mL);治疗结束时病毒学应答(end treatment virologic response,ETVR):抗病毒治疗结束时HCV RNA 低于检测下限(<1.18logIU/mL);持续病毒学应答(sustained virologic response,SVR):抗病毒疗程结束后12 周时血清HCV RNA 低于检测下限(<1.18logIU/mL)。(2)血常规、血清生化学、天门冬氨酸氨基转移酶/血小板比值指数(APRI)、基于4 因子的纤维化指数(FIB-4)的变化:分别统计所有患者治疗前及治疗结束后12 周时的总胆红素(TB)、丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)、白蛋白(ALB)、外周血白细胞计数(WBC)和血小板计数(PLT)。分别计算治疗前后APRI和FIB-4 的变化,APRI=(AST/正常上限值)/PLT(109/L)×100,FIB-4=[年龄(岁)×AST(U/L)]/[PLT(109/L)×ALT1/2]。
1.6 安全性评价 观察治疗后血常规、生化的变化,上呼吸道感染、乏力、皮疹等不良反应发生情况。
1.7 统计学方法 应用SPSS 20.0 统计软件进行数据分析。治疗前后的血液学指标采用Shapiro-Wilk正态分布检验,其中年龄、HCV RNA、TB、WBC、PLT符合正态分布,以均数±标准差(±s)表示,两组间比较采用t 检验。ALT、AST、ALB、APRI、FIB-4 不符合正态分布,以中位数(下四分位数,上四分位数)[M(Q1,Q3)]表示,两组间比较采用非参数wilcoxon 检验;分类资料以率(百分数)表示,组间率的比较采用χ2检验。P<0.05 认为差异有统计学意义。
2 结果
2.1 一般资料 治疗结束随访至12 周时失访1例,最终纳入研究22例,其中4例肝硬化患者,男13例,女9例,年龄(44.7±1.0)岁,基线HCV RNA 平均值为6.89logIU/mL,GT-1、2、3、6 型的比例分别为9.1%(2/22)、36.4%(8/22)、31.8%(7/22)、22.7%(5/22),代偿期肝硬化占18.2%(4/22),CTP 评级均为A 级,经治患者占9.1%(2/22),曾治疗方案均为干扰素+利巴韦林。各基因型慢性丙型肝炎患者的基线特征,见表1。

表1 22例慢性丙型肝炎患者各基因型的基线特征
2.2 病毒学应答情况(1)总体情况:22例使用索磷布韦/维帕他韦治疗的慢性丙型肝炎及代偿期肝硬化患者中,治疗4 周后有95.5%(21/22)获得RVR,12 周治疗结束时有100%(22/22)的患者获得ETVR,总体SVR12 率为95.5%(21/22);(2)各基因型情况:GT-1、2、6 型RVR、ETVR 及SVR12 率均为100%,GT-3 型患者RVR 率85.7%(6/7),ETVR 率100%(7/7),但治疗结束12 周后有1 人复阳,故该型SVR12 率为85.7%(6/7)。不同基因型间的RVR 及SVR12 率比较,差异无统计学意义(P>0.05)。见表2。
2.3 GT-3 型患者特征及应答情况(1)GT-3a 型:共4例,均无肝硬化,其中2例联合利巴韦林治疗,总体SVR12 率为100%;(2)GT-3b 型:共3例,全部联合15mg·kg-1·d-1的利巴韦林治疗,治疗失败的1例为伴有代偿期肝硬化且曾使用干扰素联合利巴韦林经治失败的患者,该例患者在服药4 周时并未获得RVR,12 周治疗结束后获得ETVR,停药后随访至12 周,再次复阳,并未获得SVR。
2.4 治疗前后血生化、血常规、APRI 指数、FIB-4 指数水平变化(1)生化指标:与治疗前相比,治疗结束后12 周时TB、ALT、AST 水平较前显著好转(P<0.05),ALB 水平治疗前后无显著差异(P>0.05);②血常规:与治疗前比较,治疗结束后12 周时WBC 水平较前显著好转(P<0.05),PLT 水平治疗前后无显著差异(P>0.05);(3)肝纤维化指标:与治疗前比较,治疗结束后12 周时APRI 指数较治疗前显著好转(P<0.01),FIB-4 指数与治疗前无显著变化(P>0.05)。见表3。
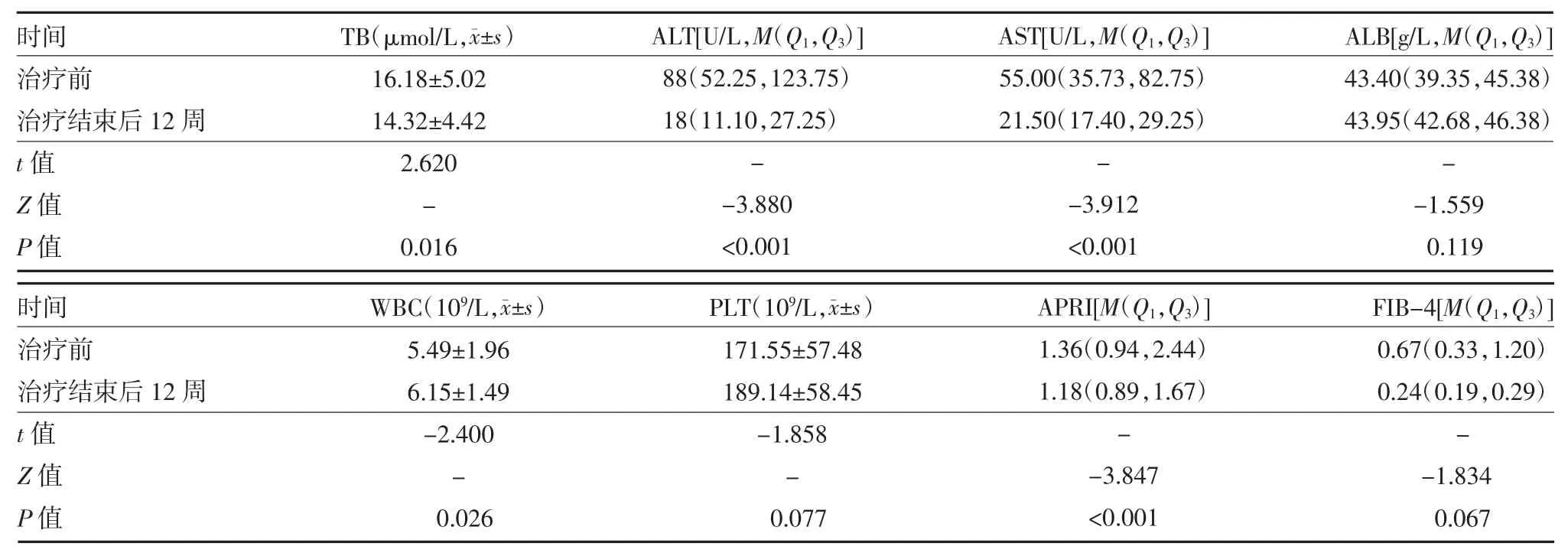
表3 22例慢性丙型肝炎患者治疗前后血生化、血常规、APRI 指数、FIB-4 指数水平变化
2.5 安全性分析 索磷布韦/维帕他韦总体安全性良好,未出现因严重不良反应而停药者,无3~4 级严重不良反应事件。最常见的不良反应事件有乏力(22.7%,5/22),上呼吸道感染(9.1%,2/22),头痛(4.5%,1/22)。上述不良反应持续时间大多较短,均在2 周内自行消失或经对症处理后消失。
3 讨论
索磷布韦/维帕他韦是治疗HCV 感染优选的泛基因型直接抗病毒药物,亚洲38个地区(包括中国、泰国、越南、新加坡、马来西亚)375例患者的Ⅲ期临床试验[7]和中国96例的临床试验[8]均证实,在GT1-6型、初治或经治、合并代偿期肝硬化或无肝硬化的慢性丙型肝炎患者中,其疗效确切,可获得极高的SVR12 率。本研究对我中心2019 年使用索磷布韦/维帕他韦治疗的慢性丙型肝炎患者进行临床疗效及安全性观察。
(1)索磷布韦/维帕他韦治疗各型慢性丙型肝炎患者总体疗效评价:尽管我国以GT-1b 型为主,但因前期索磷布韦/达拉他韦,达拉他韦/阿舒瑞韦等DAA 药物的广泛使用且疗效确切,使得目前慢性丙型肝炎患者多为相对罕见或难治的基因型,我中心以GT-2、3、6 型为主。针对GT-1、2、6 型慢性丙型肝炎患者,无论初治或经治、无肝硬化或代偿期肝硬化,SVR12 率均为100%;针对GT-3 型:我中心的比例达31.8%(7/22),其中3a 型3例(3/7)、3b 型4例(4/7),代偿期肝硬化1例(1/7)。2例(2/4)3a 型及3例(3/3)3b 型患者联合利巴韦林治疗,GT-3 型总体SVR12 率为85.7%(6/7),唯一治疗失败的患者为干扰素+利巴韦林经治的GT-3b 型代偿期肝硬化患者。索磷布韦/维帕他韦治疗12 周后,可显著改善患者APRI 指数,因本研究中大部分为无肝硬化患者,故ALB、FIB-4 指数在治疗前后改善不显著。
(2)索磷布韦/维帕他韦应用于GT-3 型慢性丙型肝炎患者的个体化方案探讨:关于GT-3 型慢性丙型肝炎患者在索磷布韦/维帕他韦基础上联合利巴韦林能否获益更多,西班牙曾开展了一项Ⅲ期临床试验,共纳入了204例GT-3 型慢性丙型肝炎患者,101例单用索磷布韦/维帕他韦,103例联合利巴韦林,结果提示:不联合组的SVR12 率为91%,失败原因主要与NS5A 基线耐药相关替代突变(resistance-associated substitutions,RASs)相关,存在NS5A 基线RASs 的患者SVR12 率达84%;而联合利巴韦林组总体SVR12 率达96%,NS5A 基线RASs 并不影响总体SVR12 率[9]。国内一项真实世界研究也印证了此观点,GT-3 型易治疗失败的原因与基线RASs 相关,其中索磷布韦/维帕他韦疗效不佳的GT-3 型患者中,A30K、Y93H 位点基线RASs 的比例分别为12%、74%[10],其中约99%的GT-3b 型患者存在NS5A 相关位点A30K+L31M RASs[11],此类患者对NS5A 抑制剂维帕他韦应答不佳。因此,对GT-3 型患者开展NS5A 基线RASs 能显著提高SVR12 率。
但德国一项多中心队列研究提出,无论是否联合利巴韦林,索磷布韦/维帕他韦针对GT-3 型HCV感染的疗效和安全性是值得肯定。该研究共纳入了293例GT-3 型患者,其中70%为男性,25.3%有肝硬化,9.2%存在HCV/HIV 共感染,21.8%为经治患者,基线RASs(Y93H、A30K、L31M)率为11.2%。所有患者均使用索磷布韦/维帕他韦治疗12 周,其中5%的非肝硬化患者,58.9%的肝硬化患者加用了利巴韦林。结果提示,总体SVR12 率为95.9%。
基于上述循证证据,针对我中心经治失败的患者,后续可考虑在严密监测肝功能情况下加用蛋白酶抑制剂伏西瑞韦,有条件则先检测NS5A 基线RASs。
(3)索磷布韦/维帕他韦治疗各型慢性丙型肝炎患者安全性评价:其总体安全性良好,治疗过程中无患者因严重的不良反应而退出治疗。在不良反应的监测中,乏力最为常见,但均能在适度休息后缓解,并不影响日常生活;部分患者存在反复呼吸道感染,但对症治疗后均能好转;极少数病例出现头痛。治疗前后TB、ALT、AST 水平较前显著好转(P<0.05),ALB水平治疗前后无显著差异(P>0.05);WBC 水平较前显著好转(P<0.05),PLT 水平治疗前后无显著差异(P>0.05)。
索磷布韦/维帕他韦可安全应用于合并肾功能不全的慢性丙型肝炎患者。最近的一项开放标签研究纳入了59例终末期肾病需要透析的HCV 感染者,29%的患者合并肝硬化,22%为经治患者,92%接受血液透析,9%接受腹膜透析,平均透析时间7 年,经过标准的12 周索磷布韦/维帕他韦治疗后,总体SVR12 率高达95%[12]。国内的一项真实世界研究结果与该研究高度一致[13]。因此,拓宽的临床适应证可让更多患者获益。
综上所述,索磷布韦/维帕他韦在我国治疗各基因型经治或初治、合并代偿期肝硬化或无肝硬化的慢性丙型肝炎患者疗效确切,我中心总体SVR12 率达95.5%,安全性良好,是值得临床推荐的优选抗病毒方案。但仍需重点关注GT-3 型患者,有条件可进行NS5A 基线RASs,联合利巴韦林可提高SVR12率。索磷布韦/维帕他韦在终末期肾病中的应用值得未来进一步深入探索。
