小檗碱对大鼠压力超负荷肥厚心肌组织miR-21-3p表达的影响及其干预心肌肥厚的作用机制
2021-09-23刘盛祥黄宇鹏杨国康金红艳
刘盛祥,黄宇鹏,杨国康,金红艳
心肌肥厚是心肌细胞为克服增高的压力负荷,保证心脏充足射血量的一种代偿性反应,长期、严重的心肌肥厚引起心肌结构及功能的失代偿,最终导致心律失常、心力衰竭及猝死等不良心血管事件的发生[1]。小檗碱是一种从植物中提取的异喹啉类生物碱,具有一定的抗心肌肥厚作用,但其在心肌肥厚中的具体分子机制尚不明确[2]。微小RNA(micro RNA,miRNA)是内源性小分子非编码RNA,大量研究证实,miRNA在心肌肥厚中发挥着关键作用[3-4]。本研究为证实小檗碱在抗心肌肥厚中的作用是否与miRNA相关,构建压力负荷诱导下的大鼠心肌肥厚模型,探讨小檗碱对心肌肥厚的影响及其可能机制,报道如下。
1 材料与方法
1.1 材料 (1)实验动物:SPF级健康雄性SD大鼠36只,8~10周龄,体质量160~200 g,由武汉科技大学实验动物中心提供,动物许可证为SYXK(新)2016-003、合格证为SCXK(新)2016-0002。(2)药物及试剂:盐酸小檗碱(上海阿拉丁生化科技股份有限公司),一抗AKT、p-AKT、GSK3β、p-GSK3β及内参GAPDH(北京科海瑞嘉生物科技有限公司),BCA蛋白定量试剂盒、SDS-PAGE凝胶制备试剂盒、反转录试剂盒、荧光定量试剂盒(赛默飞世尔科技有限公司)。(3)仪器设备:飞利浦HD11 XE超声诊断仪(德国Philips公司)、移液枪(德国Eppendorf公司)、实时荧光定量PCR仪(美国赛默飞世尔科技有限公司)、凝胶成像仪(美国Protein Simple公司)。
1.2 实验方法 2019年6月—2020年9月于武汉科技大学实验动物中心进行实验。心肌肥厚模型的构建:SPF级雄性SD大鼠36只,采用随机数字表法分为假手术组、模型组及小檗碱组,每组12只。模型制备方法参照文献[5],大鼠腹腔注射2.5%戊巴比妥麻醉,分离肌肉及组织,游离腹主动脉,模型组大鼠挂线结扎腹主动脉,超声多普勒检测腹主动脉达到70%狭窄视为造模成功;假手术组只暴露腹主动脉后关腹不做任何处理;小檗碱组大鼠在模型组基础上予以小檗碱100 mg·kg-1·d-1灌胃处理,假手术组及模型组给予等剂量的生理盐水灌胃处理。术后40 d用2.5%戊巴比妥钠麻醉大鼠后行心脏超声检测,完毕后立即取出心脏备用。
1.3 观测指标与方法
1.3.1 心脏超声指标检测:麻醉大鼠后使用高频超声诊断仪检测各组大鼠的心脏指标,包括左心室舒张末期后壁厚度(LVPWT)、左心室舒张末期内径(LVEDD)、左心室射血分数(LVEF)。
1.3.2 心体质量比检测:取出大鼠心脏后,清除心腔血液,预冷的生理盐水清洗心腔,用滤纸吸干水分后,计算心体质量比(心脏质量/体质量)。
1.3.3 心肌组织miR-21-3p、ANP、BNP基因表达:采用RT-qPCR方法检测。以Trizol法从大鼠心肌组织中提取总RNA,通过反转录试剂盒将RNA反转录为cDNA,取2 μl产物在荧光定量PCR仪器中扩增。总反应体系为20 μl,扩增步骤如下:95℃预变性30 s、95 ℃变性5 s,60℃扩增30 s,反复40个循环后进行解离:95℃持续5 s、60℃持续60 s。心房钠尿肽(ANP)、脑钠肽(BNP)表达检测以GAPDH为内参,miR-21-3p表达检测以U6为内参,引物序列见表1。

表1 RT-qPCR引物序列
1.3.4 心肌组织AKT、p-AKT、GSK3β和p-GSK3β蛋白表达检测:用含有1%蛋白酶抑制剂的裂解缓冲液裂解心肌组织,研磨匀浆后4 ℃下离心获得全蛋白质,每个样品取等量的蛋白质(20 μg)用10%凝胶进行免疫印迹,然后将其转移到PVDF膜上,用含5%脱脂牛奶的TBST封闭,加入相应比例稀释的一抗(目的基因AKT、p-AKT、GSK3β、p-GSK3β及内参GAPDH稀释比例均为1∶1 000),在4℃摇床孵育过夜;次日用TBST将膜洗涤3次,并用对应的二抗孵育1 h,用TBST洗涤3次后配制ECL发光反应液,置于凝胶成像系统中观察蛋白的表达情况 。

2 结 果
2.1 3组大鼠心脏超声指标比较 与假手术组比较,模型组 LVPWT增加(t/P=4.811/0.001), LVEDD、LVEF减小(t/P=5.303/0.001、5.855/0.000)。与模型组比较,小檗碱组大鼠LVPWT减小(t/P=2.864/0.021),LVEDD、LVEF增加(t/P=4.518/0.002、2.841/0.022),见表2。
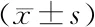
表2 3组大鼠心脏超声指标比较
2.2 3组大鼠心体质量比比较 与假手术组比较,模型组大鼠心脏质量、心体质量比均增加(t/P=6.704/0.000、9.664/0.000)。与模型组比较,小檗碱组大鼠心脏质量、心体质量比减小(t/P=3.929/0.004、3.866/0.005)。3组大鼠体质量比较,差异均无统计学意义(P>0.05),见表3。
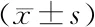
表3 3组大鼠心脏质量、体质量比较
2.3 3组大鼠心肌组织中ANP、BNP及miR-21-3p表达比较 与假手术组比较,模型组大鼠心肌组织ANP、BNP、miR-21-3p表达水平明显上调(t/P=17.043/0.000、22.445/0.000、24.254/0.000);与模型组比较,小檗碱组大鼠心肌组织ANP、BNP、miR-21-3p表达水平显著下调(t/P=8.845/0.000、9.514/0.000、15.376/0.000),见图1。
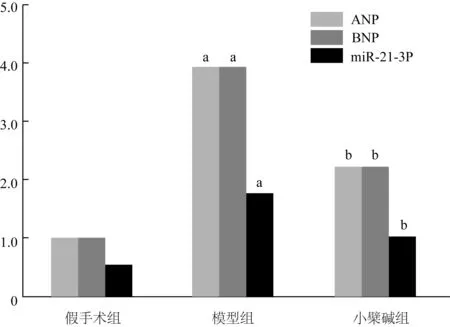
注:ANP.心房钠尿肽;BNP.脑钠肽;miRNA-21-3p.微小RNA-21-3p。与假手术组比较,aP<0.05;与模型组比较,bP<0.05
2.4 3组大鼠心肌组织中AKT、GSK3β蛋白及磷酸化水平比较 与假手术组比较,模型组大鼠心肌组织p-AKT、p-GSK3β蛋白水平显著上调(t/P=22.767/0.000、28.647/0.000);与模型组比较,小檗碱组大鼠心肌组织p-AKT及p-GSK3β蛋白水平显著下调(t/P=20.090/0.000、27.945/0.000),而3组大鼠AKT、GSK3β的蛋白表达水平比较差异无统计学意义(P>0.05),见图2。
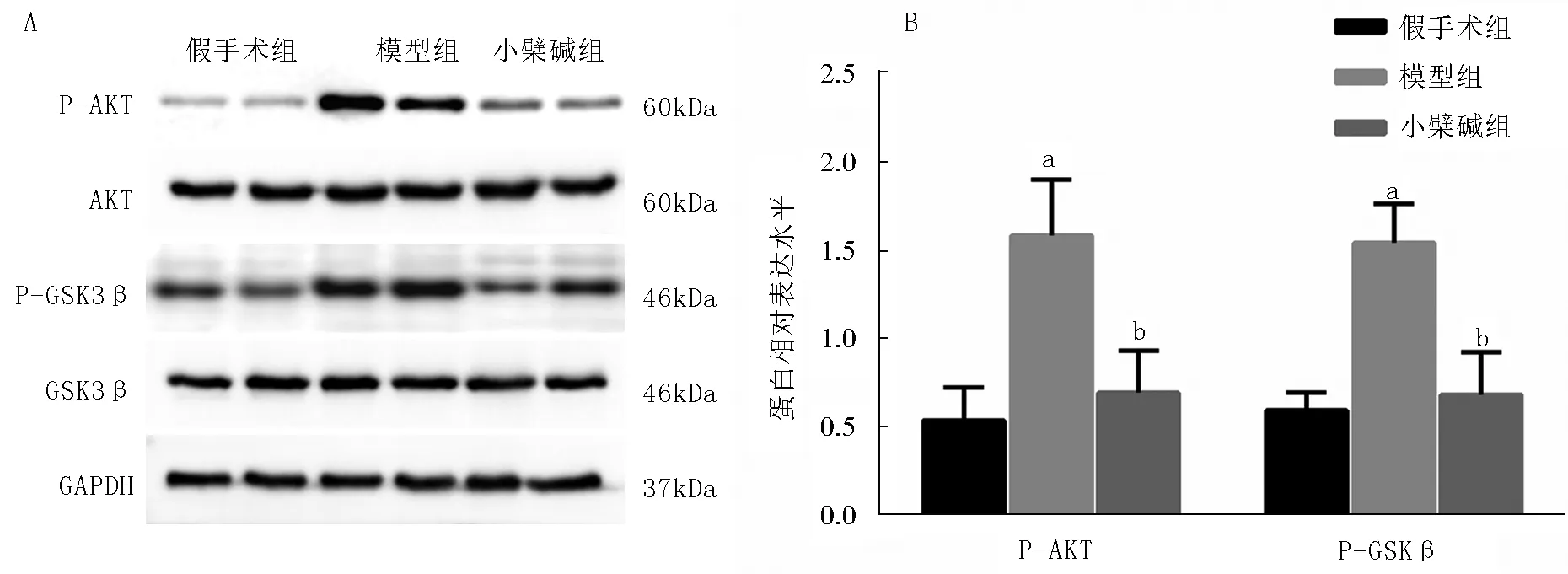
注:A.蛋白表达免疫印迹图;B.蛋白定量表达比较。与假手术组比较,aP<0.05;与模型组比较,bP<0.05
3 讨 论
心肌肥厚是指心肌组织应对心脏负荷的一种代偿性反应,早期肥大的心肌细胞可以减轻心室壁的压力维持足够的心排出量,但长期持续的高负荷状态最终引起心脏失代偿,导致心室的收缩及舒张功能障碍,最终发展成心力衰竭[6]。心肌肥厚包括心肌细胞的体积增大及心肌间质细胞的增生,多个基因及信号通路参与心肌肥厚的过程[7],但其具体机制尚未阐明。虽然有研究证实,神经体液机制参与了心肌肥厚的过程,但是对晚期心力衰竭患者的症状控制及远期预后的治疗依旧欠佳。因此,探究心肌肥厚的发病过程及其具体的作用机制,寻找针对心肌肥厚的潜在作用靶点,减轻心脏失代偿等并发症的发生,延缓心力衰竭的进展具有重要的临床意义。
miRNA是一种内源性非编码小RNA,大量的证据表明,miRNA在心肌肥厚过程中发挥着重要作用,成为治疗心肌肥厚的潜在生物靶点[3, 8-9]。miR-1通过抑制Hand2的表达,以及抑制胰岛素样生长因子(IGF1)和细胞外基质重构因子Twf1的活性来防止心肌肥厚[10]。miR-223通过靶向心肌肌钙蛋白I作用激酶(TNNI3K),拮抗ECE-1或主动脉缩窄(TAC)诱导的心肌肥厚[11]。研究发现,在TAC或其他方式诱导的心肌肥厚模型中miR-21表达明显上调[12],作为miR-21的互补序列miR-21-3p是否在心肌肥厚模型发挥作用尚未明确。笔者构建了心肌肥厚模型,发现miR-21-3p在压力负荷诱导的心肌肥厚模型中同样表达上调。同样在Yan[13]的研究中发现,miR-21-3p在TAC术后4周的心力衰竭模型中表达增高,而在TAC术后2周的心肌肥厚模型中表达下调,提示miR-21-3p在心肌肥厚不同阶段发挥不同的作用。本研究中在腹主动脉缩窄术40 d后发现miR-21-3p的表达水平上调,且反映心力衰竭的特殊标志物ANP及BNP表达水平同样上调,提示本研究运用腹主动脉缩窄法构建的心肌肥厚模型为心力衰竭模型,这一表型与Yan等[13]在TAC术后4周的表型基本一致。
小檗碱是一种从植物中提取的异喹啉类生物碱,具有一定的抗心肌肥厚作用[2],其可能通过调节Rho/ROCK信号途径及其底物磷酸化水平达到改善心肌肥厚的目的,而在本研究中发现,小檗碱通过抑制miR-21-3p水平从而抑制AKT/GSK3β信号通路达到抗心肌肥厚的作用。本研究发现在构建心肌肥厚模型40 d后,经小檗碱处理后大鼠心脏质量、心体质量比、左心室舒张末期后壁厚度减小,左心室舒张末期内径、左心室射血分数增加,提示在压力负荷诱导的心肌肥厚模型中小檗碱能够抑制心肌肥厚、改善心功能。更重要是的,经小檗碱处理后miR-21-3p的表达水平明显下调,提示小檗碱抑制心肌肥厚的作用可能与miR-21-3p的表达相关,且与这种表达呈负相关关系。AKT信号通路是心肌肥厚发生及发展过程中的关键因子,其下游靶点GSK3β同样参与了这一过程[14-15]。研究发现miR-21-3p依赖HDAC8调控AKT/GSK3β信号通路参与心肌肥厚过程[13]。本研究发现,心肌肥厚模型经小檗碱处理后miR-21-3p表达水平明显下调,而且AKT及GSK3β磷酸化水平较模型组明显下调,进一步证实了小檗碱可能通过抑制AKT/GSK3β信号通路抑制心肌肥厚。然而本研究未检测心肌肥厚模型中HDAC8的表达水平,不能确认小檗碱是否也依赖HDAC8发挥作用,为接下来研究小檗碱的抗心肌肥厚作用机制提供了新的思路。
综上所述,本研究在动物模型水平提示了小檗碱通过AKT/GSK3β信号通路抑制心肌肥厚,且这一作用与miR-21-3p的表达相关,为临床治疗心肌肥厚提供了新的思路。
利益冲突:所有作者声明无利益冲突
作者贡献声明
刘盛祥:课题设计及文章撰写;黄宇鹏:数据获取及统计分析;杨国康:收集资料及论文修改;金红艳:课题指导
