静态顶空气相色谱法测定酒中的乙酸乙酯和己酸乙酯
2021-09-01何焜鹏
◎ 何 靖,何焜鹏
(1.广东省食品工业公共实验室,广东 广州 511442;2.广东省食品工业研究所有限公司,广东 广州 511442;3.广东省食品质量监督检验站,广东 广州 511442)
中国酒文化源远流长,制酒历史悠久。酒由谷物、水果等发酵酿制而成[1],按生产工艺主要分为蒸馏酒、发酵酒和配制酒。酒的主要成分是乙醇和水,而溶于其中的醇、醛、酸和酯等化合物作为酒的香味物质[2]。酯类化合物在酒中具有芳香型,是酒体芳香形成的主要原因[3]。其中乙酸乙酯在各种香型白酒中含量占比大,在白酒香气成分扮演主要角色。不同酯类含量的高低决定了白酒的香型,如清香型白酒是以乙酸乙酯为主体香味成分的白酒,浓香型白酒的主体香味成分是己酸乙酯,而凤香型白酒则以乙酸乙酯及己酸乙酯为主体。各白酒的特征香气成分虽不尽相同,但都由酯类物质作为特征香味。
目前测定乙酸乙酯和己酸乙酯主要采用气相色谱法。现国标《白酒分析方法》(GB/T 10345—2007)中明确了乙酸乙酯和己酸乙酯的分析方法,采用气相色谱内标法进行测定;黄伟等[4]采用内标法与外标法对白酒中乙酸乙酯含量进行了比较;也有文献探究了红外光谱组合区间偏最小二乘法定量白酒中乙酸乙酯的含量[5]。鉴于目标化合物沸点低,易挥发,本文采用静态顶空色谱法测定酒中乙酸乙酯和己酸乙酯。酒在酿制过程中除了产生特征香味物质[6]还产生不易挥发物质,如氨基酸、维生素、有机酸、肉豆蔻酸、硬脂酸以及棕榈酸等[7],顶空进样有利于消除基质干扰,减少污染物进入色谱系统,且操作简单,灵敏度高,容易实现。
1 材料与方法
1.1 仪器与试剂
Agilent 7890B气相色谱仪配置FID检测器(安捷伦科技有限公司)、G1888顶空进样器(安捷伦科技有限公司)、十万分之一天平(奥豪斯(常州)有限公司)。
标准品:乙酸乙酯(99.7%,Dr.Ehrenstorfer)、己酸乙酯(100%,CNW),乙醇(色谱纯,霍尼韦尔公司),超纯水(一级,Milli-Q),实验中的酒样均购买于当地超市。
1.2 试验方法
1.2.1 溶液配制
40%乙醇溶液:移取200 mL无水乙醇于500 mL容量瓶中,用超纯水定容至刻度线,混匀待用。
95%乙醇溶液:移取95 mL无水乙醇于100 mL容量瓶中,用超纯水定容至刻度线,混匀待用。
标准储备液的配制(5 mg·mL-1):分别准确称量乙酸乙酯、己酸乙酯各0.1 g(精确到0.000 01 g),置于两个20 mL容量瓶中,用95%乙醇溶液定容至刻度线,摇匀。
标准工作曲线的配制:分别准确吸取乙酸乙酯标准储备液和己酸乙酯标准储备液0.10 mL、0.25 mL、0.50 mL、1.25 mL和2.50 mL于25 mL容量瓶,用40%乙醇溶液稀释至刻度线,得到浓度分别为20 mg·L-1、50 mg·L-1、100 mg·L-1、250 mg·L-1和500 mg·L-1的 标准混合工作曲线。准确移取5.00 mL于顶空瓶中,压盖密封,上机测定。
1.2.2 样品前处理
将酒样混匀,从中准确移取5.00 mL于20 mL顶空瓶,密封顶空瓶盖,待测。
1.2.3 气相色谱条件
色谱柱:CP-Wax 57(50 m×0.25 mm×0.2 μm);柱温升温程序:初温40 ℃保持3 min以5 ℃·min-1的速率上升至100 ℃保留1 min;进样口:温度200 ℃;进样量1 mL,分流进样,分流比5∶1,分流流量为7.5 mL·min-1;氢火焰离子化检测器(FID):温度300 ℃,氢气40 mL·min-1,空气400 mL·min-1,尾吹30 mL·min-1;载气:高纯氮气,尾吹25 mL·min-1;色谱柱流量1.5 mL·min-1。顶空条件:平衡条件,平衡温度60 ℃,定量环温度70 ℃,传输线区温度80 ℃。
2 结果与分析
2.1 标准工作曲线配制溶液的选择
样品直接上顶空测定,为准确定量,理论上标液所处顶空瓶的基质环境应与样品的基质环境保持相似,因此优先选用与样品酒精度相仿的乙醇溶液进行标准工作曲线的配制。
不同类型的酒酒精度各不相同,葡萄酒酒精度在8%Vol~15%Vol,啤酒酒精度在3%Vol~5%Vol,果味米酒酒精度约10%Vol,大部分白酒酒精度在30%Vol~40%Vol。样品酒精度范围广,配制一条曲线无法覆盖酒中所有基质情况。用乙醇含量低的溶液配制曲线容易出现乳化现象,造成乙酸乙酯和己酸乙酯溶解不充分,用乙醇含量过高的溶液配制曲线,与酒样环境有差异,造成目标化合物在标曲和酒样的溶解和挥发程度不一致,难以准确定量。最终选用40%乙醇溶液作为曲线的配制溶液。40%乙醇溶液能充分溶解乙酸乙酯和己酸乙酯,且与大部分酒的基质环境相似,配制出的曲线线性关系较好,线性系数均在0.999以上。
2.2 色谱柱的选择
本方法采用非极性、中极性和强极性色谱柱对乙酸乙酯和己酸乙酯的出峰情况进行比对,混标配制浓度为100 mg·L-1,分别使用DB-1(30 m×0.25 mm×0.25 μm)、DB-17(30 m×0.25 mm×0.25 μm)和DB-Wax(30 m×0.25 mm×0.25 μm)3条不同极性色谱柱,在1.2.3的色谱条件下运行100 mg·L-1混标标点,探究其出峰情况。因乙酸乙酯和己酸乙酯的极性较强,使用非极性色谱柱DB-1和中等极性DB-17得到的目标峰峰型较差,不能很好地保留化合物。而DB-Wax极性较强,与乙酸乙酯、己酸乙酯极性相似,能使乙酸乙酯和己酸乙酯得到较强保留和实现分离,因此选用极性色谱柱。
在实际试验测定白酒的乙酸乙酯、己酸乙酯时,发现白酒中乙酸乙酯和乙缩醛保留时间几乎完全重合,采用调低初温、减缓升温速率等方法让其实现分离,效果不甚理想。选用有更好分离优势的极性色谱柱,发现使用CP-Wax 57能将乙酸乙酯和乙缩醛分离开,且分离效果较好,目标峰峰型对称尖锐,响应值大,使用该柱子得到的目标化合物色谱图见图1。
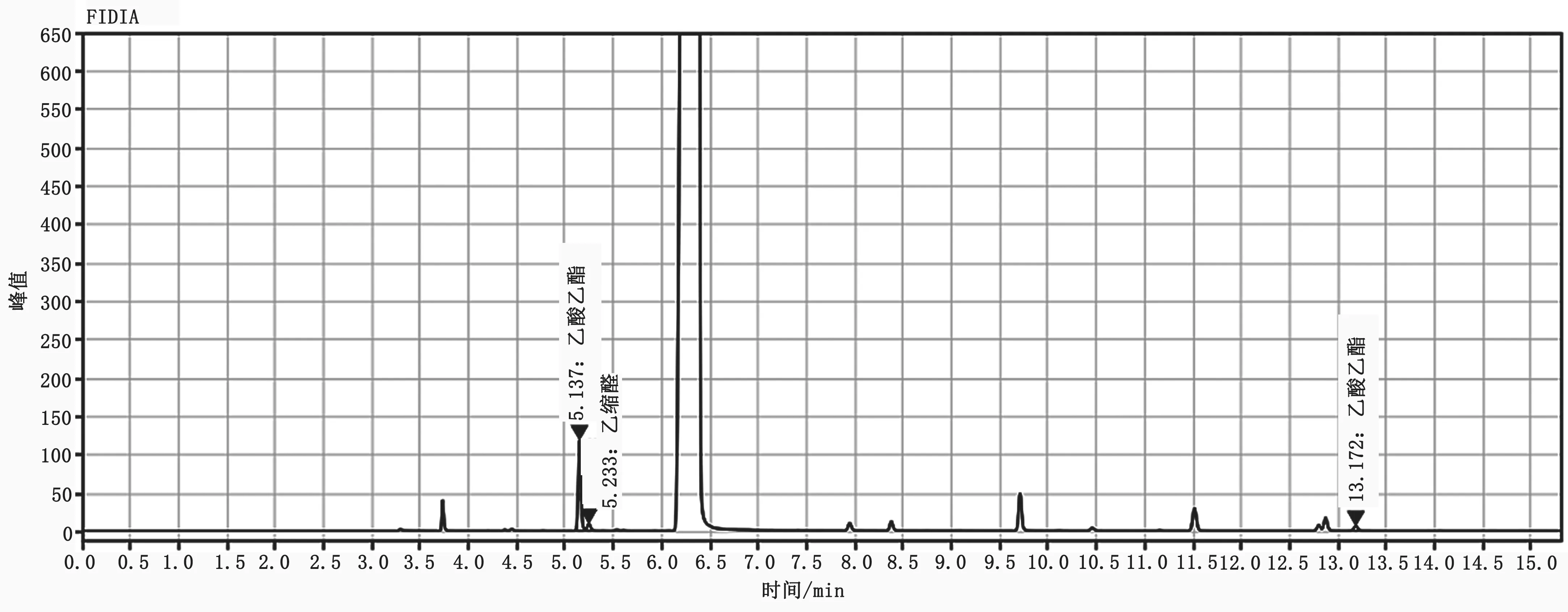
图1 CP-Wax 57测定白酒的气相色谱图
2.3 顶空平衡温度与平衡时间的探究
顶空平衡温度越高,有机物挥发程度越高,目标化合物含量的增加可以提高响应值和仪器灵敏度。由于样品主要成分是水和乙醇,如果设置平衡温度过高,顶空瓶瓶压升高或样品沸腾,容易造成顶空瓶内气体泄漏或顶空瓶破裂等情况,故本试验选取50 ℃、60 ℃、70 ℃和80 ℃作为平衡温度,配制100 mg·L-1标准浓度点,控制顶空平衡时间为30 min,检测被测物质的响应值,以探究本实验合适的顶空平衡温度。测试结果发现随着温度升高,被测物响应值增大,在60 ℃以后响应值增速减缓并趋于稳定。由于酯类物质沸点较低,为防止爆沸,最终选择60 ℃作为最优平衡温度。
控制顶空平衡温度为60 ℃,考察标准浓度点在平衡时间为20 min、30 min、40 min和50 min时被测物响应值的大小,用于探究合适的顶空平衡温度。结果显示,随着平衡时间延长,被测物响应增大,当平衡时间超过30 min,被测物响应值几乎不再增大,且平衡时间过长可能造成酯类物质的热分解,因此选择30 min作为平衡时间。
综上,本方法以平衡温度60 ℃,顶空平衡30 min作为最优顶空条件。
2.4 线性范围及检出限
以标准工作液浓度为横坐标,化合物峰面积为纵坐标,绘制校正曲线。乙酸乙酯线性回归方程为Y=0.770 7X+1.074 4,线 性 拟 合R=0.999 96;己酸乙酯线性回归方程为Y=0.727 9X+3.621 9,线性拟合R=0.999 57。结果表明乙酸乙酯和己酸乙酯在20~500 mg·L-1线性关系良好,线性系数均在0.999以上。逐级稀释标准品储备液,以信噪比S/N=3时的浓度为本方法的检出限,得到乙酸乙酯检出限为0.8 mg·L-1,己酸乙酯检出限为1.0 mg·L-1。
2.5 样品加标回收实验和重复性实验
从商场购得多种酒样,按照1.2方法,在3个不同添加水平下进行加标回收实验和精密度实验,以考察乙酸乙酯和己酸乙酯的加标回收率和精密度情况,结果见表1。平均回收率在93.9%~104.0%,精密度在4.0%以下(n=6)。
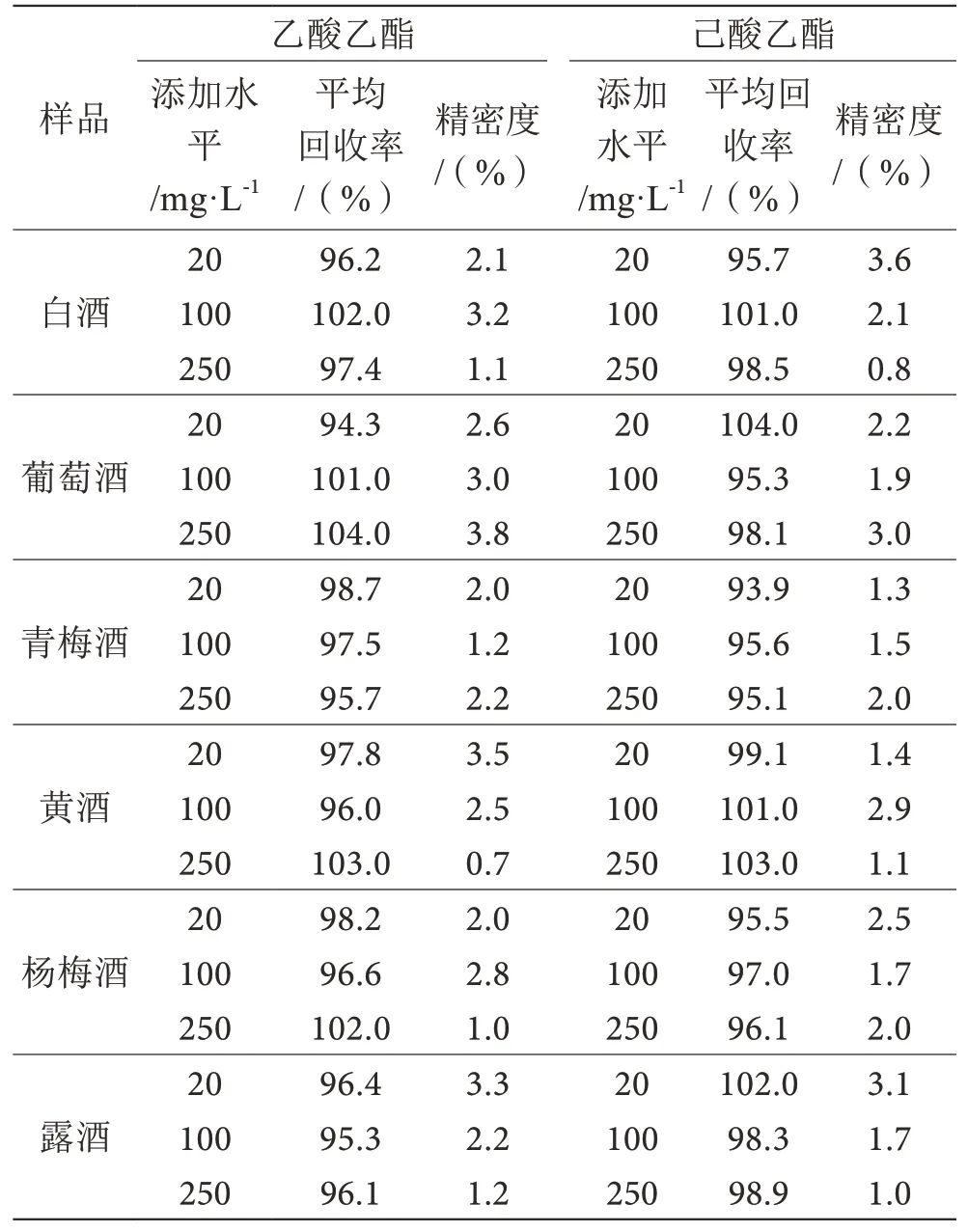
表1 不同酒样不同添加浓度下乙酸乙酯、己酸乙酯的回收率和精密度表(n=6)
2.6 实际样品测定
从商场购得多种酒样,能覆盖到酒的类别尽可能多,按照1.2的方法对样品进行测定。具体结果见表2。由表2可知,酒中检出乙酸乙酯含量基本在200 mg·L-1以上。己酸乙酯检出率较低,只有以己酸乙酯和乙酸乙酯为主体的凤香型白酒检出己酸乙酯含量较高,该酒符合国家标准GB/T 14867—2007一级低度凤香型白酒的限值要求。

表2 不同基质的酒乙酸乙酯、己酸乙酯的测定值表
3 结论
本文采用静态顶空进样方式测定各种酒中乙酸乙酯和己酸乙酯含量,对色谱柱的选择、顶空条件的确定、样品回收率及稳定性等方面进行探究。本方法采用标准曲线进行定量,较《白酒分析方法》(GB/T 10345—2007)中的单点校正的定量更加准确,且适用范围广,不仅限于白酒,还适用于成分复杂的配制酒、果酒、中药保健酒等。静态顶空进样可以减少各种基质中脂类、糖分、蛋白质等非挥发性物质对色谱系统的污染,且得到的目标化合物在峰宽、峰型、基线平稳度等方面更具有优势。本方法目标化合物的相关性良好、检出限低、样品的加标回收好、精密度好,实验过程简单,适用于各种酒中乙酸乙酯、己酸乙酯含量的测定。
