肠气囊肿症2例并文献复习
2021-07-06王倩倩周元琛尹腾飞姚树坤
王倩倩,周元琛,尹腾飞,姚树坤
例1,女,75岁,因腹胀3个月,腹泻1周于2020年8月10日入院。患者3个月前无诱因出现腹胀,持续不缓解,近1周出现腹泻,8~9次/d,呈稀糊便。既往2019年6月10日因非特异性间质性肺炎行左肺移植手术,术后规律服用醋酸泼尼松片、他克莫司及吗替麦考酚酸酯。查体:T 36.6℃,P 78次/min,R 18次/min,BP 136/78 mmHg,恶病质状态。右肺呼吸音低,腹部膨隆,上腹与下腹部轻压痛,叩诊呈鼓音,肠鸣音5次/min。实验室检查:血WBC 6.63×109/L,RBC 3.32×1012/L,PLT 213×109/L,Hb 108g/L,ALB 33.5g/L,BNP 169.4 pg/ml,肿瘤标志物细胞角蛋白19片段(CYFRA21-1)6.31 ng/ml,自身免疫抗体均阴性。胸腹部CT示:右颈部及纵隔气肿,腹腔大量游离积气(图1)。经多学科会诊后,诊断为肠气囊肿症、自发性气腹,并予改变饮食结构、调节肠道菌群等治疗。治疗7 d后,腹胀较前减轻,大便次数较前减少。
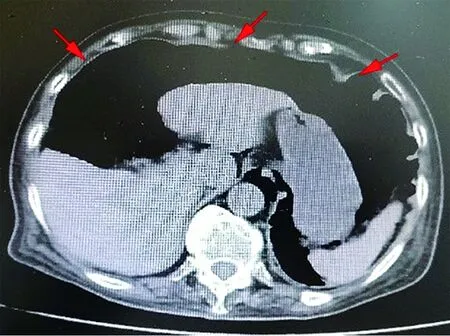
图1 例1腹部CT示腹腔大量游离积气
例2,男,30岁,因上腹胀、嗳气1年余于2020年8月16日入院。患者1年余前无诱因出现上腹胀、嗳气,多于餐后出现,自发病以来,体质量下降16 kg。既往体健。查体:T 36.5℃,P 66次/min,R 15次/min,BP 106/70 mmHg,营养中等。腹平软,全腹无压痛,肝脏于剑突下3 cm,质韧,表面光滑。实验室检查:血WBC 5.32×109/L,RBC 3.65×1012/L,Hb 124 g/L,PLT 305×109/L,ALT 54 IU/L,前白蛋白162.7 mg/L,TG 2.26 mmol/L,肿瘤标志物及自身抗体均阴性。结肠镜检查:回盲部及升结肠可见散在黏膜下隆起,透明,呈囊性改变,活检后黏膜隆起可变小(图2)。腹盆增强CT+小肠重建:升结肠肠壁间可见气体密度影(图3)。诊断为结肠气囊肿症,予改变饮食结构、调节肠道菌群等治疗。治疗20 d后随访,餐后腹胀较前缓解。
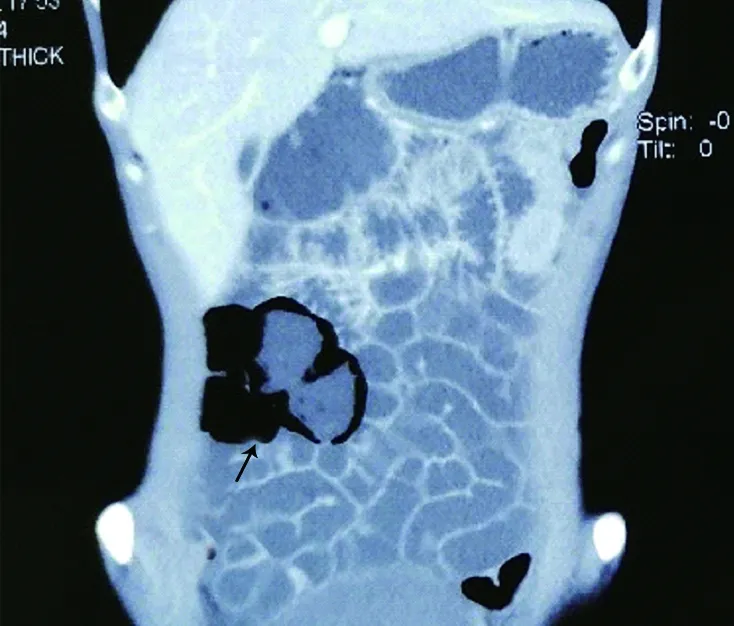
图3 例2腹部CT冠状面+小肠重建示
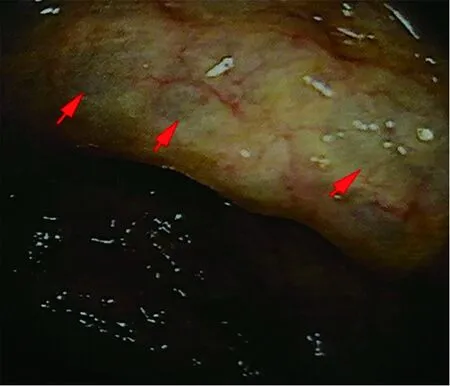
图2 例2结肠镜示升结肠黏膜下隆起
讨 论肠气囊肿症(pneumatosis cystoides intestinalis,PCI)是指肠壁黏膜下或浆膜下单发或多发含气囊肿为特征的一种疾病,常累及结肠和小肠,临床少见,容易误诊。本病的总体发病率约为0.03%,可发生于任何年龄,中青年男性多见,男女比例2.4∶1,在我国高原地区报道较多[1-3]。
该病病因和发病机制尚不明确,可能的发病机制:(1)机械学说,肠黏膜屏障受损、通透性增加、肠腔内压力升高;(2)细菌学说,产气细菌进入肠壁产生气体引起肠气囊肿;(3)肺源性学说,肺泡内压力升高,肺泡破裂,形成纵隔气肿,气体沿血管周围间隙到达肠系膜及肠壁浆膜下,形成肠气囊肿;(4)其他因素包括药物(如α葡萄糖苷酶抑制剂、糖皮质激素、免疫抑制剂)、自身免疫性疾病、器官移植等。
该病缺乏特异性的临床表现,多表现为腹胀、腹泻、腹痛等非特异性消化道症状,严重者可表现为急腹症、脓毒性休克等[3]。并发症包括自发性气腹、肠出血、肠穿孔及门静脉系统气体栓塞等,极少有癌变风险[2, 4]。
目前尚未形成统一的诊断标准。常用的诊断方法包括:(1)腹部CT,肺窗观察积气征象更直观,可以清楚显示气囊肿的部位、大小、形态及累及范围[5];(2)结肠镜,可表现为单发或多发囊性结构突向肠腔,气囊壁透明,活检钳触之有明显弹性感,夹破后气囊肿塌陷[4];(3)超声内镜,有研究推荐将超声内镜作为无创诊断的首选方法[6],可表现为黏膜下或浆膜下的囊状低回声区,局部肠壁分界不清;(4)病理学,活检病理可见局灶性囊状结构,伴有多核巨细胞及其他炎性改变[3]。
治疗包括改变饮食结构、去除病因、高压氧治疗、药物治疗,必要时内镜或手术治疗。若无特殊临床表现,可先通过改变饮食结构,避免进食产气类(如豆制品)、生冷油腻食物,密切观察。非手术治疗症状缓解率可达70%[3],必要时可予活检钳夹破囊壁排气、硬化剂或无水酒精注射等内镜下治疗。
综上,PCI是一种病因、病机尚不清楚的疾病,多由于腹胀、腹泻等非特异性症状就诊,易与肠息肉、肠癌或炎性肠病混淆,诊断主要依靠腹部CT、超声内镜和结肠镜检查。治疗包括高压氧治疗、药物治疗、内镜治疗和手术。应个体化分析,避免不必要的手术。如无严重并发症,总体预后良好。
