利拉鲁肽对肥胖型糖尿病患者空腹血糖、餐后2 h血糖、糖化血红蛋白水平产生的影响
2021-04-30王晶璞卢燕王会杨娅娟
王晶璞 卢燕 王会 杨娅娟
随着我国社会经济水平的不断提高,人们的生活及饮食习惯也发生了巨大改变,导致糖类、脂类的摄入量明显增加,而日常活动、运动明显减少,糖尿病的发病概率随之上升,且呈现低龄化趋势发展,引起了公共卫生领域的广泛关注。2型糖尿病是成年人主要的糖尿病类型,约占糖尿病发病的90%以上[1]。临床研究显示,2型糖尿病的发生发展与患者体内血糖浓度过高有关,常合并糖代谢及脂代谢紊乱。临床统计显示,约80%的2型糖尿病患者存在超重或肥胖。而体重的增加是大多数传统降糖药物在治疗过程中不可避免的不良反应,是肥胖2型糖尿病患者血糖达标的主要障碍。同时,肥胖2型糖尿病患者发生脂肪肝、心脑血管疾病的概率明显升高,已成为心血管疾病的独立危险因素[2]。因此,如何控制肥胖2型糖尿病患者的血糖及体重,是临床需要解决的问题。利拉鲁肽为新型肠促胰素类药物,是一种人胰高血糖素样肽-1类似物(GLP-1),能改善胰岛β细胞功能,稳定血糖水平,降低低血糖发生率,还具有调脂作用,可降低体重指数(BMI),且无明显肝脏毒性作用[3]。本研究进一步分析利拉鲁肽对肥胖型糖尿病患者空腹血糖(FPG)、餐后2 h血糖(2hPG)、糖化血红蛋白(HbA1c)水平产生的影响,报告如下。
1 资料与方法
1.1 一般资料 选择2017年1月至2019年1月在我院内分泌科治疗的肥胖型2型糖尿病患者81例,随机分为2组。观察组41例,男25例,女16例;年龄30~68岁,平均年龄(45.2±8.4)岁;体重指数(BMI)28~35 kg/m2,平均(30.8±2.9)kg/m2。对照组40例,男21例,女19例;年龄29~67岁,平均年龄(45.6±8.3)岁;BMI 28~35 kg/m2,平均(30.9±2.7)kg/m2。2组的年龄、性别比、病程、BMI等差异无统计学意义(P<0.05),具有可比性。本研究经医院医学伦理委员会批准,所有患者知情同意,自愿加入研究。
1.2 纳入与排除标准
1.2.1 纳入标准:患者均符合中华医学会糖尿病学分会制定的《中国2型糖尿病防治指南(2017年版)》[4]中2型糖尿病诊断标准;HbA1c≥7%,BMI≥25 kg/m2,腰围:男>90 cm,女>85 cm,均属于肥胖型2型糖尿病;患者心肝肾功能均正常。
1.2.2 排除标准:合并严重糖尿病并发症者;合并其他内分泌相关肿瘤或炎症者;近半年内使用GLP-1 类似物及胰岛素者;长期接受激素治疗者;合并心肝肾等主要脏器严重器质性疾病者。
1.3 方法 对照组使用常规治疗,指导患者合理饮食、积极运动锻炼、学会日常自我监测血糖,对可能出现的不良反应给予指导,服用二甲双胍片(北京双鹤现代医药技术有限责任公司),1 g/次,2次/d,整个治疗期间剂量保持不变[5]。在此基础上,观察组使用利拉鲁肽治疗,利拉鲁肽注射液(丹麦Novo Nordisk A/S),皮下注射,起始剂量0.6 mg,1次/d,要求患者每天测定并记录FPG及三餐中任意一餐的2hPG,每周根据血糖情况调整药物剂量,如FBG>7.0 mmol/L,则增加利拉鲁肽剂量至1.2 mg/d,最大可增加至1.8 mg/d,直至血糖达标[6]。2组血糖达标值为:FBG为4.0~7.0 mmol/L,2hPG<10 mmol/L[7]。2组均治疗12周后。
1.4 疗效判定 (1)显效:FPG、2 h PG控制在正常范围内,HbA1c下降≥1%,且无不良反应发生;(2)有效:FPG、2hPG明显下降,但未降至正常范围内,HbA1c下降0.3%~1%;(3)无效:FPG、2hPG下降不明显,HbA1c下降不足0.3%,或出现较为严重的不良反应[8]。总有效率=(显效+有效)/总数×100%。
1.5 观察指标 (1)治疗前后检测血糖各指标,应用葡萄糖氧化酶法检测FPG、2hPG,应用色谱法检测HbA1c;(2)治疗前后测量身高及体重,计算BMI值;(3)治疗前后检测胰岛β细胞功能,包括空腹胰岛素(FINS),采用放射免疫法检测,计算胰岛素抵抗指数(HOMA-IR),HOMA-IR=FPG×FINS/22.5;(4)治疗前后检测血脂各指标,包括总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白(HDL-C)、低密度脂蛋白(LDL-C),采用血生化仪检测;(5)治疗前后评估生活质量,使用SF-36量表,内容包括社会功能、角色功能、认知功能、躯体功能等,每项100分,得分越高则生活质量越好。
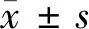
2 结果
2.1 2组疗效比较 观察组治疗有效率为95.12%明显高于对照组的75.00%,差异有统计学意义(P<0.05)。见表1。

表1 2组疗效比较 例(%)
2.2 2组治疗前后血糖、胰岛功能、BMI水平比较 2组治疗前FPG、2hPG、HbA1c、BMI、FINS、HOMA-IR水平差异无统计学意义(P>0.05);观察组治疗后12周后的FPG、2hPG、HbA1c、BMI、HOMA-IR水平明显低于对照组,而FINS水平明显高于对照组,差异有统计学意义(P<0.05)。见表2。

表2 2组治疗前后血糖、胰岛功能、BMI水平比较
2.3 2组治疗前后血脂指标比较 2组治疗前TC、TG、HDL-C、LDL-C水平差异无统计学意义(P>0.05);观察组治疗后12周后的TC、TG、LDL-C水平明显低于对照组,而HDL-C水平明显高于对照组,差异有统计学意义(P<0.05)。见表3。
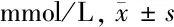
表3 2组治疗前后血脂指标比较
2.4 2组治疗前后SF-36量表评分比较 2组治疗前社会功能、角色功能、认知功能、躯体功能等SF-36评分差异无统计学意义(P>0.05),观察组治疗后12周后的社会功能、角色功能、认知功能、躯体功能等SF-36评分明显高于对照组,差异有统计学意义(P<0.05)。见表4。

表4 2组治疗前后SF-36量表评分比较 分,
3 讨论
2型糖尿病临床表现为血糖升高引起的糖代谢紊乱,常合并脂肪代谢紊乱,导致肥胖型2型糖尿病的发病率较高[9]。临床统计显示,肥胖人群发生2型糖尿病的概率是正常体重人群的2.6倍[10]。2012年WHO资料显示,约44%的糖尿病负担归因于超重及肥胖[11]。肥胖型2型糖尿病对机体的损害较大,长期的高血糖状态可严重损害靶器官功能,导致心、肾、神经、血管等并发症,严重损伤身体功能,预后较差[12,13]。因此,临床需要在降低血糖的同时减少BMI,以提升临床疗效。但传统降糖药物在降低血糖的效果上并不稳定,容易造成低血糖,还可造成BMI增加,最终可导致血糖控制失败[14]。
利拉鲁肽属于GLP-1类似物,与人胰高素样肽-1具有97%的序列同源性,通过促进胰岛β细胞增殖、分化达到增加自身胰岛素分泌的作用,并具有葡萄糖浓度依赖的特性,能在调节血糖的同时防止低血糖的发生,达到良好的降糖效果[15,16]。有研究显示,机体缺乏GLP-1可能导致胰岛素抵抗、胰岛β细胞分泌功能减弱、胰高血糖素分泌过多等,在2型糖尿病的发生发展过程中有重要作用[17]。因此,提高体内GL-1水平是治疗2型糖尿病的重要途径,有助于改善机体胰岛素抵抗,修复受损的胰岛β细胞功能。药理研究表明,利拉鲁肽可同时作用于α细胞和β细胞,机体普通糖升高时能有效刺激胰岛素的分泌,并拮抗胰高血糖素的生成,双调节α、β细胞功能,达到有效降低血糖的目的[18,19]。而在葡萄糖平稳状态下,不会刺激胰岛素分泌,调节血糖的作用呈葡萄糖依赖性,因此发生低血糖的概率较低[20]。对于肥胖者来说,利拉鲁肽还可抑制食欲,延缓胃排空,从而降低BMI[21]。这与糖尿病健康管理的理念相符合,尤其适用于BMI>28 kg/m2的肥胖患者[22]。因此,利拉鲁肽在良好控制血糖的同时,可有效减轻BMI,而对肥胖型2型糖尿病患者来说,BMI的减轻又可降低胰岛素抵抗,从而形成良性循环,有助于病情的控制,降低靶器官并发症发生率,与传统降糖药物相比,有明显优势[23,24]。
本研究结果显示,观察组治疗有效率为95.12%,明显高于对照组的75.00%(P<0.05)。2组治疗前FPG、2hPG、HbA1c、BMI、FINS、HOMA-IR水平无明显差异(P>0.05),观察组治疗后12周后的FPG、2hPG、HbA1c、BMI、HOMA-IR水平明显低于对照组,而FINS水平明显高于对照组(P<0.05。;2组治疗前TC、TG、HDL-C、LDL-C水平无明显差异(P>0.05),观察组治疗后12周后的TC、TG、LDL-C水平明显低于对照组,而HDL-C水平明显高于对照组(P<0.05)。观察组治疗后12周后的社会功能、角色功能、认知功能、躯体功能等SF-36评分明显高于对照组(P<0.05)。证明利拉鲁肽治疗肥胖型2型糖尿病12周后,血糖、血脂明显降低,胰岛素抵抗明显减轻,BMI明显减少,能有效延缓糖尿病相关大血管病变的发生率,提高生活质量[25]。
综上所述,利拉鲁肽对肥胖型糖尿病患者FPG、2hPG、HbA1c有积极影响,兼具降糖、降脂、降BMI等功效,值得在临床推广使用。
