废菌渣活性炭的制备及对废水中硝基苯的吸附
2020-11-26李红艳严铁尉崔建国张峰王芳李尚明
李红艳,严铁尉,崔建国,张峰,王芳,李尚明
(1 太原理工大学环境科学与工程学院,山西晋中030600;2 山西省市政工程研究生教育创新中心,山西晋中030600;3 山西省生物研究院有限公司食用菌研究中心,山西太原030006;4 太原理工大学材料科学与工程学院,山西太原030024)
废菌渣(mushroom residue,MR)是食用菌收获后留下的农业废弃物[1],富含有机质及多种微量元素[2]。MR 每年大约有800 多万吨通过焚烧、填埋等传统方式处理[3]。因此,以廉价的MR为碳源制备活性炭,一方面可以避免常规处理MR 的方式对资源的浪费和环境的污染;另一方面,由MR 等农林废弃物制得的活性炭具有独特的理化结构、丰富的孔隙结构、较大的比表面积和较强的吸附能力,可用来去除废水中的污染物,保护环境[4]。
金属盐中浸渍并热处理是改性活性炭的常用方式。Zemskova 等[5]通过碳纤维吸附钼酸钠得到钼改性碳纤维,研究表明改性后的活性炭具有较好的吸附性能。佟国宾等[6]制备载钼活性炭,发现钼改性活性炭比未改性活性炭对苯的吸附有明显提高。但是,通过简单的吸附、浸渍方式制备得到的载钼活性炭分散性较差。由于氧化钼可以与氧化铝表面羟基[7]、活性炭表面含氧官能团[8]发生强相互作用,有利于钼的分散。因此本文作者以废菌渣为碳源和钼源,用硫酸铝与硝酸复合改性制备废菌渣活性炭(mushroom residue activated carbon,MRAC),并研究其对硝基苯的吸附性能,考察pH、投加量、初始浓度等因素对MRAC 吸附水中硝基苯的影响,并对吸附等温模型、吸附热力学进行了探讨,研究结果可为资源化利用MR及吸附去除废水中硝基苯提供理论依据。
1 材料与方法
1.1 试剂与仪器
试剂:废菌棒产自山西;硫酸铝、硝基苯、硝酸均为分析纯;实验用水为超纯水,自制。
仪器:马弗炉(XL-1 型),研磨机(FW200型),紫外分光光度计(752 型),电子分析天平(STP 型),电热恒温鼓风干燥箱(CMD-20X 型),数显恒温振荡器(THZ-82B 型),精密pH 计(FE20型)。
FTIR 表征采用仪器TENSOR 27,德国布鲁克公司;EDS 表征采用仪器JSM-7800F,日本JEOL公司。
1.2 MRAC的制备
将废菌渣用研磨机粉碎后过10 目筛,获得MR。取12g MR 与浓度为1.2g/L 的硫酸铝溶液20mL充分混合,静置15h。将浸渍材料置于100mL的坩埚中,加盖置于马弗炉中800℃煅烧1.5h。冷却至常温后,活性炭的质量与1.25mol/L 的硝酸体积按1∶5的比例充分混合,静置20h。将浸渍材料置于100mL 的坩埚中,加盖置于马弗炉中800℃煅烧2.5h。先酸洗,再水洗至中性,烘干,粉碎,过100目筛。
1.3 MRAC性能测定
称取一定量的MRAC 置于一系列100mL 锥形瓶中,分别加入50mL 一定含量的硝基苯模拟废水溶液,振荡反应一定时间后,过滤,并用752型分光光度计测定剩余硝基苯的含量(测定波长为268nm)。硝基苯的去除率E计算如式(1),吸附容量q的计算如式(2)。

式中,C0和Ct分别为溶液中硝基苯初始和t时刻的质量浓度;V为溶液体积;m为MRAC 的质量。为保证实验的准确性与重现性,每组实验均重复3次。
使用pH位移法测定等电点(pHpzc)为8.8。
2 结果与讨论
2.1 MRAC的表征
2.1.1 FTIR分析
吸附前后MRAC的FTIR分析见图1。由图1可知,MRAC中含有丰富的官能团。且在3412cm-1处有一个—OH 伸缩振动峰,1620cm-1处的峰是由C==O 伸缩振动形成的。1430cm-1处的峰是芳香性C==O、C==C 伸缩振动引起的。1047cm-1的最强峰是C—O伸缩振动峰,856cm-1处的峰是由Mo==O伸缩振动形成的,而712cm-1、570cm-1处则是由Al—O—Al键形成的。
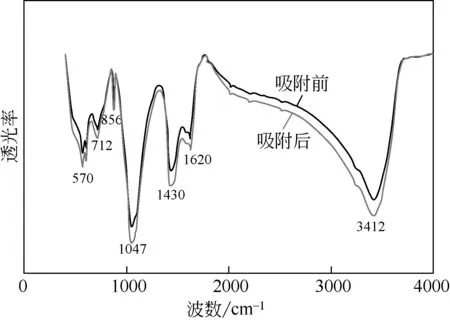
图1 MRAC的FTIR表征
比较吸附前后红外光谱,吸收峰形状整体变化不大,只是吸附后透光率略有下降。在1047cm-1、1430cm-1处透光率有明显下降,可能是由于吸附硝基苯后芳香性物质增多。
2.1.2 EDS分析
吸附前后MRAC 元素分析见表1。由表1 可以看出,MRAC 主要由C、O、Al、Mo 四种元素组成,其中Mo 元素来自废菌渣。且吸附后碳元素含量明显升高,表明硝基苯被吸附在MRAC 表面。O、Al、Mo含量均有下降,这一方面可能是相应官能团与硝基苯作用的结果,另一方面与碳含量升高、各元素含量占比减小有关。
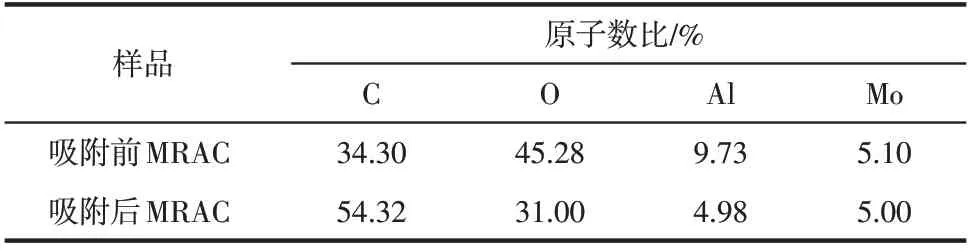
表1 样品元素分析
MRAC 的EDS 扫描图见图2。由图2 可知,C、Al、Mo 三种元素分布比较均匀,没有明显团聚现象。
2.2 pH对MRAC去除硝基苯的影响
将50mL 含10mg/L 硝基苯溶液放入7 个锥形瓶中,使用盐酸和氢氧化钠分别调节pH为1、3、5、7、9、11、13,并各加入0.15g MRAC,于25℃下振荡90min,测量其剩余浓度,并计算吸附容量,结果见图3。
由图3可知,MRAC 对硝基苯的去除率、吸附容量均随pH 的增大而下降。由于最佳pH 不在pHpzc附近,因此氢键不是MRAC吸附硝基苯的主要机理[9]。而由于随着pH的持续升高,OH-的含量不断增加,与MRAC表面酸性官能团结合,并与掺杂的氧化钼反应[10],抑制对硝基苯的吸附,因此硝基苯的去除率随pH升高而降低。
鉴于虽然pH=1 时去除率最高,但是与实际硝基苯废水的pH(pH 接近7)时的降解率相差不大,从成本角度考虑,后续试验在中性pH 下进行。
2.3 初始浓度对MRAC去除硝基苯的影响
向5 个锥形瓶中依次装入50mL 浓度为5mg/L、10mg/L、20mg/L、50mg/L、100mg/L 硝基苯溶液,并各加入0.15g MRAC,于25℃下振荡90min,测量其剩余浓度,并计算吸附容量,结果见图4。

图2 MRAC的EDS扫描图

图3 pH对硝基苯去除的影响
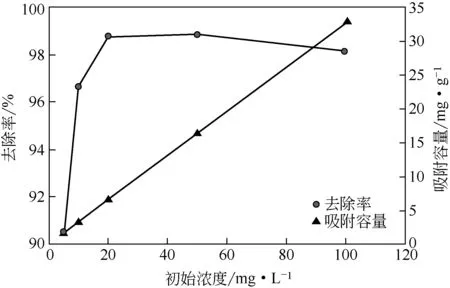
图4 硝基苯初始浓度对硝基苯去除的影响
由图4可知,MRAC 对硝基苯的去除率随初始浓度的增加而升高后略有下降,而吸附容量随硝基苯浓度的升高一直上升。这可能的原因是升高硝基苯溶液的初始浓度,吸附在活性炭上的硝基苯与水溶液中的浓度差也随之增大,硝基苯分子易扩散到MRAC表面。且初始浓度在50mg/L以下时,MRAC可以提供充足的活性位点,因此随浓度升高,去除率与吸附容量均升高。当硝基苯初始浓度在50mg/L时,吸附位点趋于饱和,随后提高硝基苯初始浓度,MRAC吸附硝基苯的数量不再增多,因此去除率略有下降。而溶液中剩余浓度提高的量远小于初始浓度升高的量,因此吸附容量仍然升高。
2.4 吸附时间对MRAC去除硝基苯的影响
向4 个 装 有5mL 10mg/L、20mg/L、50mg/L、100mg/L 硝基苯溶液的锥形瓶中加入0.15g MRAC,于25℃下振荡,分别于1min、2min、10min、15min、30min测量其剩余浓度,并计算吸附容量,结果见图5。
由图5 可知,在硝基苯初始浓度为10mg/L、20mg/L、50mg/L、100mg/L 时,MRAC 对硝基苯的吸附平衡时间均为1min,且吸附平衡30min内浓度没有明显变化,表明MRAC 对硝基苯的吸附较快。较高的吸附速率可能是由于硝基苯分子具有较强疏水性,可以促进硝基苯从水相吸附到MRAC的疏水表面[11]。而且硝基苯的C—H 键会被MRAC 表面的氧化钼活化,再经羧基羰基等官能团进行氧化去除,加快MRAC对硝基苯的吸附[6]。

图5 吸附时间对硝基苯去除的影响
2.5 吸附等温线
吸附等温线采用Freundlich、Langmuir 和Temkin 吸附模型进行拟合,Freundlich 吸附模型如式(3),Langmuir 吸附模型如式(4),Temkin 吸附模型如式(5)。
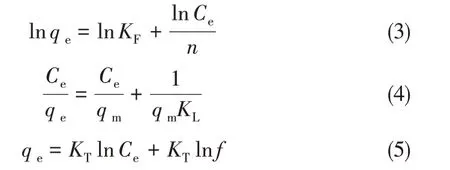
式中,Ce为吸附平衡时硝基苯的浓度,mg/L;qe为吸附平衡时MRAC 的吸附容量,mg/g;KF和n分别为与吸附量和吸附强度有关的常数;qm和KL分别为固相负载物的最大吸附容量和吸附热力相关的能量常量;KT与f分别为与温度和吸附物性质有关的常数。
图6为MRAC对硝基苯的吸附等温线。
从lnqe与lnCe的相关曲线的截距与斜率可求得Freundlich 等温模型的相关参数,从Ce/qe与Ce的相关曲线的截距与斜率可求得Langmuir 等温模型的相关参数,从qe与lnCe的相关曲线的截距和斜率可求得Temkin等温线的相关参数,在表2中列出。其中R2值表示拟合度。

表2 吸附等温线拟合参数
由表2 可知,Freundlich 等温模型(R2>0.95)能够很好地对等温数据进行拟合。拟合结果表明,MRAC对硝基苯的吸附为多层吸附,且吸附位点不均匀。特征参数Kf随温度升高而降低,说明升温不利于MRAC 对硝基苯的吸附,该吸附是放热的过程。这可能是由于随温度升高,硝基苯在水中的溶解度增加,疏水性降低,MRAC与硝基苯之间的疏水键力减弱,硝基苯去除率下降[12]。特征常数nF值均大于1,说明该吸附是优惠吸附,较容易吸附且n值接近1,说明线性吸附可以用来解释MRAC 对硝基苯的吸附,该过程以分配作用为主。这可能与较强的疏水作用有关。
2.6 吸附热力学
热力学参数可以衡量温度对吸附平衡的影响,由式(6)可求得吉布斯自由能变化(ΔG)。

式中,R为气体常数,8.31J/(mol·K);T为吸附温度,K;Kc为吸附平衡常数。
计算得到的ΔG、ΔH和ΔS见表3。

表3 吸附热力学参数
由表3 可知,在各温度条件下,ΔG<0,ΔH<0。因此MRAC 对硝基苯的吸附为自发的放热反应。温度升高不利于MRAC对硝基苯的吸附。且|ΔH|>20kJ/mol,表明MRAC对硝基苯的吸附是物理吸附与化学吸附共同作用的结果。ΔS<0可能是由于吸附后硝基苯被束缚于MRAC,自由度下降,表明MRAC对硝基苯的吸附是稳固有效的[13]。
2.7 硝酸改性对MRAC去除硝基苯的影响
活性炭主要通过孔洞吸附、静电作用、疏水性驱动、形成氢键及π-π 键等方式吸附有机物。而硝基苯在水中以分子形式存在,因此静电作用影响很小。大多研究表明,强酸改性活性炭会形成大量酸性含氧官能团,并通过孔洞坍塌、降低活性炭表面疏水性、与水以氢键形式结合、吸引活性炭石墨层π 电子等方式抑制对疏水性有机物的吸附[14-15]。因此本文作者对不同投加量下硝酸改性前(Al-MRAC)与改性后MRAC 对硝基苯的吸附进行对比,结果见图7。

图7 投加量对MRAC与Al-MRAC去除硝基苯的影响
由图7 可知,MRAC 及Al-MRAC 对硝基苯的去除率随投加量的增加而升高后几乎不变,这可能的原因是吸附50mL浓度为10mg/L的硝基苯溶液所需的活性位点是一定的,在最佳投加量之前,吸附位点随投加量的增加而增加,有更多的孔洞和官能团用于吸附硝基苯,吸附硝基苯的量增加,去除率提高。在最佳投加量时,MRAC所提供的活性位点已足以满足吸附硝基苯的需求,因此,后续增加投加量对硝基苯的去除率影响不大。
比较MRAC 与Al-MRAC 对硝基苯的去除可以发现:各投加量条件下,MRAC对硝基苯的去除均好于Al-MRAC。这与前人的结论不符,可能是由于硝酸改性使活性炭表面形成较多氧化性较强的官能团,有利于氧化去除被氧化钼活化的硝基苯。结合之前的分析,MRAC对硝基苯较好的去除性能主要是由于硝基苯较强的疏水性和氧化钼的活化作用。
3 结论
(1)FTIR 和EDS 分析表明 MRAC 主要由碳、氧、铝、钼四种元素组成,并在表面形成羧基、羟基等多种官能团。
(2)MRAC 对硝基苯的最佳吸附条件为:常温中性pH下,初始浓度50mg/L的硝基苯溶液。此时降解率高达98%,出水水质满足《污水综合排放标准》(GB 8978-1996)中对硝基苯含量的要求。
(3)吸附时间分析表明,MRAC对硝基苯具有较快的吸附速率,1min 接近平衡。且MRAC 对硝基苯的吸附是自发的放热反应,可以用Freundlich模型可以很好地拟合。
(4)活性炭中氧化钼的活化作用与硝基苯的疏水性对MRAC吸附硝基苯起主要作用。
