炭化活化条件对Cu/AC表面Cu价态及其催化降解苯酚的影响
2020-11-26王宏宇李国强朱沛宇张舒婷赵永乐段丽媛张永发
王宏宇,李国强,朱沛宇,张舒婷,赵永乐,段丽媛,张永发
(1 太原理工大学煤科学与技术教育部和山西省国家重点实验室,山西太原030024;2 中国石油大学(华东)新能源学院,山东青岛266580)
湿式氧化法(WAO)是一种适用于处理含酚等有毒、有害有机废水的高效、友好的高级氧化法[1-2]。尽管WAO 具有很好的处理含酚等工业废水的潜能,但其所需要的高压(0.5~20MPa)、高温(200~300℃)操作条件限制了它的实际应用。因此,催化湿式氧化法(CWAO)被提出,通过催化剂的使用,有效降低操作条件,缩短反应时间并加强有机物的氧化效率[3-4]。
催化湿式氧化过程中常用的催化剂包括均相催化剂和非均相催化剂。由于均相催化剂有着催化剂易流失、容易造成二次污染的缺点,非均相催化剂得到了学者的持续关注[5]。Cu基催化剂在氧化过程中表现出较高的活性[6-7],被广泛用于研究催化湿式氧化处理难降解有机废水。常见的用于CWAO法催化剂制备的载体有Al2O3[8]、CeO2[9]、ZrO2、TiO2[10]等金属氧化物以及活性炭[11]、分子筛[12]、离子交换树脂[13]等。其中,活性炭具有比表面积高、孔道结构丰富、表面基团多样、吸附性能优异等特点,作为催化剂载体负载活性金属被广泛地用于CWAO领域[14]。
以廉价的生物质作为碳前体,合成各类功能碳材料以降解有机污染物的方法已得到广泛的研究。Li 等[15]以芦苇秸秆生物炭为载体制备Fe3O4/BiOBr/BC,用于光催化降解水溶液中卡马西平,发现生物炭的引入促进光电空穴对的分离,使Fe3O4/BiOBr/BC具有更好的光催化活性。Yi等[16]用不同类型的生物质合成4种磁性生物炭,作为催化剂用于水溶液中甲硝唑的类芬顿降解,发现磁性生物炭中的Fe(Ⅱ)在降解反应中起主要作用,而生物质类型显著影响磁性生物炭中的Fe(Ⅱ)含量。Fu等[17]以狐尾藻为前体,一步合成具有石墨结构、分级多孔、强磁性的Fe3O4/MC,在用于活化过一硫酸盐降解有机污染物中发现,Fe(Ⅱ)/Fe(Ⅲ)的氧化还原循环、石墨化程度和介孔率是增强降解效果的主要原因。在本文作者课题组[18]之前的研究中发现,采用前体浸渍法制备Cu/AC,可以提高Cu/AC表面活性金属含量、金属分散度以及(Cu++Cu0)相对含量,在固定床反应器中反应8.5h后,Cu/AC的苯酚、COD转化率仍分别达到95.5%和85.7%。但是,制备过程中炭化活化条件对Cu/AC催化湿式氧化性能的影响以及对Cu/AC 的孔结构特性、表面Cu 价态变迁规律的影响未做研究。
本文以核桃壳为原料,以铜氨溶液为铜源,采用前体浸渍法在不同炭化活化条件下制备一系列Cu/AC。以O2为氧化剂,在固定床反应器中测试Cu/AC 催化湿式氧化降解苯酚性能,考察不同炭化活化条件对苯酚废水去除效果的影响;采用N2-吸附脱附、X 射线衍射、X 射线表面光电子能谱等技术,分析Cu/AC 比表面积、孔结构、表面元素组成在Cu/AC 催化湿式氧化降解苯酚过程中的影响。
1 实验部分
1.1 药品与试剂
核桃壳,购自河南郑州;五水合硫酸铜(CuSO4·5H2O)、氨水(NH3·H2O,25%~28%)、氢氧化钠(NaOH)、4-氨基安替比林(C11H13N3O)、铁氰化钾(K3[Fe(CN)6]),均为分析纯;去离子水。
1.2 分析测试仪器
固定床反应器(直径25mm,长度250mm),实验室自制; ASAP2020 物理吸附, 美国Micromeritics 公司;D/max-2200 型X 射线衍射仪(XRD),日本Rigaku 公司;Axis Ultra DLD 型多功能电子能谱仪(XPS),英国Kratos 公司;ICAP 6000 Series 型电感耦合等离子体发射光谱仪(ICP),美国Thermo Fisher公司;723N可见分光光度计,上海精密科学仪器有限公司;6B-12型智能消解仪,江苏盛奥华环保科技有限公司;101-1A型电热鼓风干燥箱,天津市泰斯特有限仪器有限公司;分析电子天平,日本岛津公司;VERTEX 70型红外光谱仪(FTIR),德国Bruker公司。
1.3 催化剂的制备
铜氨溶液制备:配制饱和的硫酸铜溶液及质量分数10%的氢氧化钠溶液,取适量硫酸铜溶液,向其中滴加氢氧化钠溶液过量至溶液pH 约为12,所得沉淀为氢氧化铜。将沉淀水洗3~4 次并抽滤,在80℃、真空度0.06MPa 下真空干燥12h。再逐滴滴加浓氨水至氢氧化铜全部溶解,所得溶液即为铜氨溶液。
Cu/AC催化剂的制备:将核桃壳用自来水、蒸馏水各洗涤3次,除去表面杂质。洗涤后的核桃壳在110℃下干燥24h,然后粉碎、磨至12~16目。取一定量(40g)的核桃壳颗粒与120mL 铜氨溶液混合,搅拌浸渍24h,过滤,然后在110℃下干燥24h。Cu/AC催化剂的炭化活化装置见图1。将所得样品置于高温活化炉中,在N2气氛下10℃/min 升温至炭化温度(500℃、600℃、700℃、800℃),恒温炭化一定时间(1h、2h、3h、4h)。随后继续在N2气氛下维持或以相同速率升温至活化温度(800℃、840℃、880℃、900℃、920℃),将N2切换为CO2恒温活化一定时间(1h、1.5h、2h、2.5h、3h),停止加热,在N2氛围下冷却至室温,最终产物用去离子水洗涤,过滤,在105℃下干燥12h,得到Cu/AC 催化剂,筛分得到12~18 目的固体颗粒,Cu/AC催化剂具体炭化活化条件和对应标记如表1所示。
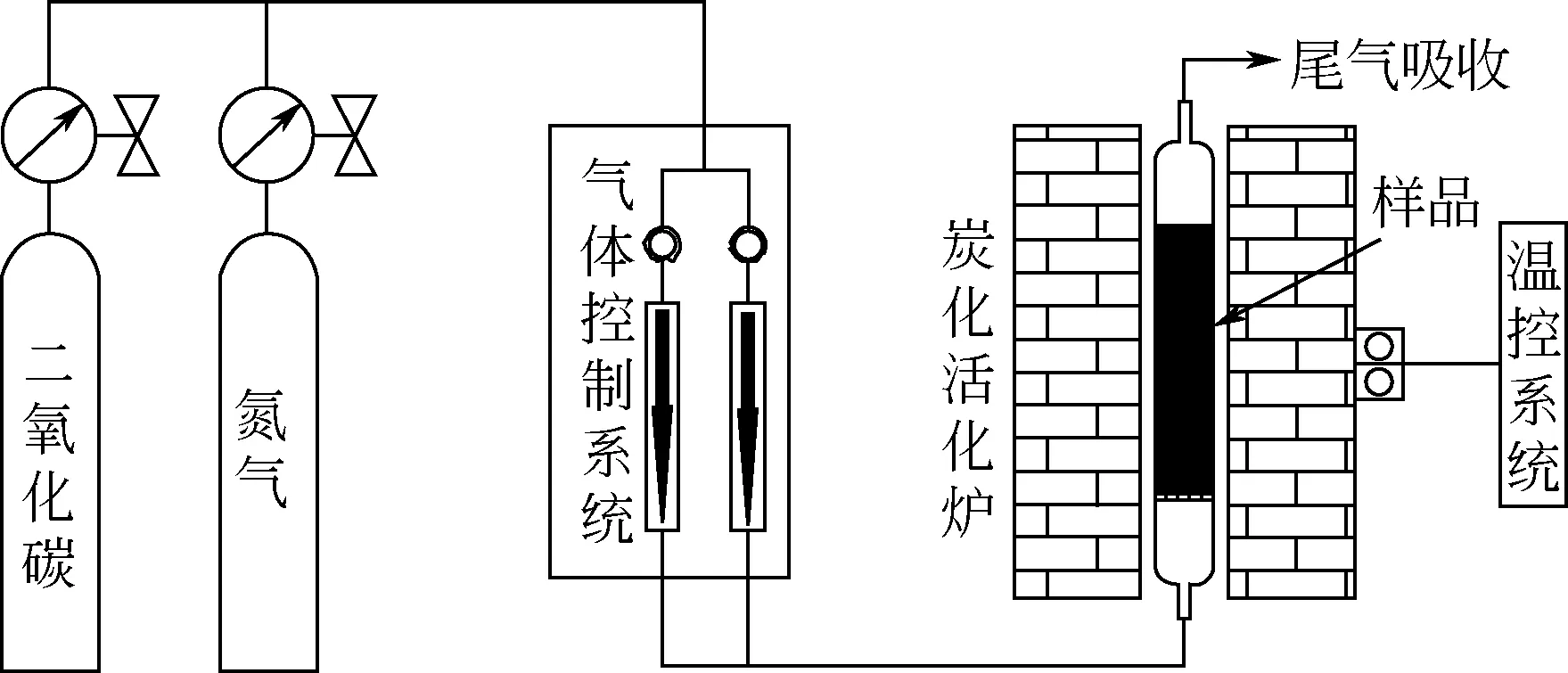
图1 Cu/AC催化剂的炭化活化装置示意图
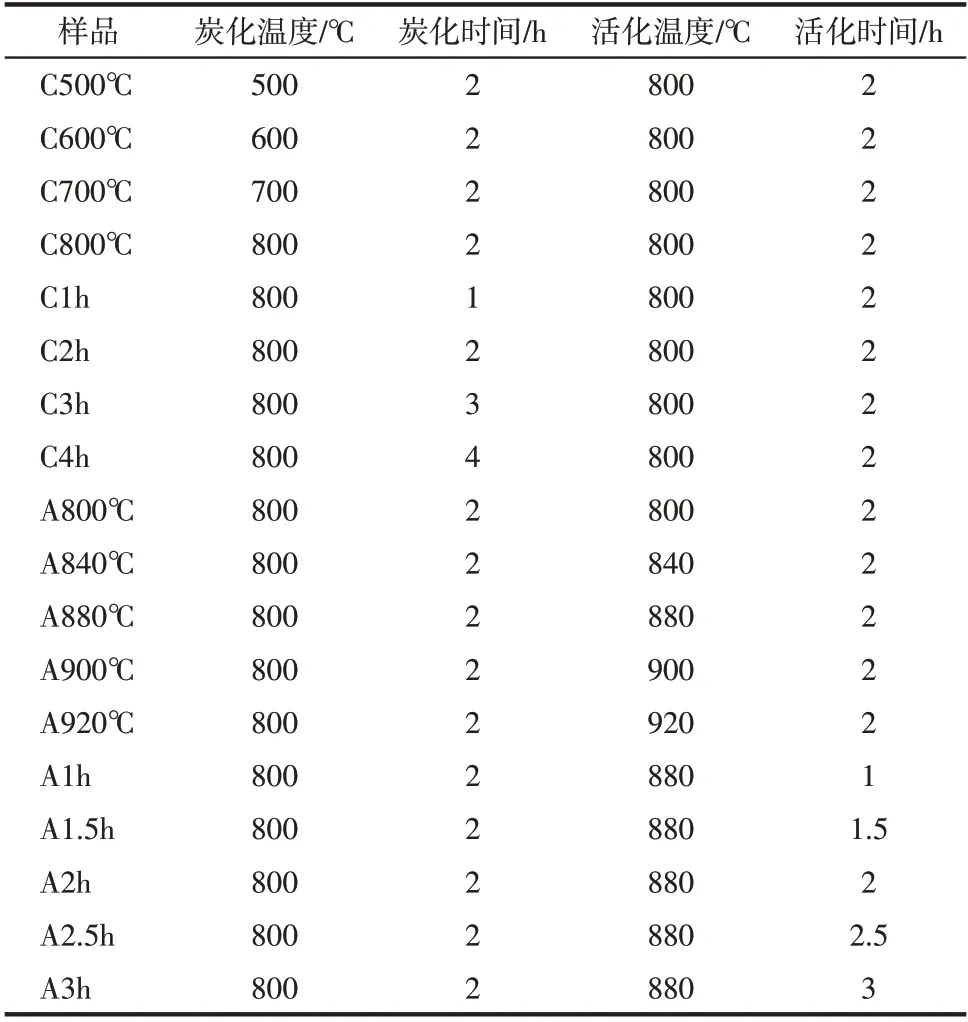
表1 Cu/AC催化剂标记及对应炭化活化条件
收率是指制备所得Cu/AC催化剂的质量与炭化活化前核桃壳颗粒质量的比值。催化剂收率的计算见式(1)。
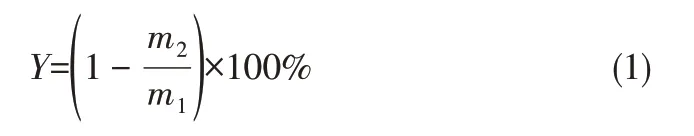
式中,Y为收率,%;m1为原核桃壳颗粒质量,g;m2为制备所得Cu/AC催化剂的质量,g。
1.4 催化活性测试

图2 固定床反应器流程
催化湿式氧化降解苯酚试验在不锈钢固定床反应器中进行,反应装置如图2所示。为使苯酚溶液获得更好地分布并使催化剂处于反应器中段,催化剂填充在惰性氧化铝球(2~3mm)中间。反应条件为催化剂质量2g(床层高度7.60mm,直径25mm),苯酚溶液浓度1000mg/L, 液体进料速率0.5mL/min,气体流速150mL/min,反应温度160℃,反应压力3MPa。每隔一定时间采集反应后溶液并测定其苯酚浓度及化学需氧量(COD)。
苯酚浓度由4-氨基安替比林可见分光光度法测得,苯酚转化率(ΧPhenol,%)由式(2)计算。

2 结果与讨论
2.1 Cu/AC催化剂的表征
2.1.1 催化剂的BET分析
通过N2物理吸附评估样品的孔结构特性。表2总结了不同制备条件得到的各Cu/AC催化剂的比表面积、总孔容、微孔孔容、平均孔径和收率。由表2 可知,当炭化温度升高、炭化时间延长时,Cu/AC 的比表面积、总孔容、微孔孔容、平均孔径均略有增大,收率从25.6%下降到8.9%。与此同时,孔径分布仍以微孔为主,这说明炭化温度升高、炭化时间延长对活化过程中造孔反应略有促进,催化剂中有更多的微孔形成。这归因于炭化温度较低或炭化时间较短时,生物质炭化过程中热分解产生的挥发分析出不完全,炭化程度低,生成的活性位点较少,不利于后期活化造孔过程,使得催化剂孔道发育不完全,比表面积较小,形成的孔结构较少。
而活化条件对催化剂比表面积、孔结构特性影响明显,活化温度从800℃升高到920℃时,Cu/AC的比表面积、总孔容、微孔孔容分别从544.5m2/g、0.3035cm3/g、 0.2500cm3/g 增 大 到 1096.1m2/g、0.5699cm3/g、 0.5073cm3/g, 同 时 平 均 孔 径 从2.2294nm 减小到2.0794nm,收率从11.2%下降到4.1%;当活化时间从1h 增大到3h 时,Cu/AC 的比表面积、总孔容、微孔孔容分别从677.6m2/g、0.3512cm3/g、 0.3078cm3/g 增 大 到 1017.4m2/g、0.5305cm3/g、0.4742cm3/g,而平均孔径从2.1042nm减小到2.0857nm,收率从11.2%下降到2.5%。当活化温度升高、活化时间延长时,Cu/AC的比表面积、总孔容、微孔孔容显著增大,平均孔径略有下降,与此同时孔径分布仍以微孔为主,这说明活化温度的升高、活化时间的延长明显促进活化过程中造孔反应,Cu/AC 中有大量微孔生成。CO2活化反应是吸热过程,活化温度对活化反应过程有着直接影响[19-20]。当活化温度较低时,需要的活化时间较长,造成生产过程能耗增加,收率降低。随着活化温度的升高,活化反应速率得以加快,CO2在炭化料表面的浓度与进入物料内部的CO2浓度达到动态平衡,有利于均匀微孔的生成[21]。当活化温度过高时,活化反应速率过快,CO2容易在炭化料表面反应而很难进入到物料内部,孔隙发育不充分。同时,生成的微孔容易继续被烧蚀成中大孔,不利于微孔的形成[22]。而活化时间较短时,活化反应不充分,CO2与炭化料接触时间较短,CO2没有及时地在炭化料表面开孔。随着活化时间的延长,形成更多的微孔,但过长的活化时间又增加了生产成本,Cu/AC收率降低,比表面积的增长幅度降低。

表2 不同制备条件得到的Cu/AC催化剂的孔结构特性
2.1.2 催化剂的FTIR分析
图3 为C2h 催化剂CWAO 反应前后的FTIR 谱图。从图3 中可以看到,C2h 催化剂在3426cm-1、2974cm-1、 2918cm-1、 2848cm-1、 1739cm-1、1633cm-1、1089cm-1、1050cm-1和880cm-1出现红外特征峰。在3426cm-1位置出现的红外峰普遍认为是O—H 官 能 团 的 伸 缩 振 动 峰[23]; 在2974cm-1、2918cm-1和2848cm-1位置出现的红外峰为环烷烃和脂肪烃C—H伸缩振动峰[24-25];1739cm-1出现的红外峰为脂肪族上C==O 伸缩振动峰[24];在1089cm-1和1050cm-1处出现的红外峰为内酯、酚和醚等中的C—O 伸缩振动[24],表明Cu/AC 表面具有丰富的含氧官能团。对比反应前后C2h催化剂的FTIR谱图,参加反应8.5h 后的C2h 催化剂在2974cm-1、2918cm-1和2848cm-1处的红外峰强度减弱,而3426cm-1、1089cm-1和1050cm-1处 的 红 外 峰 增 强,这表明反应过程中C—H被O2氧化或消耗,催化剂表面有O—H、C—O等官能团形成。

图3 Cu/AC催化剂反应前后的FTIR谱图
2.1.3 催化剂的XRD分析
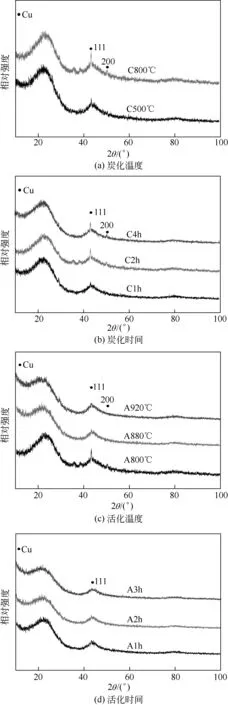
图4 不同炭化活化条件得到的Cu/AC催化剂的XRD谱图
图4为不同炭化活化条件下制备的Cu/AC催化剂的XRD 谱图。如图所示,各Cu/AC 催化剂都出现了位于23°和43.1°的特征衍射峰,归属于具有一定程度sp2杂化的无定形碳。此外,不同制备条件得到的Cu/ACs出现了位于43.2°、50.3°处的特征衍射峰,分别归属于金属Cu(JCPDs NO.04-0836)的(111)、(200)晶面[26-27],这表明催化剂表面有金属Cu 负载。样品中均没有出现明显的对应于晶体态CuO 或Cu2O 的衍射峰,表明其可能以高度分散的状态或无定形态分布在催化剂表面[28]。随着炭化温度的升高和炭化时间的延长,金属Cu(111)、(200)晶面的衍射峰强度增强,这说明炭化温度的升高、炭化时间的延长使催化剂表面的金属Cu 结晶程度更加完好。但当活化温度升高时,金属Cu 的衍射峰强度却随之减弱,A880℃、A920℃样品中无(200)晶面的衍射峰。同时,活化时间延长使得金属Cu(200)晶面的衍射峰强度逐渐减弱,A1h、A2h、A3h样品中无Cu(200)晶面的衍射峰。这说明活化温度、活化时间对催化剂中Cu 物种暴露的晶面有影响[29]。
2.1.4 催化剂的XPS分析
采用XPS对不同制备条件得到的Cu/AC催化剂进一步分析。各Cu/AC 催化剂的Cu 2p 的XPS 谱图如图5 所示,Cu 2p3/2和Cu 2p1/2的结合能分别为933.0eV 和953.2eV,并且伴有结合能为943.2eV 的卫星峰,这说明各催化剂中均存在Cu2+[30]。由于在XRD 谱图中并未观察到明显的对应于CuO 的特征衍射峰,说明催化剂中CuO 是以高度分散的状态存在于催化剂表面。无定形CuO 聚集成小晶簇(小于4nm),小到XRD 无法检测。Cu 2p1/2可以拟合为位于954.5eV 和952.5eV 的两个峰,分别对应于Cu2+和(Cu++Cu0)[31]。Cu 2p3/2可以分别拟合为位于934.2eV 处的Cu2+峰和位于932.4eV 处的(Cu++Cu0)峰[32]。
表3列出了不同制备条件得到的Cu/AC催化剂中的表面Cu 原子占比以及Cu、O 元素组成。由表3可知,随着炭化温度的升高,Cu/AC表面Cu含量增大,(Cu++Cu0)表面相对含量上升,Cu2+表面相对含量下降。较高的炭化条件下,炭化过程中有更多的挥发分产生,使得(Cu++Cu0)相对含量有所增大,而Cu2+相对含量降低。通过XAES 谱图可以区分Cu+和Cu0,但由于Auger信号太弱,无法准确确定其组成[33]。随着炭化时间的延长,Cu/AC 表面Cu 含量先增大后减小,C2h 表面Cu 含量最高,为0.36%;(Cu++Cu0)表面相对含量下降,Cu2+表面相对含量上升。随着活化温度的升高和活化时间的延长,(Cu++Cu0)表面相对含量下降,Cu2+表面相对含量上升。这可能是因为在较高的活化条件下,炭化过程中还原出的(Cu++Cu0)进一步被氧化形成Cu2+。同时,Cu/AC表面Cu含量随着活化温度的升高呈现下降趋势,而随着活化时间的延长先增大后减小,A2h表面Cu含量最高。
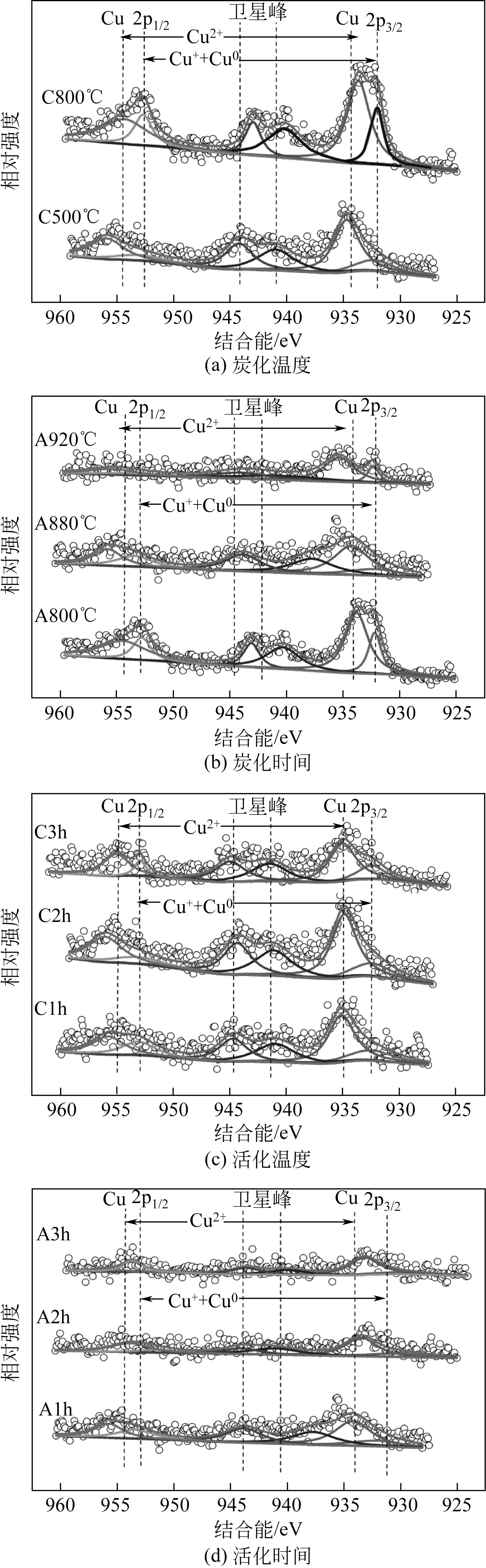
图5 不同炭化活化条件得到的Cu/AC催化剂的Cu 2p XPS谱图

表3 Cu/AC催化剂表面Cu、O组成
由图6中不同炭化温度制备的Cu/AC催化剂的O 1s XPS 谱图可见,O 1s 谱图可以拟合为3 种峰,其中529.6~530.2eV 之间的是晶格氧(Oβ),531.2~531.8eV 之间的是化学吸附氧(Oα)以及在532.7~533.5eV 之间属于C—O 键上结合的氧(Oγ)[34]。由表3 可知,随着炭化温度的升高,Cu/AC 催化剂中Oβ的相对含量下降,而Oα和Oγ含量均有所增加,表明较高的炭化温度下催化剂表面产生了更多的吸附氧以及含氧官能团。随着炭化时间的延长,Cu/AC催化剂中Oβ的相对含量增加,Oα含量稍有下降,而Oγ含量变化不明显,晶格氧的增加是由于CuO较好地并入活性炭载体中。随着活化温度的升高、活化时间的延长,Oβ的相对含量上升,而Oα和Oγ含量均有所下降。Cu2O、CuO较好地并入活性炭载体使得催化剂的晶格氧含量增加;同时,高温下活性炭载体中连接芳香结构体的脂肪类的桥键断裂,使得大量含氧官能团分解[35],从而将炭化过程中还原生成的Cu、Cu2O再次氧化为CuO。
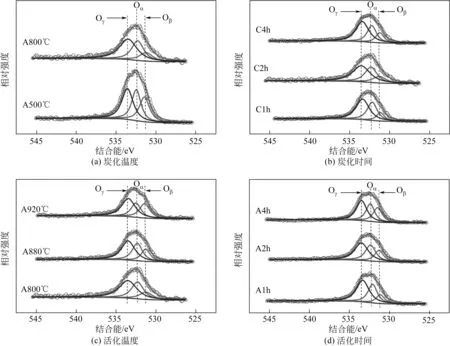
图6 不同炭化活化条件得到的Cu/AC催化剂的O 1s XPS谱图
2.1.5 催化剂的ICP分析
通过ICP对不同制备条件得到的各Cu/AC催化剂的Cu含量进行了分析,结果如表3所示。由表3可知,尽管所制备催化剂有着相同的浸渍比,但不同炭化活化条件下所得各Cu/AC 催化剂的Cu 含量均在0.31%~0.41%之间。这表明虽然不同炭化活化条件下所得Cu/AC催化剂的收率有很大的差异,但炭化活化条件对Cu/AC催化剂的Cu含量影响较小。
2.2 炭化温度对Cu/AC 催化湿式氧化降解苯酚废水性能的影响

图7 炭化温度对Cu/AC催化湿式氧化降解苯酚废水性能的影响
图7 为不同炭化温度下制备的Cu/AC 催化剂CWAO降解苯酚废水性能的催化活性图。随着炭化温度升高,Cu/AC 的催化活性逐渐增加。从图7(a)中可以看出,各催化剂在反应初始阶段苯酚转化率都能达到96%以上,但在反应1.5h 后,苯酚转化率随着反应进行逐渐下降并趋于稳定。C500℃在反应8.5h 内苯酚转化率达在90%以上,而C800℃在反应8.5h内苯酚转化率维持在95%以上。图7(b)中所示的各催化剂COD 转化率随反应时间的变化规律与苯酚转化率变化呈现相同的规律。C500℃的COD 转化率由反应0.5h 的96.1%降至反应8.5h 的68.4%,而C600℃、C700℃、C800℃反应8.5h 时COD转化率分别达到85.2%、88.4%、89.5%。炭化过程中,生物质中C—OH、C—O—C、C—H 等基团大量分解,产生自由基,进而形成CO、CO2、H2、CxHy和CxHyOz等还原性气体和焦油蒸气等,形成的挥发分在高温下具有较强的还原能力,促进高价态的Cu2+还原为低价态的Cu+和Cu0[36-37]。
湿式氧化反应为自由基反应,在反应过程中发生的反应见式(4)~式(10),生成HO·、HO2·、PhOO、PhO·、O-2·等自由基[式(4)~式(9)],进一步,Cu+/Cu2+氧化还原循环产生H2O2[式(10)],并促进更多的自由基产生,HO·、O-2·等自由基将苯酚氧化为小分子中间产物并最终氧化为CO2和H2O[18]。其中,自由基的生成为CWAO 反应的速度控制步骤。相较于Cu2+,Cu+对活化H2O2有着更高的活性[38]。更高含量的Cu+存在,可以加快Cu+/Cu2+氧化还原循环,加快反应速率从而有效促进CWAO 反应的进行,提高苯酚、COD转化率[18]。随着炭化温度的升高,Cu/AC 催化剂表面Cu 含量以及(Cu++Cu0)表面相对含量均增大,从而促进Cu/AC 催化活性的提升,使C800℃表现出较高的催化活性。
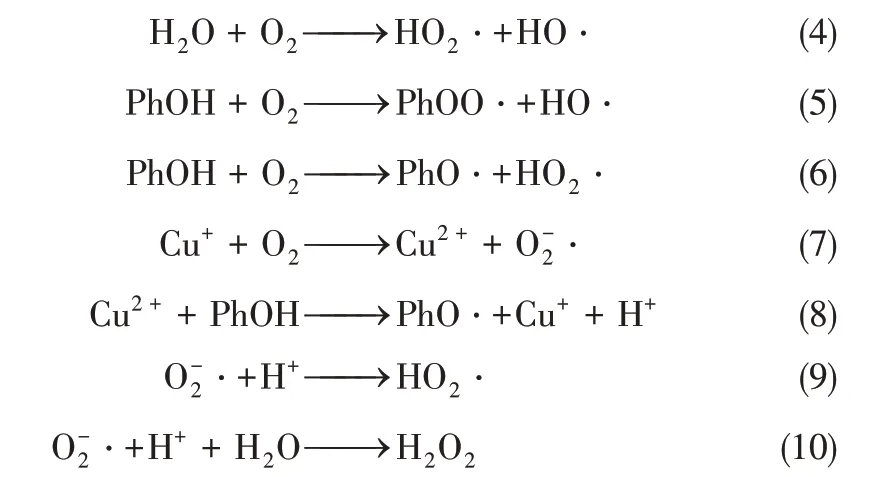
2.3 炭化时间对Cu/AC 催化湿式氧化降解苯酚废水性能的影响
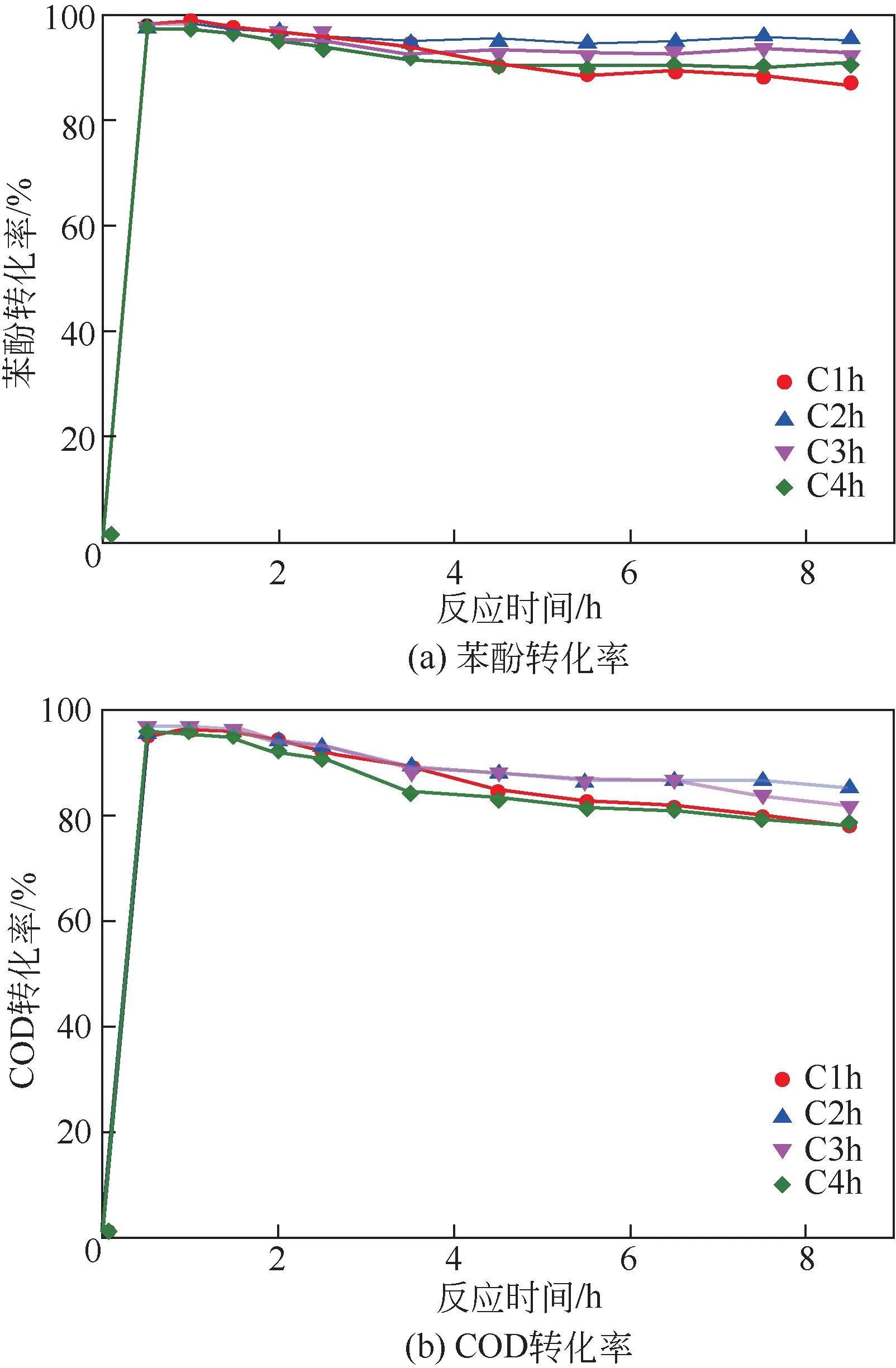
图8 炭化时间对Cu/AC催化湿式氧化降解苯酚废水性能的影响
图8为不同炭化时间制备的催化剂CWAO降解苯酚废水的催化活性图。从图中可以看出,随着炭化时间的延长,Cu/AC 的催化活性先增强后减弱。如图8(a)所示,反应0.5h时各催化剂苯酚转化率快速升高至97%以上,但在反应1h 后均出现下降,C1h、C3h 及C4h 苯酚转化率下降较剧烈,到反应8.5h 分别下降至86.8%、92.6%、90.8%;而C2h 苯酚转化率较为稳定,反应8.5h 时为95.1%。由图8(b)可知,反应0.5h时各催化剂COD转化率快速升高至95%左右。1h 后COD 转化率均开始缓慢下降,反应8.5h 时C1h、C2h、C3h 及C4h 的COD 转化率分别为77.8%、85.2%、81.9%及78.6%。炭化时间的延长对催化剂的比表面积、孔结构没有明显的影响,但催化剂表面晶格氧含量持续增加。同时对于非贵金属催化剂,催化剂表面晶格氧对催化过程起到重要的作用[39]。C2h由于其较高的Cu含量和(Cu++Cu0)表面相对含量,表现出较好的催化活性和稳定性。
2.4 活化温度对Cu/AC 催化湿式氧化降解苯酚废水性能的影响
图9为不同活化温度制备的催化剂催化湿式氧化降解苯酚废水性能的催化活性图。如图9(a)所示,反应0.5h,各催化剂的苯酚转化率快速升高至97%以上,C840℃、C880℃、C900℃、C920℃的苯酚转化率更是接近100%,与此同时COD转化率也随反应的进行快速升高,反应2h时接近100%。但在反应2h 后,苯酚、COD 转化率出现下降,在反应8.5h 时分别维持在90%以上和80%以上。随着活化温度的升高,制得的催化剂比表面积、微孔体积显著增大。此外,由XPS表征结果可知,活化温度的升高促进晶格氧含量增大,但同时导致Cu 含量及(Cu++Cu0)含量下降。显著增大的比表面积和发达的微孔结构,使得催化剂对污染物的吸附性能大幅提高,同时高的表面Cu 组分为湿式氧化反应提供了充分的活性位,提高了催化剂的催化性能。活化温度为880℃时制得的Cu/AC 催化剂表现出较好的催化活性和稳定性,但当活化温度继续升高时,Cu/AC催化活性提升不明显,同时Cu/AC收率持续下降,因此880℃为最适活化温度。
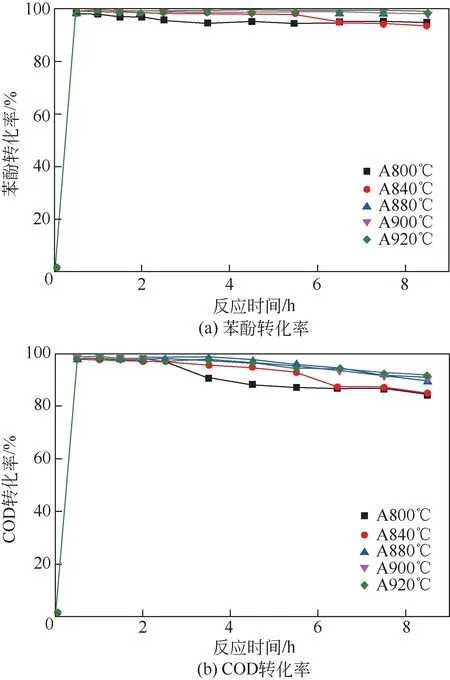
图9 活化温度对Cu/AC催化湿式氧化降解苯酚废水性能的影响
2.5 活化时间对Cu/AC 催化湿式氧化降解苯酚废水性能的影响
图10 为不同活化时间制备的Cu/AC 催化剂CWAO降解苯酚废水的催化活性图。从图中可以看出,随着活化时间的增加,Cu/AC的催化活性逐渐增加。如图10(a)所示,反应0.5h 时各催化剂苯酚转化率快速升高至99%以上,但在反应2h后A1h、A1.5h 苯酚转化率出现下降,到反应8.5h 时分别下降至93.4%、94.9%;而A2h、A2.5h 及A3h 苯酚转化率均较为稳定,反应8.5h 时分别为98.5%、99.0%、99.0%。由图10(b)可知,反应0.5h 时各催化剂COD 转化率快速升高至98%左右。反应0.5h后,A2h 和A2.5h 的COD 转化率略微下降,反应8.5h 时分别为91.1%、90.6%;A1h、A1.5h 及A3h的COD 转化率在反应0.5h 后出现持续下降,到反应8.5h时分别下降至83.4%、86.3%、86.5%。活化时间的延长,促进Cu/AC的比表面积持续增大,有更多的微孔生成,使得催化剂吸附性能优异,提高了催化湿式氧化反应性能。过长的活化时间降低了催化剂Cu含量及表面(Cu++Cu0)含量,使得催化剂Cu+活性中心减少。同时,延长活化时间使得催化剂晶格氧含量上升,利于催化湿式氧化反应的进行。当活化时间大于2h 后,Cu/AC 催化活性增长有限,但Cu/AC收率下降明显,综合考虑活化时间2h较为适宜。
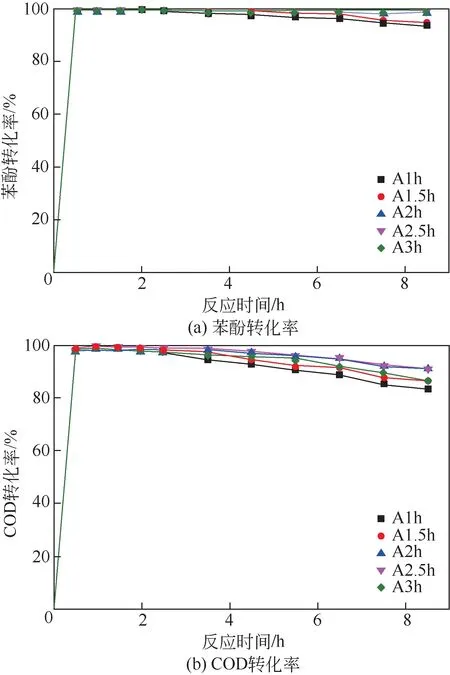
图10 活化时间对Cu/AC催化湿式氧化降解苯酚废水性能的影响
2.6 Cu/AC的Cu浸出与催化稳定性
为了研究反应过程中活性金属Cu的浸出情况,采用ICP 分析反应前后A880℃催化剂中Cu 元素含量,结果如图11 所示。参与反应8.5h 后,A880℃催化剂的Cu 含量由反应前的0.41%下降到0.39%。由此计算得出反应后溶液中浸出Cu 离子平均浓度为1.57mg/L,这显著低于文献中高达17~200mg/L的Cu 离子浸出浓度[40-41],表明Cu 组分稳定地存在于所制备的Cu/AC催化剂中。
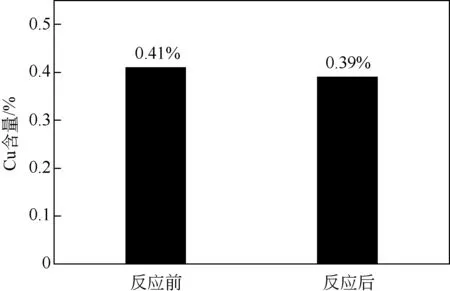
图11 反应前后A880℃催化剂Cu含量
为了研究Cu/AC催化剂的稳定性,在上述反应条件下使用A2h催化剂在固定床反应器中连续运行30h。同时,不间断地检测苯酚、COD 转化率,结果如图12 所示。由图12 可知,Cu/AC 催化剂保持较好的催化活性,在反应24h时苯酚、COD转化率分别达到97.1%和87.4%,在反应30h 时分别下降到94.5%和85.2%。
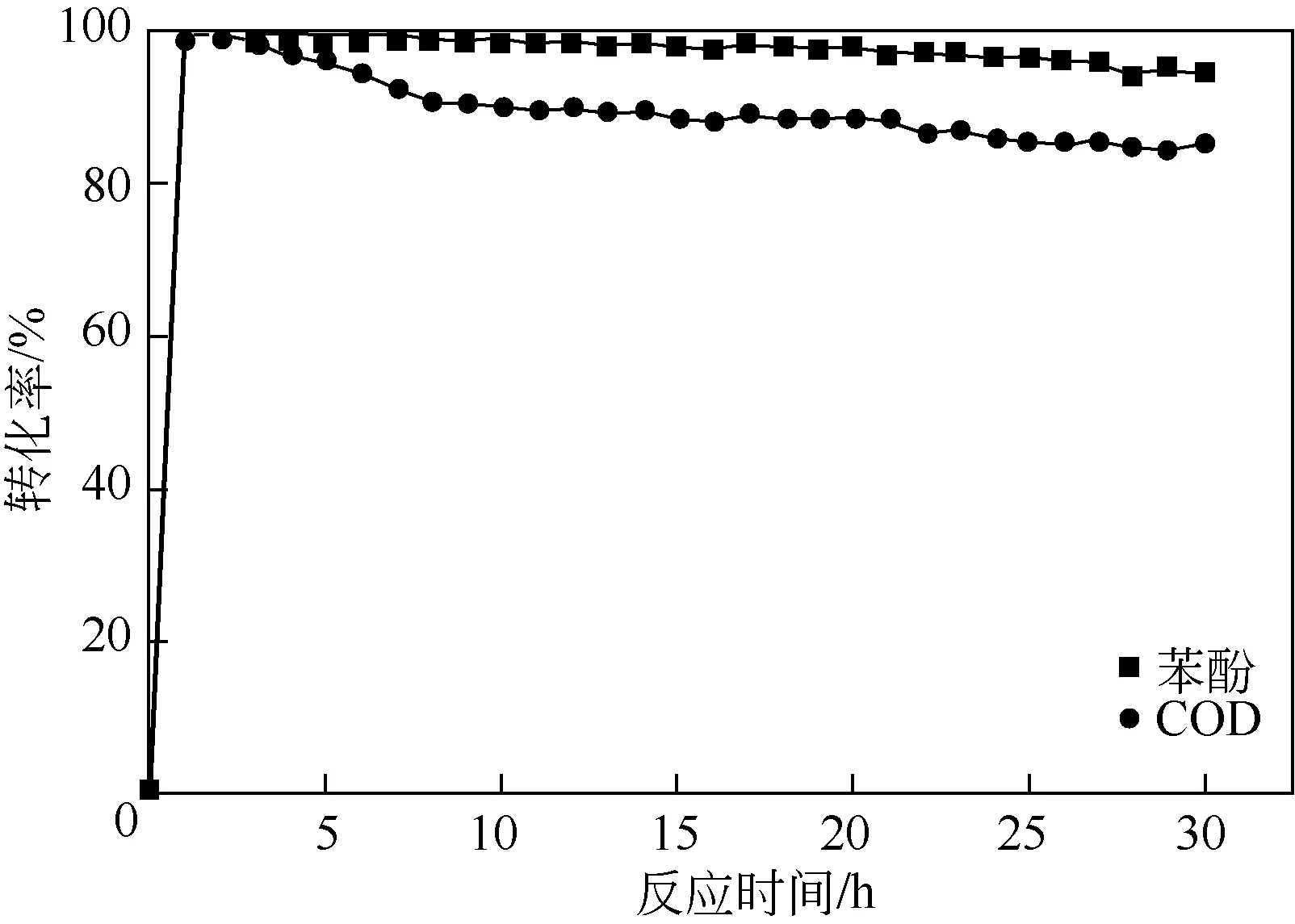
图12 Cu/AC催化剂稳定性
3 结论
当炭化温度升高、炭化时间延长时,Cu/AC的比表面积、微孔孔容略有增大;当活化温度升高和活化时间延长时,Cu/AC的比表面积、微孔孔容分别 从544.5m2/g、0.2500cm3/g 增 大 到1096.1m2/g、0.5073cm3/g。比表面积增大,形成的微孔增多,提高了Cu/AC 吸附性能,促进苯酚、COD 转化率升高。
Cu/AC 表面Cu 物种以Cu2+和(Cu++Cu0)共存。随着炭化温度的升高,炭化过程中有更多的挥发分产生,促进Cu2+还原为Cu+和Cu0,使得(Cu++Cu0)含量增大,苯酚、COD 转化率随之升高。炭化时间延长,(Cu++Cu0)含量下降,Cu2O、CuO较好地并入载体使晶格氧含量增加,苯酚、COD 转化率先增高后略有降低。随着活化温度的升高和活化时间的延长,Cu/AC中大量含氧官能团分解将炭化过程中还原生成的(Cu++Cu0) 再次氧化为Cu2+,(Cu++Cu0)含量下降,晶格氧含量增加,在孔结构特性、Cu/AC 表面(Cu++Cu0)和晶格氧共同作用下,苯酚、COD转化率随着Cu/AC活化温度的升高逐渐增高,随着Cu/AC活化时间的延长先增高后略有降低。
催化湿式氧化降解苯酚过程中,Cu/AC催化剂具有良好的稳定性和低的Cu 离子浸出浓度(平均仅为1.57mg/L)。Cu/AC 的最优制备条件为炭化温度800℃,炭化时间2h,活化温度880℃,活化时间为2h,该Cu/AC 催化剂在反应8.5h 内实现了98.5%的苯酚转化率和91.1%的COD转化率。
