我国部分地区送检样品3种常见猪病血清学和病原学检测
2020-10-10梁俊超王辉之刘晓东刘红祥孔宪好马振乾胡继明
梁俊超,王辉之,刘晓东,刘红祥,李 坤,孔宪好,马振乾,胡继明,刘 东,于 录
(1.吉林大学动物医学学院人兽共患病研究所,人兽共患病研究教育部重点实验室,吉林长春 130062;2.动物基因工程疫苗国家重点实验室,青岛易邦生物工程有限公司,山东青岛 266000)
猪瘟(classical swine fever,CSF)是由猪瘟病毒(classical swine fever virus,CSFV)引起的一种烈性传染病,临床上主要导致母猪繁殖障碍,商品猪实质器官出血、坏死和死亡率高等[1]。CSFV毒力的强弱导致感染猪群的临床病变、发病周期及死亡率均存在差异[2-3]。猪繁殖与呼吸综合征病毒(porcine reproductive and respiratory syndrome virus,PRRSV)可导致猪繁殖与呼吸综合征(porcine reproductive and respiratory syndrome,PRRS)[4]。PRRS临床上主要引发种猪繁殖障碍,商品猪呼吸道症状和高死亡率[5]。PRRSV能逃避机体的免疫清除,侵害猪肺泡巨噬细胞系统,导致机体免疫抑制从而继发其他病原感染。此外,PRRSV可在猪体中形成持续性感染[6]。伪狂犬病病毒(pseudorabies virus,PRV)可导致伪狂犬病(pseudorabies,PR),临床上主要引发母猪繁殖障碍,商品猪呼吸道症状、神经症状和高死亡率[7-8]。自2011年以来,我国多个省份陆续报道猪场出现PRV变异毒株[9-11]。但目前发现,PRV变异毒株主要是基因型的改变,血清型仍只有1个[12-13]。据杨汉春等[14]报道,2018年我国PRRS呈现散发和常发态势,CSF以零星散发为主,PR仍有散发。为了解目前我国这几种常见疫病的流行情况,对2019年不同省(自治区)的送检样本进行血清学和病原学检测,分析其流行特点,以期为猪场相关疫病防控提供参考。
1 材料和方法
1.1 送检样品
2019年我国11个省(自治区)172个猪场送检的3 550份猪血清样品,9个省(自治区)72个猪场送检的371份猪肺脏、脾脏、肾脏、肝脏、淋巴结及脑等组织病料(表1)。送检样品猪场均免疫了CSF和PR疫苗,部分猪场免疫了PRRS疫苗(不同省份占比为13%~33%)。
1.2 主要试剂与仪器
CSFV、PRRSV、PRV-gE ELISA抗体检测试剂盒,均购自美国爱德士公司;一步法RT-PCR试剂盒,购自Vazyme公司;DNA提取试剂盒,购自上海碧云天生物技术有限公司;RNA提取试剂盒,购自北京天恩泽生物技术有限公司。PCR仪(型号T100),购自Bio-Rad公司;酶标仪(型号TECAN),购自瑞士帝肯公司;离心机(型号TGL-16),购自湘仪离心机有限公司。
1.3 血清抗体检测
按照3种病毒相应的ELISA抗体检测试剂盒说明书进行操作,检测结果判定标准见表2。

表1 不同省(自治区)送检血清样本和病料样本信息统计
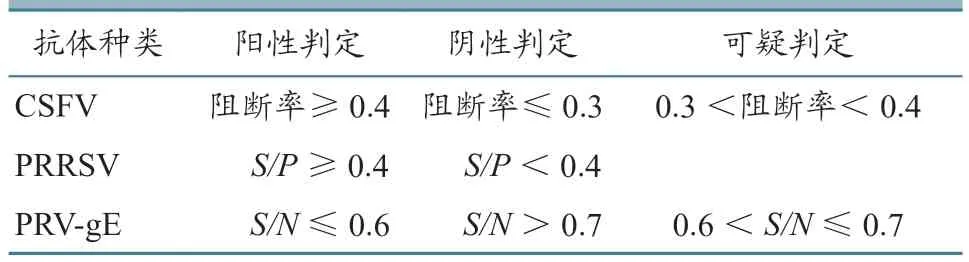
表2 3种病原抗体检测结果判定标准
1.4 病料病原检测
CSFV与PRRSV,采用RNA试剂盒提取并进行RT-PCR检测;PRV,采用DNA提取试剂盒提取并进行PCR检测,然后用1%琼脂糖凝胶电泳检测,如出现目的条带判定为阳性,反之为阴性。
1.5 数据统计分析
检测结果应用Excel 2013软件进行统计学分析处理。
2 结果与分析
2.1 血清抗体检测
2.1.1 总体情况 血清抗体检测结果(图1)显示:CSFV、PRRSV抗体阳性率分别为82.75%、84.08%,均超过了国家要求的70%的最低标准,但因免疫了疫苗,所以无法区分是免疫抗体还是感染抗体;PRV-gE抗体阳性率为31.86%,表明PRV野毒感染率较高。
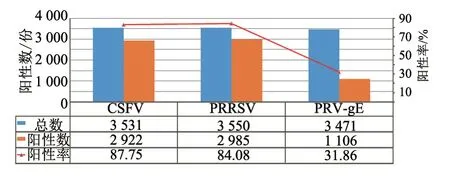
图1 3种疫病病原血清抗体检测结果
2.1.2 CSFV抗体水平 从图2和图3中可知:保育猪群的CSFV抗体平均阻断率最低,为44.62%,且抗体整齐度差,CV为58.26%;阳性个体中,阻断率>40%的占54.39%,>70%的仅占20.46%,表明保育猪群CSFV抗体水平整体不理想。公猪和母猪的平均CSFV抗体阻断率较高,分别为78.66%和75.47%,且抗体整齐度较好,CV分别为24.47%和26.79%;阳性个体中,阻断率>40%的分别占93.91%和92.04%,>70%的分别占80%和74.16%,表明种猪群CSFV抗体水平整体较好。后备猪群的平均CSFV抗体阻断率为68.07%,CV为33.97%;阳性个体中,阻断率>40%的占86.55%,>70%的占59.23%,表明后备猪群CSFV抗体水平好于保育猪群和育肥猪群。
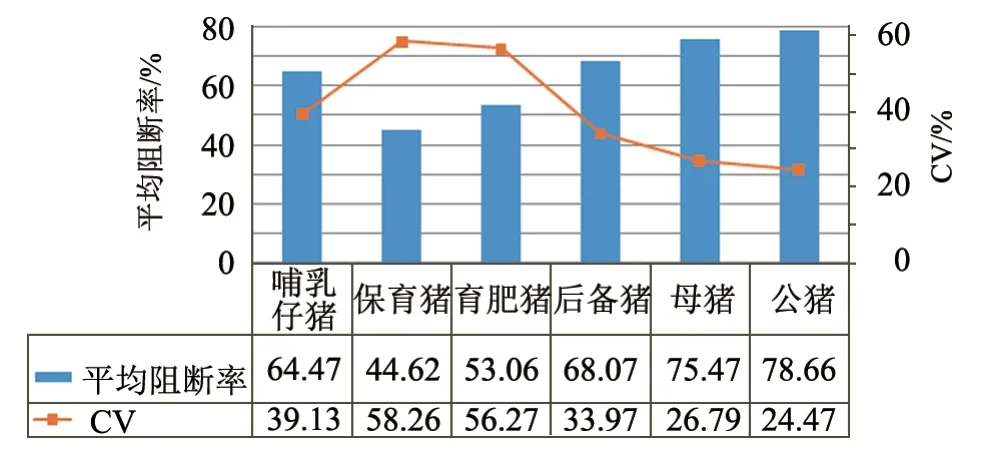
图2 2019年不同阶段猪群CSFV抗体阳性率
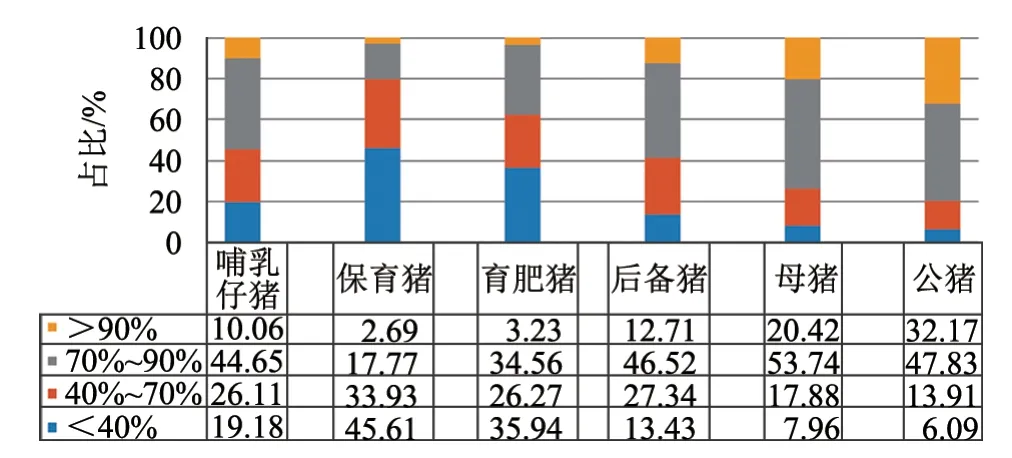
图3 2019年不同阶段猪群CSFV抗体分布
2.1.3 PRRSV抗体水平 从图4和图5中可知:育肥猪群PRRSV抗体S/P平均值最高,为2.32,且抗体较整齐,CV为35.65%;育肥猪群S/P>2.5的占比最高,为46.3%,S/P>3.0占比也最高,为3.24%。而其他各阶段猪群S/P平均值为1.0~2.0,且抗体整齐度较差。公猪CV最高,为88.66%;哺乳仔猪、保育及后备猪群次之,在65.00%~75.00%之间;母猪相对最低,为57.14%。

图4 2019年不同阶段猪群PRRSV抗体阳性率
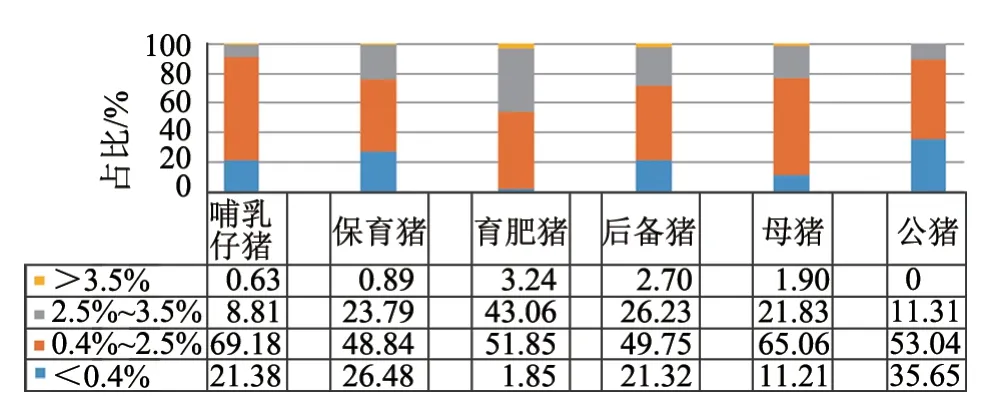
图5 2019年不同阶段猪群PRRSV抗体分布
2.1.4 PRV-gE抗体水平 从图6中可知:育肥猪群PRV-gE抗体阳性占比最高,为36.82%;母猪群次之,为35.31%;公猪阳性比例最低,为15.65%。
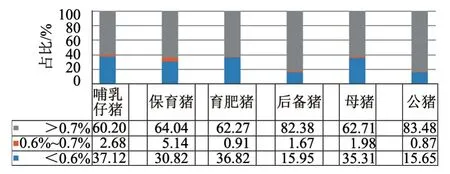
图6 2019年不同阶段猪群PRV-gE抗体分布
2.2 病料病原检测
从表2可知:PRRSV抗原阳性率最高,为26.15%;CSFV次之,为2.62%;PRV最低,为1.67%。CSFV+PRRSV混合感染检出率为2.03%,CSFV+PRV及PRRSV+PRV均未检出。
从表3可知:保育阶段猪群病料的PRRSV检出率最高,为37.68%;CSFV主要在哺乳仔猪和保育猪群病料中被检出,检出率分别为3.57%和3.00%;PRV主要从死胎/木乃伊胎及哺乳仔猪病料中检测到,检出率分别为8.70%和2.99%。CSFV+PRRSV混合感染主要集中在哺乳仔猪及保育猪,检出率分别为5.00%和4.35%。

表3 2019年3种抗原单一及混合感染检测结果

表4 2019年3种抗原在不同阶段猪群病料中的分布
3 讨论
近年来,环保、疫病等因素导致我国养猪存栏大幅下降[15]。猪场密度降低虽对猪病防控有积极作用,但从2019年3种常见猪病抗原及抗体检测结果可知,3种疫病对猪群仍有不同程度的威胁,尤其是PRRS,仍旧是猪场防控的重要对象。
从PRRSV检测结果可知,PRRSV抗体及抗原阳性率总体较高,相比CSFV和PRV,其对猪场威胁更大。母猪PRRSV抗体S/P>2.5的样品占比较高,且死胎/木乃伊胎及哺乳仔猪病料抗原检出率较高,表明母猪群仍存在较高比例的PRRSV感染。保育猪PRRSV抗体S/P>2.5的样品占比也较高,且病料PRRSV抗原检出率最高,表明保育阶段猪群仍是PRRS高发群体。据相关文献报道,仔猪体内PRRSV母源抗体在3周龄时下降加剧[16],至5周龄时下降显著[17],而仔猪免疫系统发育较晚,4~5周龄时才开始发挥作用[18]。此外,保育前期猪群应激因素较多,如断奶、换料、转群及打针等,导致抵抗力下降,从而使猪群保育前期成为PRRSV感染高风险时期。育肥猪PRRSV抗体S/P>2.5的样品占比最高,且病料抗原检出率也较高,表明育肥猪群PRRSV感染也较重,但由于育肥猪抗病力较强,所以临床发病程度轻于保育猪。由上述结果可知,2019年国内猪群PRRSV感染压力并未因外界环境因素改变而得到较大改善。我国PRRS流行比较复杂,除高致病性PRRSV毒株外,类NADC30毒株近年来流行也在加剧[19-20],而用于防疫的弱毒活疫苗毒株繁多(如TJM-F92、JXA1、VR2332、CH-1R等),导致疫苗毒株选择混乱,此外猪场间生物安全及饲养管理水平差距较大,因而增加了我国PRRS防控难度。猪场PRRS综合防控,首先要重视后备猪隔离驯化,加强饲养管理,提升猪场生物安全水平;其次要根据猪场自身PRRSV感染状态,选用合适的疫苗种类及免疫方案。
从CSFV检测结果可知,公猪和母猪抗体水平相对更好,后备猪次之,而保育猪最差,与之前相关报道[21]结果一致。这主要是因为保育猪群CSFV抗体易受母源抗体、应激及PRRS引起的免疫抑制等不利因素影响。CSFV抗原主要从保育猪及哺乳仔猪病料中被检出,检出率较往年有明显下降[22]。CSFV阳性病料共9份,其中7份是CSFV+PRRSV混合感染,且主要集中于保育猪,这可能与PRRSV感染导致机体免疫抑制密切相关。CSF防控是猪场的基础防疫,其防控效果与疫苗质量、免疫程序及免疫抑制性疾病控制存在较大关联。此外,猪场务必重视母猪群CSF防控,定期进行抗原及抗体监测,并结合临床及时调整免疫程序,母猪群的CSF防控对猪场生产及CSFV净化均具有重要意义。
从PRV检测结果可知,公猪、母猪及育肥猪群体仍存在较高的感染率。据相关报道,PRV野毒感染在我国多个地区仍较严重,PRV-gE抗体阳性率>30%[23-24],场阳性率达30%~70%[25-26]。近年我国猪群PRV野毒感染率一直维持在较高水平,这与PR疫苗质量、免疫程序、免疫抑制病流行、生物安全及流行毒株变异等有较大关联[27]。至今为止,疫苗免疫仍是当下PR防控的重要手段。后备猪群应做好隔离监测,种猪定期进行抗体检测,确保留种的后备猪为PRV阴性;对于已转阳的猪场,可通过阴性后备猪逐渐更新、提升猪场生物安全水平等措施,有效降低PRV感染风险,这也有助于PRV阳性猪场逐渐转阴及阴性猪场保持。
本次抗原检测的样品主要由发病猪场提供,抗体检测样品多为猪场常规抗体检测时采集。受非洲猪瘟影响,2019年的样品送检量虽然较往年大幅下降,但在一定程度上也能反映当下猪场3种疫病的免疫水平及感染状态,可对猪场疾病防控提供参考。国内猪病种类多,流行情况相对复杂,猪场需根据猪群疾病实际感染压力,科学免疫,同时提升猪场生物安全及饲养管理水平,保证猪群安全稳定生产。
4 结论
检测表明,PRRS对我国不同阶段猪群威胁较大,是猪场防控的重要对象;保育猪群CSF免疫保护效果不理想,暴发疫情风险较高;公猪、母猪及育肥猪群体普遍存在PR流行,尤其是母猪群。因此,各猪场应采取免疫、监测、净化等综合措施,加强这3类常见疫病的控制。
