壳聚糖/N-乙烯基吡咯烷酮接枝共聚物的制备及其性能
2020-09-23刘旭光辛梅华李明春许军凯王林
刘旭光,辛梅华,李明春,许军凯,王林
(华侨大学材料科学与工程学院,环境友好功能材料教育部工程中心,福建厦门361021)
壳聚糖(CS)是自然界中唯一的碱性多糖,其储量仅次于纤维素[1-2]。壳聚糖具有无毒、生物相容性、生物可降解性和广谱抗菌性等优点,广泛应用于医用材料、生物农药、保健食品等领域[3]。但壳聚糖只溶于酸性水溶液中,限制了其应用。因此,如何改善壳聚糖的溶解性是研究的热点之一。Layek 等[4]将聚乙二醇接枝于壳聚糖侧链,合成了具有亲水性的壳聚糖衍生物,再通过壳聚糖的羟基与己酰氯反应,制备具有双亲性的壳聚糖衍生物作为DNA 载体。Hattori 等[5]采用碳二亚胺做催化剂,利用乳糖酸的羧基与壳聚糖的氨基反应,制备了具有良好水溶性的乳糖化壳聚糖,作为药物吸收助剂能够显著提升胃黏膜的药物吸收效果。
聚乙烯基吡烷酮(PVP)是一种非离子型水溶性高分子化合物,具有优良的溶解性能,能溶于水和多种有机溶剂[6]。PVP 的分子链结构与简单蛋白质结构类似,具有良好的生理惰性和生物相容性,不参与人体代谢,对人体不产生明显刺激,无口服毒性[7-8],因此被广泛用于高分子材料改性及药物助剂等领域。Park等[9]采用卡托丙酸作为链转移剂,通过自由基聚合得到具有端羧基的PVP,再用碳二亚胺作催化剂,制备了聚乙烯基吡咯烷酮接枝壳聚糖衍生物,作为DNA 运输载体。Zhang 等[10]将壳聚糖与PVP 的乙酸溶液混合,通过紫外光照射使其紫外交联,制备壳聚糖-聚乙烯基吡咯烷酮共混膜,作为蒸汽分离膜,对乙醇水蒸气有明显的分离效果。Sizílio 等[11]将壳聚糖与PVP 溶液混合,通过溶剂蒸发法制备壳聚糖-聚乙烯基吡咯烷酮共混膜,研究了不同配比对聚合物网络结构的影响。最后将不同药物加入共混材料中,研究药物释放行为,结果表明共混材料中的药物释放曲线遵循Korsmeyer 和Peppas 模型,具有良好的药物释放功能。目前,PVP改性壳聚糖主要存在以下问题:一是壳聚糖与PVP只进行简单的溶液共混,利用PVP的成膜能力来制备共混膜材料,进行简单的应用;二是通过化学反应将壳聚糖与PVP 结合,通常反应过程长,反应条件有限制,难以工业化。为了改善上述壳聚糖与PVP 结合的问题,本文采用抗坏血酸/过氧化氢共引发剂引发壳聚糖,再通过自由基反应将N-乙烯基吡咯烷酮接枝共聚于壳聚糖侧链,制备PVP 接枝共聚壳聚糖,改善了壳聚糖的溶解性能,合成路线如图1所示,系统研究了引发剂配比、反应温度和反应时间等因素对接枝共聚反应程度以及产物吸湿性和亲水性能的影响。改性后的壳聚糖还具有大量未反应的活性基团,可以通过进一步的化学改性提高材料的功能性,将其应用于医疗器械、食品等行业。
1 实验部分
1.1 仪器和试剂
IS 50 傅里叶变换红外光谱仪(FTIR,美国Nicolet 公司),AVANCEⅢ500M 核磁共振波谱仪(1H NMR,德国BRUKER 公司),TGA-50H热分析仪(TG,日本岛津制作所),JC2000DS 光学视频接触角测定仪(德国Kruss 公司),FD-1B-50 真空冷冻干燥机(北京博医康实验仪器有限公司)。
壳聚糖(CS,-Mw=5×104,DD=89%,浙江澳兴生物科技有限公司),聚乙烯基吡咯烷酮(PVP,-Mw=3×103,上海阿拉丁试剂有限公司),N-乙烯基吡咯烷酮(NVP,上海阿拉丁试剂有限公司),抗坏血酸(Vc)、过氧化氢(AR,上海国药集团有限公司),冰乙酸、丙酮、乙醇等均为市售分析纯。
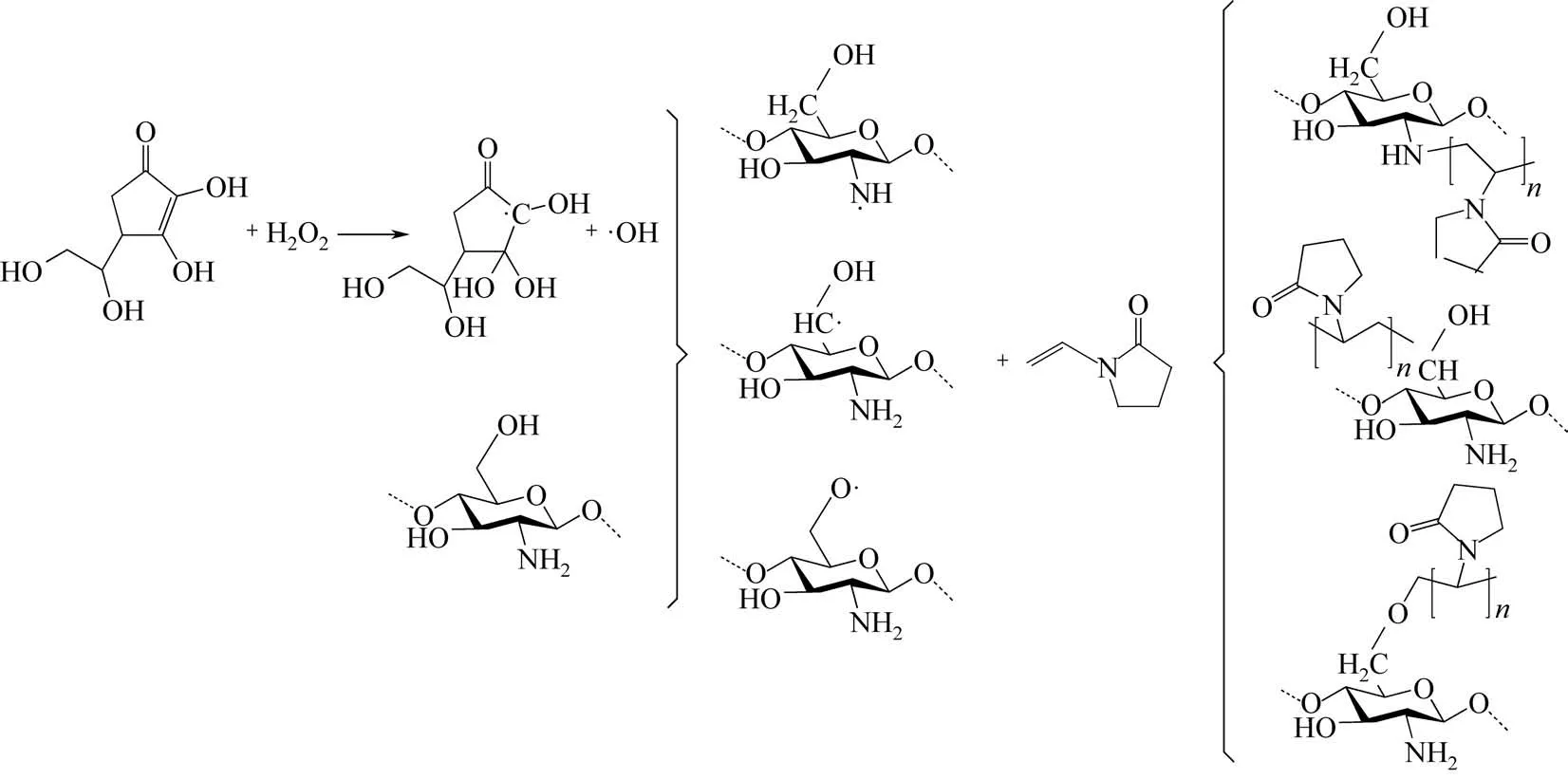
图1 接枝共聚物的合成路线
1.2 壳聚糖/N-乙烯基吡咯烷酮接枝共聚物的制备
称取0.5g 壳聚糖于100mL 圆底烧瓶,加入45mL 1%乙酸水溶液,磁力搅拌下使其完全溶解。待溶解后通N230min,加入抗坏血酸,溶解完全后加入过氧化氢引发剂,在室温下引发30min[12]。加入5g N-乙烯基吡咯烷酮,60℃反应12h,反应液用8000kDa透析袋于蒸馏水中透析两天,透析液冷冻干燥,称重。接枝率、接枝效率、单体转化率分别由式(1)~式(3)计算[13]。
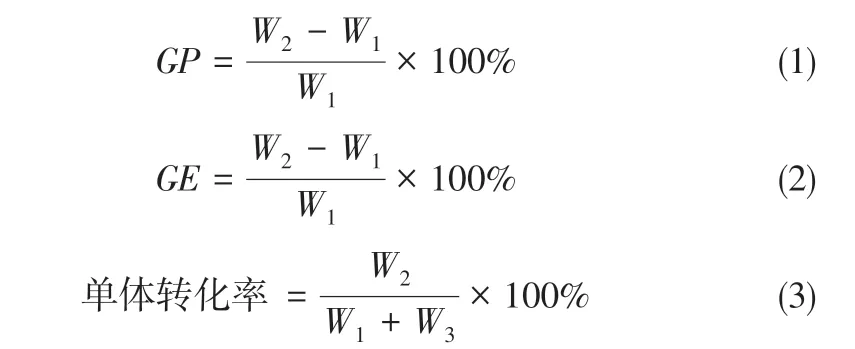
式中,GP为接枝率,%;GE为接枝效率,%;W1为壳聚糖用量,g;W2为接枝共聚产物质量,g;W3为N-乙烯基吡咯烷酮用量,g。
1.3 表征及性能测试
1.3.1 FTIR
采用IS 50 型傅里叶变换红外光谱仪测定原料和产物的红外光谱。用ATR 附件对壳聚糖和接枝共聚产物的粉末进行分析,在400~4500cm-1的中红外区扫描,扫描次数32次。
1.3.2 1H NMR
分别称取25mg 壳聚糖溶于0.5mL 10%的氘代盐酸,25mg 接枝共聚产物溶解于0.5mL 氘代水。用BRUKER AVIII 500 M 核磁共振波谱仪测定原料和产物的1H NMR,测定温度22℃,采样次数64,空扫1次,弛豫时间2s。
1.3.3 分子量测定
取0.15g不同反应条件下制得的产物溶于20mL蒸馏水中,3 号垂熔玻璃漏斗过滤,移取15mL 滤液注入到干燥洁净的乌氏黏度计粗管中,25℃的水浴恒温15min,用秒表准确测量溶液在乌氏黏度计中的下落时间,重复3 次,每次误差不超过0.2s,取平均值[14]。
1.3.4 残留单体的测定
根据美国药典第21版的方法,取10g产物溶于80mL 蒸馏水中,加入1g 乙酸钠,用0.1mol/L 碘溶液滴定至溶液不再褪色,再另加入3mL 0.1mol/L碘溶液,放置10min,然后用0.1mol/L 的硫代硫酸钠溶液滴定过量的碘,当接近终点时加3mL 淀粉指示剂,继续滴加至溶液颜色褪去,并与空白试验对照,通过式(4)计算单体残留量。

式中,V1为空白样品消耗碘溶液量,mL;V2为样品消耗碘溶液量,mL;N为碘溶液浓度,mol/L;m为样品质量,g;1mmol NVP的质量为0.106g。
1.3.5 TG
采用TGA-50H 热分析仪对壳聚糖和接枝共聚产物进行热重分析。分别称取干燥至恒重的样品5~10mg,在Ar气保护下,以10℃/min的升温速率,从30℃升温至600℃。
1.3.6 吸湿性能
分别称取0.5g壳聚糖、聚乙烯基吡咯烷酮和接枝共聚产物碾磨成粉末,烘干后平铺于3cm直径的表面皿中,置于装有饱和硫酸铵水溶液(相对湿度81%)与饱和氯化钙水溶液(相对湿度31%)的干燥器中,放置24h后称重[15]。由式(5)计算吸湿率。

式中,mo与mn分别为吸湿前后的样品质量。
1.3.7 接触角
将接枝共聚壳聚糖的黏稠液均匀涂布在载玻片上,室温烘干成膜。在不同时间内采用光学视频接触角测定仪JC2000DS在涂膜表面测定其水接触角。
1.3.8 溶解性能
称取0.1g壳聚糖、聚乙烯基吡咯烷酮和接枝共聚产物,分别加入10mL 去离子水、1%HAc 溶液、甲醇、乙醇、异丙醇、氯仿、丙酮、二甲基亚砜(DMSO)等溶剂,室温下观察其溶解情况。
采用浊度法测定不同pH 下壳聚糖和接枝共聚产物的水溶性。分别称取0.1g样品于20mL 1%HAC溶液中,缓慢滴加2%NaOH 溶液调节溶液的pH。采用pH 计测定溶液的pH,待稳定后,用UV-3100 PC 型可见分光光度计于600nm 处测定溶液在pH为1~14内的透光率,以pH为3的澄清溶液作为参比[16]。
2 结果与讨论
2.1 接枝共聚条件对反应的影响
2.1.1 引发剂配比
壳聚糖的质量为0.5g,N-乙烯基吡咯烷酮用量为5g,过氧化氢用量为0.1mL,反应时间为6h,反应温度为60℃,通过改变抗坏血酸的用量考察引发剂配比对接枝共聚反应的影响,结果见图2。从图中可见,随着抗坏血酸用量的增加,接枝率、接枝效率及单体转化率先增加后降低,在引发剂配比为等摩尔比时达到最大。这是因为抗坏血酸与过氧化氢为等摩尔反应,当抗坏血酸用量小于过氧化氢时,过氧化氢没有完全反应,无法产生足够的自由基来引发壳聚糖;而当抗坏血酸用量大于过氧化氢时,过多的抗坏血酸会与产生的自由基反应,从而降低了引发效率,导致接枝率与接枝效率降低[17]。
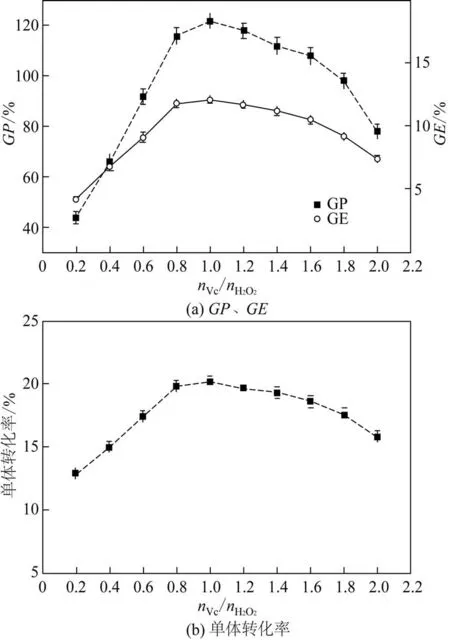
图2 引发剂配比对接枝共聚反应的影响
图3是不同引发剂配比下接枝共聚产物的紫外吸收光谱。从图中可以看出,随着抗坏血酸用量的增加,紫外吸收强度先升高后降低,当引发剂配比为等摩尔比时产物的紫外吸收强度最高,进一步说明此时产物的接枝率、接枝效率及单体转化率最大。本文选择抗坏血酸/过氧化氢的摩尔比为1∶1进行实验。

图3 不同引发剂配比下接枝共聚产物的UV谱图
2.1.2 反应温度和时间
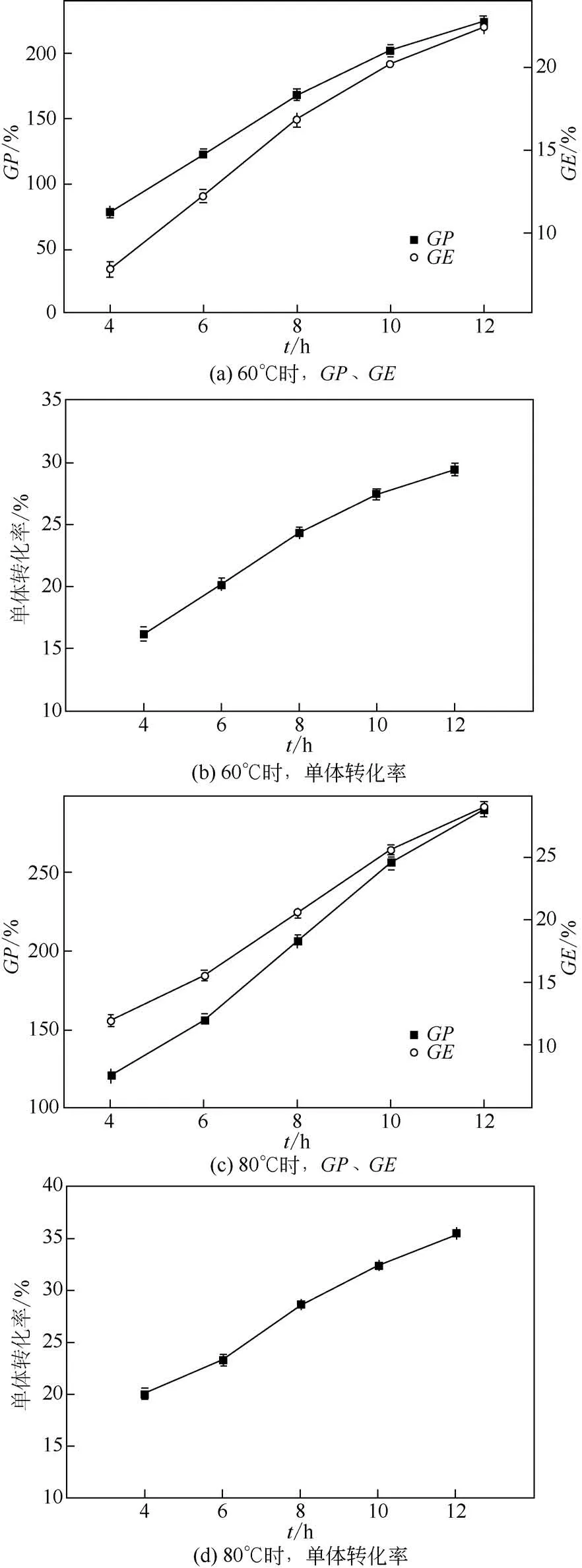
图4 反应温度和时间对接枝共聚的影响
壳聚糖的质量为0.5g,N-乙烯基吡咯烷酮用量为5g,过氧化氢用量为0.1mL,抗坏血酸用量为0.1635g,改变反应时间和反应温度,试验两者对接枝共聚反应的影响结果如图4。从图中可见,随着反应时间与反应温度的增加,接枝率、接枝效率及单体转化率增加。在相同反应时间下,80℃下N-乙烯基吡咯烷酮的接枝量比60℃高。这是因为随着温度的升高,引发剂引发能力增强,接枝聚合反应加快。同时随着反应时间的增加,更多单体发生聚合反应。
对不同条件下制得的产物进行水溶性实验,结果60℃下的产物能完全溶于水中,溶液透明,而80℃下的产物其水溶液中含有许多不溶的絮状物和溶胀物,溶解性能不好。这可能是因为随着反应温度的升高,壳聚糖自由基交联的几率增大,发生了自由基交联产生不溶的交联产物[17]。为了进一步证明自由基交联的存在,进行了空白对照试验,在引发结束后,不加入单体直接进行升温反应。在加热一定时间后烧瓶底部出现白色细沙状沉淀,不溶于水,FTIR 测试,表明为壳聚糖,证明反应过程中有发生壳聚糖自由基交联的可能性。为保证反应具有高的接枝率与接枝效率,同时考虑产品的水溶性,本文选择反应温度为60℃、反应时间为12h进行实验。
2.2 接枝共聚物的分子量测定
按照1.3.3 节的方法测得60℃下不同反应时间所得产物的黏度,见表1。由表1 可见,随着反应时间的延长,产物溶液的流出时间增加,相对黏度相应增加。说明随着反应时间的增加,产物的分子量增大。
2.3 单体残留量的测定
按照1.3.4 节的方法测定不同反应条件下透析产物的单体残留量,结果见图5。由图可见,通过透析处理后,产物中小分子物质被很好的除去,不同条件下产物的单体残留量均小于0.1%,说明透析处理能够很好除去未反应的NVP 单体。
2.4 接枝共聚物的FTIR分析
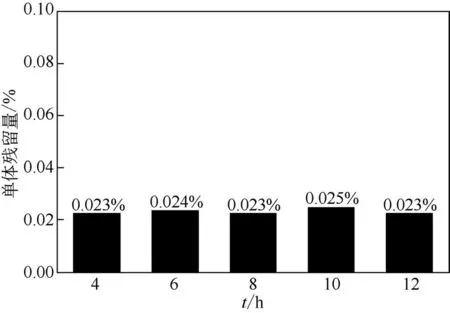
图5 60℃下,不同反应时间下产物的单体残留量
采用IS50 傅里叶变换红外光谱仪测得壳聚糖和产物的红外光谱如图6。由图中可见,与壳聚糖相比,产物的红外光谱图出现了5 个新的吸收峰, 分 别 是2960cm-1、 2920cm-1、 1648cm-1、1422cm-1 和1290cm-1。2960cm-1 和2922cm-1 处 是 接枝聚合到壳聚糖分子链上的聚乙烯基吡咯烷酮的烷烃链C—H 伸缩振动吸收峰,1648cm-1处是聚乙烯基吡咯烷酮的—C==O 伸缩振动吸收峰[18],说明乙烯基吡咯烷酮已接枝共聚到壳聚糖侧链。而1422cm-1附近的峰是C—O—C 的伸缩振动吸收峰,1290cm-1处为仲胺的—C—N 伸缩振动吸收峰,说明N-乙烯基吡咯烷酮已接枝共聚到壳聚糖的羟基和氨基上。
2.5 接枝共聚物的1H NMR分析

图6 壳聚糖和接枝共聚产物的FTIR图

表1 不同产物的黏度测定结果
将接枝共聚产物溶于氘代水,壳聚糖溶于10%的氘代盐酸,测定其1H NMR,结果见图7。图7(a)中3.71~3.90 处为壳聚糖H3、H4、H5 和H6的质子峰,3.1为壳聚糖骨架上H2的质子峰,2.00为壳聚糖乙酰化基团的甲基质子峰[19]。图7(b)中1.50~1.60 是N-乙烯基吡咯烷酮上β-亚甲基的质子峰;1.90 是H4 处的质子峰;2.30~2.40 是吡咯环酮结构中O==C—CH2的质子峰;3.27 是吡咯环酮结构中N—CH2的质子峰;3.61~3.75 是PVP 上α-亚甲基的质子峰[8]。由1H NMR 进一步证明N-乙烯基吡咯烷酮已接枝共聚到壳聚糖侧链。
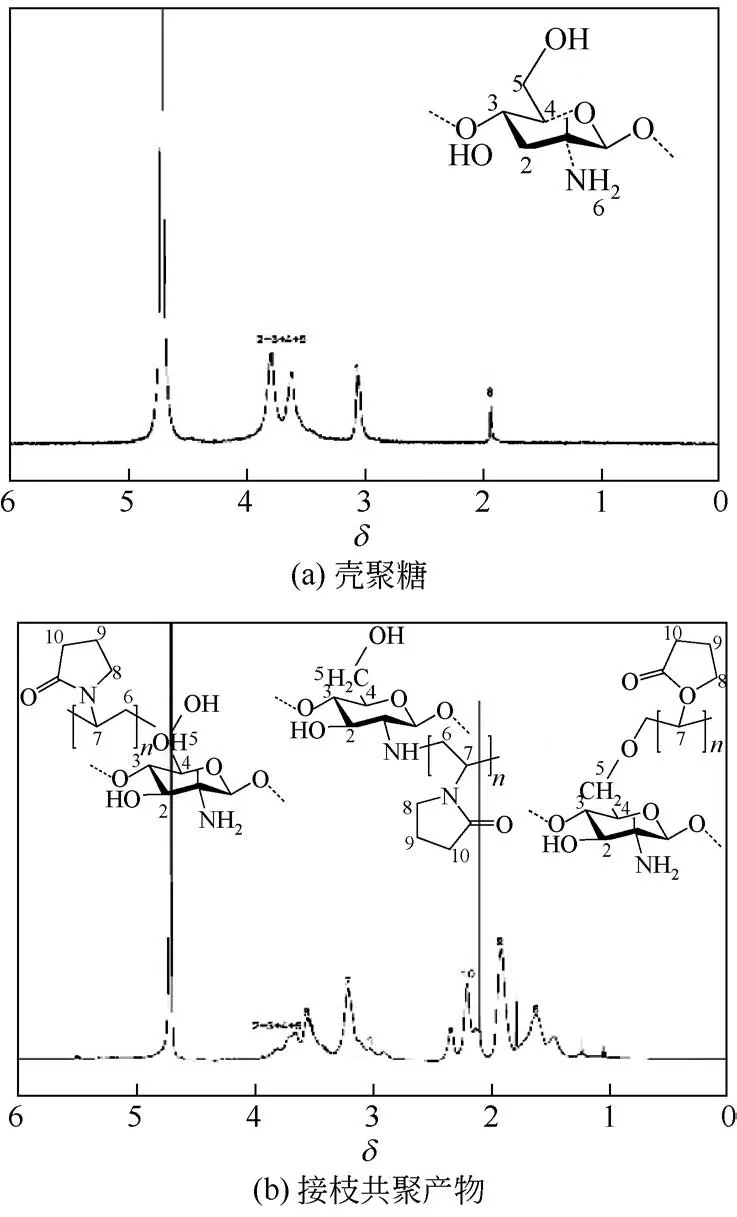
图7 壳聚糖和接枝共聚产物的1H NMR图
2.6 接枝共聚物的TG分析
分别称取壳聚糖、PVP和60℃、12h下产物5~10mg,测得TG、DTG 曲线如图8。图8 中曲线a 为壳聚糖的TG 与DTG 曲线,在100℃以下和268℃处分别出现两个失重,第一阶段失重为壳聚糖中结合水与自由水的丢失,而第二阶段为壳聚糖的主链分解[20]。曲 线b 为PVP 的TG 与DTG 曲 线,同 样 在100℃以下出现了失水峰,在395℃开始发生热分解。曲线c 为接枝共聚物的TG 与DTG 曲线,在100℃以下的结合水与自由水的失重高于壳聚糖,这是因为接枝N-乙烯基吡咯烷酮后,产物比壳聚糖具有更好的吸水性能,能从环境中吸收更多的水分。在100℃的失水阶段结束后,产物在150℃左右开始分解,并且没有明显的热分解平台,其热稳定性不如壳聚糖。这是因为接枝共聚了N-乙烯基吡咯烷酮后破坏了壳聚糖的结晶结构,导致产物的耐热性能下降。
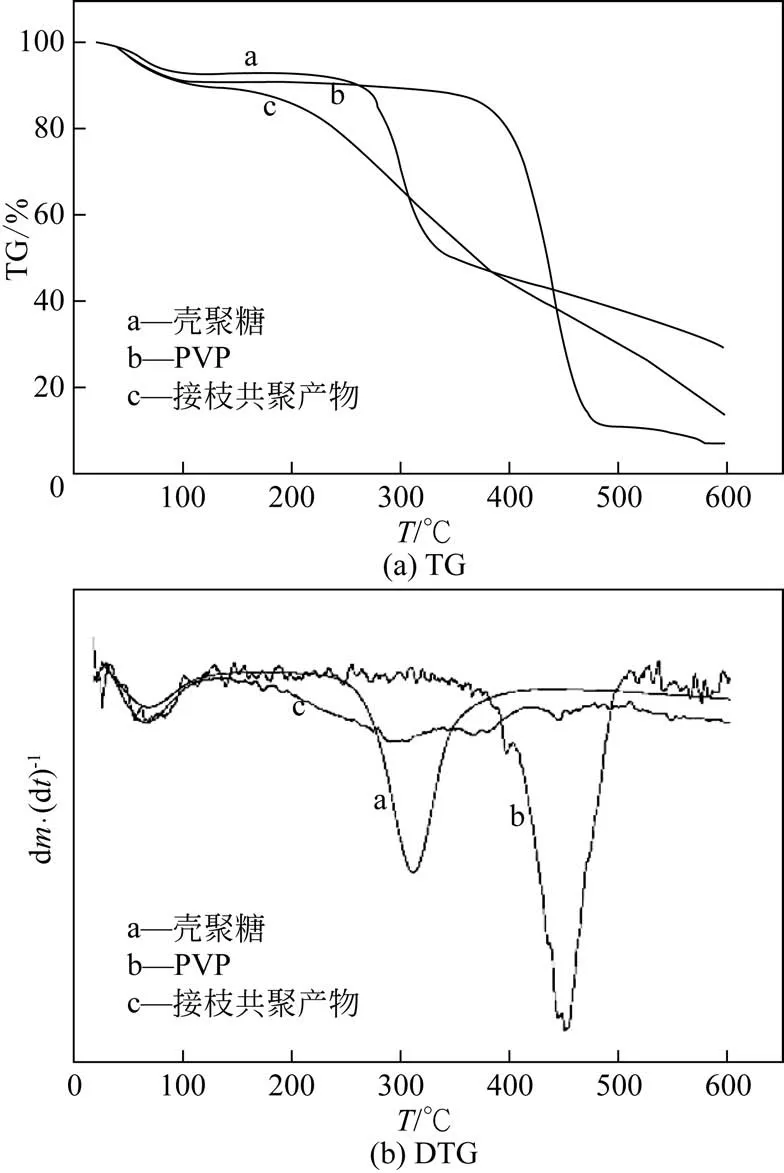
图8 壳聚糖、PVP和接枝共聚产物的TG与DTG图
2.7 接枝共聚物的吸湿性能
按照1.3.5 节的方法测得壳聚糖、聚乙烯基吡咯烷酮及60℃、12h 下产物的吸湿性能见表2。从表中可以看出,在饱和硫酸铵(相对湿度81%)的高湿度环境中放置24h 后,3 个样品均吸收了一定的水分。接枝共聚产物的吸湿性能明显大于壳聚糖,吸湿率为23.1%,但比具有良好水溶性能的聚乙烯基吡咯烷酮吸湿率低。在饱和氯化钙(相对湿度31%)的低湿度环境下,3个样品的吸湿率均较低,但产物的吸湿率仍高于壳聚糖,为3.60%。由以上可见,与壳聚糖相比,共聚产物的吸湿性能明显提高,产物具有一定的亲水性。
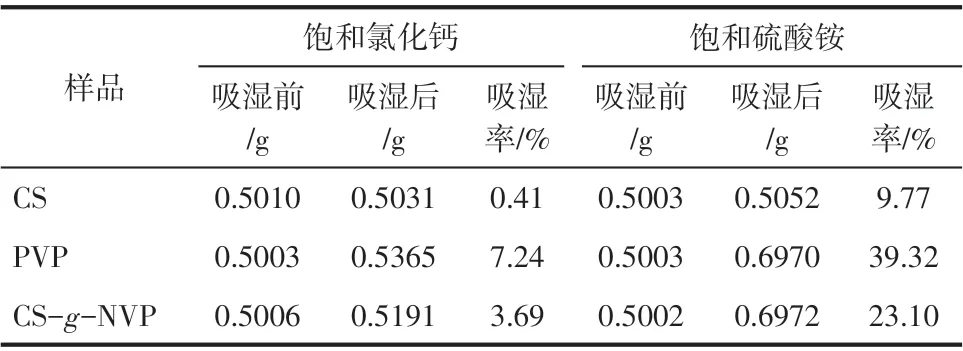
表2 原料与产物的吸湿率

图9 不同时间下,接枝共聚壳聚糖的水接触角
2.8 接枝共聚物的水接触角分析
将60℃、12h下产物的溶液均匀涂布在载玻片上,室温烘干成膜后,每间隔10s 测定其水接触角,结果如图9。从图中可以看出,随着时间的增加,水滴在薄膜表面逐渐铺展开来,水接触角逐渐减小,从65.09°下降至35.26°,显示出良好的亲水性。证明了接枝共聚产物具有良好的亲水性能。
2.9 接枝共聚物的溶解性能
按1.3.6 节的方法测定壳聚糖、聚乙烯基吡咯烷酮和产物在几种常用溶剂的溶解性能,结果见表3。由表中可见,壳聚糖除溶解于体积分数为2%乙酸溶液外,不溶于水和常见有机溶剂中;聚乙烯基吡咯烷酮溶解性能好,能够溶解于水及大多数常见的有机溶剂中;而接枝共聚产物能够溶解于水和2%乙酸溶液,但不能溶解于有机溶剂中。

表3 原料和产物的溶解性能
为了进一步考察接枝共聚产物的水溶性,试验了不同pH 下产物的溶解情况,结果如图10 所示。由图可见,壳聚糖只溶于酸性水溶液,在中性或碱性条件下几乎不溶,当pH>6 时,壳聚糖溶液迅速沉淀浑浊,溶液透射率急剧下降;聚乙烯基吡咯烷酮在酸性或碱性条件下均有较好的水溶性;而接枝共聚产物与壳聚糖相比,其溶解性能有较大改善,能够溶解于酸性和碱性水溶液中。
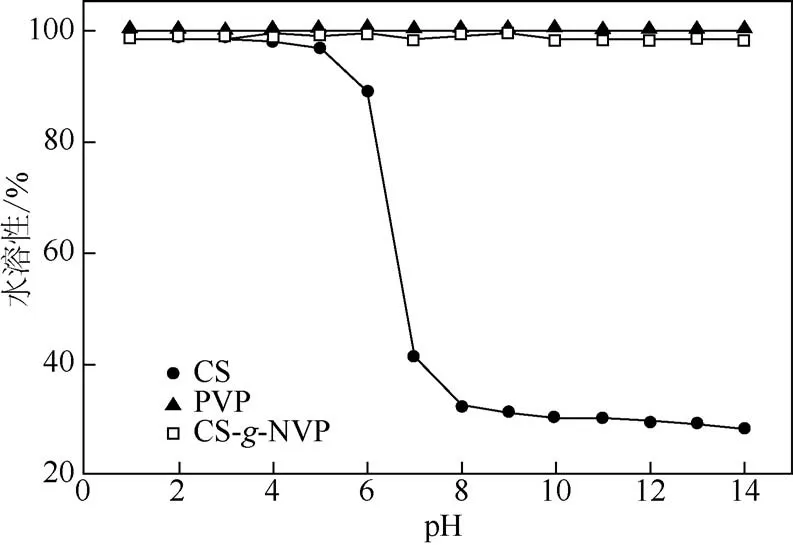
图10 壳聚糖、PVP和产物在不同pH下的水溶性
3 结论
(1)以壳聚糖和N-乙烯基吡咯烷酮为原料,采用过氧化氢和抗坏血酸共引发剂引发,制备壳聚糖/N-乙烯基吡咯烷酮的接枝共聚物。实验结果表明,接枝共聚反应的最佳条件为:引发剂抗坏血酸/过氧化氢的摩尔比为1∶1、反应温度60℃、反应时间12h。
(2)采用红外光谱仪与核磁共振波谱仪对产物进行表征,证明产物为壳聚糖/N-乙烯基吡咯烷酮接枝共聚物。
(3)吸湿性和亲水性能试验结果表明,接枝共聚产物在高湿度和低湿度环境下吸湿率分别为23.1%和3.69%,与壳聚糖相比,产物的吸湿性能明显提高,并且具有良好的亲水性能,能够溶解于酸性和碱性水溶液中,拓宽了壳聚糖在医疗器械、食品添加剂等领域的应用。
