均三嗪衍生物比色识别Cu2+及荧光识别Zn2+
2020-08-17李丽妹王梅阁杨秋生段中余
李丽妹,王梅阁,杨秋生,2,段中余,2
(1 河北工业大学化工学院,天津300130;2 天津市本质安全化工技术重点实验室,天津300130)
锌和铜是大多数生物必需的微量元素,也是人体内第二和第三重要的金属元素[1-2],在细胞呼吸、结缔组织发育等基本生理过程中起重要作用。锌和铜过量存在于人体内会引起严重的神经退行性疾病,比如阿尔茨海默症、前列腺癌、威尔逊氏病等[3-7];缺铜可能会导致血液和神经系统问题[8-9]。同时,过量的锌和铜金属排放还会引起严重的环境问题。因此,对金属锌和铜的识别检测至关重要,是化学领域的研究热点之一。目前对金属锌和铜的检测方法很多,如原子吸收分光光度法(AAS)、电感耦合等离子体质谱法(ICP-MS)及原子荧光分光光度法(AFS)等。离子探针作为检测、识别离子的一种方法,具有合成简单、灵敏度高、选择性好、响应速度快等特点,被广泛应用于生物、食品分析、药物诊断等方面,具有广阔前景[10-12]。
均三嗪是一种含大共轭结构的含氮芳杂环,在热稳定性、耐化学腐蚀、耐酸碱性、高强度等方面具有优异性能。均三嗪衍生物具有较强的电子亲和能力,易发生特定反应,在分子识别、自组装、传感器及构建树状分子中均占有重要地位[13]。席夫碱类化合物因其结构特殊,含有C==N,是一种良好的配体,并且合成方法比较简单[14]。将席夫碱与均三嗪结合,为离子识别提供了更多的可能性。本文以对氨基苯腈、邻叔丁基苯酚以及3,5-二叔丁基水杨醛为原料利用醛胺缩合反应合成了两种含均三嗪结构对称三爪离子探针(见图1),更加有利于专一性识别离子。探针1 可高选择性识别Zn2+,探针2 通过观察颜色变化可裸眼识别Cu2+,具有潜在的应用前景。
1 实验方法
1.1 仪器与试剂
Bruker AC 400MHz 型核磁共振波谱仪(德国Bruker 公司生产,内标为TMS,溶剂为CDCl3,DMSO-d6);Bruker Vector-22 型傅里叶交换红外光 谱 仪(KBr 压 片); Hermo-Finnigan TLCQ Advantage 型和Shimadzu LCMS-2020 液质联用仪(ESI模式);SDT-TG Q600型热重分析仪(美国TA公司生产);UV-6100 紫外-可见分光光度仪(上海元析仪器有限公司);F-4600 Hitachi荧光光谱仪(天美科学仪器有限公司)。对氨基苯腈、三氟甲磺酸、邻叔丁基苯酚、3,5-二叔丁基水杨醛均来自市售分析纯;其他试剂均经标准方法纯化后使用。
1.2 化合物制备
1.2.1 1,3,5-三-(4-胺基-苯基)三嗪(TAPT)的合成[15]
将3.86g(0.0325mol)4-氨基苯甲腈加入单口瓶中,冰浴,氩气环境下滴加15mL(0.1665mol)三氟甲磺酸。撤去冰浴,室温下反应24h。加入25mL的蒸馏水,产生橙黄色沉淀,加入2mol/L的NaOH溶液调节pH=7,沉淀溶解后变成淡黄色悬浊液,用300mL蒸馏水多次洗涤,过滤,取固体于55℃真空干燥12h,得到3.32g 淡黄色固体,产率86%。1H NMR(400MHz,DMSO-d6)δ=8.339~8.360(d,J=8.4Hz,6H), 6.677~6.698 (d,J=8.4Hz, 6H), 5.918(s,6H)。

图1 离子探针1和2的合成路线
1.2.2 邻叔丁基水杨醛的合成
将5.0g(0.033mol)邻叔丁基苯酚加入到双口瓶中,加入9.8g(0.103mol)无水氯化镁,氩气环境下加入100mL 四氢呋喃,开启搅拌,加入13mL(0.101mol)三乙胺,25℃下搅拌20min,颜色变青色,再加入3.5g(0.116mol)多聚甲醛,升温至回流,反应5h。加入80mL蒸馏水,加入浓盐酸调节pH=2~3,颜色为橙黄色,再加入100mL二氯甲烷搅拌,分层,将有机层用饱和食盐水洗涤3次,无水硫酸钠干燥有机相过夜,抽滤,旋蒸,得到黄绿色液体。柱层析(SiO2,石油醚/乙酸乙酯=200∶1)收集第一组分,得到2.36g浅黄色液体,产率40%。
1H NMR(400MHz,CDCl3)δ=11.82(s,1H),9.91(s,1H),7.47(s,1H),7.34(s,1H,ph-H),6.90(s,1H),1.34(s,9H)。
1.2.3 探针1的合成
将0.7g(0.002mol)TAPT 放入双口瓶中,氩气环境下加入100mL 乙醇,搅拌,升温到85℃,加入1.87g (0.008mol) 邻叔丁基水杨醛,反应24h。趁热将反应液倒入冷乙醇中,过滤,用50mL 冷乙醇反复洗涤, 35℃真空干燥12h,得1.23g 黄色固体,产率73.8%。1H NMR(400MHz,DMSO-d6)δ=14.068 (s,3H),9.122 (s,3H),8.882~8.860 (d,J=8.8Hz,6H),7.739~7.718(d,J=8.4Hz,6H),7.593~7.570 (d,J=9.2Hz,3H),7.455~7.385 (t,J=14Hz,3H),6.996~6.957 (t,J=7.8Hz, 3H), 1.406 (s, 27H);13C NMR (100MHz, DMSO-d6)δ=28.2, 29.7,33.5,119.2,121.9,129.2,134.4,135.6,159.0,162.3; IR (KBr)ν: 3448 ( —OH), 3080(Imine==C—H),2860(tert-butyl —C—H),1627(—C==N—),912,810(triazine)cm-1;ESI-MS(m/z):[M+Na]+:857.42,Found:856.30。
1.2.4 探针2的合成
将1.05g(0.003mol)TAPT 放入双口烧瓶中,氩气环境下加入30mL DMF 使之溶解,将2.43g(0.01mol)3,5-二叔丁基水杨醛溶于100mL 无水乙醇,用注射器将其加入双口瓶中,在氩气环境下,85℃反应48h。待反应完毕,冷却至室温,抽滤,并用无水乙醇冲洗,取固体60℃真空干燥,得1.60g 淡黄色固体, 产率53.8%。1H NMR(400MHz,CDCl3)δ=8.872~8.894 (d,J=8.8Hz,6H),8.778(s,3H),7.525~7.530(d,J=2.0Hz,6H),7.496~7.517 (d,J=8.4Hz,3H),7.312~7.318(d,J=2.4Hz,3H),1.527(s,27H),1.381(s,27H);13C NMR (100MHz CDCl3)δ=171.0,164.8,158.5,152.5,140.8,137.2,134.3,130.3,128.6,127.1,121.5,121.4,118.2,35.1,34.2,31.5,29.4;IR (KBr)ν:3403 (—OH),2950,1913,2867(tert-butyl C—H),1621(—C==N—),873,811(triazine)cm-1;LCMS(m/z):[M+Na]+:1026.39,Found:1027.5。
1.3 离子识别实验
向1.0×10-5mol/L浓度的探针1 和2的N,N-二甲基甲酰胺(DMF)溶液中加入2.0×10-5mol/L的不同阳离子(Cr3+、Mn2+、Fe3+、Co2+、Ni2+、Cu2+、Zn2+、Cd2+、Hg2+、K+、Na+)的DMF溶液,混合均匀后,进行紫外吸收光谱测试,观察金属离子加入前后的谱图变化。向1.0×10-6mol/L浓度的探针1 和2 的DMF溶液中加入2.0×10-6mol/L的不同阳离子(Cr3+、Mn2+、Fe3+、Co2+、Ni2+、Cu2+、Zn2+、Cd2+、Hg2+、K+、Na+)的DMF溶液,混合均匀后,进行荧光光谱测试,观察金属离子加入前后的谱图变化。
2 结果与讨论
2.1 热稳定性
通过对两种探针的热稳定性分析,探针1的热分解温度为272℃,探针2 的热分解温度为340℃,见图2。探针2 的热稳定性比探针1 好,可能是由于叔丁基增多,使得探针共轭程度增强。表明引入叔丁基基团可以提高热稳定性。

图2 探针1和2的热重分析
2.2 探针1和2识别性能
2.2.1 紫外-可见光吸收光谱分析
为了探究探针1 和2 对金属离子的识别性能,向探针1 和2 溶液中分别加入2.0×10-5mol/L 不同金属离子(Cr3+、Mn2+、Fe3+、Co2+、Ni2+、Cu2+、Zn2+、Cd2+、Hg2+、K+、Na+),紫外吸收光谱变化如图3所示。由于探针分子具有大的共轭体系,n→π*跃迁,探针1在λ=360nm有最大吸收峰,加入Hg2+后,吸收峰强度显著降低,其他离子的加入没有引起明显变化。探针2 在λ=345nm、373nm 处有最大吸收峰,出现双峰可能是由另一个叔丁基的引入造成的。加入Cu2+后,吸收峰发生明显变化,λ=345nm处吸收峰蓝移,λ=373nm 处吸收峰消失并且在λ=430nm处出现新的吸收峰,自然光下,加入Cu2+后的探针溶液由无色变为黄色;加入Hg2+后在λ=360nm形成新的吸收单峰,其他离子的加入没有引起明显变化。以上结果表明通过紫外吸收光谱探针1和2均能对Hg2+有识别作用,并且探针2对Cu2+还可以实现高选择性的裸眼识别。
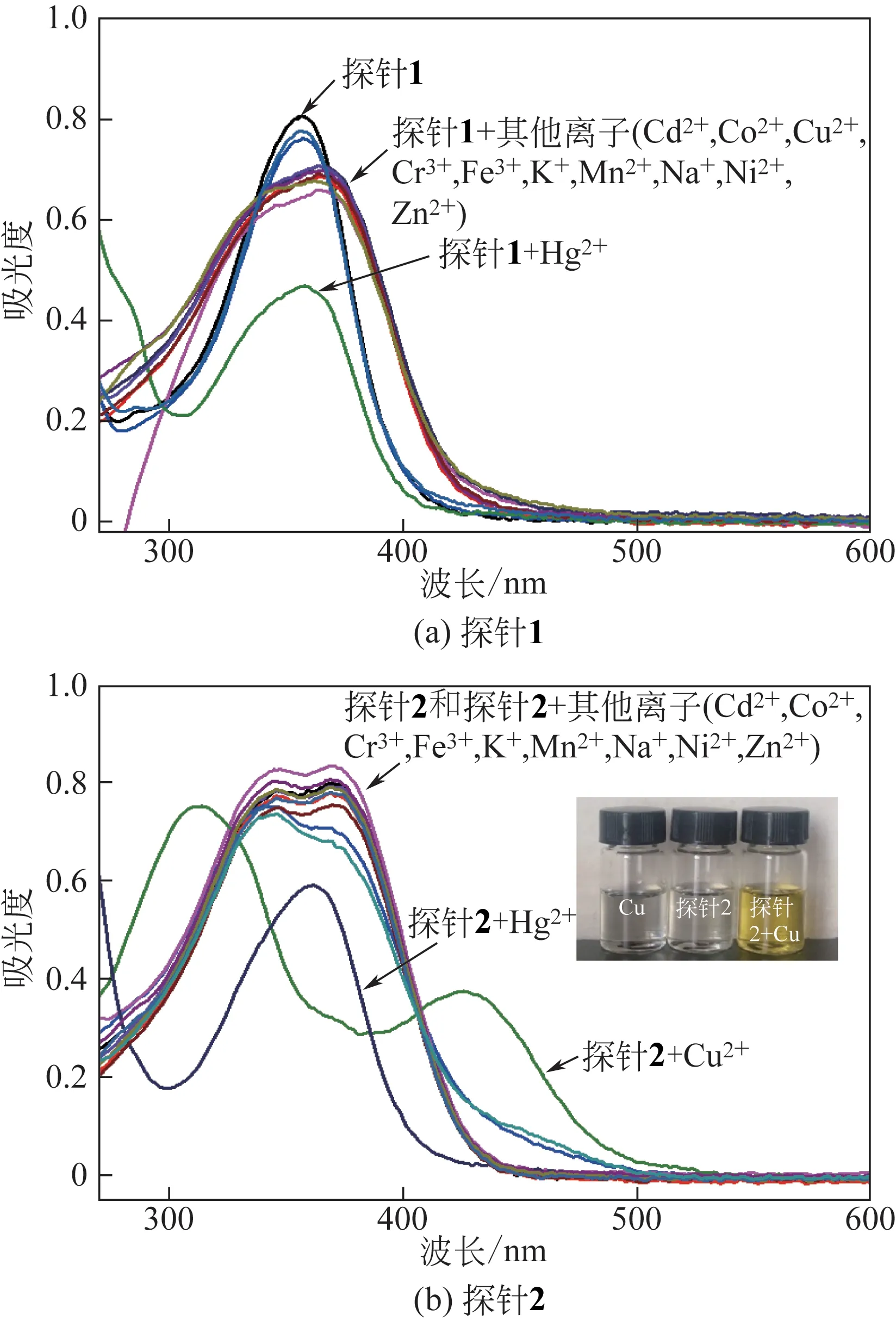
图3 不同金属离子对探针(1.0×10-5mol/L)的紫外吸收光谱的影响
通过探针2 与Cu2+的紫外滴定实验,定量研究了不同浓度的Cu2+对探针2 紫外吸收光谱的影响。如图4 所示,随着Cu2+浓度增加,探针2 在λ=316nm 的吸收峰蓝移,λ=373nm 吸收峰逐渐消失,λ=430nm 处逐渐出现新的吸收峰并且吸收峰强度逐渐增强。在λ=327nm 和407nm 处形成两个等吸收点,表明Cu2+与探针2 形成稳定的配合物。通过数据的线性拟合[16-17],计算出探针2对Cu2+的紫外最低检出限LOD 为2.24×10-6mol/L,因此探针2 可定量检测Cu2+。
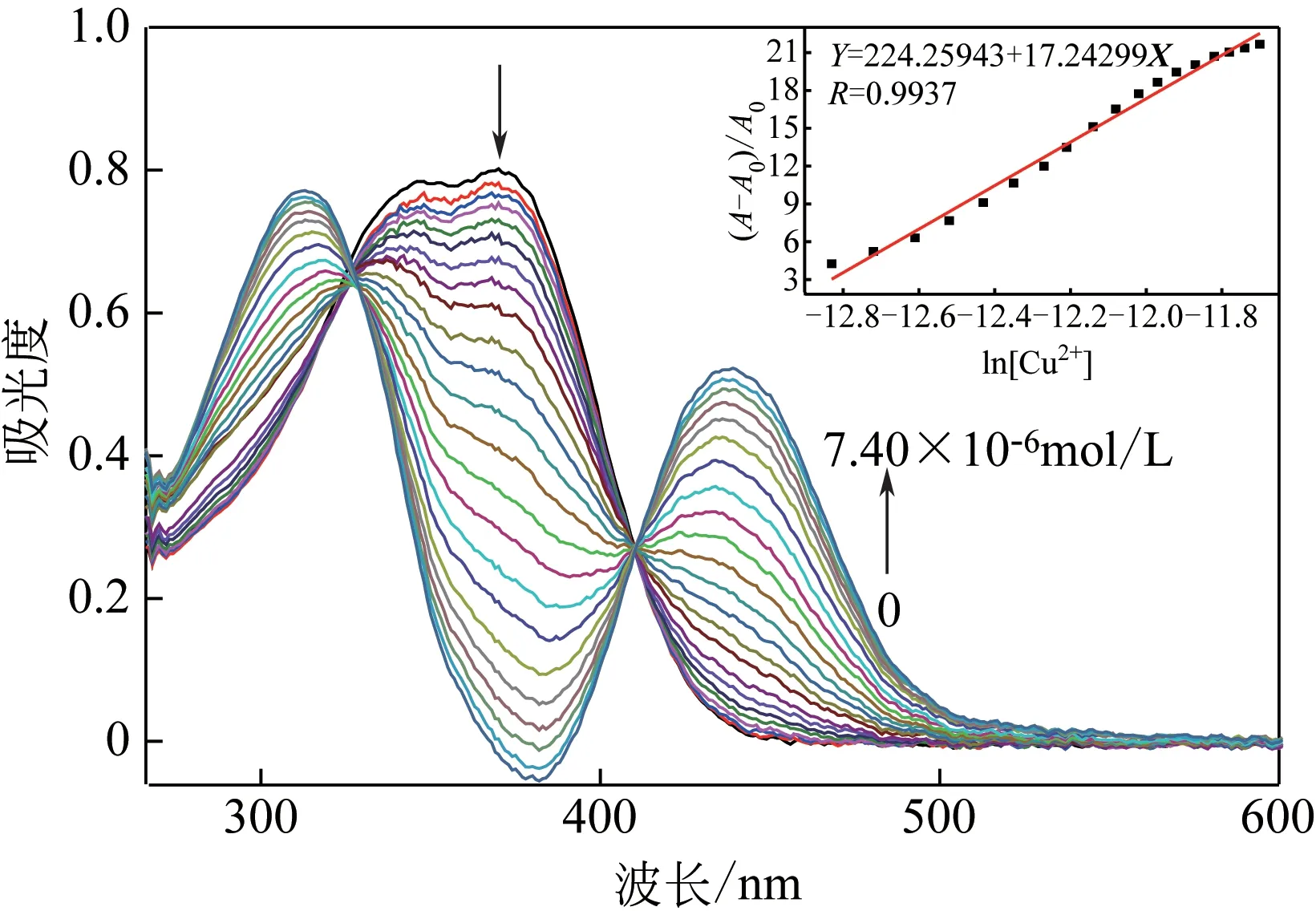
图4 Cu2+浓度对探针2(1.0×10-5mol/L)紫外-可见光吸收光谱图
2.2.2 荧光光谱分析
向探针1 和2(1.0×10-6mol/L)溶液中分别加入不同金属离子(Cr3+、Mn2+、Fe3+、Co2+、Ni2+、Cu2+、Zn2+、Cd2+、Hg2+、K+、Na+),进行荧光光谱测试。如图5(a)所示,探针1 荧光强度很弱,加入Zn2+后荧光强度发生显著增强。这可能是由于探针1 中的C==N 双键发生异构化使其表现出很弱的荧光,加入Zn2+后,与C==N 的氮原子及—OH 的氧原子配位,C==N 异构化受阻,分子刚性增强,分子内电子转移受阻,使得荧光强度增强[18-19]。在460nm 和540nm 出现两个峰是由于形成配合物时,探针1 结构发生构型变化,出现了双发射通道[20]。而加入其他金属离子的荧光谱图没有明显变化,这说明探针1 对Zn2+具有极高的选择性。如图5(b)所示,向探针2 中加入金属离子后谱图均没有明显变化。荧光谱图表明,探针1 可以高选择性地识别Zn2+。
通过探针1 与Zn2+的荧光滴定谱图(图6)可以看出,随着Zn2+浓度的不断增加,荧光强度不断增强并逐渐趋于饱和状态,说明探针1 与Zn2+已形成稳定配合物。通过线性拟合计算出探针1 对Zn2+荧光最低,检出限LOD为1.02×10-6mol/L。
2.3 探针识别离子的抗干扰性能
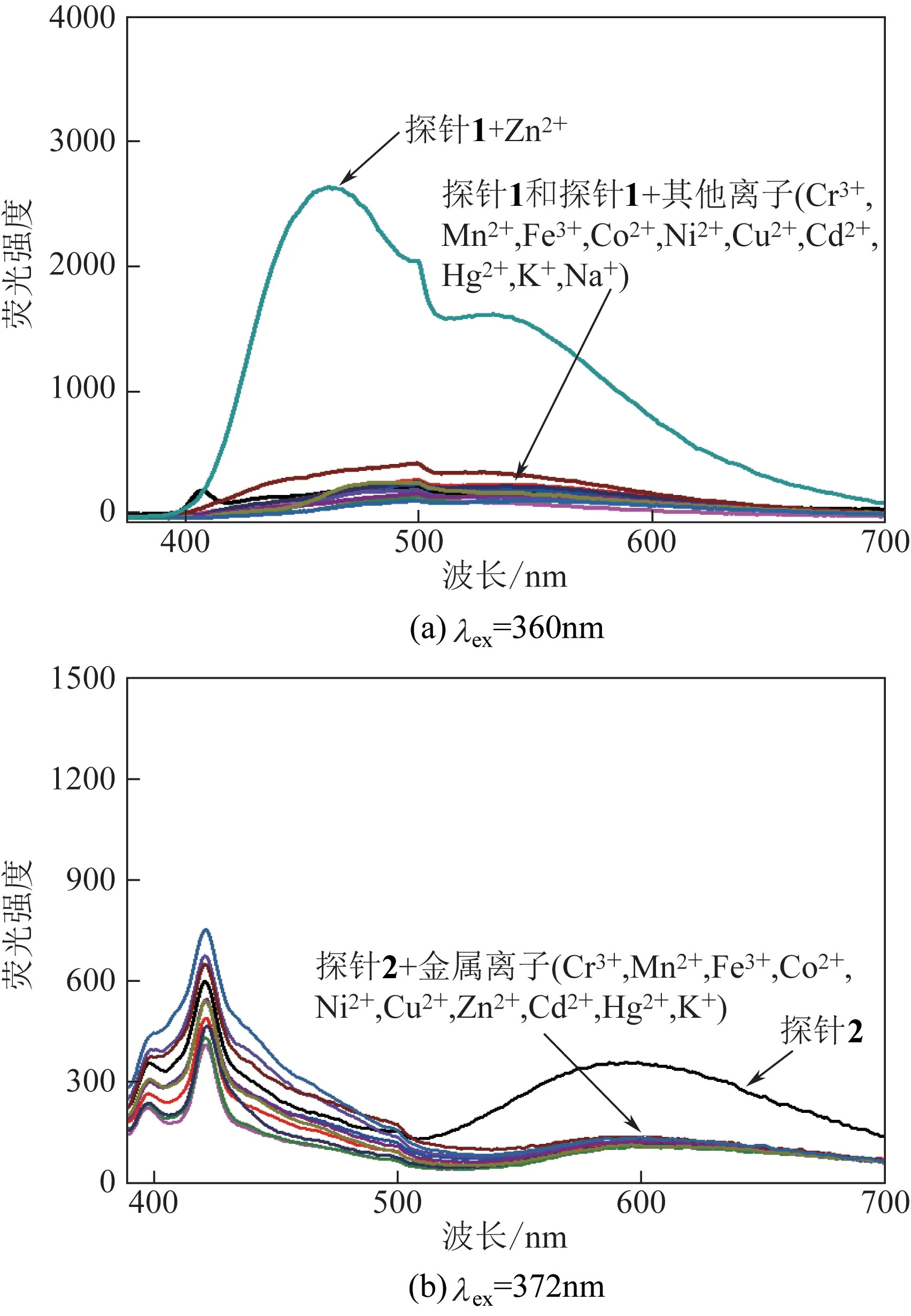
图5 不同金属离子对探针(1.0×10-6mol/L)荧光光谱的影响
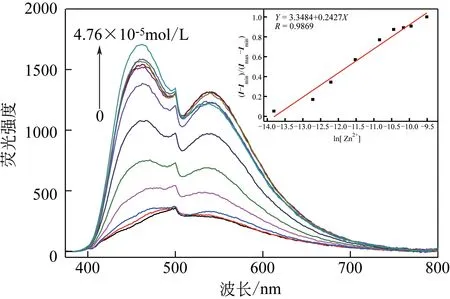
图6 Zn2+浓度对探针1(1.0×10-6mol/L)荧光强度影响
为了检测其他金属离子的存在对探针1 荧光识别Zn2+以及探针2 紫外识别Cu2+有无干扰,首先进行了探针1 在Zn2+和其他金属离子共存时的干扰实验,结果如图7(a)所示。在其他金属离子(Cr3+、Mn2+、Fe3+、Co2+、Ni2+、Cu2+、Cd2+、Hg2+、K+、Na+)存在时,向探针1 加入Zn2+引起的荧光增强现象基本没有发生变化,由此说明探针1 识别Zn2+有很好的抗干扰性。同样进行了探针2 的抗干扰实验,如图7(b)所示。在其他金属离子(Cr3+、Mn2+、Fe3+、Co2+、Ni2+、Zn2+、Cd2+、Hg2+、K+、Na+)存在时,向探针2 加入Cu2+使λ=430nm处出现新吸收峰且强度增强,而加入Hg2+基本没有变化。Hg2+的加入使λ=430nm吸收峰强度有所减弱,这表明当Hg2+与Cu2+共存时,探针2 识别Cu2+会受到一定的干扰,探针2 抗干扰性相对探针1 较差。
2.4 探针识别机理
为了进一步研究探针对金属离子的相互作用,利用核磁共振氢谱探究了探针1 和Zn2+的作用机理,结果如图8 所示。对比探针1 和向探针1 加入Zn2+的核磁共振氢谱可以看出Ha消失,表明探针1 与Zn2+结合时发生去质子化[16];与羟基相连的苯环中的He、Hc、Hd的化学位移均向高磁场低位移方向偏移,表明羟基参与配位,这是由于氢键被破坏,去屏蔽效应消失,质子峰向高场移动;亚胺键的Hf同样向高场偏移,表明亚胺键中的N 原子参与配位。这些变化表明探针1 中的—OH、—C==N—的N 原子与Zn2+配位形成1-Zn2+配合物,配位模式如图9所示。

图7 金属离子和Zn2+、Cu2+共存时,对探针的荧光强度和吸光度的影响

图8 加入Zn2+后探针1氘代DMSO中的1H NMR对比图
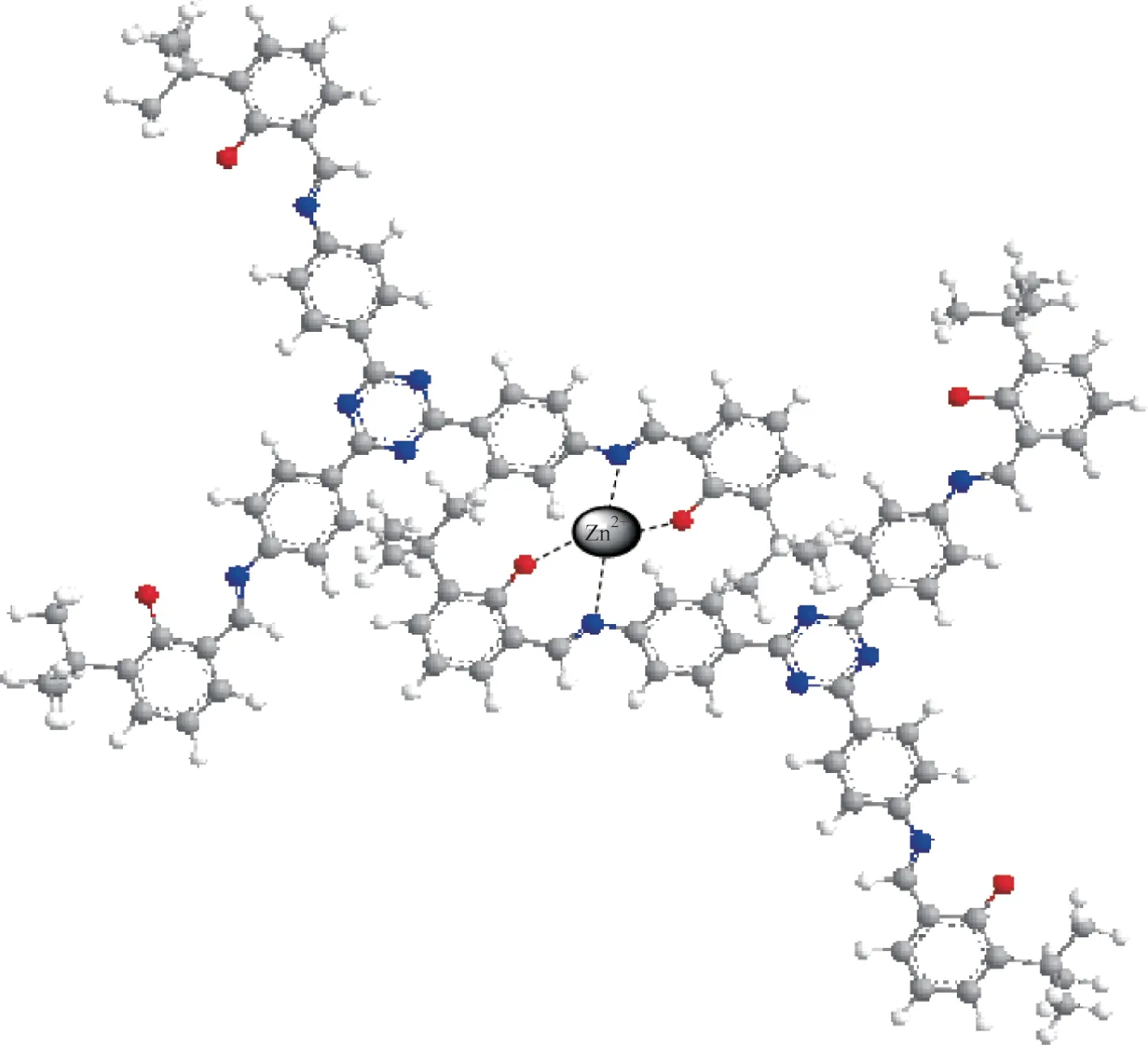
图9 探针1识别Zn2+的机理
3 结论
通过醛胺缩合反应制备了两种含均三嗪结构的离子探针,具有良好的热稳定性能。探针1作为一种荧光增强型探针,利用荧光光谱可高选择性地识别Zn2+;探针2是一种可裸眼识别的Cu2+探针,同时紫外吸收光谱中长波长处出现新吸收峰,可以高选择性地识别Cu2+。该方法简便高效,为实际应用提供一定依据。
