三嗪环类高能产气衍生物分子设计及性能的理论计算
2019-03-04段英杰王建华荆苏明王国栋武秋红
段英杰,王建华,荆苏明,王国栋,2,武秋红
(1.中北大学环境与安全工程学院,山西 太原 030051;2.陆军工程大学,河北 石家庄 050003)
引 言
目前,国内外气体发生剂配方主要有3类:火药类及其改进的配方;新型产气剂;烟火类混合药剂。高能产气衍生物是指在燃烧爆炸过程中能在产生一定能量的同时生成大量气体产物的一系列含能化合物,可作为气体产生剂的重要组分。由于富氮杂环具有高密度、高正生成焓、热稳定性好等优点,可作为气体发生剂、固体推进剂燃料以及烟火剂[1]。目前气体发生剂中常用的富氮杂环主要为唑类和胍类,嗪类在气体发生剂中的应用较少。三嗪环张力较小,稳定性好,含氮量极高,具有较高的生成焓。三嗪环有3个可修饰的位点,可以与亲核试剂反应得到一系列的衍生物。张玉根等[2]以均三嗪为基本结构合成了耐热性能良好的新型叠氮-均三嗪类含能化合物;Yang K等[3]将硝基引入三嗪环计算得到爆炸性质与HMX和RDX相似的2-氨基-4、6-二硝基-1、3-3-三嗪(ADNTA)和2,4,6-三硝基-1,3,5-三嗪(TNTA);Kizhnyaev V N等[4]通过在三嗪环上引入硝基三唑合成了一系列含4-硝基-1,2,3-三唑的1,3,5-三嗪;L.I.Vereshchagin等[5]用四唑取代含氯三嗪中的氯,从而得到了多种新型富氮含能化合物。
在含能化合物的常见基团中,硝基能提高含能化合物的能量,氨基与硝基交替存在能在提高能量的基础上保持结构的稳定性,而叠氮基的含氮量极高,燃烧产生的氮气能够提高产物中气体的摩尔体积,达到产气的目的。因此本研究选择1,3,5-三嗪为研究对象,以三嗪环为基本结构单元,引入叠氮基、硝基、氨基,设计了15种三嗪环类高能产气衍生物分子,利用量子化学中的密度泛函理论对所设计分子的几何构型、密度、生成焓、爆轰参数、产气量、静电势和撞击感度等进行了理论研究,为三嗪环类高能产气衍生物的合成提供候选物。
1 计算方法
以1,3,5-三嗪环为基本结构单元设计了15种三嗪环类高能产气衍生物分子:2-叠氮基-1,3,5-三嗪(A1)、2-硝基-1,3,5-三嗪(A2)、2-氨基-1,3,5-三嗪(A3)、2-硝基-4,6-二叠氮基-1,3,5-三嗪(B1)、2-氨基-4,6-二叠氮基-1,3,5-三嗪(B2)、2-叠氮基-4,6-二硝基-1,3,5-三嗪(B3)、2-氨基-4,6-二硝基-1,3,5-三嗪(B4)、2-叠氮基-4,6-二叠氨基-1,3,5-三嗪(B5)、2-硝基-4,6-二氨基-1,3,5-三嗪(B6)、4,4′-二硝基-2,2′-联1,3,5-三嗪(C1)、4,4′-二氨基-2,2′-联1,3,5-三嗪(C2)、4,4′-二叠氮基-2,2′-联1,3,5-三嗪(C3)、4-氨基-4′-硝基-2,2′-联1,3,5-三嗪(C4)、4-氨基-4′-叠氮基-2,2′-联1,3,5-三嗪(C5)、4-硝基-4′-叠氮基-2,2′-联1,3,5-三嗪(C6)。15种化合物的结构见图1。

图1 三嗪环含能化合物的结构Fig.1 Structure of triazine ring-containing energetic compounds
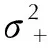
在B3LYP/6-31G*基组水平计算目标化合物分子体积Vm,并利用Rice等[7]提出的公式预测了化合物的理论密度ρ:
(1)
式中:Vm为分子摩尔体积;M为分子摩尔质量。


图2 三嗪环化合物的等键反应Fig.2 Isotope reactions of triazine ring compounds


(2)
(3)
基于目标化合物的密度和固相生成焓,运用Kamlet-Jacobs方程计算其理论爆速(D)和理论爆压(p)[10]:
(4)
(5)

Pospisil等[11]认为,分子表面静电势与含能化合物的撞击感度有密切的联系,并提出了撞击感度预测公式。本研究在B3LYP/6-31G*基组水平下绘制了部分化合物的静电势分布图,并采用如下经验关系式预测化合物的撞击感度H50(落锤质量为2.5kg):
(6)

爆容为单位质量的含能化合物爆炸后生成的产物在标准条件下占有的体积,而含能化合物爆炸产生的固体产物体积基本可以忽略,因此单位质量的产气量可以用爆容来估算。爆容可通过阿佛加德罗(Avogadro)定律求得[12]:
(7)
式中:V0为爆容,cm3/g;n为爆炸生成的气体组分的摩尔数;M为摩尔质量,g/mol。
2 结果与讨论
2.1 结构分析
通过振动频率分析的输出文件发现,15种化合物的结构均无虚频,所以优化后的结构是相对稳定的结构。为了更好地分析目标化合物的结构,表1列出了目标化合物A3、B3、B4、B6和C1的部分原子Mulliken电荷值。

表1 化合物A3、B3、B4、B6和C1的部分原子电荷Table 1 Partial atomic charges of compounds A3,B3,B4,B6 and C1
由表1可知,目标化合物A3、B3、B4、B6和C1的三嗪环上原子的总Mulliken电荷均在0.415~0.649e之间,硝基上N原子的Mulliken电荷均在0.207~0.408e之间,氧原子的电荷均为负。目标化合物B4和C1中原子的Mulliken电荷呈对称分布,与结构对称性相一致。
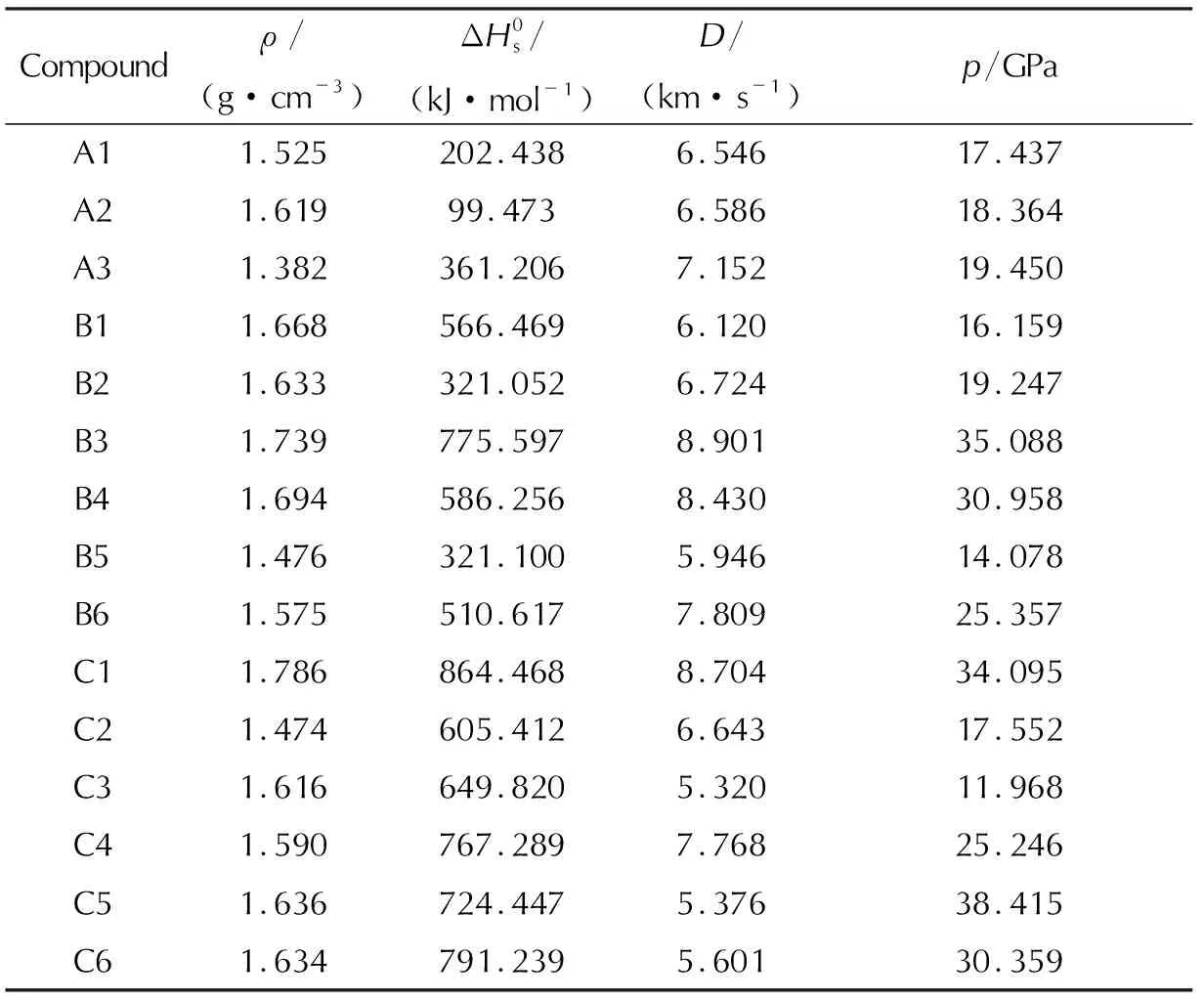
2.2 密 度
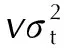

表2 化合物的分子体积、静电势参数和密度Table 2 Molecular volume, electrostatic potential parameters, and density of the compounds
2.3 气固相生成焓


表3 参考物质的总能量E0、零点能EZPE、热校正值HT和气相生成焓Table 3 Total energy E0, zero point energy EZPE, enthalpy correction HT and gas phase enthalpy of formation for reference substances

表4 目标化合物的气相生成焓升华焓ΔsH0以及固相生成焓Table 4 Gas phase enthalpy of formation enthalpy of sublimation ΔsH0 and solid phase enthalpy of formation of the target compound
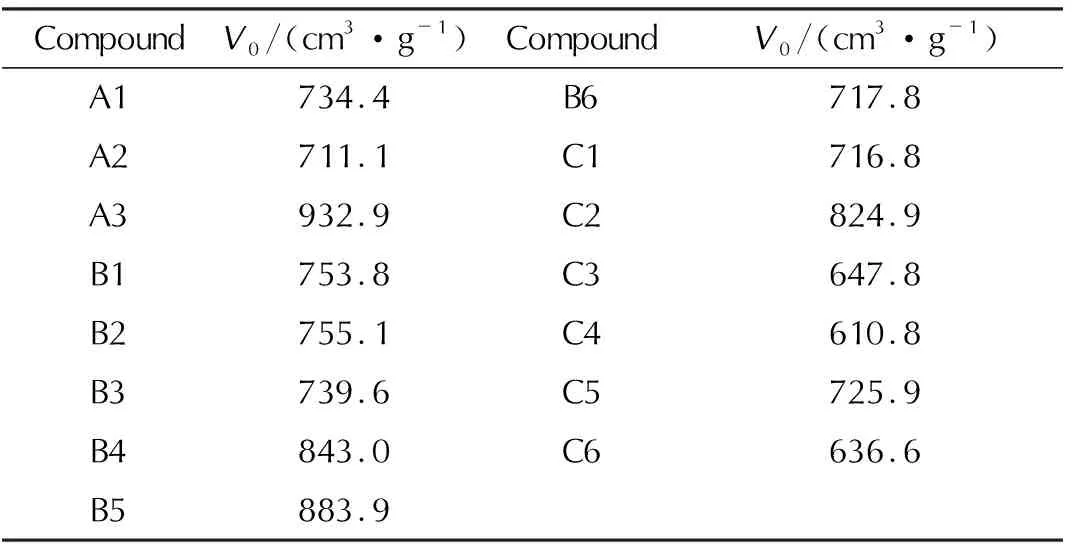
由表4可以发现,B3和C1具有较高的生成焓;不同的含能基团对生成焓的贡献大小关系为:—NO2>—N3>—NH2;对于相同的含能基团,环数的增加会导致化合物的生成焓增加:A1 基于15种三嗪环化合物的密度和固相生成焓,运用Kamlet-Jacobs方程,结合式(4)、式(5)计算其爆轰参量(爆速和爆压),计算结果见表5。 表5 目标化合物的密度、固相生成焓和爆轰参数Table 5 Density, solid phase enthalpy of formation, detonation parameters of the target compound 从表5可以看出,对于相同的含能基团,环数的增多会导致化合物的爆速和爆压上升;当含能基团有—NO2时,化合物的爆速、爆压有明显提高。含能基团为—NH2与—NO2的三嗪环化合物(如B4)与含能基团中只有—NO2的三嗪环化合物(如C1)相比,其密度、爆速和爆压有所下降,表明—NH2会降低三嗪环类化合物的能量水平。 利用式(7)计算了单位质量的目标化合物的产气量(爆容),结果见表6。 表6 目标化合物单位质量的产气量Table 6 Gas production per unit mass of the target compound 从表6可以看出,对于单个三嗪环,当只有一个取代基时,不同含能基团对产气量的贡献为:氨基>叠氮基>硝基。当有多个取代基时—NH2的存在会提高化合物的产气量,不同含能基团对产气量的贡献依然满足:氨基>叠氮基>硝基。对于联三嗪,当取代基为一种时,—NO2对产气量的贡献最大;当取代基为两种时,含—NO2的化合物产气量有所降低。 在B3LYP/6-31G*水平下,计算了15种化合物的最高占据轨道(HOMO)能量、最低空轨道(LUMO)能量以及两者的能极差,结果见表7。 表7 目标化合物的HOMO能量、LUMO能量以及两者之差Table 7 HOMO energy, LUMO energy of the target compounds and the difference between the two 从表7可以得出,15种化合物的HOMO能量的负值表示其第一电离能,电离能越低说明越容易失去电子,同理LUMO能量也为负,且负值越大越容易得到电子。HOMO和LUMO的差值比较小,说明分子容易被激发,在外界刺激下发生反应的可能性较高。 分子的静电势图能比较直观地反映分子的静电势分布情况。从密度和生成焓的计算结果可以看出,化合物A2、B3、B4、B6和C1的密度与生成焓较高,性能相对优良,所以本研究重点分析了这5种化合物0.001a.u.的电子密度等值面上的立体静电势分布图,结果见图3。 从图3可以看出,3种化合物都是正静电势,主要分布在三嗪环的环结构上,面积较小,负静电势主要分布在硝基的氧原子附近,面积较大,这与Klaptke等[15]对含能材料的定性研究相符合,为潜在的含能材料。 用化合物静电势的部分参量,利用式(6)计算化合物的撞击感度,以特性落高H50表示,结果见表8。 图3 化合物A2、B3、B4、B6和C1的静电势分布(图中蓝色部分为正静电势,橘红色部分为负静电势)Fig.3 Electrostatic potential distribution of compounds A2、B3、B4、B6 and C1(The blue part in the figure is positive electrostatic potential, and the orange-red part is negative electrostatic potential) Compoundvσ2+/(kJ2·mol-2)H50/cmA10.242506251565.391855A20.235228242163.546353A30.230472490.257651B10.2246791605.176050B20.2067112822.129245B30.1310172401.876427B40.1338764824.819127B50.2032832999.457245B60.1905963978.581141C10.2263522619.224250C20.2456442792.301755C30.227866765.473051C40.2219992210.242149C50.2493223458.819356C60.2438882458.326455 注:v为静电平衡系数;σ2+为正静电势方差。 由表8可以看出,不论是单环还是多环化合物,取代基为同一种时,由于三嗪环本身的稳定性很好,所以几种物质的撞击感度差别不大;对于多种取代基同时存在的化合物,其感度略高于只有一种取代基的化合物,并且随着—NO2的数量增加,感度也相应提高。 基于理论计算结果,从15种化合物中筛选出B4作为三嗪环类高能产气衍生物合成的候选产物,表9列出了B4以及常见含能化合物TNT和RDX的性能参数,其中TNT和RDX的密度、生成焓、爆轰参数和单位质量的产气量(爆容)均取自文献[16]。 表9 优选的一种三嗪环化合物及常见含能化合物的性能参数Table 9 Performance parameters of a preferred triazine ring compound and common energetic compounds 从表9可知,B4的密度大于1.65g/cm3,固相生成焓、爆速和爆压较高且远高于TNT,且B4的产气量远高于TNT。化合物B4可作为三嗪环类高能产气衍生物的合成候选物。 (2)三嗪环的存在能有效提高含能化合物的能量水平;—NO2对能量的贡献高于—N3与—NH2;—NO2对爆速与爆压的增加有明显的作用;而—NH2则会降低三嗪环类化合物的能量水平。 (3)依据理论计算结果,考虑其产气量和爆轰性能,筛选出2-氨基4,6-二硝基-1,3,5-三嗪(B4)作为三嗪环类高能产气衍生物的候选产物,是具有应用潜力的含能产气化合物。2.4 爆轰性能
2.5 单位质量的产气量
2.6 分子前线轨道

2.7 静电势与撞击感度


2.8 优选三嗪环类高能产气衍生物及其综合性能对比
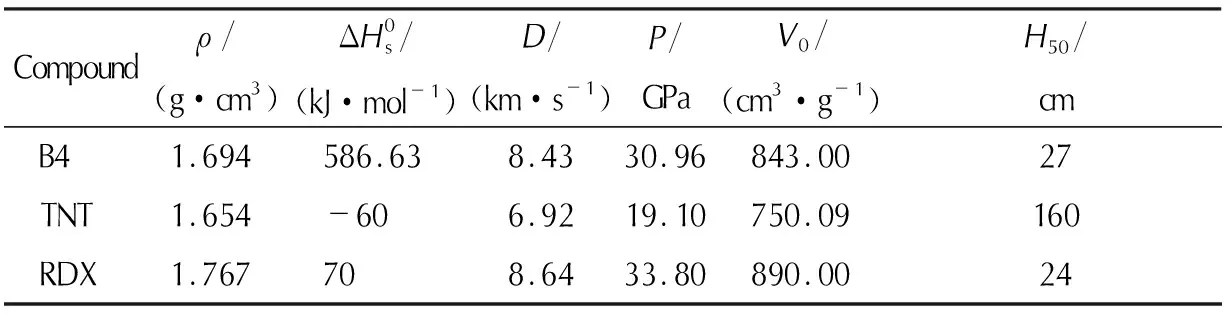
3 结 论

