布鲁氏菌抗原检测试剂用国家参考品的研制
2020-06-19张园园张平平王春娥赵爱华杨瑞馥魏东
张园园,张平平,王春娥,赵爱华,杨瑞馥,魏东
·论著·
布鲁氏菌抗原检测试剂用国家参考品的研制
张园园*,张平平*,王春娥,赵爱华,杨瑞馥,魏东
102629 北京,中国食品药品检定研究院卫生部生物技术检定方法及其标准化重点实验室(张园园、王春娥、赵爱华、魏东);100071 北京,军事科学院军事医学研究院微生物流行病研究所病原微生物生物安全国家重点实验室(张平平、杨瑞馥)
研制布鲁氏菌抗原检测试剂评价用国家参考品。
将 3 株布鲁氏菌标准株和 10 株阴性参考菌株在各自适宜的培养基和温度下进行培养,收集新鲜培养物并灭活,采用比浊法制备阳性和阴性参考品菌液;分光光度法制备最低检出量和重复性参考品菌液。对参考品进行均匀性检测和稳定性试验,组织 4 个实验室对布鲁氏菌抗原检测试剂用参考品进行协作标定。
建立了由 3 株布鲁氏菌为阳性参考品、10 株阴性菌为阴性参考品、最低检出量参考品及重复性参考品组成的布鲁氏菌抗原检测试剂评价用国家参考品。该参考品具有较好的均匀性及稳定性。协作标定结果为阳性参考品符合率均为 100%,阴性参考品符合率均为 90%,最低检出量参考品的检出限为 1 × 107~ 1 × 106个/ml 之间,重复性参考品均符合规定。
研制的布鲁氏菌抗原检测试剂评价用国家参考品可用于布鲁氏菌抗原检测试剂的质量控制。
布鲁氏菌;抗原; 国家参考品; 均匀性; 稳定性
布鲁氏菌病(简称布病)是由布鲁氏菌(简称布氏菌)引起的一类人畜共患疾病,是《中华人民共和国传染病防治法》中规定报告的乙类传染病。布病在世界范围内广泛流行,是全球特别是发展中国家面临的主要公共卫生问题[1-2]。布病可通过口腔黏膜、鼻腔、眼结膜、生殖道,甚至未损伤的皮肤感染[3]。布病不仅影响畜牧业和相关产业的发展,造成社会经济损失,还对人类的健康构成重大威胁[4],美国疾病预防控制中心将布氏菌列为潜在的生物恐怖战剂[5-6]。我国是布病的历史疫区,近年来布病流行较为严重,且发病率逐年递增,2018 年发病率为 2.73/10 万,已经连续十年年发病人数超过 3 万。
布鲁氏菌抗原检测是疾病诊断中重要的实验室检查项目,而我国尚无布鲁氏菌抗原检测试剂评价用国家参考品。为此,我们研制了布鲁氏菌抗原检测试剂评价用参考品,其对于布鲁氏菌抗原检测试剂的注册管理、指导我国该类试剂的健康有序发展,均具有重要意义。现将布鲁氏菌抗原检测试剂评价用参考品研制情况报道如下。
1 材料与方法
1.1 主要材料
1.1.1 菌种 牛种布氏菌 104M 株(CMCC55010)、猪种布氏菌 S2 株(CMCC55007)、羊种布氏菌 M5 株(CMCC55009)、大肠埃希菌(CMCC44113)、小肠结肠炎耶尔森菌 O:3 血清型(CMCC52203)、小肠结肠炎耶尔森菌 O:8 血清型(CMCC52211)、小肠结肠炎耶尔森菌 O:9 血清型(CMCC52212)、土拉热弗朗西丝菌 LVS 株、鼠疫耶尔森菌(CMCC52006)、炭疽芽孢杆菌(CMCC63001)、霍乱弧菌(CMCC18001)、伤寒沙门菌(CMCC50071)、志贺氏菌(CMCC51105)均由中国医学细菌保藏管理中心(CMCC)提供。
1.1.2 试剂 胰酪大豆胨琼脂培养基(TSA)、脑心浸液琼脂培养基均购自美国 BD 公司;中国细菌浊度标准国家标准品及皮上划痕用鼠疫、布氏、炭疽活疫苗菌浓度测定通用参考品均由我院制备;布鲁氏菌上转发光免疫层析检测试剂(批号:20190601)由北京热景生物技术股份有限公司生产;布鲁氏菌抗原检测试剂(胶体金法)(批号:20190101801)由北京金豪制药股份有限公司生产。
1.1.3 实验仪器 生物安全柜购自美国 Nuaire 公司;MIR-153 型恒温培养箱购自日本三洋公司;UV-2401 型紫外可见分光光度计购自日本岛津公司。
1.2 方法
1.2.1 不同灭活方式及保存温度对布氏菌抗原性影响 将新鲜制备的布氏菌液(CMCC55010)分别经 70 ℃灭活 1 h 和 1% 甲醛溶液灭活,每种灭活菌液分别稀释成1.0 × 108个/ml,分别放置 4 ℃、–20 ℃及–80 ℃保存,1 个月后将菌液稀释成 1.0 × 107个/ml 进行抗原性检测。
1.2.2 菌液的制备
1.2.2.1 阳性参考品菌液制备 将布氏菌株接种 TSA 平皿,35 ~ 37 ℃培养 44 ~ 48 h 后收获。将收获菌液用中国细菌浊度标准国家标准品测定浓度后稀释成 1.0 × 1010个/ml,70 ℃灭活1 h。经灭活验证合格后分装,–80 ℃保存。
1.2.2.2 阴性参考品菌液制备 将菌株接种于各自适宜生长的培养基上,并于最适温度下进行培养后收获。将收获菌液用中国细菌浊度标准国家标准品测定浓度后稀释成 1.0 × 1010个/ml,经适当方式灭活。经灭活验证合格后分装,–80 ℃保存。
1.2.2.3 最低检出量和重复性参考品菌液的制备 将布氏菌株(CMCC55010)接种 TSA 平皿,35 ~ 37 ℃培养 44 ~ 48 h 后收获。将收获菌液经分光光度法测定浓度后稀释成 1.0 × 1010个/ml,70 ℃灭活 1 h。经灭活验证合格后分装,–80 ℃保存。
1.2.3 参考品的制备
1.2.3.1 阳性参考品的制备 将 3 株布氏菌原始菌液以生理盐水稀释至 1.0 × 108个/ml 浓度,定量分装,0.5 ml/管,–20 ℃以下保存,分别编号为 P1 ~ P3。
1.2.3.2 阴性参考品的制备 将 10 株阴性菌的原始菌液以生理盐水稀释至 1.0 × 108个/ml浓度,定量分装,0.5 ml/管,–20 ℃以下保存,分别编号为 N1 ~ N10。
1.2.3.3 最低检出量及重复性参考品的制备 将布氏菌原始菌液(CMCC55010)用冻干保护剂稀释至 1.0 × 108个/ml,定量分装,0.5 ml/支,冻干后封口,–20 ℃以下保存。分装精确度不高于 1%,水分不高于 3.0%。
1.2.4 均匀性检测 随机抽取冻干的最低检出量参考品 10 支,分别加入 0.5 ml 生理盐水复溶,稀释到 2.5 × 107个/ml。用布鲁氏菌上转发光免疫层析检测试剂进行检测,每支样品重复测定 3 次,将测定值进行单因子方差分析。
1.2.5 参考品的稳定性研究
1.2.5.1 冻融稳定性试验 从–20 ℃冰箱中取出最低检出量参考品、阳性参考品及阴性参考品中小肠结肠炎耶尔森菌 O:9 血清型菌株,于室温放置约 8 h,再放回 –20 ℃冰箱。按此步骤重复 1 次或 3 次。将所有样品再次从–20 ℃冰箱中取出,平衡至室温后,用检测试剂进行检测。
1.2.5.2 加速稳定性试验 从–20 ℃冰箱中取出最低检出量参考品、阳性参考品及阴性参考品中小肠结肠炎耶尔森菌 O:9 血清型菌株,分别于 4、25、37 ℃各放置 2 套,3 d 和5 d 后各取出 1 套,用检测试剂进行检测。
1.2.5.3 长期稳定性试验 对最低检出量参考品进行了长期稳定性研究,现已完成 1 个月、3 个月、6 个月检测。
1.2.6 参考品协作标定 2 家生产单位使用各自生产的试剂进行检测,中国食品药品检定研究院检验人员(未参与样品编盲)使用布鲁氏菌抗原检测试剂(胶体金法)进行检测,军事科学院军事医学研究院微生物流行病研究所使用布鲁氏菌上转发光免疫层析检测试剂进行检测。4 个实验室编号分别为 1、2、3、4。
1.3 统计学处理
采用 SPSS 统计软件,将测定结果进行单因素方差统计分析,结果以< 0.05 表示差异有统计学意义。
2 结果
2.1 不同灭活方式及保存温度对布氏菌抗原性影响
抗原性检测结果见表 1。热灭活方式对抗原性影响明显小于甲醛灭活,4 ℃保存样品抗原性不稳定,–20 ℃及–80 ℃保存抗原稳定性较好且未见明显差异。最终确定布氏菌灭活方式为 70 ℃ 1 h,保存条件为–20 ℃。
2.2 均匀性检测
结果见表 2。临界值0.05(9,20)= 2.42,计算的值为 2.229,该值<临界值,= 0.065 > 0.05,这表明在 0.05 显著性水平时,样品中的抗原量是均匀的。
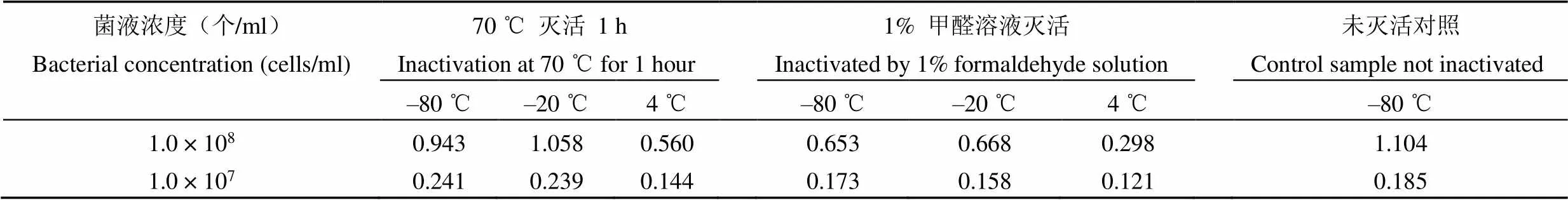
表 1 不同灭活方式及保存温度对布氏菌体抗原性影响(T/C)

表 2 均匀性检查结果(T/C)
2.3 稳定性试验
2.3.1 冻融稳定性试验 冻融 1 次及 3 次后最低检出量参考品的检出限度与未冻融对照无差别,结果见表 3。3 株阳性参考品及阴性参考品中小肠结肠炎耶尔森菌 O:9 血清型菌株冻融 1 次及 3 次后仍均为阳性。研究结果表明最低检出量参考品、阳性参考品及阴性参考品中小肠结肠炎耶尔森菌 O:9 血清型菌株具有较好的冻融稳定性。
2.3.2 加速稳定性试验 所有加速试验后最低检出量参考品的检出限度与–20 ℃保存的对照样品无差别,结果见表 4。3 株阳性参考品及阴性参考品中小肠结肠炎耶尔森菌 O:9血清型菌株加速试验后仍均为阳性。研究结果表明最低检出量参考品、阳性参考品及阴性参考品中小肠结肠炎耶尔森菌 O:9 血清型菌株具有较好的加速稳定性。
2.3.3 长期稳定性试验 观察期内最低检出量参考品的最低检出限度未见变化,结果见表 5,表明最低检出量参考品具有较好的长期稳定性。
2.4 协作标定
4 个实验室的阳性参考品符合率均为 100%。4 个实验室的阴性参考品符合率均为 90%,小肠结肠炎耶尔森菌 O:9 血清型菌株均出现了假阳性。最低检出量参考品方面,1 家企业试剂的最低检出量为 1 × 106个/ml,另 1 家试剂的最低检出量为 1 × 107个/ml。重复性参考品方面,两家企业试剂均检测为阳性,且平行检测 10 次,显色度均一或 CV 值小于 10%,结果见表 6。

表 3 最低检出量参考品冻融试验结果
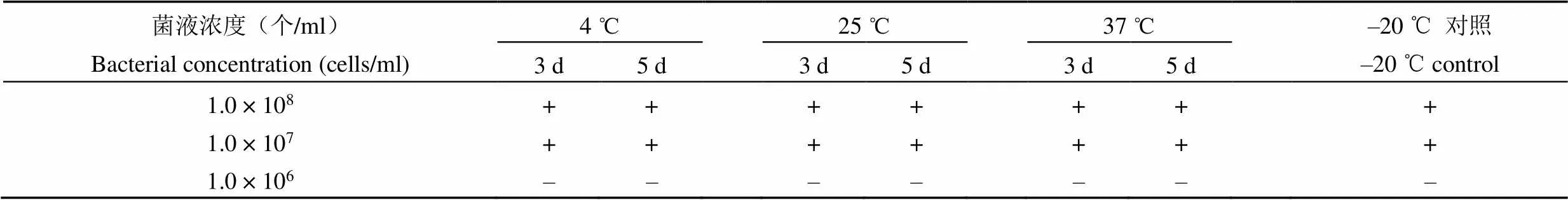
表 4 最低检出量参考品加速试验结果
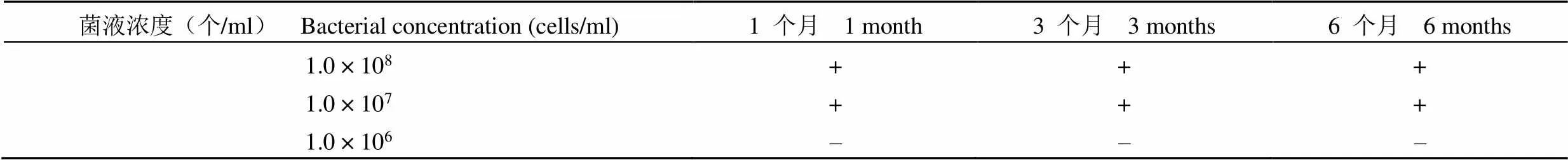
表 5 长期定性试验结果

表 6 协作标定结果
3 讨论
在世界范围内,引起人类布病的主要是羊种、牛种和猪种布氏菌[7-8]。所以,本套参考品中的阳性参考品分别设置了羊种、牛种和猪种布氏菌。阴性参考品包括与布氏菌感染症状相近的菌株,也包括了文献报道与布氏菌有交叉的菌株,如霍乱弧菌、土拉热弗朗西丝菌、小肠结肠炎耶尔森菌 O:9 血清型菌株等[9-10]。
在阴性参考品的筛选过程中发现小肠结肠炎耶尔森菌 O:9 血清型菌株与布氏菌存在明显的抗原交叉。为进一步验证该结果的可靠性,我们将小肠结肠炎耶尔森菌 O:9 血清型菌株进行了单克隆化,随机选取 3 个单克隆菌落,进行了抗原性检测及 16S rDNA 测序,结果表明单克隆菌落为小肠结肠炎耶尔森菌,3 个单克隆菌落经布鲁氏菌抗原检测试剂检测均为阳性。该结果表明现有检测方法尚无法鉴别布氏菌与小肠结肠炎耶尔森菌 O:9 血清型菌株。
最低检出量参考品是评价产品检测能力的最重要工具[11]。对于诊断产品,最低检出量参考品是评价产品检测下限的依据,其稳定性对于检测试剂的质量控制非常重要。为保证参考品的稳定性,我们对最低检出量参考品进行了冻干处理,研究结果表明该参考品具有较好的稳定性。
本研究所建立的布鲁氏菌抗原检测试剂评价用参考品,可用于布鲁氏菌抗原检测试剂的质量评价,对于提高产品质量具有重要意义。
[1] Pappas G, Papadimitriou P, Akritidis N, et al. The new global map of human brucellosis. Lancet Infect Dis, 2006, 6(2):91-99.
[2] Qiu YH, Wang J, He SY. Research progress on the epidemic, detection and prevention of human brucellosis. Chin J Clin Pathologist, 2015, 7(3):187-188, 172. (in Chinese)
邱宇鹤, 王锦, 何淑云. 人布鲁氏菌病的流行、检测与防治研究进展. 实用检验医师杂志, 2015, 7(3):187-188, 172.
[3] Franco MP, Mulder M, Gilman RH, et al. Human brucellosis. Lancet Infect Dis, 2007, 7(12):75-76.
[4] Olsen SC, Palmer MV. Advancement of knowledge of Brucellosis over the past 50 years. Vet Pathol, 2014, 51(6):1076-1089.
[5] Greenfield RA, Drevets DA, Machado LJ, et al. Bacterial pathogens as biological weapons and agents of bioterrorism. Am J Med Sci, 2002, 323(6):299-315.
[6] Doganay GD, Doganay M. Brucella as a potential agent of bioterrorism. Recent Pat Antiinfect Drug Discov, 2013, 8(1):27-33.
[7] Liu ZG, Wang M, Liu RH, et a1. Species identification and epidemiological characteristics analysis of Brucella in Ulanqab, Inner Mongolia, China. Chin J Zoonoses, 2016, 32(7):618-622, 631. (in Chinese)
刘志国, 王妙, 刘日宏, 等. 内蒙古乌兰察布布氏菌分离株种型鉴定及流行病学特征分析. 中国人兽共患病学报, 2016, 32(7):618- 622, 631.
[8] Schurig GG, Sriranganathan N, Corbel MJ. Brucellosis vaccines: past, present and future. Vet Microbiol, 2002, 90(1-4):479-496.
[9] Sun YX, Zhang FL. Cross-response observation and differential diagnosis of suspected cases of Brucellosis and Yersinia enterocolitica Serotype 0:9. Chin J Endemiology, 2001, 20(6):477. (in Chinese)
孙养信, 张福利. 布鲁氏杆菌与0:9型耶尔森氏菌血清学交叉反应观察及其可疑病例的鉴别诊断. 中国地方病学杂志, 2001, 20(6):477.
[10] Xiao YC, Qiu HY, Wang B, et a1. Screen and its amplification of specific mAb of Yersinia enterocolitica serotype O:9. Chin J Vector Bio Control, 2005, 16(6):459-461. (in Chinese)
肖玉春, 邱海燕, 王冰, 等. 小肠结肠炎耶尔森菌O:9血清型特异性单克隆抗体筛选及其应用. 中国媒介生物学及控制杂志, 2005, 16(6):459-461.
[11] Dong JC. Establishment of internal reference products for in vitro diagnostic reagents for qualitative testing. J Radioimmunolgy, 2011, 24(1):50-51. (in Chinese)
董劲春. 定性检测用体外诊断试剂的企业内部参考品的设置. 放射免疫学杂志, 2011, 24(1):50-51.
Preparation of national reference for detection reagentantigen
ZHANG Yuan-yuan, ZHANG Ping-ping, WANG Chun-e, ZHAO Ai-hua, YANG Rui-fu, WEI Dong
Key Laboratory of the Ministry of Health for Research on Quality and Standardization of Biotech Products, National Institute for Food and Drug Control, Beijing 102629, China (ZHANG Yuan-yuan, WANG Chun-e, ZHAO Ai-hua, WEI Dong); State Key Laboratory of Pathogens and Biosecurity, Institute of Microbiology and Epidemiology, Academy of Military Medical Sciences, Academy of Military Sciences, Beijing 100071, China (ZHANG Ping-ping, YANG Rui-fu)
To prepare national reference for detection reagent ofantigen.
Three standard strains ofand ten reference strains of non-were cultured in appropriate culture media at appropriate temperatures respectively. Fresh and uncontained cultures were collected, based on which positive and negative reference bacterial liquids were prepared by turbidimetry, and the reference bacterial liquids for minimum detection limit and repeatability were prepared by spectrophotometry. The prepared references were subjected to uniformity and stability test. Four laboratories were organized to coordinate the calibration of reference materials.
Positive reference consisted of three samples ofliquids, while negative reference consisted of ten samples of non-liquids. The reference for minimum detection and reproducibility consisted of frozen dried bacteria. The reference had good uniformity and stability. The collaborative calibration results of four laboratories showed that three positive references were 100% positive, ten negative references were 90% negative, and the lowest detection amount was between 107cells/ml and 106cells/ml. Repetitive reference test results were found to be consistent.
The reference can be used for quality control ofantigen detection reagent.
; Antigen; National reference; Uniformity; Stability
WEI Dong, Email: weidong1994@sina.com; YANG Rui-fu, Email: 13801034560@163.com
10.3969/j.issn.1673-713X.2020.03.006
国家科技重大专项(2018ZX10102-001);国家重点研发计划(2018YFC200500)
魏东,Email:weidong1994@sina.com;杨瑞馥,Email:13801034560@163.com
2019-11-04
*同为第一作者
